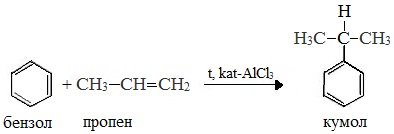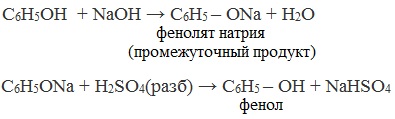Гидроксисоединения – это органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Гидроксисоединения делят на спирты и фенолы.
| Спирты – это гидроксисоединения, в которых группа ОН соединена с алифатическим углеводородным радикалом R-OH. Если гидроксогруппа ОН соединена с бензольным кольцом, то вещество относится к фенолам. |
Общая формула предельных нециклических спиртов: CnH2n+2Om, где m ≤ n.
- Классификация фенолов
- По числу гидроксильных групп:
- Строение фенолов
- Химические свойства фенолов
- 1.1. Взаимодействие с раствором щелочей
- 1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
- 2. Реакции фенола по бензольному кольцу
- 2.1. Галогенирование
- 2.2. Нитрование
- 3. Поликонденсация фенола с формальдегидом
- 4. Взаимодействие с хлоридом железа (III)
- 5. Гидрирование (восстановление) фенола
- Получение фенолов
- 1. Взаимодействие хлорбензола с щелочами
- 2. Кумольный способ
- 3. Замещение сульфогруппы в бензол-сульфокислоте
- Получение фенола из гексана уравнение
- Получение фенола в промышленности
- Как из н — гексана получить фенол?
- Бензол в лаборатории можно получить :а) тримеризацией ацетиленаб) дегидроциклизацией гексанав) гидрированием фенолаг) сплавлением бензола натрия с гидроксидом натрия?
- 1)Распознайте вещ — ва : фенол, глицерин, гексен, Гексано — 1, гексан?
- Как из метана получить гексан?
- Как получить из гексана — бензен?
- Как из пропана получить гексан?
- Получить фенол из толуола?
- Получите фенол всевозможными способами?
- Реакцией Вюрца получите из хлорпропана – гексан?
- Как из этилового спирта получить фенол?
- Что получится?
Классификация фенолов
По числу гидроксильных групп:
- фенолы с одной группой ОН — содержат одну группу -ОН. Общая формула CnH2n-7OH или CnH2n-6O.
- фенолы с двумя группами ОН — содержат две группы ОН. Общая формула CnH2n-8(OH)2 или CnH2n-6O2.
| Соединения, в которых группа ОН отделена от бензольного кольца углеродными атомами – это не фенолы, а ароматические спирты: |
Строение фенолов
В фенолах одна из неподеленных электронных пар кислорода участвует в сопряжении с π–системой бензольного кольца, это является главной причиной отличия свойств фенола от спиртов.
Химические свойства фенолов
| Сходство и отличие фенола и спиртов. |
Сходство: как фенол, так и спирты реагируют с щелочными металлами с выделением водорода.
Отличия:
- фенол не реагирует с галогеноводородами: ОН- группа очень прочно связана с бензольным кольцом, её нельзя заместить;
- фенол не вступает в реакцию этерификации, эфиры фенола получают косвенным путем;
- фенол не вступает в реакции дегидратации.
- фенол обладает более сильными кислотными свойствами и вступает в реакцию со щелочами.
1. Кислотные свойства фенолов
| Фенолы являются более сильными кислотами, чем спирты и вода, т. к. за счет участия неподеленной электронной пары кислорода в сопряжении с π-электронной системой бензольного кольца полярность связи О–Н увеличивается. |
Раствор фенола в воде называют «карболовой кислотой», он является слабым электролитом.
1.1. Взаимодействие с раствором щелочей
В отличие от спиртов, фенолы реагируют с гидроксидами щелочных и щелочноземельных металлов, образуя соли – феноляты.
| Например, фенол реагирует с гидроксидом натрия с образованием фенолята натрия |
Так как фенол – более слабая кислота, чем соляная и даже угольная, его можно получить из фенолята, вытесняя соляной или угольной кислотой:
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Фенолы взаимодействуют с активными металлами (щелочными и щелочноземельными). При этом образуются феноляты. При взаимодействии с металлами фенолы ведут себя, как кислоты.
| Например, фенол взаимодействует с натрием с образованием фенолята натрия и водорода . |
2. Реакции фенола по бензольному кольцу
| Наличие ОН-группы в бензольном кольце (ориентант первого рода) приводит к тому, что фенол гораздо легче бензола вступает в реакции замещения в ароматическом кольце. |
2.1. Галогенирование
| Фенол легко при комнатной температуре (без всякого катализатора) взаимодействует с бромной водой с образованием белого осадка 2,4,6-трибромфенола (качественная реакция на фенол). |
2.2. Нитрование
Под действием 20% азотной кислоты HNO3 фенол легко превращается в смесь орто- и пара-нитрофенолов.
| Например, при нитровании фенола избытком концентрированной HNO3 образуется 2,4,6-тринитрофенол (пикриновая кислота): |
3. Поликонденсация фенола с формальдегидом
С формальдегидом фенол образует фенолоформальдегидные смолы.
4. Взаимодействие с хлоридом железа (III)
При взаимодействии фенола с хлоридом железа (III) образуются комплексные соединения железа, которые окрашивают раствор в сине-фиолетовый цвет. Это качественная реакция на фенол.
5. Гидрирование (восстановление) фенола
Присоединение водорода к ароматическому кольцу.
Продукт реакции – циклогексанол, вторичный циклический спирт.
Получение фенолов
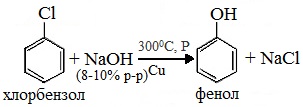
1. Взаимодействие хлорбензола с щелочами
При взаимодействии обработке хлорбензола избытком щелочи при высокой температуре и давлении образуется водный раствор фенолята натрия.
При пропускании углекислого газа (или другой более сильной кислоты) через раствор фенолята образуется фенол.
2. Кумольный способ
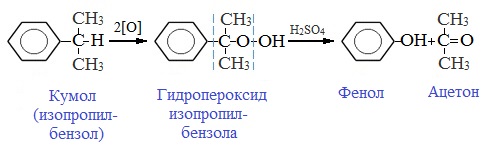
Фенол в промышленности получают из каталитическим окислением кумола.
Первый этап процесса – получение кумола алкилированием бензола пропеном в присутствии фосфорной кислоты:
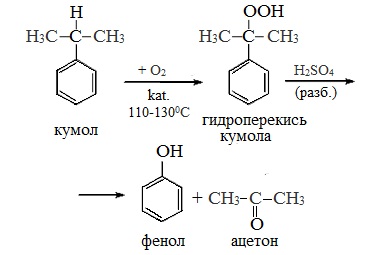
Второй этап – окисление кумола кислородом. Процесс протекает через образование гидропероксида изопропилбензола:
Суммарное уравнение реакции:
3. Замещение сульфогруппы в бензол-сульфокислоте
Бензол-сульфокислота реагирует с гидроксидом натрия с образованием фенолята натрия:
Получается фенолят натрия, из которого затем выделяют фенол:
Получение фенола из гексана уравнение
Фенолы выделяют из каменноугольной смолы, а также из продуктов пиролиза бурых углей и древесины (деготь).
Промышленный способ получения самого фенола С6Н5ОН основан на окислении ароматического углеводорода кумола (изопропилбензол) кислородом воздуха с последующим разложением получающейся гидроперекиси, разбавленной H2SO4. Реакция проходит с высоким выходом и позволяет получить сразу два технически ценных продукта – фенол и ацетон.
Получение фенола в промышленности
1. Кумольный способ
(СССР, Сергеев П.Г., Удрис Р.Ю., Кружалов Б.Д., 1949 г.). Преимущества метода: безотходная технология (выход полезных продуктов > 99%) и экономичность. В настоящее время кумольный способ используется как основной в мировом производстве фенола.
В качестве исходного сырья используют бензол и пропилен, из которых получают изопропилбензол (кумол), подвергающийся дальнейшим превращениям:
1 стадия – получение кумола
2 стадия – каталитическое окисление
2. Из каменноугольной смолы (как побочный продукт – выход небольшой)
Каменноугольную смолу, содержащую в качестве одного из компонентов фенол, обрабатывают вначале раствором щелочи (образуются феноляты), а затем – кислотой:
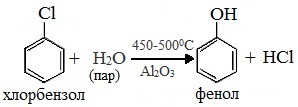
3. Взаимодействие галогенпроизводных ароматических УВ со щелочами
или с водяным паром
4. Сплавлением солей аренсульфокислот с твёрдыми щелочами
Как из н — гексана получить фенол?
Химия | 10 — 11 классы
Как из н — гексана получить фенол?
C6H14 = C6H6 + 4H2
C6H6 + Cl2 = C6H5Cl + HCl C6H5Cl + NaOH = C6H5OH + NaCl.
C6H14 = C6H6 + 4H2
C6H6 + Cl2 = C6H5Cl + HCl
C6H5Cl + 2NaOH = C6H5ONa + NaCl
C6H5ONa + HCl = C6H5OH + NaCl.
Бензол в лаборатории можно получить :а) тримеризацией ацетиленаб) дегидроциклизацией гексанав) гидрированием фенолаг) сплавлением бензола натрия с гидроксидом натрия?
Бензол в лаборатории можно получить :
а) тримеризацией ацетилена
б) дегидроциклизацией гексана
в) гидрированием фенола
г) сплавлением бензола натрия с гидроксидом натрия.
1)Распознайте вещ — ва : фенол, глицерин, гексен, Гексано — 1, гексан?
1)Распознайте вещ — ва : фенол, глицерин, гексен, Гексано — 1, гексан.
Напишите уравнения всех реакций.
Укажите их признаки и условия их протекания.
Как из метана получить гексан?
Как из метана получить гексан?
Как получить из гексана — бензен?
Как получить из гексана — бензен.
Как из пропана получить гексан?
Как из пропана получить гексан?
Получить фенол из толуола?
Получить фенол из толуола.
Получите фенол всевозможными способами?
Получите фенол всевозможными способами.
Реакцией Вюрца получите из хлорпропана – гексан?
Реакцией Вюрца получите из хлорпропана – гексан.
Как из этилового спирта получить фенол?
Как из этилового спирта получить фенол.
Что получится?
На этой странице сайта, в категории Химия размещен ответ на вопрос Как из н — гексана получить фенол?. По уровню сложности вопрос рассчитан на учащихся 10 — 11 классов. Чтобы получить дополнительную информацию по интересующей теме, воспользуйтесь автоматическим поиском в этой же категории, чтобы ознакомиться с ответами на похожие вопросы. В верхней части страницы расположена кнопка, с помощью которой можно сформулировать новый вопрос, который наиболее полно отвечает критериям поиска. Удобный интерфейс позволяет обсудить интересующую тему с посетителями в комментариях.
Zn — >K2ZnO2 — >ZnSO4 — >K2[Zn(OH)4] — >Zn(NO3)2 — >ZnO 1)4Zn + KNO3 + 7KOH = NH3 + 4K2ZnO2 + 2H2O 2)K2ZnO2 + 2H2SO4 = K2SO4 + ZnSO4 + 2H2O 3)ZnSO4 + 4KOH = K2[Zn(OH)4] + K2SO4 4)K2[Zn(OH)4] + 4HNO3 = 2KNO3 + Zn(NO3)2 + 4H2O 5)2Zn(NO3)2 = 2ZnO + 4NO2..
Ca + H2O = Ca(OH)2 + H2n(Ca) = 6 г / моль : 40 г = 0, 15 мольV(Ca) = 0, 15моль * 22, 4 л / моль = 3, 36л3, 36л — 100%3 л — х%х = 89%.
Дано : Жк₁ = 11 мг — экв / л Жк₂ = 3 мг — экв / л Vв = 100 м³ Найти : m(Ca(OH)₂) Решение. Переведем единицы заданияв более удобные мг — экв / л = г — экв / м³ Снизить карбонатную жесткость с 11 г — экв / м³до 3г — экв / м³ — значит убрать из каждого..
Масса О2 = 0, 888. Если реак. 2Fe + O2 = 2FeO.
1 — Ответ 6NaOH + Al2O3 + 3H2O = 2Na3[Al(OH)6] NaOH + HCl = H2O + NaCl.
2) CH3 — CH2 — CH(CH3) — CH(CH2 — CH3) — CH2 — CH2 — CH3 3) CH3 — CH2 — CH2 — Cl + 2Na + Cl — CH2 — CH2 — CH3 — > CH3 — CH2 — CH2 — CH2 — CH2 — CH3 + 2NaCl.
Ca — 2e = Ca( + 2) коэффициент 4 Восстановитель, окисление 2N( + 5) + 8e = 2 N ( + 1) коэффициент 1 Окислитель, восстановление 4Ca + 10HNO3 = 4Ca(NO3)2 + N2O + 5H2O Если помог, нажми кнопку Спасибо)).
5 граммов раствора чтобы приготовить.
Cl2 — 1 молекула хлора, 3Cl — 3 атома хлора, 2H2 — две молекулы водорода, О2 — кислород, 3Н + — тритий, вроде, 5H2O — пять молекул водорода.
Ch3 — ch(br) — c(f)(f) — ch2 — ch2 — ch2 — ch3.