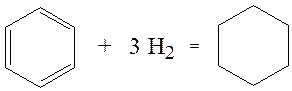Арены (ароматические углеводороды) – это непредельные (ненасыщенные) циклические углеводороды, молекулы которых содержат устойчивые циклические группы атомов (бензольные ядра) с замкнутой системой сопряженных связей.
Общая формула: CnH2n–6 при n ≥ 6.
- Химические свойства аренов
- 1. Реакции присоединения
- 1.1. Гидрирование
- 1.2. Хлорирование аренов
- 2. Реакции замещения
- 2.1. Галогенирование
- 2.2. Нитрование
- 2.3. Алкилирование ароматических углеводородов
- 2.4. Сульфирование ароматических углеводородов
- 3. Окисление аренов
- 3.1. Полное окисление – горение
- 3.2. О кисление гомологов бензола
- 4. Ориентирующее действие заместителей в бензольном кольце
- 5. Особенности свойств стирола
- Гидрирование бензола
- Гидрирование бензола
- Назначение
- Сырье и продукты
- Технологическая схема
- Реакционная секция
- Секция разделения продуктов
- Секция стабилизации
- Материальный баланс
- Достоинства и недостатки
- Недостатки
- Достоинства
- Существующие установки
- 📹 Видео
Видео:ВСЕ ПРО АЛКАНЫ за 8 минут: Химические Свойства и ПолучениеСкачать

Химические свойства аренов
Арены – непредельные углеводороды, молекулы которых содержат три двойных связи и цикл. Но из-за эффекта сопряжения свойства аренов отличаются от свойств других непредельных углеводородов.
Для ароматических углеводородов характерны реакции:
- присоединения,
- замещения,
- окисления (для гомологов бензола).
| Из-за наличия сопряженной π-электронной системы молекулы ароматических углеводородов вступают в реакции присоединения очень тяжело, только в жестких условиях — на свету или при сильном нагревании, как правило, по радикальному механизму |
| Бензольное кольцо представляет из себя скопление π-электронов, которое притягивает электрофилы. Поэтому для ароматических углеводородов характерны реакции электрофильного замещения атома водорода у бензольного кольца. |
Ароматическая система бензола устойчива к действию окислителей. Однако гомологи бензола окисляются под действием перманганата калия и других окислителей.
Видео:6.3. Ароматические углеводороды (бензол и его гомологи): Химические свойства. ЕГЭ по химииСкачать

1. Реакции присоединения
Бензол присоединяет хлор на свету и водород при нагревании в присутствии катализатора.
1.1. Гидрирование
Бензол присоединяет водород при нагревании и под давлением в присутствии металлических катализаторов (Ni, Pt и др.).
При гидрировании бензола образуется циклогексан:
При гидрировании гомологов образуются производные циклоалканы. При нагревании толуола с водородом под давлением и в присутствии катализатора образуется метилциклогексан:
1.2. Хлорирование аренов
Присоединение хлора к бензолу протекает по радикальному механизму при высокой температуре, под действием ультрафиолетового излучения.
При хлорировании бензола на свету образуется 1,2,3,4,5,6-гексахлорциклогексан (гексахлоран).
Гексахлоран – пестицид, использовался для борьбы с вредными насекомыми. В настоящее время использование гексахлорана запрещено.
Гомологи бензола не присоединяют хлор. Если гомолог бензола реагирует с хлором или бромом на свету или при высокой температуре (300°C), то происходит замещение атомов водорода в боковом алкильном заместителе, а не в ароматическом кольце.
| Например, при хлорировании толуола на свету образуется бензилхлорид |
| Если у гомолога бензола боковая цепь содержит несколько атомов углерода – замещение происходит у атома, ближайшему к бензольному кольцу («альфа-положение»). |
| Например, этилбензол реагирует с хлором на свету |
Видео:Химические свойства бензола и его гомологов. 1 часть. 11 класс.Скачать

2. Реакции замещения
| Реакции замещения у ароматических углеводородов протекают по ионному механизму (электрофильное замещение). При этом атом водорода замещается на другую группу (галоген, нитро, алкил и др.). |
2.1. Галогенирование
Бензол и его гомологи вступают в реакции замещения с галогенами (хлор, бром) в присутствии катализаторов (AlCl3, FeBr3).
При взаимодействии с хлором на катализаторе AlCl3 образуется хлорбензол:
Ароматические углеводороды взаимодействуют с бромом при нагревании и в присутствии катализатора – FeBr3 . Также в качестве катализатора можно использовать металлическое железо.
Бром реагирует с железом с образованием бромида железа (III), который катализирует процесс бромирования бензола:
| Гомологи бензола содержат алкильные заместители, которые обладают электронодонорным эффектом: из-за того, что электроотрицательность водорода меньше, чем углерода, электронная плотность связи С-Н смещена к углероду. На нём возникает избыток электронной плотности, который далее передается на бензольное кольцо. |
| Поэтому гомологи бензола легче вступают в реакции замещения в бензольном кольце. При этом гомологи бензола вступают в реакции замещения преимущественно в орто— и пара-положения |
| Например, при взаимодействии толуола с хлором образуется смесь продуктов, которая преимущественно состоит из орто-хлортолуола и пара-хлортолуола |
Мета-хлортолуол образуется в незначительном количестве.
При взаимодействии гомологов бензола с галогенами на свету или при высокой температуре (300 о С) происходит замещение водорода не в бензольном кольце, а в боковом углеводородном радикале.
| Если у гомолога бензола боковая цепь содержит несколько атомов углерода – замещение происходит у атома, ближайшему к бензольному кольцу («альфа-положение»). |
Например, при хлорировании этилбензола:
2.2. Нитрование
Бензол реагирует с концентрированной азотной кислотой в присутствии концентрированной серной кислоты (нитрующая смесь).
При этом образуется нитробензол:
| Серная кислота способствует образованию электрофила NO2 + : |
Толуол реагирует с концентрированной азотной кислотой в присутствии концентрированной серной кислоты.
В продуктах реакции мы указываем либо о-нитротолуол:
Нитрование толуола может протекать и с замещением трех атомов водорода. При этом образуется 2,4,6-тринитротолуол (тротил, тол):
2.3. Алкилирование ароматических углеводородов
- Арены взаимодействуют с галогеналканами в присутствии катализаторов (AlCl3, FeBr3 и др.) с образованием гомологов бензола.
| Например, бензол реагирует с хлорэтаном с образованием этилбензола |
- Ароматические углеводороды взаимодействуют с алкенами в присутствии хлорида алюминия, бромида железа (III), фосфорной кислоты и др.
| Например, бензол реагирует с этиленом с образованием этилбензола |
| Например, бензол реагирует с пропиленом с образованием изопропилбензола (кумола) |
- Алкилирование спиртами протекает в присутствии концентрированной серной кислоты.
| Например, бензол реагирует с этанолом с образованием этилбензола и воды |
2.4. Сульфирование ароматических углеводородов
Бензол реагирует при нагревании с концентрированной серной кислотой или раствором SO3 в серной кислоте (олеум) с образованием бензолсульфокислоты:
Видео:Уравнивание реакций горения углеводородовСкачать

3. Окисление аренов
Бензол устойчив к действию даже сильных окислителей. Но гомологи бензола окисляются под действием сильных окислителей. Бензол и его гомологи горят.
3.1. Полное окисление – горение
При горении бензола и его гомологов образуются углекислый газ и вода. Реакция горения аренов сопровождается выделением большого количества теплоты.
Уравнение сгорания аренов в общем виде:
При горении ароматических углеводородов в недостатке кислорода может образоваться угарный газ СО или сажа С.
Бензол и его гомологи горят на воздухе коптящим пламенем. Бензол и его гомологи образуют с воздухом и кислородом взрывоопасные смеси.
3.2. О кисление гомологов бензола
Гомологи бензола легко окисляются перманганатом и дихроматом калия в кислой или нейтральной среде при нагревании.
При этом происходит окисление всех связей у атома углерода, соседнего с бензольным кольцом, кроме связи этого атома углерода с бензольным кольцом.
Толуол окисляется перманганатом калия в серной кислоте с образованием бензойной кислоты:
Если окисление толуола идёт в нейтральном растворе при нагревании, то образуется соль бензойной кислоты – бензоат калия:
Таким образом, толуол обесцвечивает подкисленный раствор перманганата калия при нагревании.
| При окислении других гомологов бензола всегда остаётся только один атом С в виде карбоксильной группы (одной или нескольких, если заместителей несколько), а все остальные атомы углерода радикала окисляются до углекислого газа или карбоновой кислоты. |
| Например, при окислении этилбензола перманганатом калия в серной кислоте образуются бензойная кислота и углекислый газ |
| Например, при окислении этилбензола перманганатом калия в нейтральной кислоте образуются соль бензойной кислоты и карбонат |
Более длинные радикалы окисляются до бензойной кислоты и карбоновой кислоты:
При окислении пропилбензола образуются бензойная и уксусная кислоты:
Изопропилбензол окисляется перманганатом калия в кислой среде до бензойной кислоты и углекислого газа:
Видео:Химические свойства бензола и его гомологов. 2 часть. 11 класс.Скачать

4. Ориентирующее действие заместителей в бензольном кольце
Если в бензольном кольце имеются заместители, не только алкильные, но и содержащие другие атомы (гидроксил, аминогруппа, нитрогруппа и т.п.), то реакции замещения атомов водорода в ароматической системе протекают строго определенным образом, в соответствии с характером влияния заместителя на ароматическую π-систему.
| Заместители подразделяют на две группы в зависимости от их влияния на электронную плотность ароматической системы: электронодонорные (первого рода) и электроноакцепторные (второго рода). |
Типы заместителей в бензольном кольце
| Заместители первого рода | Заместители второго рода |
| Дальнейшее замещение происходит преимущественно в орто— и пара-положение | Дальнейшее замещение происходит преимущественно в мета-положение |
| Электронодонорные, повышают электронную плотность в бензольном кольце | Электроноакцепторные, снижают электронную плотность в сопряженной системе. |
|
|
| Например, толуол реагирует с хлором в присутствии катализатора с образованием смеси продуктов, в которой преимущественно содержатся орто-хлортолуол и пара-хлортолуол. Метильный радикал — заместитель первого рода. |
В уравнении реакции в качестве продукта записывается либо орто-толуол, либо пара-толуол.
| Например, при бромировании нитробензола в присутствии катализатора преимущественно образуется мета-хлортолуол. Нитро-группа — заместитель второго рода |

Видео:Как решать ОРГАНИЧЕСКИЕ ЦЕПОЧКИ? Основные типы химических реакцийСкачать

5. Особенности свойств стирола
Стирол (винилбензол, фенилэтилен) – это производное бензола, которое имеет в своем составе двойную связь в боковом заместителе.
Общая формула гомологического ряда стирола: CnH2n-8.
| Молекула стирола содержит заместитель с кратной связью у бензольного кольца, поэтому стирол проявляет все свойства, характерные для алкенов – вступает в реакции присоединения, окисления, полимеризации. |
Стирол присоединяет водород, кислород, галогены, галогеноводороды и воду в соответствии с правилом Марковникова.
| Например, при гидратации стирола образуется спирт: |
| Стирол присоединяет бром при обычных условиях, то есть обесцвечивает бромную воду |
При полимеризации стирола образуется полистирол:
Как и алкены, стирол окисляется водным раствором перманганата калия при обычных условиях. Обесцвечивание водного раствора перманганата калия — качественная реакция на стирол:
При жестком окислении стирола перманганатом калия в кислой среде (серная кислота) разрывается двойная связь и образуется бензойная кислота и углекислый газ:
При окислении стирола перманганатом калия в нейтральной среде при нагревании также разрывается двойная связь и образуется соль бензойной кислоты и карбонат:
Видео:Гидрируем и дегидрируем углеводородыСкачать

Гидрирование бензола
Гидрирование бензола осуществляется в паровой фазе при давлении1,6-2,0 МПа (16-20 атм.), температуре125-250 о С на никельхромовом катализаторе в 2-х реакторах: трубчатом реакторе со съемом тепла кипящим конденсатом и в колонном реакторе адиабатического типа.
Реакция гидрирования бензола в циклогексан протекает по уравнению:
Гидрирование бензола проводится водородом из азотоводородной фракции, поступающей с производства аммиака, а также используется отбросной водород из отделения дегидрирования анола.
Давление в системе не более 2,0 МПа и мольное соотношение газ-бензол поддерживается за счет циркуляции водорода после гидрирования с помощью циркуляционного компрессора и подачи свежего водорода с давлением 2,0-2,4 МПа.
Молярное соотношение газ — бензол поддерживается равным 8:1 регулированием подачи бензола и циркуляционного водорода.
Для исключения проскока бензола концентрация водорода в циркуляционном газе поддерживается в пределах 20-30 % об. за счет сдувок части циркуляционного газа из системы. Кроме этого необходимо иметь определенную объемную скорость бензола на катализаторе. Максимальная объемная скорость бензола на никельхромовом катализаторе 1,5 л бензола на 1 л катализатора в час. При этом обеспечивается полное превращение бензола в циклогексан.
Однако, реакция гидрирования бензола по высоте слоя катализатора проходит неравномерно: не менее 90 % бензола превращается в циклогексан на 30 % от общего объема катализатора, т.е. при высокой объемной скорости.
Особенность процесса гидрирования бензола требует разбавления катализатора в 1-ом реакторе: в верхнем слое 1 : 8, в среднем 1: 2, нижнем –чистый катализатор. Во 2-ом реакторе колонного типа загружается около 40 % общего объема катализатора без разбавления.
Реакция гидрирования- процесс экзотермический, поэтому для поддержания температуры в пределах 125-250 о С необходим съем тепла. Тепло реакции в реакторе трубчатого типа снимается кипящим конденсатом, тепло реакции во 2-ом реакторе снимается рабочей смесью за счет увеличения ее теплосодержания.
При повышении температуры реакции выше 250 о С происходит изомеризация циклогексана в метилциклопентан.
К качеству бензола предъявляются высокие требования и оно должно соответствовать нормам по ГОСТ 9572-93, представленным в таблице 2
| Наименование | Норма для марок | |||
| высшей очистки | очищенный | для синтеза | ||
| второй | первый | |||
| 1. Внешний вид и цвет | Прозрачная жидкость не содержащая пос-торонних примесей и воды , не темнее раствора 0,003 г К2Сr2О7 в 1 дм 3 воды | |||
| 2. Плотность при 20 о С, г/см 3 | 0,878-0,880 | 0,878-0,880 | 0,878-0,880 | 0,878-0,880 |
| 3. Пределы перегонки 95 %, о С, не более (включая температуру кипения чистого бензола 80,1 о С) | — | — | 0,6 | 0,6 |
| 4. Температура кристаллизации, о С, не ниже | 5,40 | 5,40 | 5,35 | 5,30 |
| 5. Массовая доля основного вещества, %, не менее | 99,9 | 99,8 | 99,7 | 99,5 |
| 6. Массовая доля примесей, %, не более: н-гептана метилциклогексана + толуола метилциклогексана толуола | 0,01 0,05 0,02 — | 0,06 0,09 0,04 0,03 | 0,06 0,13 0,08 — | — — — — |
| 7. Окраска серной кислоты, номер образцовой шкалы, не более | 0,1 | 0,1 | 0,1 | 0,15 |
| 8. Массовая доля общей серы, %, не более | 0,00005 | 0,00010 | 0,00010 | 0,00015 |
| 9. Реакция водной вытяжки | нейтральная |
Прежде всего, жесткие нормы установлены по содержанию серы, н- гептана, метилциклогексана и толуола. При гидрировании бензола первые 2 примеси не подвергаются изменениям, а толуол превращается в метилциклогексан.
При окислении циклогексана н- гептан и метилциклогексан окисляются до гептанона –2, который имеет точку кипения, близкую к точке кипения , циклогексанона , поэтому его трудно отделить ректификацией.
Гептанон-2 на стадиях оксимирования и перегруппировки превращается в амиды кислот , что ухудшает качество капролактама.
Следует отметить, что никельхромовый катализатор очень чувствителен к серосодержащим примесям, которые являются контактными ядами. Наиболее сильным каталитическим ядом является тиофен. Его отравляющее действие в 5 раз выше, чем сероводорода и сероуглерода.
Серосодержащие соединения хемосорбируются поверхностью катализатора необратимо отравляя его, снижается активность катализатора и степень превращения бензола.
Для обеспечения длительной эксплуатации никельхромового катализатора при содержании в бензоле и в водороде серы более 1,5 ррм предусматривается форконтактная очистка бензола и водорода на медьсодержащих катализаторах или цинковым поглотителем.
Снижение активности никельхромового катализатора вызывает также наличие аммиака в водороде в количестве более 300 мг / м 3 .
Видео:6.1. Ароматические углеводороды (бензол и его гомологи): Строение, номенклатура, изомерияСкачать

Гидрирование бензола
Видео:ЭТО ПОМОЖЕТ разобраться в Органической Химии — Алкены, Урок ХимииСкачать

Назначение
Циклогексан является относительно стабильным циклоалканом, присутствующим в сырой нефти в концентрациях, варьирующихся от 0,1 до 1,0%. Этот циклоалкан представляет собой бесцветную легковоспламеняющуюся жидкость, широко используемую в качестве промежуточного звена в производстве нейлона.
Почти весь производимый в промышленности циклогексан используется для производства адипиновой кислоты и капролактама, предшественников нейлона. Небольшая часть полученного циклогексана расходуется на различные виды использования, такие как растворители и полимерные реакционные разбавители.
- при производстве синтетических волокон (особенно полиамида 6).
- в щетинных щетках, текстильных элементах жесткости, пленочных покрытиях, синтетической коже, пластмассах, пластификаторах, красках для транспортных средств, сшивке для полиуретанов, а также в синтезе лизина.
Россия производит 8% мирового объема капролактама и внутреннее потребление его растёт на 6-8% ежегодно. Для укрепления позиций на мировом рынке товаров химической промышленности, в том числе полиамидных пластмасс, необходимо расширение существующих производственных мощностей капролактама на основе последних достижений в этой области.
Видео:Химия с нуля — АЛКИНЫ, Тройная связь, Типы Гибридизации // Органическая ХимияСкачать

Сырье и продукты
В промышленном масштабе циклогексан получают гидрированием бензола в присутствии никелевых катализаторов. На производителей циклогексана приходится примерно 11,4% мирового спроса на бензол. Реакция гидрирования бензола является сильно экзотермической.
В качестве сырья процесса выступает бензол и водород. Продуктом является циклогексан – ценное сырье нефтехимических синтезов, а также топливный газ, как результат реакций
расщепления и примесей нежелательных углеводородов в исходном сырье.
Видео:6.2. Ароматические углеводороды (бензол и его гомологи): Способы получения. ЕГЭ по химииСкачать

Технологическая схема
Процесс состоит из трех основных секций:
- реакционная;
- секция разделения продуктов;
- стабилизации.
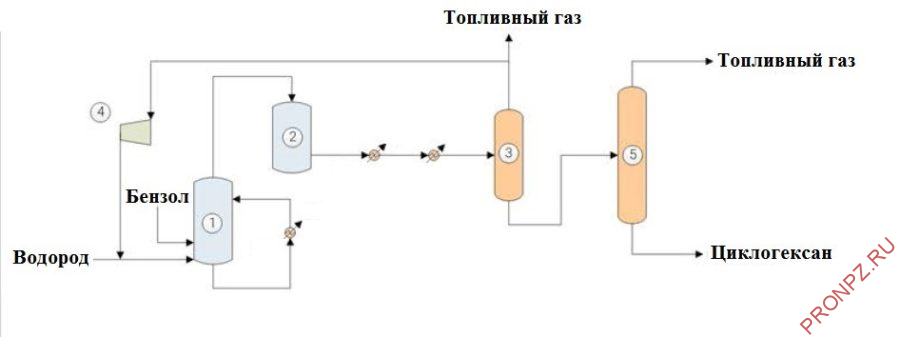
Реакционная секция
Бензол подают в первичный реактор (1) вместе со свежим и рециркулирующим водородом. Реакцию гидрирования проводят в реакторе с барботажной колонной в присутствии катализатора на основе никеля.
Катализатор поддерживается в виде суспензии с помощью внешнего циркуляционного контура. Большая часть тепла реакции удаляется путем испарения потока продукта; оставшееся тепло реакции отводится во внешний контур. Пропуская поток флегмы реактора через теплообменник, нагревается химочищенная питательная вода, производя пар низкого давления. На этом этапе большая часть бензольного сырья превращается в циклогексан. Поток верхнего газообразного продукта направляется в реактор с неподвижным слоем (2), где непрореагировавший бензол превращается в циклогексан. Завершающую реакцию гидрирования проводят в присутствии катализатора на основе твердого никеля, нанесенного на оксид алюминия.
Секция разделения продуктов
Поток продукта подается в сепаратор-отбойник (3), работающий под высоким давлением. Большая часть циклогексана в сырье конденсируется с образованием двух потоков, газообразного обогащенного водородом и потока жидкого циклогексана. Водорода направляется в рециркуляционный компрессор (4), где он компримируется до давления реакции первичного реактора и поступает на реакторный блок.
Секция стабилизации
В дистилляционной колонне (5) поток, обогащенный жидким циклогексаном, очищается от более легких углеводородов, таких как метан, этан и растворенный водород. Легкие газы, выходящие из верхней части колонны, используются в качестве топлива, в то время как поток циклогексана с остаточным содержанием бензола ниже 100 ppm выходит из нижней части колонны.
Видео:Химия с нуля — Химические свойства АлкеновСкачать

Материальный баланс
Материальный баланс действующей установки гидрирования бензола приведен в таблице.
| №п/п | Приход | №п/п | Расход | ||||
| Наименование статей прихода | кг/ч | % мас. | Наименование статей расхода | кг/ч | % мас. | ||
| 1. | Бензол технический, в том числе: | 1. | Циклогексан технический, в том числе: | ||||
| А) бензол | 7974 | 99,80 | А) циклогексана | 8576 | 99,78 | ||
| Б)низкокипящие | 0,4 | 0,01 | Б) азота | 3 | 0,03 | ||
| В) высококипящие | 15,6 | 0,20 | В) низкокипящие | 0,4 | 0,00 | ||
| Г) высококипящие | 15,6 | 0,18 | |||||
| Итого | 7990 | 100,00 | Итого | 8595 | 100,00 | ||
| 2. | Водород, в том числе: | 2. | Газы дросселированния, в том числе: | ||||
| А) водород | 624 | 69,64 | А) циклогексан | 6 | 18,52 | ||
| Б) азот | 272 | 30,36 | Б) водород | 0,6 | 1,85 | ||
| В) азот | 25,8 | 79,63 | |||||
| Итого | 896 | 100,00 | Итого | 32,4 | 100,00 | ||
| 3. | Отдувочные газы, в том числе: | ||||||
| А) циклогексан | 6 | 2,32 | |||||
| Б) водород | 9,4 | 3,63 | |||||
| В) азот | 243,2 | 94,04 | |||||
| Итого | 258,6 | 100,00 | |||||
| Всего (общее) | 8886 | Всего (общее) | 8886 | ||||
Видео:Бензол. Строение и свойства | Химия ЕГЭ для 10 класса | УмскулСкачать

Достоинства и недостатки
Недостатки
- Побочные реакции, в частности изомеризация циклогексана в метилциклопентан (при более высоких температурах происходит разрыв нафтенового кольца с образованием нежелательных С5 и более легких продуктов)
- Высокие требования по качеству исходного сырья, его чистоте и содержанию сернистых соединений.
Достоинства
- Относительно низкая стоимость катализаторов на основе никеля.
- Высокая чистота получаемого циклогексана, порядка 99,9 %.
Видео:Бензол. Механизм реакции электрофильного замещения. Нитрование бензола.Скачать

Существующие установки
Крупнейшими потребителями продукта гидрирования бензола – циклогексана являются производители капролактама.
Капролактам производится перегруппировкой циклогексаноноксима при смешении с олеумом. Циклогексаноноксим, в свою очередь, производится из циклогексанона и гидроксиламинсульфата. Циклогексанон получают окислением циклогексана кислородом воздуха.
В России капролактам производят 3 компании:
- OАО «Куйбышевазот» (Тольятти),
- ОАО «Азот» (Кемерово; холдинг СИБУР)
- ОАО «Щекиноазот» (Тульская область).
Компания «КуйбышевАзот» является крупнейшим производителем капролактама и полиамида-6 в России. Далее, в порядке снижения мощностей по производству капролактама, следует Кемеровское ОАО «Азот».
Третий производитель капролактама в России – ОАО «Щекиноазот» (входит в ОХК «Щекиноазот»).
Все перечисленные компании производят капролактам из циклогексана, полученного гидрированием бензола.
📹 Видео
ГидрированиеСкачать

Химические свойства гомологов бензола Получение ареновСкачать

7 ВАЖНЕЙШИХ РЕАКЦИЙ, которые тебе нужно знать (Алкины)Скачать

Получение бензола и его гомологов. 1 часть. 11 класс.Скачать

Химические свойства бензола и его гомологов. 3 часть. 11 класс.Скачать

Гидратация VS Гидрирование || Почему все путают нас?Скачать