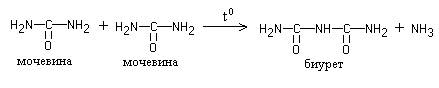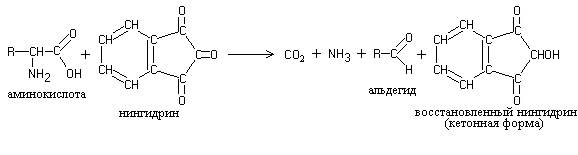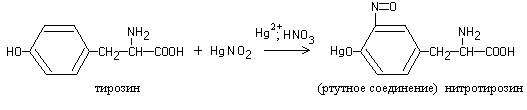История химии в школьном курсе
РЕАКЦИЯ ПИОТРОВСКОГО (БИУРЕТОВАЯ РЕАКЦИЯ)
В белках аминокислоты связаны друг с другом по типу полипептидов и дикетопиперазинов. Образование полипептидов из аминокислот происходит путем отщепления молекулы воды от аминогруппы одной молекулы аминокислоты и карбоксильной группы другой молекулы:
Образующаяся группа –С(О)–NН– называется пептидной группой, связь С–N, соединяющая остатки млекул аминокислот, – пептидной связью.
При взаимодействии дипептида с новой молекулой аминокислоты получается трипептид и т. д.
Дикетопиперазины образуются при взаимодействии двух молекул аминокислот с отщеплением двух молекул воды:
Дикетопиперазины были выделены из белков Н.Д.Зелинским и В.С.Садиковым в 1923 г.
Наличие в белке повторяющихся пептидных групп подтверждается тем, что белки дают фиолетовое окрашивание при действии небольшого количества раствора медного купороса в присутствии щелочи (биуретовая реакция).
Описание опыта. 2–3 мл раствора белка нагревают с 2–3 мл 20%-го раствора едкого кали или натра и несколькими каплями раствора медного купороса. Появляется фиолетовое окрашивание вследствие образования комплексных соединений меди с белками.
- РЕАКЦИЯ РУЭМАННА (НИНГИДРИНОВАЯ РЕАКЦИЯ (1911))
a -Аминокислоты реагируют с нингидрином, образуя сине-фиолетовый комплекс (пурпур Руэманна), интенсивность окраски которого пропорциональна количеству аминокислоты.
Реакция идет по схеме:
Реакция с нингидрином используется для визуального обнаружения a -аминокислот на хроматограммах (на бумаге, в тонком слое), а также для колориметрического определения концентрации аминокислот по интенсивности окраски продукта реакции.
Описание опыта. В пробирку наливают 1 мл 1%-го раствора глицина и 0,5 мл 1%-го раствора нингидрина. Содержимое пробирки осторожно нагревают до появления сине-фиолетового окрашивания.
- Реакция Сакагучи
Эта реакция на аминокислоту аргинин основана на взаимодействии аргинина с a -нафтолом в присутствии окислителя. Ее механизм еще полностью не выяснен. По-видимому, реакция осуществляется по следующему уравнению:
Поскольку производные хинониминов (в данном случае нафтохинона), у которых водород иминогруппы –NH– замещен на алкильный или арильный радикал, всегда окрашены в желто-красные тона, то, по-видимому, оранжево-красный цвет раствора при проведении реакции Сакагучи объясняется возникновением именно производного нафтохинонимина. Не исключена, однако, вероятность образования еще более сложного соединения за счет дальнейшего окисления оставшихся NH-групп аргининового остатка и бензольного ядра a -нафтола:
Описание опыта. В пробирку наливают 2 мл 0,01%-го раствора аргинина, затем добавляют 2 мл 10%-го раствора едкого натра и несколько капель 0,2% спиртового раствора a -нафтола. Содержимое пробирки хорошо перемешивают, приливают 0,5 мл раствора гипобромита и вновь перемешивают. Немедленно добавляют 1 мл 40%-го раствора мочевины для стабилизации быстро развивающегося оранжево-красного окрашивания.
- РЕАКЦИЯ ФОЛЯ
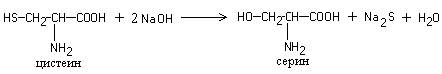
Это реакция на цистеин и цистин. При щелочном гидролизе «слабосвязанная сера» в цистеине и цистине достаточно легко отщепляется, в результате чего образуется сероводород, который, реагируя со щелочью, дает сульфиды натрия или калия. При добавлении ацетата свинца(II) образуется осадок сульфида свинца(II) серо-черного цвета.
Описание опыта. В пробирку наливают 1 мл раствора цистина, прибавляют 0,5 мл 20%-го раствора гидроксида натрия. Смесь нагревают до кипения, а затем добавляют 0,5 мл раствора ацетата свинца(II). Наблюдается выпадение серо-черного осадка сульфида свинца(II):
- РЕАКЦИЯ С ФОРМАЛЬДЕГИДОМ
При взаимодействии a -аминокислот с формальдегидом образуются относительно устойчивые карбиноламины – N-метилольные производные, содержащие свободную карбоксильную группу, которую затем титруют щелочью:
Эта реакция лежит в основе количественного определения a -аминокислот методом формального титрования (метод Сёренсена).
Описание опыта. В пробирку наливают 5 капель 1%-го раствора глицина и прибавляют 1 каплю индикатора метилового красного. Раствор окрашивается в желтый цвет (нейтральная среда). К полученной смеси добавляют равный объем 40%-го раствора формальдегида (формалин). Появляется красное окрашивание (кислая среда):
- РЕАКЦИЯ Циммермана
Это реакция на аминокислоту глицин.
Описание опыта. К 2 мл 0,1%-го раствора глицина, доведенного добавлением 10%-го раствора щелочи до рН = 8, приливают 0,5 мл водного раствора о-фталевого диальдегида. Реакционная смесь начинает медленно окрашиваться в ярко-зеленый цвет. Через несколько минут выпадает зеленый осадок.
- ОБРАЗОВАНИЕ КОМПЛЕКСОВ С МЕТАЛЛАМИ
a -Аминокислоты образуют с катионами тяжелых металлов внутрикомплексные соли. Со свежеприготовленным гидроксидом меди(II) все a -аминокислоты в мягких условиях дают хорошо кристаллизующиеся внутрикомплексные (хелатные) соли меди(II) синего цвета:
В таких солях ион меди координационными связями соединен с аминогруппами.
Описание опыта. В пробирку наливают 3 мл 3%-го раствора сульфата меди(II), добавляют несколько капель 10%-го раствора гидроксида натрия до образования голубого осадка. К полученному осадку гидроксида меди(II) приливают 0,5 мл концентрированного раствора глицина. При этом образуется темно-синий раствор глицината меди:
- КСАНТОПРОТЕИНОВАЯ РЕАКЦИЯ
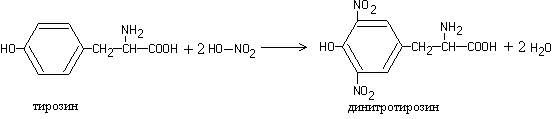
Эта реакция используется для обнаружения a -аминокислот, содержащих ароматические радикалы. Тирозин, триптофан, фенилаланин при взаимодействии с концентрированной азотной кислотой образуют нитропроизводные, имеющие желтую окраску. В щелочной среде нитропроизводные этих a -аминокислот дают соли, окрашенные в оранжевый цвет.
Описание опыта. В пробирку наливают 1 мл раствора тирозина и добавляют 0,5 мл концентрированной азотной кислоты. Смесь нагревают до появления желтой окраски. После охлаждения добавляют 1–2 мл 20%-го раствора гидроксида натрия до появления оранжевой окраски раствора:
- ОСАЖДЕНИЕ БЕЛКА СОЛЯМИ ТЯЖеЛЫХ МЕТАЛЛОВ
Описание опыта. В две пробирки наливают по 1–2 мл раствора белка и медленно, при встряхивании, добавляют по каплям в одну пробирку насыщенный раствор сульфата меди, а в другую – 20%-й раствор ацетата свинца. Образуются осадки труднорастворимых солеобразных соединений белка. Опыт иллюстрирует применение белка как противоядия при отравлении солями тяжелых металлов.
- Открытие аминного азота в белках
Описание опыта. В сухую пробирку помещают немного сухого белка, например желатины. Прибавляют пятикратное количество натронной извести (смесь едкого натра и гидроксида кальция), перемешивают встряхиванием и подогревают. Выделяется аммиак, вызывающий посинение розовой лакмусовой бумажки, смоченной водой. Одновременно ощущается запах жженого волоса, что всегда наблюдается при сжигании белковых веществ.
- Открытие серы в белках
Описание опыта. В пробирку наливают около
0,5 мл раствора уксуснокислого свинца и прибавляют раствор едкого кали до растворения образовавшегося осадка гидроксида свинца. В другую пробирку наливают
2–3 мл раствора белка и приливают такой же объем полученного раствора плюмбита. Нагревают смесь до кипения в течение 2–3 мин. Появление темного окрашивания указывает на образование сульфида свинца.
- РЕАКЦИЯ НА ПРИСУТСТВИЕ СЕРОСОДЕРЖАЩИХ a -АМИНОКИСЛОТ В БЕЛКЕ
Качественной реакцией на серосодержащие a -аминокислоты является реакция Фоля. Белки, содержащие остатки цистеина или цистина, также дают эту реакцию.
Описание опыта. В пробирку наливают 10 капель раствора яичного белка и вдвое больший объем 20%-го раствора гидроксида натрия. Содержимое пробирки нагревают до кипения (1–2 мин). К полученному щелочному раствору добавляют 5 капель раствора ацетата свинца(II) и вновь кипятят реакционную смесь. Наблюдается появление серо-черного осадка.
- РЕАКЦИЯ НА ТРИПТОФАН
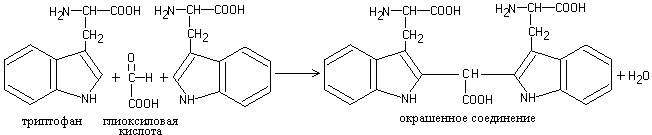
Триптофан, реагируя в кислой среде с альдегидами, образует окрашенные продукты конденсации. Например, с глиоксиловой кислотой (являющейся примесью к концентрированной уксусной кислоте) реакция протекает по уравнению:
По аналогичной схеме протекает и реакция триптофана с формальдегидом.
В ходе проведенного исследования мы выявили по литературным источникам имеющуюся информацию о цветных качественных реакциях на белковые аминокислоты; выполнили ряд перечисленных реакций и составили базу данных. Эта база может быть использована в школьной практике как в теоретическом плане, так и в практическом, т. к. мы приводим краткие, но подробные описания выполнения всех опытов.
Из предложенных 18 качественных реакций каждая практически осуществима в школьном курсе химии и имеет важное практическое значение. Сопровождение реакций химическими уравнениями конкретизирует и углубляет знания по биологической и органической химии, особенно знания учащихся специализированных биологических и химических классов.
Использованная литература
Ермаков А.Н., Арасимович В.В., Смирнова-Иконникова М.И., Мирри И.К. Методы биохимического исследования растений. М.,1952, 520 с.
Полянская А.С., Шевелева А.О. Методическая разработка по лабораторным работам: «Аминокислоты» и «Белки». Л., 1976, 37 с.
Пустовалова Л.М. Практикум по биохимии. 1999, 541 с.
Руководство к практическим занятиям по органической химии. Под ред. В.М.Родионова. М., 1954, 111 с.
Соловьев Н.А. Лабораторные работы по биологической химии. Методическая разработка. СПб., 1996, 70 с.
Филиппович Ю.Б., Егорова Т.А., Севастьянова Г.А. Практикум по общей биохимии. М., 1982, 311 с.
З.Саитов, С.В.Телешов, Б.Харитонцев,
секция «Юный химик» РХО им. Д.И.Менделеева (г. Тобольск)
РЕАКЦИЯ НА СЕРУ В БЕЛКАХ (РЕАКЦИЯ ФОЛЯ)
Реакцию Фоля дают белки, содержащие цистин и цистеин.
Если к раствору белка добавить крепкой едкой щелочи, уксуснокислого свинца и прокипятить, развивается темное окрашивание. При кипячении белка со щелочью слабосвязанная сера указанных аминокислот отщепляется и образуется сульфид натрия, который вступает во взаимодействие с уксуснокислым свинцом с образованием сульфида свинца черного цвета:
Уксуснокислый свинец реагирует со щелочью с образованием плюмбита натрия:
Сульфид натрия при взаимодействии с плюмбитом образует осадок сульфида свинца черного цвета:
Ход работы: К раствору белка 1 мл прилить 2-3 мл 10% едкого натрия и вскипятить. В горячий раствор прибавить небольшое количество уксуснокислого свинца. Раствор темнеет, образуя черный осадок сульфида свинца.
Метионин, как известно, хотя и содержит серу, но этой реакции не дает (сера прочно удерживается метальной группой).
РЕАКЦИЯ ПАУЛИ (ДИАЗОРЕАКЦИЯ)
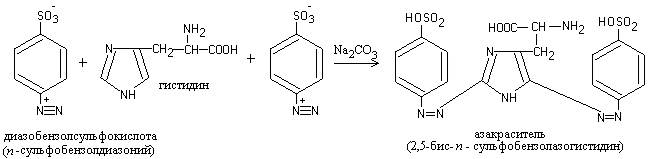
Раствор белка, содержащий в своем составе аминокислоты тирозин и гистидин, при обработке диазореактивом в щелочной среде образует окрашенное в оранжевый цвет соединение.
Реакция обусловлена тем, что названные выше аминокислоты имеют подвижные атомы в ароматической части радикала, за счет которых они и вступают в реакцию азосочетания с диазотированной сульфаниловой кислотой (диазореактивом).
Образованием азосоединения и обусловлено появление окраски. Протекающие при этом реакции можно записать следующим образом:
Ход работы: К 4-5 каплям раствора белка добавляют 4 капли раствора соды и 8-10 капель диазореактива. Образуется азосоединение оранжевого цвета.
РЕАКЦИЯ САКАГУШИ
Эта реакция обнаруживает в белке аминокислоту аргинин, которая в присутствии гипобромита (NаВrO) теряет аминогруппу, а продукт окисления конденсируется с ά-нафтолом, образуя вещество красного цвета.
Происходящие при этом реакции можно представить следующей схемой:
Ход работы: К 1 мл раствора белка добавляют 0,5 мл 10%-ного раствора едкого натра, 0,5 мл 0,1%-ного раствора ά-нафтола и содержимое пробирки перемешивают.
Добавляют 0,5 мл раствора гипобромита натрия и наблюдают появление продукта конденсации красного цвета.
НИНГИДРИНОВАЯ РЕАКЦИЯ
Реакция нингидрина с аминокислотами используется для обнаружения и количественного определения аминокислот.
Нингидрин, являющийся сильным окислителем, вызывает окислительное дезаминирование аминокислот, приводящее к образованию СО2, соответствующего альдегида и восстановленной формы нингидрина (1).
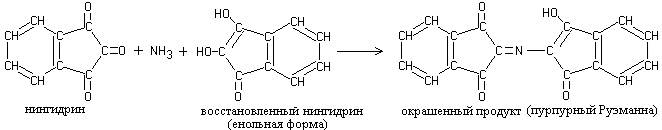
Восстановленная форма нингидрина реагирует с избытком нингидрина и NН3. При этом образуется продукт сине-фиолетового цвета (2). Протекающие реакции можно записать следующим образом:
продукт конденсации фиолетового цвета (2)
Ход работы: К 1 мл белка добавляют 2 мл водного 1% р-ра нингидрина и кипятят. Образуется осадок сине-фиолетового цвета.
Цветные реакции
КАЧЕСТВЕННЫЕ РЕАКЦИИ НА АМИНОКИСЛОТЫ И БЕЛКИ
Цель работы:изучить качественные реакции, используемые для обнаружения белков и определения их аминокислотного состава
Цветные реакции
Для обнаружения белка применяют цветные реакции, которые делят на два типа: общие или универсальные и специфические. К универсальным реакциям относятся биуретовая (на пептидную связь) и нингидрировая (на α-аминокислоты). С их помощью можно обнаружить любой белок. К специфическим относятся реакции на отдельные аминокислоты, которые позволяют обнаружить специфические функциональные группы в составе радикалов аминокислот.Цветные реакции на белки лежат в основе методов установления белковой природы веществ, изучения аминокислотного состава и количественного содержания белков.
Работа 1. Биуретовая реакция (реакция Пиотровского).
В щелочной среде белки, а также продукты их гидролиза (полипептиды) дают фиолетовое или красно-фиолетовое окрашивание с сульфатом меди. Реакция обусловлена присутствием в балках пептидных связей, которые образуют окрашенные солеобразные комплексные соединения. Интенсивность окраски зависит от количества пептидных связей в молекуле и количества медной соли.
Свое название реакция получила от производного мочевины – биурета, который дает эту реакцию. Биурет образуется при нагревания мочевины с отщеплением от нее аммиака:
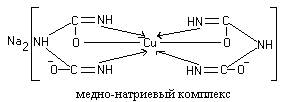
Две молекулы диенольной формы биурета взаимодействуют с образующимся в щелочной среде гидроксидом меди (II). Продуктом реакции является комплексное соединение (окрашенная медно-натриевая соль биурета), в котором координационные связи образованы за счет электронных пар атомов азота иминных групп:
Подобным образом построены окрашенные медно-натриевые соли пептидов и белков.
Биуретовую реакцию дает также аспарагин (амид аспарагиновой кислоты) и аминокислоты гистидин, серии, треонин.
Ход работы. В одну пробирку наливают 10-12 капель раствора яичного или растительного белка, в другую насыпают 20-30 мг мочевины и нагревают на спиртовке до исчезновения запаха аммиака и охлаждают. В обе пробирки добавляют по 10 капель 10-процентного раствора гидроксида натрия и по 1-2 капли 1-процентного раствора сульфата меди (II). В обеих пробирках появляется сине-фиолетовое или красно-фиолетовое окрашивание.
Работа 2. Нингидриновая реакция.
Белки, полипептиды и аминокислоты при нагревании с нингидрином дают синее и сине-фиолетовое окрашивание. Нингидриноваяреакция обусловлена наличием α-аминокислот и является одной из наиболее чувствительных для обнаружения α-аминогрупп.
Сущность реакции заключается в том, что α-аминокислоты и пептиды, реагируя с нингидрином, подвергаются окислительному дезаминированию и декарбоксилированию:
Восстановленный нингидрин взаимодействует с аммиаком и второй молекулой нингидрина, в результате чего образуется сложное окрашенное соединение мурексидного строения:
Ход работы. В две пробирки наливают: в одну 10 капель раствора яичного или растительного белка, в другую 10 капель 0,1-процентного раствора глицина. В каждую из них добавляют по 2-3 капли 0,1-процентного раствора нингидрина и нагревают. Через 1-2 мин появляется розовое, затем красное, а затем синее окрашивание.
Работа 3. Ксантопротеиновая реакция (реакция Мульдера)
При нагревании растворов большинства белков с концентрированной азотной кислотой образуется желтое окрашивание, переходящее в щелочном растворе в оранжевое.
Реакция обусловлена присутствием циклических аминокислот, которые при взаимодействии с азотной кислотой образуют нитропроизводные желтого цвета, например:
Продукты нитрования циклических аминокислот, реагируя с едким натром или гидроксидом аммония, образуют соответствующие соли, имеющие оранжевую окраску:
Ход работы. В пробирку наливают 8-10 капель яичного или растительного белка, добавляют З-5 капель концентрированной азотной кислоты и нагревают. В пробирке появляется желтое окрашивание. После охлаждения к смеси добавляют избыток концентрированного раствора аммиака или 30-процентного раствора гидроксида натрия. Желтая окраска переходит в оранжевую.
Работа 4. Реакция на тирозин (реакция Миллона)
Нагревание большинства белков с реактивом Миллона (раствор нитратов и нитритов ртути (I) и (II) в азотной кислоте) приводит к образованию красного осадка.
Реакция обусловлена присутствием в белке аминокислоты тирозина, которая при взаимодействии с реактивом Миллона дает нитрозопроизводное, ртутное соединение которого окрашено в красный цвет:
Ход работы.К 8-10 каплям раствора белка добавляют 2-3 капли реактиваМиллона и осторожно нагревают. Жидкость окрашивается в красный цвет и выпадает красно-коричневый осадок.
Работа 5. Диазореакция на гистидин и тирозин (реакция Паули)
При добавлении к щелочному раствору белка диазореактива жидкость приобретает оранжево-красное окрашивание.
Реакция обусловлена присутствием в белке аминокислот гистидина и тирозина, которые, реагируя с диазобензолсульфокислотой,образуют азокраситель красного цвета:
Ход работы.К свежеприготовленномудиазореактиву (3 капли 1-процентного раствора сульфаниловой кислоты в 2-процентном растворе соляной кислоты и 3 капли 5-процентного раствора нитрита натрия) добавляют 6-8 капель раствора белка и после перемешивания 3-5 капель 10-процентного раствора карбоната натрия. Развивается интенсивная красная окраска.
Работа 6. Реакции на триптофан
Реакции основаны на способности триптофана в кислой среде вступать во взаимодействие с альдегидами, образуя при этом окрашенные продукты конденсации.
а) Реакция Адамкевича. Взаимодействие триптофана с глиоксиловой кислотой (которая всегда присутствует в ледяной уксусной кислоте) приводит к образованию соединения красно-фиолетового цвета:
Ход работы. К 5-6 каплям раствора белка добавить 5 капель концентрированной уксусной кислоты, слегка подогреть и подслоить (осторожно. по стенке наклоненной пробирки) равный объем концентрированной серной кислота. На границе двух слоев жидкости появляется красно-фиолетовое кольцо.
б) Реакция Шульца-Распайля. Триптофан, взаимодействуя с оксиметилфурфуролом (образующимся при гидролизе сахарозы и обезвоживании моносахаридов под действием концентрированной серной кислоты) образует комплекс вишнево-красного цвета.
Ход работы.К 5-6 каплям раствора белка приливают 1 каплю 10- процентного раствора сахарозы и подслаивают 1 мл концентрированной серной кислоты. На границе раздела жидкостей появляется вишнево-красное окрашивание.
Работа 7. Реакция Фоля на содержащие серу аминокислоты
Нагревание белка со щелочью и плюмбитом приводит к появлению бурого или черного осадка. Реакция обусловлена наличием в белке содержащих серу аминокислот, которые под действием щелочи разрушаются с образованием сульфида щелочного металла; последний с плюмбитом дает осадок сульфида свинца:
Ход работы.К 5-6 каплям раствора белка добавляют 10 капель 30-процентного раствора гидроксида натрия и 1каплю 5-процентного раствора ацетата свинца. При длительном нагревании выпадает черный осадок сульфида свинца.