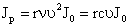Рассеяние света — одно из общих свойств высоко- и среднедисперсных систем и растворов ВМС, размеры частиц которых соизмеримы с длиной волны видимого света, — заключается в изменении характеристик светового потока, в частности — его направления. Проявлением рассеяния света являются опалесценция и эффект Тиндаля.
При боковом освещении системы наблюдается характерное переливчатое, как правило, голубоватое или желтоватое свечение, особенно хорошо видное на темном фоне (рис. 3.2). Это свойство, связанное с рассеянием света частицами дисперсной фазы, называют опалесценцией (от лат. opalus — названия опала, полупрозрачного минерала голубоватоили желтовато-белого цвета). Опалесценция характерна для дисперсных систем, состоящих из бесцветных или слабо окрашенных фаз.
Рис. 3.2. Опалесценция
Эффект Тиндаля описан английским физиком Дж. Тиндалем в 1868 г. и заключается в том, что при освещении коллоидного раствора сбоку пучком света от сильного источника наблюдается яркий равномерно светящийся след (рис. 3.3, а)> тогда как в случае растворов низкомолекулярных веществ жидкость кажется оптически пустой, т.е. след луча невидим (рис. 3.3, б).
Рис. 3.3. При боковом освещении коллоидного раствора наблюдается светящийся след луча — эффект Тиндаля («), при освещении низкомолекулярного раствора жидкость кажется оптически пустой (б)
? ?На практике с проявлением эффекта Тиндаля в золях вы познакомитесь при выполнении лабораторной работы 1 «Получение и свойства дисперсных систем» (см. параграф Л.1).
При большой толщине освещаемой системы заметно, что световой след расходится (рис. 3.4), поэтому эффект также называют конус Тиндаля.
Рис. 3.4. Конус Тиндаля
Подобный эффект можно наблюдать в аэрозолях: солнечные лучи, расходящиеся конусом от облаков, от крон деревьев или от окна в затемненном помещении (рис. 3.5); наблюдение возможно только в том случае, если воздушная среда содержит частицы дыма, пыли, мельчайшие капли тумана. Грубодисперсные частицы выделяются в луче в виде отдельных блесток, находящихся в хаотическом движении.
Рис. 3.5. Проявление эффекта Тиндаля в воздушной среде
Эффект Тиндаля проявляется только в том случае, если освещаемая система содержит частицы, размеры которых соизмеримы с длиной световой волны. Э го свойство используют для обнаружения дисперсной фазы.
Опалесценция — голубоватое свечение при освещении системы боковым светом. Эффект Тиндаля — видимый равномерно светящийся след луча при боковом освещении. Опалесценция и эффект Тиндаля — проявление рассеяния света в дисперсных системах и растворах ВМС.
- Рассеяние света коллоидными системами. Конус Тиндаля. Закон Релея и его анализ
- Оптические свойства коллоидных растворов.
- Оптические свойства коллоидных систем
- Теория светорассеяния Рэлея
- Анализ закона Рэлея
- Нефелометрия
- Ультрамикроскопия
- Поточный ультрамикроскоп (Дерягин и Власенко)
- Электронная микроскопия
- Окраска коллоидных систем
Рассеяние света коллоидными системами. Конус Тиндаля. Закон Релея и его анализ
3. Рассеяние света коллоидными системами. Конус Тиндаля. Закон Релея и его анализ
Тиндаль (1869г.) наблюдал образование светящегося конуса при пропускании пучка света через коллоидный раствор.
Светорассеивание наблюдается только тогда, когда длина световой волны больше размера частицы дисперсной фазы. Если длина световой волны много меньше диаметра частицы, происходит отражение света, проявляющиеся в мутности, заметной визуально.
Все коллоидные растворы способны рассеивать свет (опалесцировать). Опалесценция становится особенно заметной, если через раствор пропускать пучок сходящихся лучей, поставив между источником света и кюветой с раствором линзу. При этих условиях в коллоидном растворе, наблюдаемом сбоку, виден ярко светящийся конус (конус Тиндаля).
Релей вывел уравнение, связывающее интенсивность падающего света 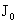
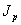
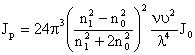
где 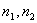
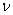
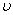
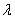
Уравнение Релея применимо для частиц, размер которых составляет не более 0,1 длины световой волны. Для частиц большего размера 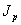
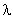
Когда частицы становятся настолько велики, что их размер значительно превышает 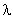
Из уравнения Релея можно сделать следующие выводы:
· Для частиц данного размера интенсивность рассеянного света прямо пропорциональна концентрации золя.
· Интенсивность рассеянного света пропорциональна квадрату объема частицы или для сферических частиц шестой степени их радиуса.
· При опалесценции под действием белого света при боковом освещении бесцветные коллоидные системы обнаруживают синеватую окраску.
· Опалесценция золей интенсивнее, чем растворов ВМС из-за большей плотности.
· Опалесценция истинных растворов весьма незначительна, т.к. вследствие малого объема частиц выражение 
4. Оптические методы исследования: нефелометрия, ультрамикроскопия, турбидиметрия, электронная микроскопия
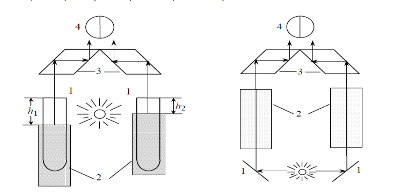
В нефелометрии измеряется интенсивность света, рассеянного дисперсной системой. Вместо измерения абсолютных значений рассеянного света на практике проводят сравнение интенсивностей лучей, рассеянных стандартным и исследуемым золем. На рис. 2,а приведена схема визуального нефелометра Кляйнмана (нефелометры иногда называют тиндалеметрами). При измерении подниманием или опусканием экранов изменяют высоту осветленной части пробирок с золями, добиваясь одинаковой осветленности в обеих половинах окуляра. При подчинении исследуемой монодисперсной системы уравнению Рэлея для интенсивности рассеянного света можно записать
Рис.2 Схема нефелометра -а Схема турбидиметра — б
а — 1 – зеркала, 2 – кюветы, 3 – призмы, 4 – окуляр.
б — 1 – пробирки с золями, 2 — экраны, 3 –призмы, 4 – окуляр
В турбидиметрии измеряют интенсивность света, прошедшего через стандартную и исследуемую дисперсную систему. Схема визуального турбидиметра приведена на рис. 2,б. Оптическая плотность раствора пропорциональна концентрации и объему частиц дисперсной фазы
При одинаковой осветленности поля зрения в окуляре имеем равенство cстандVстанд = cхVх, применение, которого аналогично рассмотренному для нефелометрии.
Ультрамикроскопия и электронная микроскопия.
Коллоидные частицы нельзя наблюдать в обычном микроскопе, так как их размеры меньше разрешающей способности микроскопа. Для средней части видимой области спектра можно достигнуть разрешающей способности не выше, чем 0,2 мкм. Ультрафиолетовый свет, специальная кварцевая оптика и фотографическая регистрация позволяют увеличить разрешающую способность и довести ее до 0,1 мкм, что является верхней границей коллоидной дисперсности. Р. Зидентопф и Р. Зигмонди в 1903 г. предложили так называемый ультрамикроскопический метод исследования коллоидных систем. Они применили сильное боковое освещение наблюдаемого под микроскопом раствора таким образом, чтобы свет не попадал в объектив микроскопа. При этом коллоидные частицы были видны как отдельные светлые точки, что позволяет установить их присутствие в растворе и наблюдать за их движением.
При ультрамикроскопическом наблюдении можно судить о том, в какой степени коллоидные частицы сферически симметричны. Свет, рассеиваемый сферическими частицами, имеет постоянную интенсивность при их движении в растворе. Если частицы не сферичны, а имеют, например, палочкообразную или пластинчатую форму, то при движении они мерцают.
В электронной микроскопии используется поток быстрых электронов с длиной волны до 10-9 м, что дает очень высокое разрешение, соответствующее увеличению до 105. Метод дает сведения о размерах и форме частиц, макромолекул и надмолекулярных образований. Электронная микроскопия существенно дополняет ультрамикроскопию. Электронный микроскоп позволяет увидеть мельчайшие частички и многие особенности их строения, но необходимость работы в высоком вакууме требует удаления жидкой дисперсионной среды.
III. Раздел «Структурно – механические свойства дисперсных систем»
1. Структурирование в коллоидных и полимерных системах. Гели и студни. Их свойства, механизм образования и практическое значение. Тиксотропия и синтерезис
Согласно А.И. Рабинерсону и Г.И. Фуксу, структуры, образующиеся в высокодисперсных системах, можно классифицировать по их плотности:
Оптические свойства коллоидных растворов.
По оптическим свойствам коллоидные растворы существенно» отличаются от истинных растворов низкомолекулярных веществ, а также от грубодисперсных систем. Наиболее характерными оптическими свойствами коллоидно-дисперсных систем являются опалесценция, эффект Фарадея — Тиндаля и окраска. Все эти явления обусловлены рассеянием и поглощением света коллоидными частицами.
В зависимости от длины волны видимого света и относительных размеров частиц дисперсной фазы рассеяние света принимает различный характер. Если размер частиц превышает длину световых волн, то свет от них отражается по законам геометрической оптики. При этом часть светового излучения может проникать внутрь частиц, испытывать преломление, внутреннее отражение и поглощаться.
Если размер частиц меньше длины полуволны падающего света, наблюдается дифракционное рассеяние света; свет как бы обходит (огибает) встречающиеся на пути частицы. При этом имеет место частичное рассеяние в виде волн, расходящихся во все стороны. В результате рассеяния света каждая частица является источником новых, менее интенсивных волн, т. е. происходит как бы самосвечение каждой частицы. Явление рассеяния света мельчайшими частицами получило название опалесценции. Оно свойственно преимущественно золям (жидким и твердым), наблюдается только в отраженном свете, т. е. сбоку или на темном фоне. Выражается это явление в появлении некоторой мутноватости золя и в смене («переливах») его окраски по сравнению с окраской в проходящем свете. Окраска в отраженном свете, как правило, сдвинута в сторону большей частоты видимой части спектра. Так, белые золи (золь хлорида серебра, канифоли и др.) опалесцируют голубоватым цветом.
Эффект Фарадея — Тиндаля. Дифракционное рассеяние света впервые было замечено М. В. Ломоносовым. Позднее, в 1857 г., это явление наблюдал Фарадей в золях золота. Наиболее детально явление дифракции (опалесценции) для жидких и газовых сред было изучено Тиндалем (1868).
Если взять один стакан с раствором хлорида натрия, а другой — с гидрозолем яичного белка, трудно установить, где коллоидный раствор, а где истинный, так как на вид обе жидкости бесцветны и прозрачны (рис. 6.5). Однако эти растворы можно легко различить, проделав следующий опыт. Наденем на источник света (настольную лампу) светонепроницаемый футляр с отверстием, перед которым в целях получения более узкого и яркого пучка света поставим линзу. Если на пути луча света поставить оба стакана, в стакане с золем увидим световую дорожку (конус), в то время как в стакане с хлоридом натрия луч почти не заметен. По имени ученых, впервые наблюдавших это явление, светящийся конус в жидкости был назван конусом (или эффектом) Фарадея — Тиндаля. Этот эффект является характерным для всех коллоидных растворов.
Появление конуса Фарадея — Тиндаля объясняется явлением рассеяния света коллоидными частицами размером 0,1—0,001 мкм.
Длина волн видимой части спектра 0,76—0,38 мкм, поэтому каждая коллоидная частица рассеивает падающий на нее свет. Он виден в конусе Фарадея — Тиндаля, когда луч зрения направлен под углом к проходящему через золь лучу.Таким образом, эффект Фарадея — Тиндаля —явление, идентичное опалесценции, и отличается от последней только видом коллоидного состояния, т. е. микрогетерогенности системы.
Теория рассеяния света коллоидно-дисперсными системами была разработана Рэлеем в 1871 г. Она устанавливает зависимость интенсивности (количества энергии) рассеянного света (I) при опалесценции и в конусе Фарадея — Тиндаля от внешних и внутренних факторов. Математически эта зависимость выражается в виде формулы, получившей название формулы Рэлея:
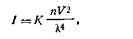 | 6.1 |
где I — интенсивность рассеянного света в направлении, перпендикулярном к лучу падающего света; К — константа, зависящая от показателей преломления дисперсионной среды и дисперсной фазы; n — число частиц в единице объема золя; λ — длина волны падающего света; V — объем каждой частицы.
Из формулы (6.1) следует, что рассеяние света (I) пропорционально концентрации частиц, квадрату объема частицы (или для сферических частиц — шестой степени их радиуса) и обратно пропорционально четвертой степени длины волны падающего света. Таким образом, рассеяние коротких волн происходит относительно более интенсивно. Поэтому бесцветные золи в проходящем свете кажутся красноватыми, в рассеянном — голубыми.
Окраска коллоидных растворов.В результате избирательною поглощения света (абсорбции) в сочетании с дифракцией образуется та или иная окраска коллоидного раствора. Опыт показывает, что большинство коллоидных (особенно металлических) растворов ярко окрашено в самые разнообразные цвета, начиная от белого и кончая совершенно черным, со всеми оттенками цветового спектра. Так, золи As2S3 имеют ярко-желтый, Sb2S3 — оранжевый, Fe(OH)3 — красновато-коричневый, золота — ярко-красный цвет и т. п.
Один и тот же золь имеет различную окраску в зависимости от того, в проходящем или отраженном свете она рассматривается. Золи одного и того же вещества в зависимости от способа приготовления могут приобретать различную окраску— явление полихромии (многоцветности). Окраска золей в данном случае зависит от степени дисперсности частиц. Так, грубодисперсные золи золота имеют синюю окраску, большей степени дисперсности — фиолетовую, а высокодисперсные — ярко – красную. Интересно отметить, что цвет металла в недисперсном состоянии не имеет ничего общего с его цветом в коллоидном состоянии.
Необходимо отметить, что интенсивность окраски золей в десятки (а то и в сотни) раз больше, чем молекулярных растворов. Так, желтая окраска золя As2S3 в слое толщиной в 1 см хорошо заметна при массовой концентрации 10 -3 г/л, а красный цвет золя золота заметен даже при концентрации 10 -5 г/л.
Красивая и яркая окраска многих драгоценных и полудрагоценных камней (рубинов, изумрудов, топазов, сапфиров) обусловлена содержанием в них ничтожных (не определимых даже на лучших аналитических весах) количеств примесей тяжелых металлов и их оксидов, находящихся в коллоидном состоянии. Так, для искусственного получения яркого рубинового стекла, употребляемого для автомобильных, велосипедных и прочих фонарей, достаточно на 1000 кг стеклянной массы добавить всего лишь 0,1 кг коллоидного золота.
Ультрамикроскоп. На явлении светорассеяния в конусе Фарадея — Тиндаля основан один из важнейших методов исследования высокодисперсных систем — с помощью ультрамикроскопа.
В отличие от обычного микроскопа в ультрамикроскопе применено боковое освещение. При этом свет от осветителя не попадает в объектив микроскопа и в глаз наблюдателя, поэтому фон поля зрения микроскопа темный.
Этим методом можно вычислить размер коллоидной частицы по формуле
Пусть d — плотность частиц, С — массовая концентрация коллоидного раствора, V — выделенный оптический объем; ν — число частиц в объеме V;
Принимая форму частицы за куб или сферу, можно вычислить размер коллоидной частицы по формуле (6.2):
 | 6.2 |
где D — диаметр сферической частицы
d — плотность частиц, С — массовая концентрация коллоидного раствора, V — выделенный оптический объем; ν — число частиц в объеме V;
Оптические свойства коллоидных систем
Оптические свойства коллоидных систем определяются их гетерогенностью и дисперсностью. Изучение оптических свойств позволяет решить множество задач, например, можно определить наличие коллоидных частиц, их размер, форму, концентрацию.
5 видов взаимодействия световой волны с веществом:
- Поглощение;
- Преломление;
- Рассеяние;
- Отражение;
- Пропускание
Но в зависимости от длины волны и размеров частиц преобладают определенные виды:
Если в системе нет никаких частиц с другим показателем преломления, то система будет считаться оптически пустой и рассеяния не будет. Если есть, то электрическое поле волны будет возбуждать электроны и начнется испускание света, при этом длина волны падающего света будет совпадать с рассеянным. В дисперсных системах источниками рассеяния света являются частицы дисперсной фазы.
Эффект Тиндаля — оптический эффект, рассеивание света при прохождении светового пучка через оптически неоднородную среду. Обычно наблюдается в виде светящегося конуса (конус Тиндаля), видимого на тёмном фоне.
Теория светорассеяния Рэлея
Настоящее имя Рэлея Джон Уильям Стретт, Лорд Рэлей. Рэлей открыл открыл аргон.
В общем случае уравнение Рэлея упрощается к виду
Анализ закона Рэлея
Интенсивность рассеянного света:
Сильнее всего зависит от длины волны.
Красный свет рассеивается меньше всего, поэтому все сигнальные огни — красные, все маскировочные — синие.
Зависит от разницы в показателях преломления дисперсной фазы и дисперсионной среды.
Чем больше разница — тем сильнее рассеяние.
Зависит от размера частиц дисперсной фазы.
Нефелометрия
Нефелометрия — метод изучения рассеянного света дисперсной системы под определенным углом.
Упрощенное уравнение Рэлея
Обычно проводят два опыта для сравнения экспериментального значения со стандартным.
Ультрамикроскопия
Ультрамикроскопия — оптический метод изучения, который основан на регистрации рассеяния от каждой частицы дисперсной фазы. Ультрамикроскоп позволяет наблюдать частицы коллоидных размеров. 1903г. Зигмонди Рихард сконструировал ультрамикроскоп (1925г. — Нобелевская премия).
Схема работы светового микроскопа: прямой ход лучей
Схема работы ультрамикроскопа:
В ультрамикроскопе наблюдается свет рассеянный каждой коллоидной частицей — на черном фоне светящиеся точки.
С помощью ультрамикроскопа можно определить:
- наличие коллоидных частиц;
- форму частиц. Ровный световой ареол — сферическая форма, мерцание — сложная поверхность;
- можем посчитать число частиц ⇒ Rightarrow ⇒ концентрацию частиц;
- размер частиц.
Масса дисперсной фазы вычисляется уравнением
Поточный ультрамикроскоп (Дерягин и Власенко)
Поток золя протекает через кювету, на которую направлен свет. Происходят вспышки каждой коллоидной частицы в ультрамикроскопе, которые автоматически регистрируются. Используется для определения дисперсности системы.
Электронная микроскопия
Разрешающая способность микроскопа — величина, обратная минимальному расстоянию между 2 точками, которые можно видеть независимо друг от друга.
Для увеличения разрешающей способности используют иммерсионный метод.
Иммерсионный метод микроскопического наблюдения заключается во введении жидкости между объективом микроскопа и рассматриваемым предметом для усиления яркости и расширения пределов увеличения изображения.
Окраска коллоидных систем
Система окрашивается в свет — дополнительный к поглощенному.
| Поглощенный свет | Окрашенный |
|---|---|
| Желтый | Синий |
| Красный | зеленый |
Похоже на поглощение света в истинных растворах: уравнение Бугера-Ламберта-Бэра:
Поглощение света зависит от размера частиц (или от ее дисперсности) — чем меньше размер частицы, тем более короткие длины волн могут быть поглощены. Золь A u Au A u :
| Размер частиц, см | Поглощенный свет | Окрашено |
|---|---|---|
| 5 ⋅ 1 0 − 6 5cdot10^ 5 ⋅ 1 0 − 6 | Желтый | Синий |
| 2 ⋅ 1 0 − 6 2cdot10^ 2 ⋅ 1 0 − 6 | Зеленый | Красный |
| 1 0 − 6 1 0 − 6 | Синий | Желтый |
Цвет системы зависит от размера частиц. Кроме того интенсивность поглощенного света тоже зависит от размера частиц (дисперсности системы).
Флюоресценция — поглощение определенной длины волны и преобразование в волны большей длины.
Опалесценция — различие окраски систем в зависимости от угла наблюдения. Рассеиваются волны разной длины.