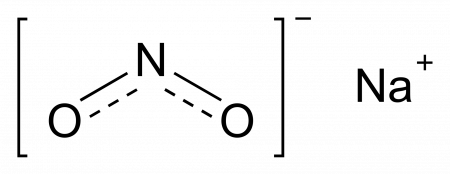
Нитрат натрия NaNO3 — соль щелочного металла натрия и азотной кислоты. Белое вещество, весьма гигроскопичное, которое плавится без разложения, при дальнейшем нагревании разлагается.
Относительная молекулярная масса Mr = 84,99; относительная плотность для тв. и ж. состояния d = 2,266; tпл = 306,5º C;
- Способ получения
- Качественная реакция
- Химические свойства
- Нитрит натрия
- Содержание
- Основные свойства
- Получение
- Области применения
- В химическом синтезе
- Производство пищевых продуктов
- Строительство и производство
- Фотография
- Медицина и биология
- Особенности обращения, биологическое действие
- Рынок
- Реакция термического разложения нитрита натрия
- Реакция термического разложения нитрита натрия
- Реакция взаимодействия сульфата лития и серной кислоты
- Реакция взаимодействия брома и водорода
- Реакция взаимодействия сульфата цинка (II) и гидроксида натрия
- Выбрать язык
- Разделы
- ТОП 5 записей
- Популярные записи
- Элементы, реакции, вещества
- Предупреждение.
Способ получения
1. Нитрат натрия можно получить путем взаимодействия гидроксида натрия и разбавленной азотной кислоты, образуется нитрат натрия и вода:
2. В результате взаимодействия горячего гидроксида натрия, оксида азота (IV) и кислорода образуется нитрат натрия и вода:
3. В результате реакции между горячим гидроксидом натрия, оксидом натрия (IV) и кислородом, происходит образование нитрата натрия и воды:
4. При комнатной температуре, в результате взаимодействия оксида азота (IV) и натрия образуется нитрат натрия и газ оксид азота (II):
2NO2 + Na = NO↑ + NaNO3
5. При смешивании горячего пероксида водорода и нитрита азота происходит образование нитрата натрия и воды:
Качественная реакция
Качественная реакция на нитрат натрия — взаимодействие с медью при нагревании в присутствии концентрированной кислоты:
1. При взаимодействии с серной кислотой и медью, нитрат натрия образует сульфат натрия, нитрат меди, газ оксид азота и воду:
Химические свойства
1. Hитрат натрия разлагается при температуре 380–500º С с образованием нитрита натрия и кислорода:
2. Н итрат натрия может реагировать с простыми веществами :
2.1. Н итрат натрия реагирует со свинцом при температуре выше 350 ºС . При этом образуется нитрит натрия и оксид свинца:
NaNO3 + Pb = NaNO2 + PbO
2.2. Нитрат натрия реагирует при комнатной температуре с цинком и разбавленной хлороводородной кислотой с образованием нитрита натрия и воды:
Нитрит натрия


Нитрит натрия (натрий азотистокислый) NaNO2 — соль натрия и азотистой кислоты.
Содержание
- 1 Основные свойства
- 1.1 Получение
- 1.2 Области применения
- 1.2.1 В химическом синтезе
- 1.2.2 Производство пищевых продуктов
- 1.2.3 Строительство и производство
- 1.2.4 Фотография
- 1.2.5 Медицина и биология
- 2 Особенности обращения, биологическое действие
- 3 Рынок
Основные свойства
Очищенный нитрит натрия представляет собой белый или слегка желтоватый кристаллический порошок. Хорошо растворим в воде и гигроскопичен. На воздухе медленно доокисляется до нитрата натрия NaNO3. Является сильным восстановителем. Токсичен в больших дозах.
Получение
Нитрит натрия NaNO2 является солью азотистой кислоты и получается обычно из оксидов азота по реакции:
Другим распространённым методом получения нитрита натрия является нагревание порошка свинца Pb с нитратом натрия NaNO3, с последующим растворением в воде полученной твёрдой субстанции. В результате растворения в осадок выпадет нерастворимый в воде оксид свинца II PbO, а нитрит натрия останется в растворе:
NaNO3 + Pb → NaNO2 + PbO
Области применения
В химическом синтезе
- Нитрит натрия применяется для образования диазоаминных соединений. Эти соединения применяются в синтезе как источник аминогрупп при реакциях с «ядром» соединения, за счёт относительно более лёгкого отделения азотных групп N2.
- В лабораторных условиях нитрит натрия используется для деактивации азида натрия реакцией со свежеполученной азотистой кислотой
2NaNO2 + H2SO4 → Na2SO4 + 2HNO2 2NaN3 + 2HNO2 → 3N2 + 2NO + 2 NaOH
- Нитрит натрия в химических реакциях проявляет окислительно-восстановительную двойственность, восстанавливаясь до оксида азота II или окисляясь до нитрата.
Например, он при дальнейшем нагревании разлагается, образуя оксид натрия, оксид азота II и кислород. Вероятно, этот процесс помог не задохнуться экипажу первой действующей субмарины Корнелия Дреббеля, поскольку оксид натрия поглощает CO2.
Производство пищевых продуктов
- Используется как улучшитель окраски и консервант в пищевой промышленности в изделиях из мяса и рыбы. Пищевая добавка E250.
- Как пищевая добавка применяется в пищевой промышленности в двух целях: как антиокислитель и как антибактериальный агент, препятствующий росту Clostridium botulinum — возбудителя ботулизма, — тяжёлой пищевой интоксикации, вызываемой ботулиническим токсином и характеризуемой поражением нервной системы (действие не доказано).
- Вступая во взаимодействие с миоглобином (белком мяса), придаёт мясным продуктам характерный розоватый цвет.
- В Евросоюзе продажа для пищевых применений разрешена только в смеси с пищевой солью, с содержанием нитрита около 0,6 %, чтобы уменьшить риск превышения суточных норм. C 2013 года сходные правила действуют в России.
- Пищевая добавка E250. Аналогичными свойствами обладает и нитрит калия — пищевая добавка E249.
- Соответствует ГОСТу 4197-74 или ТУ 6-09-590-75 (марка ОСЧ 4-7-3).
Строительство и производство
- Нитрит натрия в виде порошка по ГОСТ 19906-74 или водного раствора используется в качестве противоморозной добавки к бетонам в производстве строительных изделий и конструкций, в качестве ингибитора атмосферной коррозии, в органическом синтезе и для других целей в химической, металлургической, медицинской, целлюлозно-бумажной и других отраслях промышленности.
- В строительстве нитрит натрия рекомендован ГОСТ 24211 «Добавки для бетонов. Общие технические требования» к использованию в качестве противоморозной добавки при возведении монолитных бетонных и железобетонных конструкций, монолитных частей сборно-монолитных конструкций, замоноличивания стыков сборных конструкций при установившейся устойчивой среднесуточной температуре окружающего воздуха или грунта ниже 5 °C и минимальной суточной температуре ниже 0 °C, а также при изготовлении сборных бетонных и железобетонных конструкций в зимнее время в условиях строительной площадки.
- Он также используется при производстве диазо-красителей, нитросоединений и других органических соединений.
- Используется в крашении трафаретным и прямым (прямой печати) методом текстиля из натуральных и отбеленных натуральных волокон.
- Используется при обработке поверхности металла при фосфатировании и для снятия слоя олова.
- Используется в производстве каучуков.
- Используется для изготовления алкилнитритов (попперсов).
- Используется для приготовления раствора газогенерирующей добавки в производстве взрывчатых веществ.
Фотография
- Используется в процессе традиционной фотографии как реагент и антиокислитель (ингибитор коррозии в автоматических лабораториях).
Медицина и биология
- Нитрит натрия также используется в медицине и ветеринарии как сосудорасширяющее, бронхолитическое (расширяет бронхи), снимает спазмы кишечника, используется как слабительное, а также как антидот при отравлении цианидами.
- Проводятся исследования по применению его при серповидной анемии, сердечных приступах и ишемии сердца, аневризмах головного мозга и лёгочной гипертензии у детей.
E250 при приёме в значительном объёме (порядка нескольких граммов) может вызвать серьёзное отравление (образует метгемоглобин), вплоть до летального исхода.
Особенности обращения, биологическое действие
Поступление нитритов с пищей оценивается в 31-185 или 40-100 мг в день.
В питьевой воде, согласно требованиям ВОЗ 1970 и 2004 гг, допускается содержание нитритов не более 44-50 мг на литр.
Приемлемые уровни потребления нитритов для людей 3,7 — 7 мг / кг.
Рынок
До введения эмбарго на соль из санкционных стран 13 сентября 2016 года (вступило в силу 1 ноября 2016), нитрит натрия для пищевого производства импортировался в Россию в основном из стран Евросоюза: Дании и Германии, собственное производство в России отсутствовало. В декабре 2016 года в Ломоносовском районе Ленинградской области в России начало работу производство нитритной соли для нужд мясоперерабатывающей промышленности.
Реакция термического разложения нитрита натрия
Реакция термического разложения нитрита натрия
Уравнение реакции термического разложения нитрита натрия:
Реакция термического разложения нитрита натрия.
В результате реакции образуются оксид натрия (III), азот и кислород.
Реакция протекает при условии: при температуре 700-900 °C.
Формула поиска по сайту: 4NaNO2 → 2Na2O + 2N2 + 3O2.
Реакция взаимодействия сульфата лития и серной кислоты
Реакция взаимодействия брома и водорода
Реакция взаимодействия сульфата цинка (II) и гидроксида натрия
Выбрать язык
Разделы
ТОП 5 записей
Популярные записи
Элементы, реакции, вещества
Предупреждение.
Все химические реакции и вся информация на сайте предназначены для использования исключительно в учебных целях — только для решения письменных, учебных задач. Мы не несем ответственность за проведение вами химических реакций.
Химические реакции и информация на сайте
не предназначены для проведения химических и лабораторных опытов и работ.