Из приборов, изображённых на рисунках, выберите тот, с помощью которого можно отделить карбонат кальция от раствора нитрата калия. Какой метод разделения веществ при этом используется? Почему прибор, изображённый на другом рисунке, не может быть использован для отделения карбоната кальция?
Ниже даны описания двух химических превращений с участием веществ, перечень которых был приведён в задании 6:
(1) водород + кислород → вода;
(2) нитрат кальция + карбонат калия → карбонат кальция + нитрат калия.
Составьте уравнения указанных реакций, используя химические формулы веществ из п. 6.1.
1.
2.
В зависимости от числа и состава веществ, вступающих в химическую реакцию и образующихся в результате неё, различают реакции соединения, разложения, замещения и обмена. Выберите ЛЮБУЮ реакцию (1) или (2) и укажите её тип.
1. Реакция (1) — реакция соединения (из двух веществ получается одно вещество).
2. Реакция (2) — реакция обмена (два сложных вещества (нитрат кальция и карбонат калия) обмениваются своими составными частями (ионами), в результате чего образуются два других сложных вещества — карбонат кальция и нитрат калия).
Отделить карбонат кальция от раствора нитрата калия можно с помощью фильтрования (рисунок 2). Делительная воронка используется для разделения двух несмешивающихся жидкостей, а карбонат кальция представляет собой твёрдое вещество.
- Вопросы к параграфу 50 — ГДЗ по Химии 9 класс Учебник Рудзитис, Фельдман
- § 50. Практическая работа №7.
- Решение экспериментальных задач по теме: “Металлы”
- Вариант 1. Распознавание хлорида магния MgCl2, гидроксида натрия NaOH, карбоната натрия Na2CO3, нитрата натрия NaNO3 1. В четырёх пробирках даны следующие вещества в твёрдом виде: а) хлорид магния; 6) гидроксид натрия; в) карбонат натрия; г) нитрат натрия. При помощи химических реакций определите, в какой пробирке находится каждое из этих веществ.
- 2. При помощи характерных реакций докажите, что выданное вам вещество — сульфат алюминия.
- 3. В одной пробирке дан раствор хлорида натрия, во второй — раствор хлорида стронция, а в третьей — раствор хлорида алюминия. Определите, в какой пробирке находится каждое из выданных веществ.
- 4. Практически осуществите следующие превращения:
- Fe→FeCl2→Fe(OH)2→Fe(OH)3→Fe(NO3)3
- Вариант 2. Распознавание карбоната кальция CaCO3, нитрата стронция Sr(NO3)2, сульфата натрия NaSO4, сульфида натрия Na2S. 1. В четырех пробирках даны следующие твёрдые вещества: а) карбонат кальция; б) нитрат стронция; в) сульфат натрия; г) сульфид натрия. Определите, в какой пробирке находится каждое из перечисленных веществ.
- 2. Докажите, что кристаллы сульфата железа (III) частично окислились и содержат примеси ионов Fe3+.
- 3. В двух склянках дана вода. В одной из них вода содержит сульфат магния, а в другой — гидрокарбонат кальция. Проделайте опыты, при помощи которых можно устранить постоянную и временную жёсткость воды.
- 4. Практически осуществите следующие превращения:
- Аl→Al2(SO4)3→Аl(ОН)3→Na[Al(OH)4]
- 5. Отчёт о работе оформите в произвольной форме.
- Досрочный вариант ЕГЭ по химии-2022 Вариант 2
Вопросы к параграфу 50 — ГДЗ по Химии 9 класс Учебник Рудзитис, Фельдман
Авторы: Рудзитис Г.Е., Фельдман Ф.Г.
§ 50. Практическая работа №7.
Решение экспериментальных задач по теме: “Металлы”
Вариант 1. Распознавание хлорида магния MgCl2, гидроксида натрия NaOH, карбоната натрия Na2CO3, нитрата натрия NaNO3 1. В четырёх пробирках даны следующие вещества в твёрдом виде: а) хлорид магния; 6) гидроксид натрия; в) карбонат натрия; г) нитрат натрия. При помощи химических реакций определите, в какой пробирке находится каждое из этих веществ.
Твёрдые вещества растворили в воде, далее прилили соляную кислоту.
В одной пробирке выделяется газ без цвета и запаха:
В пробирке — карбонат натрия.
К другим растворам добавили несколько капель фенолфталеина.
Содержимое одной из пробирок окрасилось с малиновый цвет.
В пробирке — гидроксид натрия (образует щелочную среду).
К оставшимся растворам добавили нитрат серебра.
В одной пробирке выпадает белый осадок:
В одной пробирке находится хлорид магния, в пробирке с осадком — нитрат натрия.
2. При помощи характерных реакций докажите, что выданное вам вещество — сульфат алюминия.
3. В одной пробирке дан раствор хлорида натрия, во второй — раствор хлорида стронция, а в третьей — раствор хлорида алюминия. Определите, в какой пробирке находится каждое из выданных веществ.
К растворам добавили сульфат калия.
В одной пробирке выпадает белый осадок:
В пробирке — хлорид стронция.
К оставшимся растворам прилили раствор гидроксида натрия.
В пробирке — хлорид аллюминия. В пробирке с осадком — хлорид натрия.
4. Практически осуществите следующие превращения:
Fe→FeCl2→Fe(OH)2→Fe(OH)3→Fe(NO3)3
Вариант 2. Распознавание карбоната кальция CaCO3, нитрата стронция Sr(NO3)2, сульфата натрия NaSO4, сульфида натрия Na2S. 1. В четырех пробирках даны следующие твёрдые вещества: а) карбонат кальция; б) нитрат стронция; в) сульфат натрия; г) сульфид натрия. Определите, в какой пробирке находится каждое из перечисленных веществ.
Растворили твёрдые вещества и добавили к растворам соляную кислоту.
В пробирке вещество не растворилось в воде, после добавления соляной кислоты выделился газ без запаха и цвета:
В пробирке — карбонат кальция.
В другой пробирке выделяется газ с характерным запахом тухлых яиц:
В пробирке — сульфид натрия.
К остальным растворам прилили раствор серной кислоты.
В одной из пробирок выпадает белый осадок:
В пробирке — нитрид стронция, в пробирке с осадком — сульфат натрия.
2. Докажите, что кристаллы сульфата железа (III) частично окислились и содержат примеси ионов Fe3+.
Качественным реагентом на присутствие трёхвалентного железа является роданид калия. Появляется красное окрашивание.
3. В двух склянках дана вода. В одной из них вода содержит сульфат магния, а в другой — гидрокарбонат кальция. Проделайте опыты, при помощи которых можно устранить постоянную и временную жёсткость воды.
4. Практически осуществите следующие превращения:
Аl→Al2(SO4)3→Аl(ОН)3→Na[Al(OH)4]
5. Отчёт о работе оформите в произвольной форме.
Отчёт представлен выше (1,2,3,4 пункты каждого варианта).
Досрочный вариант ЕГЭ по химии-2022 Вариант 2
Досрочный вариант ЕГЭ по химии-2022. Скачать разбор досрочного варианта ЕГЭ по химии-2022 от 23 марта 2022 с ответами и решениями
Для выполнения заданий 1–3 используйте следующий ряд химических элементов:
1) Na 2) S 3) Al 4) O 5) Cr
Ответом в заданиях 1–3 является последовательность цифр, под которыми указаны химические элементы в данном ряду.
1. Определите, атомы каких из указанных в ряду элементов в основном состоянии содержат одинаковое число s-электронов. Запишите в поле ответа номера выбранных элементов.
2. Из указанных в ряду химических элементов выберите три элемента-металла. Расположите выбранные элементы в порядке возрастания восстановительных свойств образуемых ими простых веществ. Запишите в поле ответа номера выбранных элементов в нужной последовательности.
3. Из указанных в ряду элементов выберите два элемента, у которых в образуемых ими ионах ЭОх 2- совпадает степень окисления. Запишите в поле ответа номера выбранных элементов.
4. Из предложенного перечня выберите два вещества, которые имеют ионную и ковалентную неполярную связь.
1) фосфат натрия
2) метилацетат
3) бензоат аммония
4) диэтиловый эфир
5) пероксид натрия
Запишите номера выбранных веществ.
5. Среди предложенных формул веществ, расположенных в пронумерованных ячейках, выберите формулы: А) кислоты; Б) средней соли; В) кислотного оксида.
Запишите в таблицу номера ячеек, в которых расположены вещества, под соответствующими буквами.
| А | Б | В |
| 9 | 3 | 8 |
6. В одну из пробирок с порошком оксида цинка добавили слабый электролит X, а в другую – раствор вещества Y. В результате в первой пробирке наблюдали растворение твердого вещества. В пробирке с раствором вещества Y произошла реакция, которую описывает сокращенное ионное уравнение:
ZnO + 2H + = Zn 2+ + H2O
выберите вещества X и Y, которые могут вступать в описанные реакции.
1) йодоводород
2) хлорид аммония
3) гидрокарбонат натрия
4) гидроксид натрия
5) фтороводород
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
| X | Y |
| 5 | 1 |
7. Установите соответствие между формулой вещества и реагентами, с каждым из которых это вещество может взаимодействовать: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА ВЕЩЕСТВА | РЕАГЕНТЫ |
| А) CuBr2 Г) HCl(р-р) | 1) Cl2, KOH, KI 5) NaCl, H2SO4, O2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
| А | Б | В | Г |
| 1 | 3 | 2 | 4 |
8. Установите соответствие между исходными веществами, вступающими в реакцию, и продуктами, которые образуются при взаимодействии этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ИСХОДНЫЕ ВЕЩЕСТВА | ПРОДУКТЫ |
| А) Fe2O3 и HI Г) Fe3O4 и HI | 1) FeI2, I2 и H2O 6) HCl и NaНSO4 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
| А | Б | В | Г |
| 1 | 3 | 6 | 1 |
9. Задана следующая схема превращений веществ:
Fe 

Определите, какие из указанных веществ являются веществами X и Y.
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
| X | Y |
| 3 | 4 |
10. Установите соответствие между формулой вещества и классом/группой органических соединений, к которому(-ой) это вещество принадлежит: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| КЛАСС/ГРУППА | НАЗВАНИЕ ВЕЩЕСТВА |
| А) нитросоединение В) спирт | 1) тринитроглицерин 2) диизопропиловый эфир 4) нитротолуол |
Запишите в таблицу выбранные цифры под соответствующими буквами.
| А | Б | В |
| 4 | 1 | 3 |
11. Из предложенного перечня выберите два вещества, которые являются межклассовыми изомерами.
1) пропаналь
2) пропановая кислота
3) уксусная кислота
4) нитроэтан
5) глицин
Запишите в поле ответа номера выбранных веществ.
12. Из предложенного перечня выберите все вещества, которые реагируют с водородом.
1) олеиновая кислота
2) стеариновая кислота
3) ацетон
4) изопрен
5) изопропиловый спирт
Запишите в поле ответа номера выбранных веществ.
13. Из предложенного перечня выберите два вещества, которые реагируют и с глюкозой, и с фруктозой.
1) гидроксид меди (II)
2) сульфат калия
3) водород
4) медь
5) метан
Запишите в поле ответа номера выбранных веществ.
14. Установите соответствие между схемой реакции и веществом Х, принимающим в ней участие: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА РЕАКЦИИ | ВЕЩЕСТВО Х |
| А) Х + Н2О ⟶ (кат.) изопропиловый спирт Б) Х + KMnO4 + Н2О ⟶ пропандиол-1,2 В) Х + KMnO4 + H+ ⟶ пропионовая кислота Г) Х + Н2О ⟶ (кат.) ацетон | 1) бутен-1 6) бутин-2 |
Запишите в таблицу выбранные цифры под соответствующими буквами.
| А | Б | В | Г |
| 5 | 5 | 1 | 4 |
15. Установите соответствие между веществом и его способом получения: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную
цифрой.
| ВЕЩЕСТВО | СПОСОБ ПОЛУЧЕНИЯ |
| А) этанол Б) уксусная кислота Г) этаналь | 1) окисление этена перманганатом калия в нейтральной среде 2) щелочной гидролиз метилацетата 3) щелочной гидролиз 1,1-дихлорэтана 4) окисление бутена-2 перманганатом калия в кислой среде 5) термолиз ацетата кальция 6) восстановление ацетальдегида |
Запишите в таблицу выбранные цифры под соответствующими буквами.
| А | Б | В | Г |
| 6 | 4 | 1 | 3 |
16. Задана следующая схема превращений веществ:
метан ⟶ Х ⟶ бензол ⟶ Y ⟶ толуол
Определите, какие из указанных веществ являются веществами X и Y.
1) бромметан
2) этен
3) нитробензол
4) ацетилен
5) бромбензол
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
| X | Y |
| 4 | 5 |
17. Из предложенного перечня выберите все типы реакций, к которым можно отнести взаимодействие водорода с хлором.
1) гомогенная
2) замещения
3) экзотермическая
4) нейтрализации
5) окислительно-восстановительная
Запишите номера выбранных ответов.
18. И з предложенного перечня выберите все реакции, для которых будет увеличиваться скорость реакции при добавлении кислорода.
Запишите номера выбранных ответов.
19. Установите соответствие между схемой реакции и свойством элемента фосфора, которое он проявляет в этой реакции: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| СХЕМА РЕАКЦИИ | СВОЙСТВА ФОСФОРА |
| А) Mg + H3PO4 → Mg(H2PO4) 2 + H2 В) PH3 + O2 → H3PO4 | 1) является окислителем 2) является восстановителем 3) является и окислителем, и восстановителем 4) не проявляет окислительно-восстановительных свойств |
Запишите в таблицу выбранные цифры под соответствующими буквами.
| А | Б | В |
| 4 | 2 | 2 |
20. Установите соответствие между формулой соли и продуктами электролиза водного раствора этой соли, которые выделились на инертных электродах: к каждой позиции,
обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
| ФОРМУЛА СОЛИ | ПРОДУКТЫ ЭЛЕКТРОЛИЗА |
| А) бромид лития Б) сульфат натрия В) хлорид алюминия | 1) водород, галоген 2) металл, галоген 3) водород, кислород 4) металл, кислород |
Запишите в таблицу выбранные цифры под соответствующими буквами.
| А | Б | В |
| 1 | 3 | 1 |
| Для выполнения задания 21 используйте следующие справочные данные. Концентрация (молярная, моль/л) показывает отношение количества растворённого вещества (n) к объёму раствора (V). pH («пэ аш») – водородный показатель; величина, которая отражает концентрацию ионов водорода в растворе и используется для характеристики кислотности среды. 21. Д ля веществ, приведённых в перечне, определите характер среды их водных растворов, имеющих одинаковую концентрацию (моль/л). Запишите номера веществ в порядке возрастания значения pH их водных растворов. 22. У становите соответствие между способом воздействия на равновесную систему S 2− (р-р) + H2O(ж.) ⇆ HS − (р-р) + OH − (р-р) — Q и смещением химического равновесия в результате этого воздействия: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
23. В реактор постоянного объёма поместили некоторое количество серного ангидрида. В результате протекания обратимой реакции в реакционной системе установилось химическое равновесие. Используя данные, приведённые в таблице, определите равновесную концентрацию сернистого газа (X) и равновесную концентрацию кислорода (Y). Выберите из списка номера правильных ответов.
24. Установите соответствие между формулами веществ и реагентом, с помощью которого можно различить водные растворы этих веществ: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
25. Установите соответствие между названием вещества и основной областью применения этого вещества: к каждой позиции, обозначенной буквой, подберите соответствующую позицию, обозначенную цифрой.
Запишите в таблицу выбранные цифры под соответствующими буквами.
27. Синтез углекислого газа протекает в соответствии с термохимическим уравнением реакции Определите объем (в л) кислорода, который образуется в результате выделения 944 кДж тепла. (Запишите число точностью до целых.) 28. 175 г технического карбоната магния, содержащего 4% некарбонатной примеси, нагрели. Найдите объем (в л) выделившегося газа (н.у.) (Запишите число с точностью до десятых.)
29. Из предложенного перечня веществ выберите вещества, между которыми может протекать окислительно-восстановительная реакция, в которой в растворе образуется только кислоты. В ответе запишите уравнение только одной из возможных окислительно-восстановительных реакций. Составьте электронный баланс, укажите окислитель и восстановитель в этой реакции. 2Cl 0 S +4 30. Из предложенного перечня веществ выберите вещества, между которыми может протекать реакция ионного обмена, в результате которой из окрашенного раствора выпадает осадок. Запишите молекулярное, полное и сокращённое ионное уравнения только одной из возможных реакций. 31. Бромоводородной кислотой нейтрализовали карбонат калия. Через полученный раствор пропустили электрический ток. Образовавшийся на катоде газ пропустили над нагретым оксидом меди (II). Полученное простое вещество растворили в концентрированном растворе азотной кислоты. Напишите уравнения четырёх описанных реакций 2KBr + 2H2O 32. Н апишите уравнения реакций, с помощью которых можно осуществить следующие превращения: бутен-1 ⟶ Х1 ⟶ бутин-1 ⟶ Х2 ⟶ гексин-3 При написании уравнений реакций используйте структурные формулы органических веществ. CH3CH2CH=CH2 + Cl2 →
5CH3-CH2-C≡C-CH2-CH3 + 6KMnO4 + 9H2SO4 33. К раствору сульфата железа (III) массой 632 г, содержащего в общей сложности 1,806∙10 25 атомов кислорода, добавили 79 г сульфита калия. После окончания реакции к образовавшемуся раствору прилили 552 г 10%-ного раствора карбоната калия. Вычислите массовую долю сульфата калия в образовавшемся растворе. (Образованием кислых солей пренебречь.) В ответе запишите уравнения реакций, которые указаны в условии задачи, и приведите все необходимые вычисления (указывайте единицы измерения искомых физических величин). nO = 1,306·10 25 /6,02·10 23 = 30 моль тогда nFe = 2x моль, nS = 3x моль, n1(O) = 12x моль у + 12х = 30 ω(K2SO4) = (0,4+0,5)·174/(632+79+552 — 0,4·44) = 0,1257 или 12,57% 34. При взаимодействии соли первичного амина с нитратом серебра образуется органическое вещество А и бромид серебра. Вещество А содержит 25,93% азота, 7,41% водорода и 44,44% кислорода по массе. Напишите уравнение реакции получения вещества А из соли первичного амина и нитрата серебра. На основании данных условия задания: m(N) = 25,93г n(N) = 25,93/14 = 1,852143 моль |

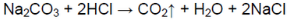
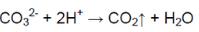
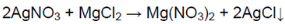

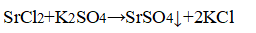
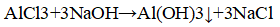
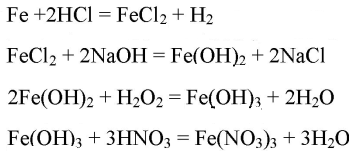

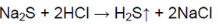
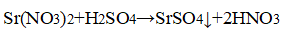
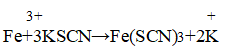
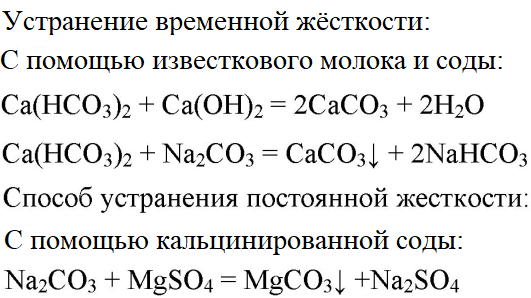
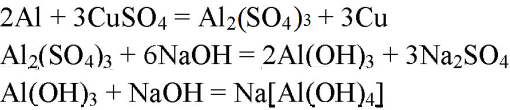



 2Cl − Cl2 0 – окислитель
2Cl − Cl2 0 – окислитель S +6 SO2 +4 – восстановитель
S +6 SO2 +4 – восстановитель H2 + 2KOH + Br2
H2 + 2KOH + Br2 Х3
Х3
 10CH3CH2COOH + 3K2SO4 + 6MnSO4 + 4H2O
10CH3CH2COOH + 3K2SO4 + 6MnSO4 + 4H2O