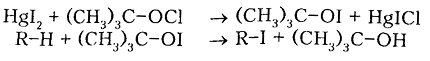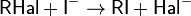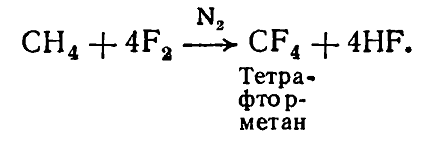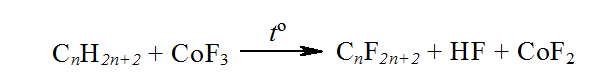Вы будете перенаправлены на Автор24
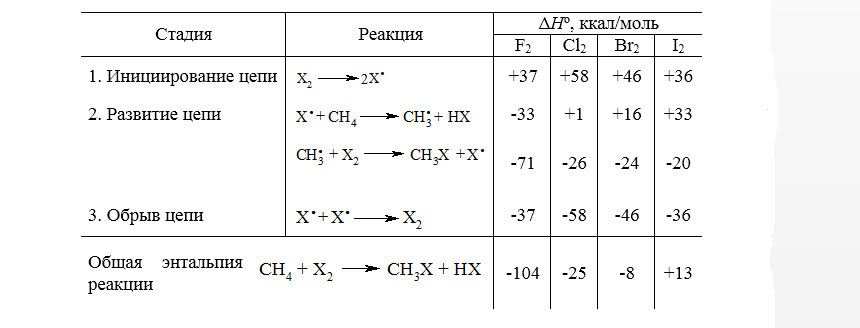
Радикальный механизм хлорирования метана, аналогичен и для реакций с остальными галогенами. Для всех галогенов это цепной радикальный процесс, который инициируется гомолизом молекул галогенов с образованием атомов галогена. Как и следовало ожидать, реакционная способность значительно уменьшается в ряду $F_2 > Cl_2 > Br_2 > I_2$. Энтальпии последовательных стадий галогенирования метана до $CH_3X$ приведены на рис.1
Рисунок 1. Энтальпии отдельных стадий галогенирования метана
Как видно по данным таблицы, относительные реакционные способности галогенов согласуются как с суммарными значениями $Delta H^circ$ всего процесса галогенирования в целом, так и со значениями $Delta H^circ$ для стадий развития цепи. Это обычный результат для радикальной реакции в газовой фазе.
- Бромирование метана
- Готовые работы на аналогичную тему
- Йодирование метана
- Фторирование метана
- Написать формулу реакции бромирования метана?
- Написать формулу метана?
- Помогите написать реакцию : тетрохлорметан из метана?
- Бром действует на метан подобно хлору?
- Помогите плиз?
- Что включает в себя реакция бромирования?
- Проведите механизм реакции : бромирования метана на свету?
- Написать уравнения реакций :а)гидратации ;б)бромирования ;в)гидробромирования ;г)гидрирования пропена?
- 1)Реакция Коновалова для бутана 2) Дегидрирование гексана 3) Бромирование пропана 4) Каталитическое окисление метана?
- Получить толуол и написать с ним реакции : ?
- Каков механизм реакции галогенирования алканов?
- Назовите процесс с которого начинается бромирование метана напишите уравнение химической реакции
- 🎥 Видео
Видео:ВСЕ ПРО АЛКАНЫ за 8 минут: Химические Свойства и ПолучениеСкачать

Бромирование метана
Бромирование по сумме всех стадий — экзотермический процесс, но уже для первой взаимодействия на стадии роста цепи необходимо предоставить примерно 59 кДж / моль (взаимодействие эндотермическая) в отличие от фторирования и хлорирования (рис. 1):
Рисунок 2. Бромирование, йодирование и фторирование метана
Энергия активации при этом равна примерно 75 кДж / моль. Поэтому только атомы брома с высокой энергией способны преодолеть высоту энергетического барьера и прореагировать с метаном.
Общая, при небольших температурах, скорость бромирования значительно меньше по сравнению с хлорированием (примерно в 250 000 раз). Однако реакция бромирования происходит с высокой селективностью.
Бромирование благодаря низкой среди галогенов экзотермичности ($Delta H- 29$ кДж / моль) и меньшей энергии свободного радикала брома происходит более селективно и дает почти чистые продукты. Известно, что селективность тем больше, чем меньше реакционная способность агента галогенирования.
Готовые работы на аналогичную тему
Легче галогенирования происходит в третичного атома углерода, затем — вюринного и, в конце, — первичного. Для Брома соотношение скоростей замещения в этих атомов 1600: 82: 1.
Высокую селективность бромирования связывают с медленным течением реакций, а также ее кинетическим контролем.
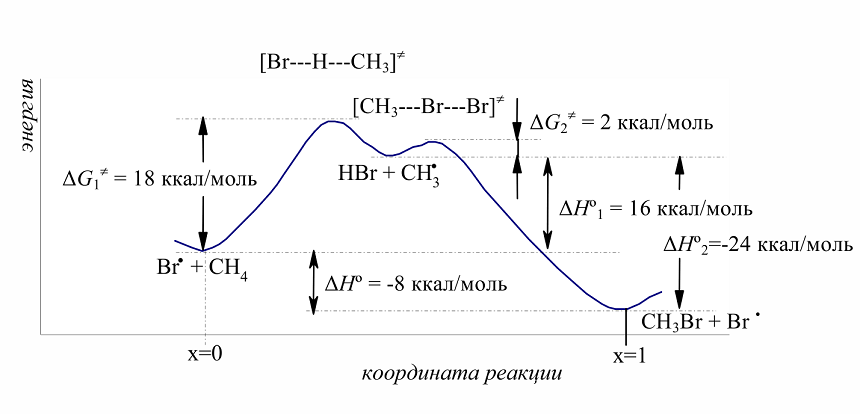
Бромирование метана происходит с меньшим выделением энергии, чем хлорирование. На первой стадии развития цепи наблюдается высокий эндотермический эффект: $Delta H^circ_1 = +16$ ккал/моль (при хлорировании $Delta H^circ_1 = +1$ ккал/моль). Это означает, что свободная энергия активации $Delta G_1^neq$ для первой стадии должна быть намного выше, чем для хлорирования. Действительно, $Delta G_1^neq$ для первой стадии развития цепи (18 ккал/моль; рис. 1) при бромировании намного превышает $Delta G_1^neq$ для хлорирования (4 ккал/моль). Тепловые эффекты второй стадии развития цепи при бромировании (- 24 ккал/моль) и при хлорировании (- 26 ккал/моль) весьма близки и энергия активации $Delta G_2^neq$ для обоих процессов тоже очень мало различаются. Значительно более высокое значение $Delta G_1^neq$ для бромирования указывает на то, что бромирование метана протекает с меньшей скоростью, чем хлорирование.
Рисунок 3. Энергетическая диаграмма свободнорадикального бромирования метана
Видео:Химические свойства алканов. 1 часть. 10 класс.Скачать

Йодирование метана
Йодирования алканов проходит с очень малой скоростью нуждается в дополнительной энергии (процесс эндотермический), а образованный $HI$ активно восстанавливает йодалкилы снова в алканы. Только применяя специальные йодирующие агенты, например трет-бутоксийодид полученный из йодида ртути $HgI_2$ действием тpeт-бутоксихлорида, возможно йодирование алканов с небольшими выходами.
Рисунок 4. Бромирование, йодирование и фторирование метана
Применяют также реакцию обмена хлора в хлоралкане йодом под действием йодида натрия NaI в ацетоновом растворе — реакция $X$. Финкельштайна, 1910 гг.:
Рисунок 5. Бромирование, йодирование и фторирование метана
Реакции Финкельштайна способствует большая растворимость NaИ в ацетоне сравнению с хлоридом натрия.
Видео:Химические уравнения // Как Составлять Уравнения Реакций // Химия 9 классСкачать

Фторирование метана
Взаимодействие алкана непосредственно с фтором происходит со взрывом в результате значительного экзотермии (выделение теплоты). Так, при монофторировании метана для разрыва одной $C-H$-связи и связи $F-F$ необходимо потратить соответственно 425 и 160 кДж / моль (рис. 1):
$H_3C-H+F-F Longrightarrow H_3C-F+HF$, $triangle H=-437$
Одновременно с образованием новых связей $C-F$ и $H-F$ выделяется соответственно -452 и -570 кДж / моль. Суммарная теплота (экзотермии) реакции составляет $[-452 + (- 570)] — (160 + 425) = -437$ кДж / моль.
Для разрыва $C-C$-связи необходимо примерно 350 кДж / моль, поэтому непосредственное фторирование происходит со взрывом:
$CH_3-CH_2-CH_3+4F_2 longrightarrow 3C_<underline> + 8HF$
Во избежание сильной экзотермии фтор разводят жидким азотом или проводят реакцию в растворителе — полностью фторированных алканах:
$CH_3-CH_3+6F_2 longrightarrow CF_3 — CF_3 + 6HF$
Разбавления фтора азотом дает возможность добывать полифторпроизводные алканов с достаточно высоким выходом:
Рисунок 6. Бромирование, йодирование и фторирование метана
Направленое фторирование алканов без разрыва связей $C-C$ также проводят кобальт (III) фторидом или фтором, который выделяется при электролизе. Через слой $CoF_3$ пропускают газообразные алканы, при этом образуется перфторалканы и фторид кобальта (II):
Рисунок 7. Бромирование, йодирование и фторирование метана
Фторид кобальта (II) регенерируют, пропуская через через него ток фтора.
Получи деньги за свои студенческие работы
Курсовые, рефераты или другие работы
Автор этой статьи Дата последнего обновления статьи: 16.09.2021
Видео:Как расставлять коэффициенты в уравнении реакции? Химия с нуля 7-8 класс | TutorOnlineСкачать

Написать формулу реакции бромирования метана?
Химия | 10 — 11 классы
Написать формулу реакции бромирования метана.
Если подобно хлору, то так
СH4 + Br2 = CH3Br + HBr
CH3Br + Br2 = CH2Br2 + HBr
CH2Br2 + Br2 = CHBr3 + HBr
CHBr3 + Br2 = CBr4 + HBr.
Видео:Химические свойства алканов | Химия ЕГЭ для 10 класса | УмскулСкачать

Написать формулу метана?
Написать формулу метана!
Видео:Как решать ОРГАНИЧЕСКИЕ ЦЕПОЧКИ? Основные типы химических реакцийСкачать

Помогите написать реакцию : тетрохлорметан из метана?
Помогите написать реакцию : тетрохлорметан из метана.
Видео:Типы Химических Реакций — Химия // Урок Химии 8 КлассСкачать

Бром действует на метан подобно хлору?
Бром действует на метан подобно хлору.
Составте уравнение реакций последовательного бромирования метана, укажите условие их протекания и назовите полученные продукты.
Видео:Составление формул органических соединений по названиюСкачать

Помогите плиз?
Составить уровнения реакций а.
Бромирования метана, б.
Видео:ОВР и Метод Электронного Баланса — Быстрая Подготовка к ЕГЭ по ХимииСкачать

Что включает в себя реакция бромирования?
Что включает в себя реакция бромирования.
Видео:Типы химических реакций. 1 часть. 8 класс.Скачать

Проведите механизм реакции : бромирования метана на свету?
Проведите механизм реакции : бромирования метана на свету.
И если можно объяснить.
Видео:Химические уравнения - Как составлять уравнения реакций // Составление Уравнений Химических РеакцийСкачать

Написать уравнения реакций :а)гидратации ;б)бромирования ;в)гидробромирования ;г)гидрирования пропена?
Написать уравнения реакций :
Видео:ВСЯ ХИМИЯ за 10 класс в 1 уроке + таймкодыСкачать

1)Реакция Коновалова для бутана 2) Дегидрирование гексана 3) Бромирование пропана 4) Каталитическое окисление метана?
1)Реакция Коновалова для бутана 2) Дегидрирование гексана 3) Бромирование пропана 4) Каталитическое окисление метана.
Видео:Химические Цепочки — Решение Цепочек Химических Превращений // Химия 8 классСкачать

Получить толуол и написать с ним реакции : ?
Получить толуол и написать с ним реакции : !
) бромирование при t 2)бромирование в присутствии AlCl3.
Видео:Все углеводороды за 6 часов | Химия ЕГЭ 2023 | УмскулСкачать

Каков механизм реакции галогенирования алканов?
Каков механизм реакции галогенирования алканов?
Дайте его описание на примере бромирования метана.
На странице вопроса Написать формулу реакции бромирования метана? из категории Химия вы найдете ответ для уровня учащихся 10 — 11 классов. Если полученный ответ не устраивает и нужно расшить круг поиска, используйте удобную поисковую систему сайта. Можно также ознакомиться с похожими вопросами и ответами других пользователей в этой же категории или создать новый вопрос. Возможно, вам будет полезной информация, оставленная пользователями в комментариях, где можно обсудить тему с помощью обратной связи.
2 — этилбутен — 1 2, 3, 4 — триметилгексан 2 — метилпроаен — 1.
ОПределим в каждом массовую долю железа. Мы знаем , что атом железа весит 56 грамм, а атом кислорода 16 грамм. В соединении FeO , 1 атом железа и 1 атом кислорода. Посчиатем молекулярную массу , 16 + 56 = 72 грамм . А теперь определим массовую до..
2. FeSO4 + 2NaOH = Fe(OH)2↓ + Na2SO4 Fe²⁺ + SO4²⁻ + 2Na⁺ + 2OH⁻ = Fe(OH)2↓ + 2Na⁺ + SO4²⁻ Fe²⁺ + 2OH⁻ = Fe(OH)2↓⁻ Fe(OH)2↓ + 2HCl = FeCl2 + 2H2O Fe(OH)2↓ + 2H⁺ + 2Cl⁻ = Fe²⁺ + 2Cl⁻ + 2H2O Fe(OH)2↓ + 2H⁺ = Fe²⁺ + 2H2O 1. K2SO3 + 2HCl = 2KCl + SO2 + H..
Нет конечно, это физическое явление, откуда оно химическое.
Видео:ЭТО ПОМОЖЕТ разобраться в Органической Химии — Алкены, Урок ХимииСкачать

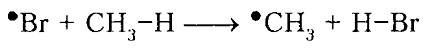
Назовите процесс с которого начинается бромирование метана напишите уравнение химической реакции
Реакция бромирования метана протекает
1) по радикальному механизму
2) в одну стадию
3) с образованием различных бромпроизводных
4) в темноте и без нагревания
5) с выделением теплоты
6) в соответствии с правилом В. В. Марковникова
метан — это вещество класса алканов. Следовательно, характерны реакции радикального замещения (ответ 1). это процесс многостадийный, с образованием нескольких бромпроизводных (ответ 3). Для бромирования, как и для остального галогенирования необходим свет, и данная реакция экзотермична — следовательно, (5). Правило Марковникова применимо для ионного механизма протекания реакций.
🎥 Видео
РЕАКЦИИ ИОННОГО ОБМЕНА, ИОННОЕ УРАВНЕНИЕ - Урок Химия 9 класс / Подготовка к ЕГЭ по ХимииСкачать

7 ВАЖНЕЙШИХ РЕАКЦИЙ, которые тебе нужно знать (Алкины)Скачать

Вся теория по алканам | Химия ЕГЭ для 10 класса | УмскулСкачать

Правило Марковникова В.В. в реакциях присоединения у алкЕнов и алкИнов.Скачать

Алканы: химические свойства. Практика. [4] Органика С НУЛЯ | Химия для 10 класса и ЕГЭ-2024Скачать
![Алканы: химические свойства. Практика. [4] Органика С НУЛЯ | Химия для 10 класса и ЕГЭ-2024](https://i.ytimg.com/vi/kTXlMZuTgIw/0.jpg)