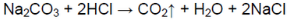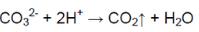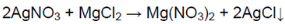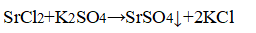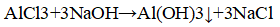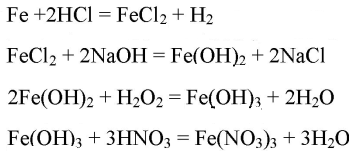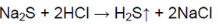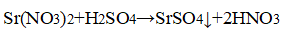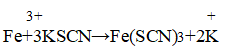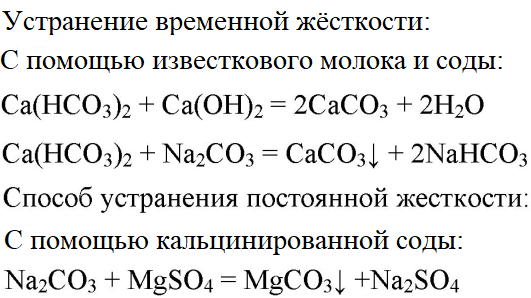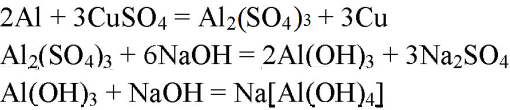- We are checking your browser. gomolog.ru
- Why do I have to complete a CAPTCHA?
- What can I do to prevent this in the future?
- Напишите уравнения трех способов получения хлорида марганца 2 сульфата меди 2
- Вопросы к параграфу 50 — ГДЗ по Химии 9 класс Учебник Рудзитис, Фельдман
- § 50. Практическая работа №7.
- Решение экспериментальных задач по теме: “Металлы”
- Вариант 1. Распознавание хлорида магния MgCl2, гидроксида натрия NaOH, карбоната натрия Na2CO3, нитрата натрия NaNO3 1. В четырёх пробирках даны следующие вещества в твёрдом виде: а) хлорид магния; 6) гидроксид натрия; в) карбонат натрия; г) нитрат натрия. При помощи химических реакций определите, в какой пробирке находится каждое из этих веществ.
- 2. При помощи характерных реакций докажите, что выданное вам вещество — сульфат алюминия.
- 3. В одной пробирке дан раствор хлорида натрия, во второй — раствор хлорида стронция, а в третьей — раствор хлорида алюминия. Определите, в какой пробирке находится каждое из выданных веществ.
- 4. Практически осуществите следующие превращения:
- Fe→FeCl2→Fe(OH)2→Fe(OH)3→Fe(NO3)3
- Вариант 2. Распознавание карбоната кальция CaCO3, нитрата стронция Sr(NO3)2, сульфата натрия NaSO4, сульфида натрия Na2S. 1. В четырех пробирках даны следующие твёрдые вещества: а) карбонат кальция; б) нитрат стронция; в) сульфат натрия; г) сульфид натрия. Определите, в какой пробирке находится каждое из перечисленных веществ.
- 2. Докажите, что кристаллы сульфата железа (III) частично окислились и содержат примеси ионов Fe3+.
- 3. В двух склянках дана вода. В одной из них вода содержит сульфат магния, а в другой — гидрокарбонат кальция. Проделайте опыты, при помощи которых можно устранить постоянную и временную жёсткость воды.
- 4. Практически осуществите следующие превращения:
- Аl→Al2(SO4)3→Аl(ОН)3→Na[Al(OH)4]
- 5. Отчёт о работе оформите в произвольной форме.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 700ef1f2aa579781 • Your IP : 87.119.247.227 • Performance & security by Cloudflare
Напишите уравнения трех способов получения хлорида марганца 2 сульфата меди 2
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
1. Реакция нейтрализации
С помощью предложенных реактивов, выданных в виде растворов (гидроксид натрия, серная кислота, азотная кислота, сульфат меди (II), фенолфталеин), проведите четыре возможных реакции нейтрализации. Запишите уравнения реакций.
Реакция 1 и 2. В пробирку налили немного раствора гидроксида натрия и добавили несколько капель индикатора фенолфталеина. В щелочной среде индикатор окрасился в малиновый цвет. После приливания раствора серной или азотной кислоты раствор обесцветился, поскольку среда стала нейтральной в результате реакции нейтрализации.
1) 2NaOH + H2SO4 = Na2SO4 + 2H2O
2) NaOH + HNO3 = NaNO3 + H2O
Реакция 3 и 4. Получим нерастворимое основание и проведем реакции нейтрализации. В пробирку налили раствора сульфата меди (II) и добавили немного раствора гидроксида натрия. Наблюдаем выпадение осадка голубого цвета.
CuSO4 + 2NaOH = Cu(OH)2↓ + Na2SO4
При приливании раствора серной или азотной кислоты осадок растворяется, поскольку происходит реакция нейтрализации.
3) Cu(OH)2 ↓ + H2SO4 = CuSO4 + 2H2O
4) Cu(OH)2↓ + 2HNO3 = Cu(NO3)2 + 2H2O
2. Получение соединений
С помощью предложенных реактивов, выданных в виде растворов (гидроксид натрия, хлорид бария, сульфат меди (II), соляная кислота,) и твёрдых веществ (железо, карбонат натрия) получите четыре соли, щёлочь и нерастворимое основание, одну кислоту и один металл. Запишите уравнения реакций.
Получение солей.
NaOH + HCl = NaCl + H2O
Fe + 2HCl = FeCl2 + H2↑
BaCl2 + Na2CO3 = 2NaCl + BaCO3↓
BaCl2 + CuSO4 = CuCl2 + BaSO4↓
Получение нерастворимого основания:
CuSO4 + 2NaOH = Na2SO4 + Cu(OH)2↓
Получение металла:
Fe + CuSO4 = FeSO4 + Cu↓
Получение щёлочи.
Ba2CO3↓ = BaO + CO2↑
BaO + H2O = Ba(OH)2 ― растворимое основание, проявляет все свойства щелочей.
3. Идентификация кислоты
Используя необходимые реактивы, проведите реакции, подтверждающие качественный состав серной кислоты. Запишите уравнения реакций.
Реактивы: лакмус или гранулы цинка, хлорид бария.
Серная кислота H2SO4 состоит из атомов водорода и кислотного остатка.
Доказать наличие водорода можно двумя способами:
1-й способ
При помощи индикатора, например, лакмуса, который окрасится в растворе кислоты в красный цвет.
2-й способ
При помощи выделения водорода.
Zn + H2SO4 = ZnSO4 + H2↑
Доказать наличие сульфат-анионов можно при помощи cоли бария, например, хлорида бария, поскольку наблюдается выпадение белого осадка:
H2SO4 + BaCl2 = 2HCl + BaSO4↓
4. Идентификация основания.
Используя необходимые реактивы, проведите реакции, подтверждающие качественный состав гидроксида кальция, выданного вам в виде известковой воды. Запишите уравнения реакций.
Реактивы: лакмус, углекислый газ.
Доказать наличие гидроксид-ионов можно при помощи индикатора, например, лакмуса, который окрасит раствор щелочи в синий цвет.
Доказать наличие кальция можно при помощи углекислого газа, поскольку наблюдается помутнение раствора, т.к. образуется малорастворимая соль СaCO3:
Ca(OH)2 + CO2 = CaCO3↓ + H2O
5. Идентификация солей.
Используя необходимые реактивы, проведите реакции, подтверждающие качественный состав:
а) хлорида бария;
Реактивы: серная кислота или сульфат натрия, нитрат серебра (I).
Доказать наличие бария можно при помощи раствора серной кислоты или её солей, например, сульфата натрия, поскольку наблюдается выпадение белого осадка:
H2SO4 + BaCl2 = 2HCl + BaSO4↓
или
Na2SO4 + BaCl2 = 2NaCl + BaSO4↓
Доказать наличие хлорид-анионов можно при добавлении раствора нитрата серебра к раствору хлорида бария, поскольку в результате реакции образуется белый творожистый осадок хлорида серебра (I):
BaCl2 + 2AgNO3 = Ba(NO3)2 + 2AgCl↓
б) сульфата аммония.
Реактивы: гидроксид натрия, влажная лакмусовая бумажка, хлорид бария.
Доказать наличие аммония можно при добавлении раствора щелочи, например, гидроксида натрия к раствору сульфата аммония, и последующем нагревании, поскольку в результате реакции выделяется аммиак, который можно распознать по запаху или с помощью влажной лакмусовой бумажки (окрасится в синий цвет) :
(NH4)2SO4 + 2NaOH = Na2SO4 + 2NH3↑ + 2H2O
Доказать наличие сульфат-анионов можно при помощи cоли бария, например, хлорида бария, поскольку наблюдается выпадение белого осадка:
(NH4)2SO4 + BaCl2 = 2NH4Cl + BaSO4↓
Вопросы к параграфу 50 — ГДЗ по Химии 9 класс Учебник Рудзитис, Фельдман
Авторы: Рудзитис Г.Е., Фельдман Ф.Г.
§ 50. Практическая работа №7.
Решение экспериментальных задач по теме: “Металлы”
Вариант 1. Распознавание хлорида магния MgCl2, гидроксида натрия NaOH, карбоната натрия Na2CO3, нитрата натрия NaNO3 1. В четырёх пробирках даны следующие вещества в твёрдом виде: а) хлорид магния; 6) гидроксид натрия; в) карбонат натрия; г) нитрат натрия. При помощи химических реакций определите, в какой пробирке находится каждое из этих веществ.
Твёрдые вещества растворили в воде, далее прилили соляную кислоту.
В одной пробирке выделяется газ без цвета и запаха:
В пробирке — карбонат натрия.
К другим растворам добавили несколько капель фенолфталеина.
Содержимое одной из пробирок окрасилось с малиновый цвет.
В пробирке — гидроксид натрия (образует щелочную среду).
К оставшимся растворам добавили нитрат серебра.
В одной пробирке выпадает белый осадок:
В одной пробирке находится хлорид магния, в пробирке с осадком — нитрат натрия.
2. При помощи характерных реакций докажите, что выданное вам вещество — сульфат алюминия.
3. В одной пробирке дан раствор хлорида натрия, во второй — раствор хлорида стронция, а в третьей — раствор хлорида алюминия. Определите, в какой пробирке находится каждое из выданных веществ.
К растворам добавили сульфат калия.
В одной пробирке выпадает белый осадок:
В пробирке — хлорид стронция.
К оставшимся растворам прилили раствор гидроксида натрия.
В пробирке — хлорид аллюминия. В пробирке с осадком — хлорид натрия.
4. Практически осуществите следующие превращения:
Fe→FeCl2→Fe(OH)2→Fe(OH)3→Fe(NO3)3
Вариант 2. Распознавание карбоната кальция CaCO3, нитрата стронция Sr(NO3)2, сульфата натрия NaSO4, сульфида натрия Na2S. 1. В четырех пробирках даны следующие твёрдые вещества: а) карбонат кальция; б) нитрат стронция; в) сульфат натрия; г) сульфид натрия. Определите, в какой пробирке находится каждое из перечисленных веществ.
Растворили твёрдые вещества и добавили к растворам соляную кислоту.
В пробирке вещество не растворилось в воде, после добавления соляной кислоты выделился газ без запаха и цвета:
В пробирке — карбонат кальция.
В другой пробирке выделяется газ с характерным запахом тухлых яиц:
В пробирке — сульфид натрия.
К остальным растворам прилили раствор серной кислоты.
В одной из пробирок выпадает белый осадок:
В пробирке — нитрид стронция, в пробирке с осадком — сульфат натрия.
2. Докажите, что кристаллы сульфата железа (III) частично окислились и содержат примеси ионов Fe3+.
Качественным реагентом на присутствие трёхвалентного железа является роданид калия. Появляется красное окрашивание.
3. В двух склянках дана вода. В одной из них вода содержит сульфат магния, а в другой — гидрокарбонат кальция. Проделайте опыты, при помощи которых можно устранить постоянную и временную жёсткость воды.
4. Практически осуществите следующие превращения:
Аl→Al2(SO4)3→Аl(ОН)3→Na[Al(OH)4]
5. Отчёт о работе оформите в произвольной форме.
Отчёт представлен выше (1,2,3,4 пункты каждого варианта).