FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 1
Какие углеводороды называют алкадиенами? Углеводороды, в молекулах которых содержатся две двойные углерод-углеродные связи и общая формула которых CnH2n-2, называют алкадиенами.
Напишите формулы одного гомолога и одного изомера пентадиена-1,3 с сопряжёнными двойными связями.
Гомолог пентадиена-1,3:
CH2=CH2―CH=CH―CH2―CH3 гексадиен-1,3
Изомер пентадиена-1,3:
CH3 ― CH=C=CH ― CH3 пентадиен-2,3
Задание 2
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
а) CH3 ― CH3 → CH3 ― CH2Br → CH3 ― CH2 ― OH → CH2=CH ― CH ― CH2
CH3 ― CH3 + Br2 ⟶ CH3 ― CH2Br + HBr
CH3 ― CH2Br + NaOH ⟶ CH3 ― CH2 ― OH + NaBr
2CH3 ― CH2 ― OH t,Al₂O₃,ZnO ⟶ H2C=CH ― CH=CH2 + 2H2O + H 2
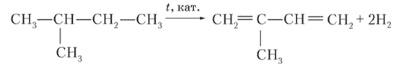
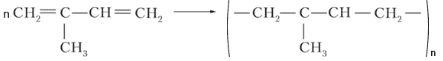
б) CH3 ― CH(CH3) ― CH2 ― CH3 → CH2=C(CH3) ― CH=CH2 → изопреновый каучук
 |
 |
Задание 3
Сравните реакции присоединения алкенов и диеновых углеводородов. Ответ подтвердите уравнениями химических реакций на примере бутена-1 и бутадиена-1,3.
Реакции галогенирования.
Общее: образуются соответствующие галогеналканы.
Отличие: алкадиены реагируют с галогенами ступенчато, с промежуточным образованием галогеналкенов.
CH2=CH ― CH2 ― CH3 + Br2 ⟶ CH2Br ― CHBr ― CH2 ― CH3
Реакции гидрирования.
Общее: образуются соответствующие а лканы.
Отличие: алкадиены реагируют с водородом ступенчато, с промежуточным образованием алкенов.
CH2=CH ― CH2 ― CH3 + H2 t, кат. ⟶ CH3 ― CH2 ― CH2 ― CH3
Реакции гидрогалогенирования.
Общее: образуются соответствующие алканы, протекают согласно правилу Марковникова.
CH2=CH ― CH2 ― CH3 + HBr ⟶ CH3 ― CHBr ― CH2 ― CH3
CH2=CH ― CH=CH2 + 2HBr ⟶ CH3 ― CHBr ― CHBr ― CH3
Задание 4
Как можно доказать непредельный характер 2-метилбутадиена-1,З? Качественная реакция на непредельные соединения, в частности на 2-метилбутадиен-1,З – обесцвечивание бромной воды:
Напишите уравнения реакций, подтверждающих ступенчатое протекание реакции.
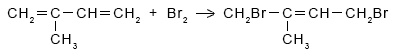 |
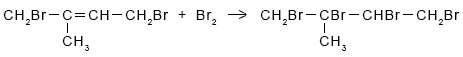 |
Задание 5
Найдите массу 2-метилбутадиена-1,З, который можно получить дегидрированием 72 кг 2-метилбутана, если выход продукта реакции составляет 80%.
Дано: m(C5H12)=72 кг, η(C5H8)=80%
Найти: mпракт.(C5H8)-?
Решение
1-й способ
1. Количество вещества 2-метилбутана рассчитываем по формуле: ʋ=m/M, где M ― молярная масса.
M( C5H12 )=72 кг/кмоль
ʋ(C5H12)=m( C5H12 )/M( C5H12 )=72 кг : 72 кг/кмоль=1 кмоль
2. Составляем химическое уравнение: C5H12 ⟶ C5H8 + 2H2
По уравнению реакции ʋ(C5H12): ʋ(C5H8)=1:1 , количества вещества одинаковые, поэтому :
ʋ(C5H8)=ʋ( C5H12 )=1 кмоль
3. Вычисляем теоретическую массу 2-метилбутадиена-1,3 количеством вещества 1 кмоль по формуле: m = ʋ •M
M( C5H8 )=68 кг/кмоль
mтеор.( C5H8 )= ʋ( C5H8 ) •M( C5H8) =1 кмоль • 68 кг/кмоль=68 кг
4. Рассчитываем массу 2-метилбутадиена-1,3, полученную практически:
mпракт.( C5H8 )= η(C5H8) •mтеор.( C5H8):100% =80% • 68 кг : 100%=54,4 кг
2-й способ
1. Составляем химическое уравнение:
72 кг х кг
C5H12 ⟶ C5H8 + 2H2
72 кг 68 кг
Над формулами соединений C5H12 и C5H8 записываем приведенную в условии задачи массу 2-метилбутана (72 кг) и неизвестную массу 2-метилбутадиена-1,3 (х кг), а под формулами соединений ― массы количества вещества согласно коэффициентам в химическом уравнении.
M( C5H12 )=72 кг/кмоль, поэтому масса 1 кмоль=72 кг
M( C5H8 )=68 кг/кмоль, поэтому масса 1 кмоль=68 кг
Теоретическую массу 2-метилбутадиена-1,3 рассчитываем с помощью пропорции:
72 кг / 72 кг = х кг / 68 кг, отсюда
х= mтеор.( C5H8)= 72 кг • 68 кг : 72 кг=68 кг
2. Рассчитываем массу 2-метилбутадиена-1,3, полученную практически:
mпракт.( C5H8 )= η(C5H8) •mтеор.( C5H8):100% =80% • 68 кг : 100%=54,4 кг
Ответ: mпракт.(C5H8)=54,4 кг
Задание 6
Англичанин Чарлз Макинтош предложил пропитывать плащевую ткань раствором натурального каучука, поэтому плащи, сшитые из такого материала, не промокали под сильным дождём; их назвали макинтошами. Однако они не были лишены недостатков, присущих натуральному каучуку: размягчались на солнце и становились хрупкими в мороз. В чём заключалось открытие американца Чарлза Гудьира, позволившее устранить эти недостатки плащевого материала? В 1839 году американский изобретатель Чарлз Гудьир открыл процесс вулканизации, который заключался в «сшивании» молекул каучука в единую пространственную трехмерную сетку с помощью серы, благодаря чему каучук становился сильнее и эластичнее, уменьшилась его растворимость.
- Бутадиеновый каучук: формула, способы получения, свойства и применение
- Немного истории
- Необходимость синтезирования каучука
- Виды искусственного каучука
- Как делают
- Исходное вещество
- Физические характеристики
- Разновидности
- Бутадиеновый каучук: формула
- Способ получения нестереорегуляторного каучука СКВ
- Как маркируется СКВ
- Синтез стереорегуляторного материала
- Сферы использования
- Как получают резину
- 1) 1, 4 дибромбутен — 2 — — 1, 4 дибромбутан — — циклобутан 2) карбид алюминия — — метан — — ацетилен — — этилен — — этанол — — дивинил — — — 1, 2, 3, 4 тетрабромбутан — написать уравнения реакций с п?
- Запишите уравнения реакций, с помощью которых можно осуществить следующие превращения : а) этилен→ этанол→ этаналь ; б) этанол→ этилен→ этиленгликоль?
- ОСУЩЕСТВИТЕ ПРЕВРАЩЕНИЯ1)хлор — хлороводород — хлорэтан — этанол — этилен2)метан — хлорметан — метанол — метаналь — метанол — диметиловый зфир3)метан — ацетилен — уксусный альдегид — этанол — этилен -?
- Составьте уравнение реакций, с помощью которых в нескольких стадий можно осуществить следующие синтезы : а) Карбид алюминия→Этанол?
- Напишите пожалуйста уравнения реакций , с помощью которых можно осуществить следующие превращения : Алюминий — Карбид алюминия — метан — ацетилен — бензол — циклогексан?
- Осуществить цепочку превращений : карбид кальция — — — ацетилен — — — этилен — — — — — этанол — — — — этилен?
- Напишите уравнения реакций, при помощи которых можно осуществить цепочку превращений веществ : Уголь — карбид алюминия — метан — метилхлорид?
- Метан — ацетилен — этилен — этиловый спирт — бутадиен — 1, 3 — бутадиеновый каучук?
- Напишите уравнение реакций, при помощи которых можно осуществить синтез метаналя из карбида алюминия?
- Составьте уравнения химических реакций, с помощью которых можно осуществить цепочку превращений, метан — углекислый газ — глюкоза — этанол — этилен?
- Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения : метан — ацетилен — этаналь — этанол — этилен — этаналь?
Бутадиеновый каучук: формула, способы получения, свойства и применение
Химической промышленностью в наше время производится несколько видов каучуков. Одним из самых востребованных при этом является бутадиеновый. Каучук этой разновидности имеет множество достоинств. Но конечно, есть у него и некоторые недостатки.
Немного истории
Натуральный каучук в Европу, как известно, был привезен из Америки Христофором Колумбом. Обнаружил это интересное вещество великий мореплаватель на острове Гаити. Местные индейцы делали из него плотные мячи для игр.
В первое время каучук в Европе, к сожалению, никого особо не заинтересовал. Однако позднее это вещество стало применяться довольно-таки широко. К примеру, во Франции из него делали подтяжки для штанов. В Англии с использованием каучука шили водонепроницаемые пальто.
В 1839 г. американский исследователь Чарльз Гурдер впервые сделал из этого материала резину. Хотя до этого изобретатель и пытался найти новые методы использования каучука, получилось у него это совершенно случайно. Однажды Гурдер чисто механически положил пластинку исследуемого материала на печку поверх уже находившегося там куска серы. Так впервые и получился материал с интересными свойствами, в последующем названный резиной.
Необходимость синтезирования каучука
Добывают каучук в Америке из дерева гевеи. В Европе и России эта тропическая культура, к сожалению, не растет. Природных источников получения резины в Северном полушарии попросту нет. Именно поэтому в конце XIX — начале XX века в России и Европе встала острая потребность синтеза искусственного каучука для получения резины, которая к тому времени уже была широко распространена и использовалась повсеместно.
Виды искусственного каучука
Со временем было создано множество технологий получения этого нужного материала. Видов каучука на настоящий момент существует несколько. К примеру, химической промышленностью выпускаются такие его типы, как винилпиридиновый, фторсодержащий, вспененный, кремнийорганический. Но наиболее востребованным является все же бутадиеновый. Каучук именно этой разновидности и был когда-то впервые получен искусственно (в 1932 году группой инженеров под руководством А. Лебедева).
Как делают
Гевей в нашей стране нет. Однако для получения синтетического каучука также используются природные материалы. В основном это зерно и картофель. Сбраживая эти с/х продукты, получают этиловый спирт. Последний служит исходным сырьем при производстве такого вещества, как бутадиен-1.3. Для получения каучука этот компонент подвергают полимеризации.
Исходное вещество
Представляет собой 1.3-бутадиен бесцветный газ, формула которого выглядит следующим образом: СН2=СН—СН=СН2. По-другому его называют дивинил. По сути, бутадиен-1.3 — это ненасыщенный углеводород, представитель группы диеновых. Характерной особенностью этого газа, помимо всего прочего, является очень неприятный запах.
Полимеризация бутадиена для получения собственно каучука производится на стереоскопических катализаторах. Сама реакция протекает с присоединением молекул друг с другом в 1,4 или 1,2 положении.
Физические характеристики
Для синтеза конечного продукта применяют обычно содержащий более 99% основного вещества бутадиен. Бутадиеновый каучук же отличается такими техническими характеристиками:
вязкость по Муни — 30-35;
температура вулканизации — 140-160 С;
плотность — 900-920 кг/м;
основной агент вулканизации — сера;
наполнители при вулканизации — технический углерод;
пластификаторы — минеральные масла.
Разновидности
Подразделяется бутадиеновый каучук на два основных типа:
Первую разновидность материала выпускают в виде брикетов. Получают стереорегуляторные каучуки:
с помощью катализаторов Циглера-Натта (никелевого, кобальтового и титанового типов);
В молекулах таких каучуков имеется не менее 85% мономерных групп. Нестереорегуляторные материалы делают в присутствии щелочных металлов. Чаще всего это металлический натрий. Именно такой материал (СКВ) и был получен когда-то впервые А. Лебедевым.
Бутадиеновый каучук: формула
Получать этот материал можно, таким образом, с использованием разных катализаторов. Формула бутадиенового каучука выглядит в любом случае следующим образом:
nCH 2 = СН – СН = CH 2 ® (– СН 2 – СН = СН – СН 2 – ) n, где n может принимать значения в несколько тысяч.
Способ получения нестереорегуляторного каучука СКВ
Изготавливают такой материал, как уже упоминалось, путем полимеризации бутадиена в присутствии металлического натрия. Длится эта процедура несколько часов при давлении в 0.9 МПа и температуре 50-60 С.
Улучшают свойства полученного каучука путем дополнительной обработки в вакуумсмесителе для удаления летучих веществ. Далее к материалу добавляют стеариновую кислоту и противостаритель. На заключительном этапе каучук обрабатывают на рафинировочных пальцах. Это позволяет придать материалу большую однородность и очистить его от разного рода жестких ненужных включений.
В зависимости от того, какой будет выбран зазор на рафинированных пальцах, можно получить брикетированный или вальцованный каучук. Упаковывают полученный материал в прорезиненные мешки. Иногда последние также пропитывают нитролаком.
Как маркируется СКВ
Итак, как получить бутадиеновый каучук нестереорегуляторный, мы выяснили. Теперь давайте посмотрим, как маркируется эта разновидность материала. Пластичность получаемого методом полимеризации нестереорегуляторного каучука СКВ может варьироваться в пределах 0.1-0.66. Исходя из этого, и маркируется материал. К примеру, каучук 40 будет иметь пластичность 0.36-0.4. Также маркировка материала содержит такие сведения, как:
использованный способ полимеризации;
Буквы в маркировке материала обозначают:
с — стрежневая полимеризация;
к — брикетированный материал;
Из каучука СКВ, маркированного буквой «д», получают резины с повышенными диэлектрическими свойствами. Материал, на этикетке которого присутствует «э», предназначен для изготовления баллонных и эбонитовых изделий. Буква «щ» в маркировке каучука означает то, что его можно использовать для изготовления резины, соприкасающейся с пищевыми продуктами.
Синтез стереорегуляторного материала
Изначально разновидность СКВ использовалась очень широко. Однако с изобретением технологии изготовления стереорегуляторного каучука, применение ее значительно сократилось. Дело в том, что стереорегулятрный бутадиеновый каучук отличается большей эластичностью и имеет лучшие технические характеристики.
Совершенствование процессов изготовления материала привело к получению новых его форм с улучшенными свойствами. Стереорегуляторный бутадиеновый каучук — полимер, изготавливать который можно с использованием комплексных катализаторов (СКД) или литиевых (СКДЛ).
Делают такие материалы по непрерывной схеме и с минимальными затратами ручного труда. При производстве наиболее распространенной разновидности СКД полимеризация производится в специальной батарее в присутствии комплексного катализатора при температуре 25-30 С и давлении 1 МПа. Общее время изготовления каучука этой разновидности составляет 4-8 часов.
На одном из этапов материал дополнительно обрабатывается в вакуумоиспарителе. Здесь к полимеризату добавляется антиоксидант. Далее материал проходит процедуру водной дегазации. Остатки растворителя от каучука отделяют путем обработки паром.
Поставляются на рынок стереорегуляторные бутадиеновые каучуки обычно в брикетах по 30 кг, завернутых в полиэтиленовую пленку.
Сферы использования
Таким образом, имеет очень даже хорошие бутадиеновый каучук свойства. И применение его поэтому оправдано при изготовлении самой разной эластичной продукции. Каучуки нестереорегуляторные бутадиеновые чаще всего используются при производстве:
резин пищевых, морозостойких, кислотощелочестойких;
эбонитовых и асбестовых изделий.
Стереорегуляторные материалы этого типа используют при изготовлении:
шин для автомобилей;
подошв обуви и перчаток;
транспортерных лент для элеваторов, предприятий легкой и тяжелой промышленности;
изоляторов для электрических проводов и кабелей;
резиновых изделий с высокой динамичной износостойкостью;
К безусловным преимуществам этого каучука относят его нетоксичность и отсутствие неприятного запаха. Поэтому очень часто такой материал применяют также для изготовления изделий, используемых в медицине и пищевой промышленности.
Как получают резину
Чаще всего для производства этого материала используются стереорегуляторные каучуки. Для получения резины в них добавляют обычно, как уже упоминалось, технический углерод. Изготавливается резина методом вулканизации. Бутадиеновый каучук, формула которого была представлена выше, в сравнении с некоторыми другими разновидностями, имеет ряд недостатков:
низкую когезионную прочность;
плохую адгезию к металлу.
Резиновые смеси на их основе дают сильную усадку. Поэтому в процессе производства такой материал часто смешивают с изопреновыми, стирольными и другими видами каучуков.
1) 1, 4 дибромбутен — 2 — — 1, 4 дибромбутан — — циклобутан 2) карбид алюминия — — метан — — ацетилен — — этилен — — этанол — — дивинил — — — 1, 2, 3, 4 тетрабромбутан — написать уравнения реакций с п?
Химия | 10 — 11 классы
1) 1, 4 дибромбутен — 2 — — 1, 4 дибромбутан — — циклобутан 2) карбид алюминия — — метан — — ацетилен — — этилен — — этанол — — дивинил — — — 1, 2, 3, 4 тетрабромбутан — написать уравнения реакций с помощью которых можно осуществить синтезы : 1) бутадиенового каучука из метана 2) дивинилового каучука из карбида кальция 3) 1, 4 дибромбутана из этанола.
1) Br — CH2 — CH = CH — CH2 — Br — — — — — — — — > ; Br — CH2 — CH2 — CH2 — CH2 — Br — — — — — — — — > ; C6H12 Ni, t
Br — CH2 — CH = CH — CH2 — Br + H2 — — — — — — — — > ; Br — CH2 — CH2 — CH2 — CH2 — Br
Br — CH2 — CH2 — CH2 — CH2 — Br + Zn — — — — — — .
2) Al3C4 — — — > ; CH4 — — — > ; C2H2 — — — > ; C2H4 — — — > ; C2H5OH — — — > ; CH2 = CH — CH = CH2 — — — > ; — — — > ; Br — CH2 — CHBr — CHBr — CH2 — Br
Al4C3 + 12H2O — — — — — — — > ; 3CH4 + 4Al(OH)3 t
2CH4 — — — — — — — — — — — — — — > ; C2H2 + 3H2 Pt, t
C2H2 + H2 — — — — — — — — — — — — — > ; C2H4 Kt
C2H4 + H2O — — — — — — — — — — — — > ; C2H5OH t
2C2H5OH — — — — — — — — — — — — > ; CH2 = CH — CH = CH2 + 2H2O + H2
CH2 = CH — CH = CH2 + 2Br2 — — — — — — — — — — — — > ; Br — CH2 — CHBr — CHBr — CH2 — Br
2) CaC2 + 2H2O — — — — — — — > ; C2H2 + Ca(OH)2 t _
2C2H2 — — — — — — — — — — — — — — — — > ; HC = C — CH = CH3 _
HC = C — CH = CH3 + H2 — — — — — — — — > ; CH2 = CH — CH = CH2
3) 2C2H5OH — — — — — — — — — — — — > ; CH2 = CH — CH = CH2 + 2H2O + H2 CH2 = CH — CH = CH2 + 2HBr — — — — — — — — — — — — > ; Br — CH2 — CH2 — CH2 — CH2 — Br.
Запишите уравнения реакций, с помощью которых можно осуществить следующие превращения : а) этилен→ этанол→ этаналь ; б) этанол→ этилен→ этиленгликоль?
Запишите уравнения реакций, с помощью которых можно осуществить следующие превращения : а) этилен→ этанол→ этаналь ; б) этанол→ этилен→ этиленгликоль.
В) метан→ ацетилен→ бензол→ хлоробензол ; г) карбонат кальция→ оксид кальция→ карбид кальция→ ацетилен→ бензол→ нитробензол.
Помогите пжл) заранее спасибо.
ОСУЩЕСТВИТЕ ПРЕВРАЩЕНИЯ1)хлор — хлороводород — хлорэтан — этанол — этилен2)метан — хлорметан — метанол — метаналь — метанол — диметиловый зфир3)метан — ацетилен — уксусный альдегид — этанол — этилен -?
1)хлор — хлороводород — хлорэтан — этанол — этилен
2)метан — хлорметан — метанол — метаналь — метанол — диметиловый зфир
3)метан — ацетилен — уксусный альдегид — этанол — этилен — этан — хлорэтан — этанол — этаналь
4)карбид кальция → ацетилен→ бензол → хлорбензол → фенол → 2, 4, 6 — трибромфенол.
Составьте уравнение реакций, с помощью которых в нескольких стадий можно осуществить следующие синтезы : а) Карбид алюминия→Этанол?
Составьте уравнение реакций, с помощью которых в нескольких стадий можно осуществить следующие синтезы : а) Карбид алюминия→Этанол.
Напишите пожалуйста уравнения реакций , с помощью которых можно осуществить следующие превращения : Алюминий — Карбид алюминия — метан — ацетилен — бензол — циклогексан?
Напишите пожалуйста уравнения реакций , с помощью которых можно осуществить следующие превращения : Алюминий — Карбид алюминия — метан — ацетилен — бензол — циклогексан.
Осуществить цепочку превращений : карбид кальция — — — ацетилен — — — этилен — — — — — этанол — — — — этилен?
Осуществить цепочку превращений : карбид кальция — — — ацетилен — — — этилен — — — — — этанол — — — — этилен.
Напишите уравнения реакций, при помощи которых можно осуществить цепочку превращений веществ : Уголь — карбид алюминия — метан — метилхлорид?
Напишите уравнения реакций, при помощи которых можно осуществить цепочку превращений веществ : Уголь — карбид алюминия — метан — метилхлорид.
Метан — ацетилен — этилен — этиловый спирт — бутадиен — 1, 3 — бутадиеновый каучук?
Метан — ацетилен — этилен — этиловый спирт — бутадиен — 1, 3 — бутадиеновый каучук.
Напишите уравнение реакций, при помощи которых можно осуществить синтез метаналя из карбида алюминия?
Напишите уравнение реакций, при помощи которых можно осуществить синтез метаналя из карбида алюминия.
Составьте уравнения химических реакций, с помощью которых можно осуществить цепочку превращений, метан — углекислый газ — глюкоза — этанол — этилен?
Составьте уравнения химических реакций, с помощью которых можно осуществить цепочку превращений, метан — углекислый газ — глюкоза — этанол — этилен.
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения : метан — ацетилен — этаналь — этанол — этилен — этаналь?
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения : метан — ацетилен — этаналь — этанол — этилен — этаналь.
На этой странице сайта размещен вопрос 1) 1, 4 дибромбутен — 2 — — 1, 4 дибромбутан — — циклобутан 2) карбид алюминия — — метан — — ацетилен — — этилен — — этанол — — дивинил — — — 1, 2, 3, 4 тетрабромбутан — написать уравнения реакций с п? из категории Химия с правильным ответом на него. Уровень сложности вопроса соответствует знаниям учеников 10 — 11 классов. Здесь же находятся ответы по заданному поиску, которые вы найдете с помощью автоматической системы. Одновременно с ответом на ваш вопрос показаны другие, похожие варианты по заданной теме. На этой странице можно обсудить все варианты ответов с другими пользователями сайта и получить от них наиболее полную подсказку.
Дано m(ppa NaOH) = 200 g W(NaOH) = 2% m(ppa HCL) = 100 g W(HCL) = 4% — — — — — — — — — — — — — — — — — — — — — — — — — — — m(NaCL) — ? M(NaOH) = 200 * 2% / 100% = 4 g m(HCL) = 100 * 4% / 100% = 4g M(NaOH) = 40 g / mol n(NaOH) = m / M = 4 / 40 = 0. ..
Решение находится на фото.
Да, потому что Ca является металлом , а к. О SO4 не металл.
36 + 10 = 56 г 55 разделить 5 = 11.
А) 3 молекулы воды б) 2 молекулы диоксида углерода в) 5 молекул карбоната кальция г) 3 молекулы серной кислоты д) 4 молекулы хлорида натрия.
Ответ навариант 1, задание первое находится на фото.
Магний находится во 2 группе 3 пириода.
Третьем, второй, главной.
N = 220 / 44 = 5 V = n * Vm V = 5 * 22, 4 = 112.
1) n(AgNO3) = c(AgNO3) * V(раствора) = 0. 25 * 0. 02 = 0. 005 моль2) m(AgNO3) = M(AgNO3) * n(AgNO3) = 0. 005 * 170 = 0. 85гОтвет : 0. 85 гAgNO3.