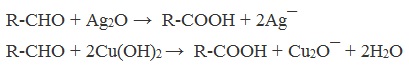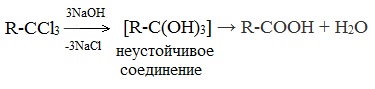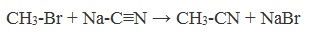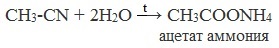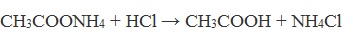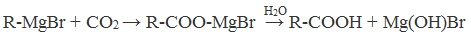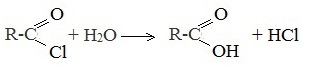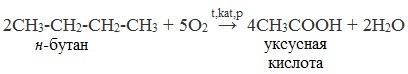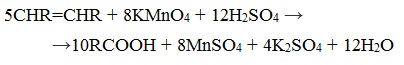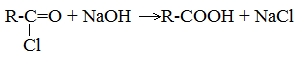FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 1
Какие вещества называют карбоновыми кислотами?
Карбоновыми кислотами называют органические вещества, содержащие в молекуле карбоксильную группу, связанную с углеводородным радикалом.
Приведите формулы и названия пяти представителей гомологического ряда предельных одноосновных карбоновых кислот.
Метановая (муравьиная) кислота H―COOH,
этановая (уксусная) кислота CH3―COOH,
пропановая (пропионовая) кислота CH3―CH2―COOH,
бутановая (маслянная) кислота CH3―CH2―CH2―COOH,
пентановая (валериановая) кислота CH3―CH2―CH2―CH2―COOH
Задание 2
Напишите формулы следующих кислот:
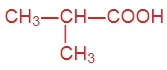 | 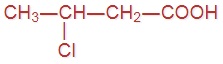 | 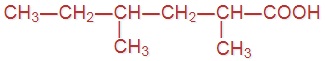 |
Задание 3
Молярная масса предельной одноосновной карбоновой кислоты равна 130 г/моль. Какова молекулярная формула этой кислоты. Дано:
Дано: M(CnH2n+1COOH)=130 г/моль
Найти: формула CnH2n+1COOH−?
Решение
По условию задачи M(CnH2n+1COOH)=130 г/моль, поэтому Mr(CnH2n+1COOH)=130
Mr(CnH2n+1COOH)=(n+1)•Ar(C)+(2n+2)•Ar(H)+2•Ar(O)=(n+1)•12+(2n+2)•1+2•16=12n+12+2n+2+32=14n+46
Составляем алгебраическое уравнение и решаем его:
14n+46=130
14n=130 — 46
14n=84
n=84 : 14
n=6, поэтому формула кислоты: C6H13COOH
Ответ: C6H13COOH
Задание 4
Какие признаки верно отражают свойства уксусной кислоты:
1) газообразное вещество;
2) без запаха;
3) с резким запахом;
4) плохо растворима в воде;
5) слабый электролит?
Задание 5
В пищевой промышленности уксусную кислоту используют как регулятор кислотности и консервант (код E260). Напишите структурные формулы предыдущего и последующего представителей данного гомологического ряда, имеющих коды E236 и E280 соответственно.
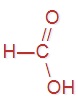 | 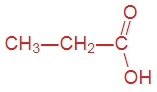 |
Напишите уравнение реакции получения каждой кислоты.
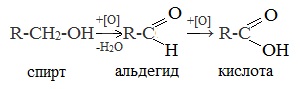
Во время кипячения спирта с окислителем спирт окисляется до карбоновой кислоты:
CH3OH + О2 t,кат. ⟶ HCOOH + H2O
C3H7OH + O2 t,кат. ⟶ C2H5COOH + H2O
Задание 6
В чём сходство и различие химических свойств неорганических и органических кислот? Ответ подтвердите уравнениями химических реакций.
Сходство.
1) Реагируют с активными металлами с образованием солей и выделением водорода:
Ca + 2HCl ⟶ CaCl2 + H2↑
Ca + 2CH3COOH ⟶ (CH3COO)2Ca + H2↑
2) Реагируют с оксидами металлов с образованием солей и воды:
MgO + 2HCl ⟶ MgCl2 + H2O
MgO + 2CH3COOH ⟶ (CH3COO)2Mg + H2O
3) Реагируют с основаниями с образованием солей и воды:
NaOH + HCl ⟶ NaCl + H2O
NaOH + CH3COOH ⟶ CH3COONa + H2O
4) Реагируют с солями, если в результате реакции выделяется газ, образуется осадок или слабый электролит:
CaCO3 + 2HCl ⟶ CaCl2 + H2O + CO2↑
CaCO3 + 2CH3COOH ⟶ (CH3COO)2Ca + H2O + CO2↑
Различие.
Карбоновые кислоты в присутствии концентрированной серной кислоты вступают во взаимодействие со спиртами, с образованием сложных эфиров (реакция этерификации):
CH3COOH + C2H5OH ⇄ CH3COOC2H5 + H2O (при H2SO4(конц.))
Задание 7
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
этан ⟶ хлорэтан ⟶ этиловый спирт ⟶ уксусный альдегид ⟶ уксусная кислота ⟶ ацетат калия и этиловый эфир уксусной кислоты.
C2H6 + Cl2 ⟶ C2H5Cl + HCl
C2H5Cl + NaOH ⟶ C2H5OH + NaCl
2C2H5OH + O2 t,кат. ⟶ 2CH3CHO + 2H2O
2CH3CHO + O2 кат. ⟶ 2CH3COOH
CH3COOH + KOH ⟶ CH3COOK + H2O
CH3COOH + C2H5OH ⇄ CH3COOC2H5 + H2O (при ⇄H2SO4(конц.))
Задание 8
Достаточно ли 100 г 66%-ного раствора уксусной кислоты для растворения 30 г карбоната кальция? Какая масса ацетата кальция при этом получится?
Дано: m(раствора)=100 г, ω(CH3COOH)=66%, m(CaCO3)=30 г
Найти: m ((CH3COO)2Ca)—?
Решение
1. Рассчитываем массу уксусной кислоты в растворе:
m( CH3COOH )=ω( CH3COOH )•m(раствора):100%=66%•100 г:100%=66 г
2. Количество вещества рассчитываем по формуле: n=m/M, где M ― молярная масса.
M( CH3COOH )=60 г/моль, M(CaCO3)=100 г/моль
n( CH3COOH )=m( CH3COOH )/M( CH3COOH )=66 г : 60г/моль=1,1 моль
n( CaCO3 )=m( CaCO3 )/M( CaCO3 )=30 г : 100 г/моль=0,3 моль
3. Составим химическое уравнение:
CaCO3 + 2CH3COOH ⟶ (CH3COO)2Ca + H2O + CO2↑
По уравнению реакции 1 моль карбоната кальция реагирует с 2 моль уксусной кислоты, поэтому с 0,3 моль карбоната кальция прореагирует в 2 раза больше количества вещества уксусной кислоты, то есть 0,6 моль. По условию задачи имеем 1,1 моль уксусной кислоты, следовательно кислота взята в избытке (её хватит), она реагирует не полностью, поэтому расчеты будем проводить по данным карбоната кальция.
По уравнению реакции количество вещества карбоната кальция и ацетата кальция одинаковое, поэтому:
n( (CH3COO)2Ca )=n( CH3COOH )=0,3 моль
4. Рассчитываем массу карбоната кальция количеством вещества 0,3 моль по формуле: m = n • M, где M ― молярная масса.
M ( (CH3COO)2Ca )=158 г/моль
m( (CH3COO)2Ca )=n ( (CH3COO)2Ca ) • M( (CH3COO)2Ca )=0,3 моль • 158 г/моль=47,4 г
Ответ: уксусной кислоты достаточно; получится 47,4 г ацетата кальция.
Задание 9
Почему жжение от ужаления муравья утихает, если потереть пострадавшее место нашатырным спиртом (водным раствором аммиака)?
Происходит нейтрализация муравьиной кислоты, которая вызывает жжение и содержится в составе жалящей жидкости, с аммиаком, содержашемся в составе нашатырного спирта:
HCOOH + NH3 ⟶ HCOONH4
Нашатырный спирт представляет собой водный раствор аммиака с массовой долей растворенного вещества 10%.
Задание 10
Докажите с помощью уравнений реакций, что муравьиная кислота может проявлять как свойства альдегидов, так и свойства кислот. Муравьиная кислота, в отличие от других карбоновых кислот, содержит альдегидную группу CНO, поэтому как и альдегиды, способна реагировать с аммиачным раствором оксида серебра (при этом происходит восстановление серебра) и со свежеполученным осадком гидроксида меди (II) при нагревании (при этом медь восстанавливается до одновалентной меди) :
HCOOH + Ag2O аммиачный р-р t → H2O + CO2 + 2Ag↓
HCOOH + 2Cu(OH)2 ⟶ Cu2O + CO2 + 3H2O
Задание 12
Есть ли у вас на кухне уксусная кислота? Какие правила техники безопасности необходимо соблюдать при её использовании? Почему?
С уксусной кислотой необходимо обращаться очень осторожно, т.к. её пары могут вызвать ожоги дыхательных путей и слизистых оболочек глаз.
- Acetyl
- Напишите уравнения реакций получения простейшей карбоновой кислоты hcooh из карбида алюминия
- Общие способы получения карбоновых кислот
- В промышленности
- В лаборатории
- Специфические способы получения важнейших кислот
- Please wait.
- We are checking your browser. gomolog.ru
- Why do I have to complete a CAPTCHA?
- What can I do to prevent this in the future?
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Напишите уравнения реакций получения простейшей карбоновой кислоты hcooh из карбида алюминияНекоторые карбоновые кислоты встречаются в природе в свободном состоянии (муравьиная, уксусная, масляная, валериановая и др.). Однако, основным источником карбоновых кислот является органический синтез. Рассмотрим основные способы получения карбоновых кислот Общие способы получения карбоновых кислот1. Окисление первичных спиртов и альдегидов под действием различных окислителей В качестве окислителей применяют KMnO4 и K2Cr2O7. Например: Для окисления альдегидов используются те же реагенты, что и для спиртов. При окислении перманганатом калия происходит обесцвечивание фиолетово-розового раствора. При окислении дихроматом калия — цвет меняется с оранжевого на зеленый. А также для них характерны реакции «серебряного зеркала» и окисление гидроксидом меди (II) – качественные реакции альдегидов: 2. Гидролиз галогензамещенных углеводородов, содержащих три атома галогена у одного атома углерода В результате реакции образуются спирты, содержащие три группы ОН у одного атома углерода. Такие спирты неустойчивы и отщепляют воду с образованием карбоновой кислоты: 3. Получение карбоновых кислот из цианидов (нитрилов) Этот способ позволяет наращивать углеродную цепь при получении исходного цианида. Дополнительный атом углерода вводят в состав молекулы, используя реакцию замещения галогена в молекуле галогенуглеводорода цианидом натрия: Образующийся нитрил уксусной кислоты CH3-CN (ацетонитрил, метилцианид) при нагревании гидролизуется с образованием ацетата аммония: При подкислении раствора выделяется кислота: 4. Использование реактива Гриньяра (по схеме) 5. Гидролиз галогенангидридов кислот С водой низшие хлорангидриды реагируют чрезвычайно энергично, образуя соответствующую карбоновую кислоту и соляную кислоту: В промышленности1. Выделяют из природных продуктов (жиров, восков, эфирных и растительных масел) 2. Окисление алканов кислородом воздуха ( в присутствии катализаторов – солей марганца или при нагревании под давлением) Обычно образуется смесь кислот. При окислении бутана единственным продуктом является уксусная кислота: 3. Окисление алкенов и алкинов При жестком окислении алкенов кипящим раствором KMnO4 в кислой среде происходит полный разрыв двойной связи: При жестком окислении (нагревание, концентрированные растворы, кислая среда) происходит расщепление углеродного скелета молекулы алкина по тройной связи и образуются карбоновые кислоты: 4. Окисление гомологов бензола (получение бензойной кислоты) Для получения бензойной кислоты можно использовать окисление монозамещенных гомологов бензола кислым раствором перманганата калия: В лаборатории1. Гидролиз сложных эфиров При кислотном гидролизе получают карбоновые кислоты и спирты (реакция обратная этерификации): 2. Из солей карбоновых кислот 3. Гидролиз ангидридов кислот При легком нагревании с водой ангидриды образуют соответствующие карбоновые кислоты: 4. Щелочной гидролиз галоген производных карбоновых кислот Специфические способы получения важнейших кислотСпособы получения НСООН 1. Взаимодействие оксида углерода (II) с гидроксидом натрия Муравьиную кислоту получают нагреванием под давлением гидроксида натрия и оксида углерода (II) под давлением и обработкой полученного формиата натрия серной кислотой: 2. Каталитическое окисление метана 3. Декарбоксилирование щавелевой кислоты Муравьиную кислоту можно получить при нагревании щавелевой кислоты: Способы получения СН3СООН Получение уксусной кислоты для химических целей 1. Синтез из ацетилена Данный способ получения уксусной кислоты основан на окислении уксусного альдегида, который в свою очередь получают из ацетилена по реакции Кучерова (ацетилен получают из очень доступного сырья — метана): 2. Каталитическое окисление бутана Большое значение имеет способ получения уксусной кислоты, основанный на окислении бутана кислородом воздуха: Процесс получения уксусной кислоты из метана является многостадийным (метан – ацетилен – уксусный альдегид – уксусная кислота). Ее получение окислениям будана сокращает число стадий, что дает большой экономический эффект. 3. Каталитическое карбонилирование метанола Получение уксусной кислоты для пищевых целей 4. Уксуснокислое брожение этанола Уксусную кислоту для пищевых целей получают уксуснокислым брожением жидкостей, содержащих спирт (вино. пиво): Please wait.We are checking your browser. gomolog.ruWhy do I have to complete a CAPTCHA?Completing the CAPTCHA proves you are a human and gives you temporary access to the web property. What can I do to prevent this in the future?If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware. If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices. Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store. Cloudflare Ray ID: 708ac9067b689734 • Your IP : 178.45.22.152 • Performance & security by Cloudflare |