Общее название жиров – триацилглицерины (триглицериды).
Существует несколько способов назвать молекулу жира.
Например, жир, образованный тремя остатками стеариновой кислоты, будет иметь следующие названия:
- Физические свойства жиров
- Химические свойства жиров
- 1.1. Кислотный гидролиз
- 1.2. Щелочной гидролиз — омыление жиров
- 2. Гидрирование (гидрогенизация) ненасыщенных жиров
- 3. Мыло и синтетические моющие средства
- ХИМИЧЕСКИЕ СВОЙСТВА ТРИГЛИЦЕРИДОВ
- Напишите уравнения реакций гидролиза жира триглицерида в кислой среде щелочной среде
- 🔍 Видео
Видео:Все реакции гидролиза в ЕГЭ за 2 часа | Химия ЕГЭ 2022 | УмскулСкачать

Физические свойства жиров
Жиры растворимы в органических растворителях и нерастворимы в воде. С водой жиры не смешиваются.
| Животные жиры — предельные | Растительные жиры (масла) — непредельные |
| Твёрдые, образованы предельными кислотами – стеариновой и пальмитиновой. Все животные жиры, кроме рыбьего – твёрдые. | Жидкие, образованы непредельными кислотами – олеиновой, линолевой и другими. Все растительные жиры, кроме пальмового масла – жидкие. |
Видео:Гидролиз солей. 9 класс.Скачать

Химические свойства жиров
1. Гидролиз (омыление) жиров
Жиры подвергаются гидролизу в кислой или щелочной среде или под действием ферментов.
1.1. Кислотный гидролиз
Под действием кислот жиры гидролизуются до глицерина и карбоновых кислот, которых входили в молекулу жира.
| Например, при гидролизе тристеарата глицерина в кислой среде образуется стеариновая кислота и глицерин |
1.2. Щелочной гидролиз — омыление жиров
При щелочном гидролизе жиров образуется глицерин и соли карбоновых кислот, входивших в состав жира.
| Например, при гидролизе тристеарата глицерина гидроксидом натрия образуется стеарат натрия . |
Видео:Гидролиз солей. 1 часть. 11 класс.Скачать

2. Гидрирование (гидрогенизация) ненасыщенных жиров
Гидрогенизация жиров — это процесс присоединения водорода к остаткам непредельных кислот, входящих в состав жира.
При этом остатки непредельных кислот переходят в остатки предельных, жидкие растительные жиры превращаются в твёрдые (маргарин).
| Например, триолеат глицерина при гидрировании превращается в тристеарат глицерина: |
| Количественной характеристикой степени ненасыщенности жиров служит йодное число, показывающее, какая масса йода может присоединиться по двойным связям к 100 г жира. |
Видео:РЕАКЦИИ ИОННОГО ОБМЕНА, ИОННОЕ УРАВНЕНИЕ - Урок Химия 9 класс / Подготовка к ЕГЭ по ХимииСкачать

3. Мыло и синтетические моющие средства
При щелочном гидролизе жиров образуются мыла – соли высших жирных кислот.
Стеарат натрия – твёрдое мыло.
Стеарат калия – жидкое мыло.
Моющая способность мыла зависит от жесткости воды. Оно хорошо мылится и стирает в мягкой воде, плохо стирает в жёсткой воде и совсем не стирает в морской воде, так как содержащие в ней ионы Ca 2+ и Mg 2+ образуют с высшими кислотами нерастворимые в воде соли.
| Например, стеарат глицерина взаимодействует с сульфатом кальция |
Поэтому наряду с мылом используют синтетические моющие средства.
Их производят из других веществ, например из алкилсульфатов — солей сложных эфиров высших спиртов и серной кислоты.
Спирт реагирует с серной кислотой с образованием алкилсульфата .
Далее алкилсульфат гидролизуется щелочью:
Эти соли содержат в молекуле от 12 до 14 углеродных атомов и обладают очень хорошими моющими свойствами. Кальциевые и магниевые соли этих веществ растворимы в воде, а потому такие мыла моют и в жесткой воде. Алкилсульфаты содержатся во многих стиральных порошках.
Видео:13.3. Сложные эфиры: Химические свойстваСкачать

ХИМИЧЕСКИЕ СВОЙСТВА ТРИГЛИЦЕРИДОВ
1. Гидролиз (омыление).
Данный процесс легко протекает при нагревании триглицеридов в растворе щелочей (щелочной гидролиз).
Соли высших жирных кислот называют мылами. Калиевые соли являются жидкими мылами, натриевые — твердыми водорастворимыми мылами. Аналогичные соли щелочноземельных (Са, ]М^) и тяжелых (Си, РЬ) металлов в воде нерастворимы. Водные растворы мыл имеют щелочную реакцию вследствие легкой гидролизуемости солей слабых жирных кислот со щелочными металлами:
Кроме того, водорастворимые мыла обладают свойствами поверхностно-активных веществ из-за амфифильности их молекул. Это определило широкое применение мыл в качестве детергентов. В жесткой воде, богатой ионами кальция, магния, моющие свойства мыла заметно снижаются вследствие образования водонерастворимых кальциевых и магниевых солей жирных кислот.
Появление первых порций мыл при щелочном гидролизе способствует эмульгированию жира, что увеличивает площадь соприкосновения жира со щелочью и обусловливает легкость протекания щелочного гидролиза триглицеридов.
Существует аналитическая характеристика пищевых жиров: число омыления, которое равно массе КОН (в мг), требуемого для нейтрализации при нагревании 1 г образца пищевого жира. Это количество щелочи затрачивается на нейтрализацию свободных жирных кислот, которые в небольшом количестве, как уже отмечалось, присутствуют в пищевых жирах, а также жирных кислот, освобождающихся в результате гидролиза триглицеридов. Количество мг КОН, затрачиваемое на нейтрализацию 1 г пищевого жира при комнатной температуре, называется кислотным числом. Оно отражает содержание в пищевом жире свободных жирных кислот, которые образуются в процессе спонтанного гидролиза триглицеридов. Разница между числом омыления и кислотным числом называется эфирным числом, оно отражает содержание в пищевом жире триглицеридов.
Кислотный гидролиз жира, приводящий к образованию свободных жирных кислот и глицерина, протекает трудно из-за нерастворимости жиров в воде, что затрудняет контакт реагента с субстратом.
2. Гидрогенизация жиров (присоединение водорода).
Очевидно, что в эту реакцию могут вступать только триглицериды, содержащие в своем составе остатки ненасыщенных жирных кислот. Именно по месту разрыва двойных связей происходит присоединение водорода (насыщение):
В результате этого процесса ненасыщенные смешанные триглицериды превращаются в насыщенные простые. Продукт этой реакции по сравнению с исходным жиром будет иметь более высокую температуру плавления. Данная реакция лежит в основе промышленного производства маргарина путем гидрогенизации относительно дешевых жидких растительных масел. Применяется она также и при производстве мыл. Гидрогенизированные жиры применяют в фармацевтической промышленности в качестве мазевой основы, поскольку они по сравнению с природными жирами более устойчивы к прогорканию.
В случае неполной гидрогенизации оставшиеся остатки ненасыщенных жирных кислот при нагревании претерпевают конформационную перестройку: природные цис-изомеры превращаются в транс-изомеры соответствующих кислот. В настоящее время доказано неблагоприятное действие на организм человека транс-изомеров ненасыщенных жирных кислот, которые могут оказаться в маргарине вследствие нарушений технологического процесса его производства.
3. Переэстерификация триацилглицеринов.
При нагревании триацилглицеринов в присутствии щелочи с низшими спиртами (метанолом, этанолом, глидерином) происходит перенос ацильных остатков с глицерина на эти спирты. Наибольшее практическое значение имеют метанолиз и глицеролиз триацилглицеринов.
При метанолизе образуются метиловые эфиры соответствующих жирных кислот, которые, в отличие от самих жирных кислот, являются летучими соединениями. Поэтому данная реакция может быть применена для подготовки липидов к анализу их жирнокислотного состава с помощью ГЖХ:
При проведении подобной реакции с глицерином образуется смесь моно- и диацилглицеринов, которые, в отличие от триацилглицеринов, обладают некоторой полярностью и применяются в качестве мазевой основы в фармации:
4. Перекисное окисление жиров.
Под действием активных форм кислорода триглицериды могут спонтанно подвергаться частичному окислению, особенно при наличии в их составе остатков ненасыщенных жирных кислот. Очевидно, что чем больше остатков таких жирных кислот содержится в составе триглицеридов, тем в большей степени они подвержены этому процессу. Активные формы кислорода образуются в результате неполного одно- или двухэлектронного восстановления его молекул. Это может быть инициировано, например, ультрафиолетовым или ионизирующим облучением, протеканием окислительно-восстановительных реакций, ионами металлов с переменной валентностью, высокой температурой и некоторыми другими факторами. Среди активных форм кислорода наиболее реакционноспособными являются радикальные частицы с неспаренным электроном, например гидроксильный радикал ОН». Этот радикал может атаковать остатки ненасыщенных жирных кислот по их метиленовым фрагментам -СН2-, расположенным по соседству с двойной связью, и отрывать от них радикал водорода Н». В результате этого гидроксильный радикал формирует молекулу воды, а из остатка жирной кислоты формируется относительно стабильный радикал аллильного типа:
На примере олеиновой кислоты этот процесс можно представить следующим образом:
Аллильный радикал далее взаимодействует с молекулярным кислородом с образованием гидропероксидного радикала. Взаимодействие этого радикала с водой ведет к образованию нестабильной гидроперекиси, самопроизвольное разрушение которой приводит к разрыву углеродного скелета жирной кислоты и окислению концевых атомов углерода в образовавшихся фрагментах до альдегидной или даже до карбоксильной группы.
На каждой стадии этого процесса образуются активные частицы, инициирующие протекание последующих стадий, поэтому перекисное окисление жирных кислот носит цепной характер.
Гидроксильный радикал также может атаковать атом углерода метиленового фрагмента и с другой стороны от двойной связи (Сп). Очевидно, что в этом случае будут образовываться несколько иные продукты окислительной деградации жирной кислоты.
Отчасти схожий в химическом плане процесс протекает с липидами тканей человека и называется перекисным окислением липидов (ПОЛ). ПОЛ имеет очень большое значение, как в норме, так и при развитии различных патологических состояний. Его протекание в норме с очень малой интенсивностью обусловлено наличием в тканях человеческого организма мощных систем антиокислитель- ной защиты, включающих как специальные ферменты (супероксиддисмутаза, каталаза и др.), так и низкомолекулярные вещества (а-токоферол, витамин С, мочевая кислота, глютатион). В настоящее время установлено, что активация перекисного окисления липидов мембран имеет место при развитии самых различных патологических состояний, является важным фактором старения организма человека. Довольно часто в лечебной практике находят применение лекарственные препараты с антиоксидантным действием. Вместе с тем в последнее время появляются научные сообщения, которые ставят под сомнение однозначную целесообразность применения антиоксидантов с профилактической и лечебной целями.
Аналогичный процесс может быть также причиной окислительной полимеризации растительных масел, богатых ненасыщенными жирными кислотами. В результате происходит их «высыхание», что определило, например, применение льняного масла для изготовления олифы.
5. Прогоркание жиров.
Прогорканием называют появление у жиров неприятных органолептических свойств (вкуса, запаха) при их хранении в условиях доступа кислорода воздуха, воды и света. Причиной этого могут быть перекисное окисление остатков ненасыщенных жирных кислот, а также гидролиз триглицеридов. «Вклад» этих процессов для различных пищевых жиров неодинаков. Например, растительные масла, богатые полиненасыщенными длинноцепочечными жирными кислотами (льняное, подсолнечное, оливковое масла), прогоркают преимущественно вследствие пе- рекисной деградации остатков этих кислот. Тогда как процесс прогоркания сливочного масла, которое практически не содержит в своем составе ненасыщенных жирных кислот, но богато короткоцепочечными жирными кислотами (например, масляной кислотой), обусловлен его гидролизом. В результате этих процессов в пищевых жирах появляются свободные короткоцепочечные жирные кислоты, альдегиды, альдегидокислоты, которые имеют неприятные вкус и запах и делают жиры непригодными для употребления в пищу.
Видео:Ступенчатый гидролиз солей по аниону. Решаем примеры.Скачать

Напишите уравнения реакций гидролиза жира триглицерида в кислой среде щелочной среде
Жиры — органические соединения, по строению являющиеся сложными эфирами трехатомного спирта глицерина и высших карбоновых (жирных) кислот.
К жирным кислотам (их формулы лучше выучить 😉 относятся:
- Пальмитиновая — C15H31COOH (предельная)
- Стеариновая — C17H35COOH (предельная)
- Олеиновая — C17H33COOH (непредельная, 1 двойная связь в радикале)
- Линолевая — C17H31COOH (непредельная, 2 двойные связи в радикале)
- Линоленовая — C17H29COOH (непредельная, 3 двойные связи в радикале)
Растительные и животные жиры
Жиры образуются в организме растений и животных, служат запасным питательным веществом. В строении растительных и животных жиров есть некоторые важные отличия.
Заметьте, что растительные жиры чаще жидкие и в них входят преимущественно остатки непредельных жирных кислот, а животные жиры — твердые и содержат остатки предельных жирных кислот.
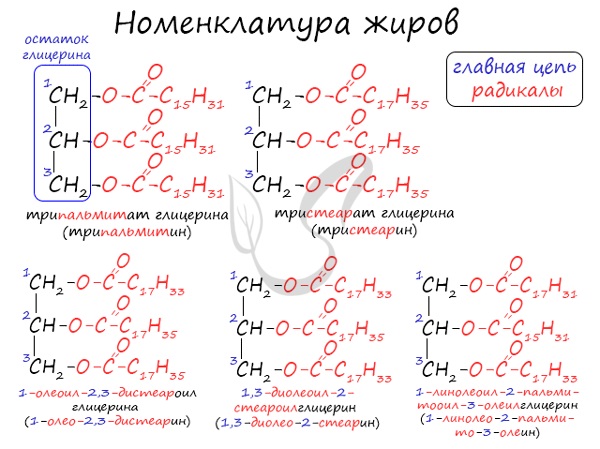
Номенклатура жиров
По систематической номенклатуре жиры принято называть триацилглицеринами. Названия жирам дают в зависимости от ацилов — остатков жирных кислот, входящих в их состав. Для формирования единого названия к остаткам кислот добавляют суффикс «оил».
В соответствии с тривиальной номенклатурой, жиры называют, добавляя окончание «ин» к названию кислоты и приставку, указывая, сколько гидроксогрупп в молекуле глицерина подверглось этерификации. В общем лучше 1 раз увидеть, чем 100 раз услышать 😉
Получение жиров
Жиры (по строению сложные эфиры) получаются в реакции этерификации, протекающей между трехатомным спиртом глицерином и высшими карбоновыми (жирными) кислотами.
В зависимости от того, какие именно кислоты участвуют в реакции, образуются различные жиры.
Химические свойства жиров
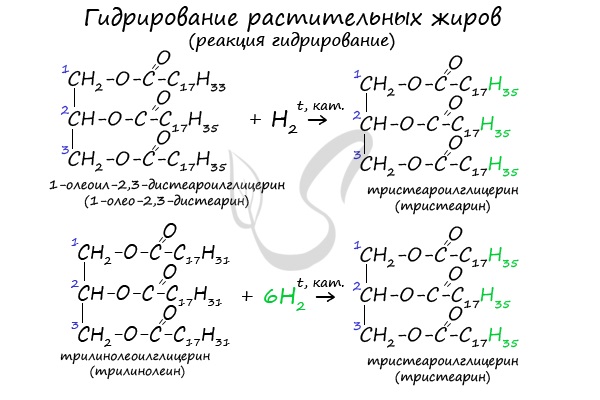
- Гидрирование растительных жиров
В состав растительных жиров входят непредельные кислоты, которые поддаются гидрированию и превращаются в предельные. Таким путем в пищевой промышленности получают маргарин.
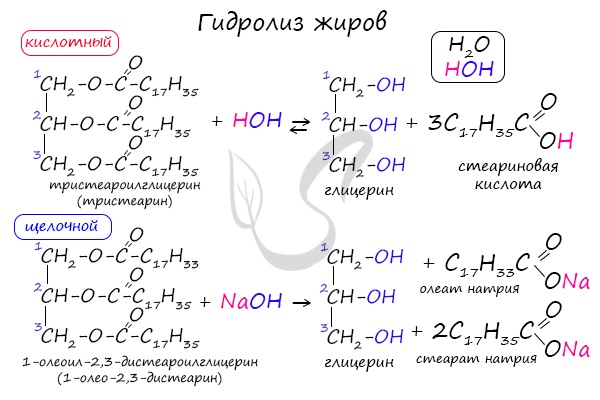
Как сложные эфиры, жиры способны вступать в реакцию гидролиза, который может быть кислотным и щелочным. В результате кислотного гидролиза образуется глицерин и исходные жирные кислоты, в результате щелочного гидролиза — глицерин и соли жирных кислот.
Реакция щелочного гидролиза жиров называется реакцией омыления, в результате получаются соли жирных кислот — мыла. Кислотный гидролиз протекает обратимо, щелочной — необратимо.
В состав твердого мыла входят соли Na, в состав жидкого — K.
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
🔍 Видео
Летучка: все реакции гидролиза | Химия ЕГЭ 2023 | УмскулСкачать

ГИДРОЛИЗ СОЛЕЙ | 9 класс | Кратко и понятноСкачать

11 класс. Гидролиз солей.Скачать

Химия 9 класс (Урок№8 - Гидролиз солей.)Скачать

Жиры. 1 часть. 11 класс.Скачать

Химические уравнения // Как Составлять Уравнения Реакций // Химия 9 классСкачать

Химия 10 класс (Урок№9 - Жиры. Моющие средства.)Скачать

Как рассчитать объём гидроаккумулятора / Water hydraulic accumulator volume estimationСкачать

Карбоновые кислотыСкачать

48. Сложные эфиры. Жиры. Мыла (часть 2)Скачать

Ионные уравнения реакций. Как составлять полные и сокращенные уравненияСкачать

Необратимый гидролиз. Примеры уравнений с объяснением.Скачать

ЕГЭ по химии: гидролизСкачать

Ревматоидный факторСкачать