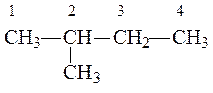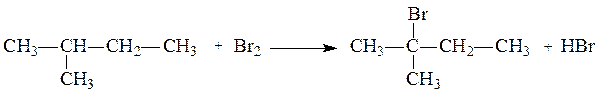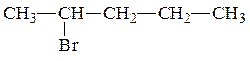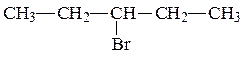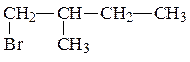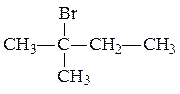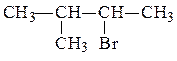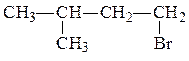«Визитной карточкой» углеводородов с малыми циклами является низкая устойчивость: для них характерны реакции присоединения водорода, галогенов и галогеноводородов, приводящие к размыканию цикла. Наиболее легко эти реакции протекают с участием циклопропана:
Циклобутан вступает в аналогичные реакции, но в более жестких условиях. Его гидрирование начинается при температуре около 180 о С:
Галогенирование и гидрогалогенирование циклобутана протекают при нагревании:
Склонность малых циклов, особенно циклопропана, к раскрытию и реакциям присоединения объясняют особенностями химических связей между атомами углерода в их молекулах. Рассмотрим в качестве примера строение молекулы циклопропана. Исходя из того, что трехчленный цикл является плоским равносторонним треугольником, валентные углы между атомами углерода должны быть равными 60 о , то есть существенно отличаться по величине от соответствующего sp 3 -гибридизации тетраэдрического угла. Такого сильного искажения валентного угла в действительности не происходит: электронные облака, связывающие атомы углерода, перекрываются не на прямой, соединяющей ядра, а вне ее (рис. 4). Поскольку в этом случае максимальная электронная плотность располагается вне линии, соединяющей ядра атомов, образовавшаяся связь приобретает частично ненасыщенный характер и становится похожей на π-связь в алкенах. Связи такого типа называют «банановыми».
Рисунок 4. Схема перекрывания электронных облаков в молекуле циклопропана (черными точками обозначены ядра атомов углерода).
Химические свойства циклоалканов с пятью и более атомами углерода в цикле
Циклоалканы с пятью и более атомами углерода в цикле по химическим свойствам практически не отличаются от алканов. Так, при их хлорировании происходит замещение атома водорода на галоген:
При действии разбавленной азотной кислоты при нагревании протекает реакция нитрования:
Характерной особенностью циклогексана и его гомологов является реакция дегидрирования с образованием ароматических углеводородов, которая протекает при пропускании их паров над никелем или платиной при температуре около 300 о С:
НАХОЖДЕНИЕ В ПРИРОДЕ И СПОСОБЫ ПОЛУЧЕНИЯ ЦИКЛОАЛКАНОВ
В природе наиболее распространены циклоалканы, содержащие наиболее устойчивые пяти- и шестичленные циклы. Они входят в состав нефти, а также содержатся в эфирных маслах некоторых растений.
Общим способом получения циклоалканов является действие активных металлов (натрия, лития, магния, цинка) на дигалогенпроизводные алканов. Так, циклопропан можно получить действием натрия на 1,3-дибромпропан, а циклопентан – действием магния на 1,5-дибромпентан:
Циклогексан чаще всего получают гидрированием бензола в присутствии катализаторов. Эта реакция обратима (сравните с реакцией дегидрирования циклогексана). Чтобы сместить равновесие в сторону образования циклогексана, процесс ведут при повышенном давлении:
ЗАДАНИЯ ДЛЯ САМОСТОЯТЕЛЬНОЙ РАБОТЫ
1. Даны вещества:
| а) | 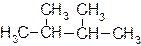 | в) |  |
| б) | 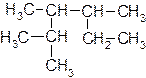 | г) |  |
Назовите каждое из веществ в соответствии с правилами номенклатуры ИЮПАК.
2. Даны вещества
| а) б) в) г) д) е) | 2,3,4-триметилпентан; 2,4-диметил-3-этилпентан; 2,2,4,4-тетраметилгексан 2-бром-3-метилпентан; 3,4-диэтил-2,5-дихлоргексан 3-нитро-3-этилпентан. |
Напишите структурные формулы этих веществ.
3. Алкан состава С7Н16 имеет девять изомеров (включая нормальный гептан). Напишите структурные формулы этих веществ и дайте им названия.
4. Напишите уравнения следующих реакций, указывая условия их протекания:
| а) б) в) | нитрования 2-метилбутана; ароматизации гексана; изомеризации пентана.* |
*В этой реакции образуется одновременно два изомера. При написании уравнения реакции достаточно в качестве продукта привести один из них.
5. Напишите уравнения реакций бромирования и хлорирования 2,3-диметилбутана. Сколько разных монохлорзамещенных продуктов образуется при хлорировании этого вещества?
6. Напишите уравнения реакций, позволяющих с помощью реакции Вюрца получить
7. Напишите структурные формулы всех алканов, образующихся при действии металлического натрия на смесь иодэтана и 2-иодпропана.
8. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
карбид алюминия → метан → бромметан → этан → нитроэтан.
9. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
бутан → изобутан → 2-бром-2-метилпропан.
10. Напишите уравнения реакций, с помощью которых можно получить 2,3-диметилбутан из пропана в две стадии.
11. Алкан, выделившийся на аноде при электролизе водного раствора пропионата натрия (CH3CH2COONa), пропустили над платиновым катализатором при температуре 300 о С. Какие продукты могли образоваться в результате? Напишите уравнения возможных реакций.
12. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
- Acetyl
- Химические свойства алканов на примере 2-метилбутана
- 1-е задание. Изомеры гептана
- 2-е задание. Гомологи 2-метил-3-этилгептана
- 3-е задание. Получение бутана
- 1. Реакция Вюрца
- 4-е задание. Химические реакции характерные для алканов на примере 2-метилбутана.
- 4) Реакции окисления.
- а) Горение (окисление кислородом воздуха при высоких температурах):
- 7) Реакции отщепления
- 8) Изомеризация алканов
- Примеры решения задач. Пример 1.Составьте уравнение реакции бромирования 2-метилбутана
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Химические свойства алканов на примере 2-метилбутанаЗадача 122. 1-е задание. Изомеры гептана2-е задание. Гомологи 2-метил-3-этилгептанаГомологи — это химические соединения, имеющие структурную формулу одного типа, например: алканы, алкены, алкины, и т. д. 2-метил-3-этилгептан (изомер декана) относится к гомологическому ряду алканов : метан, этан, пропан, бутан, пентан, гексан, гептан, октан, нонан, декан — это только первые десять, они газы. Примеры гомологов: 3-е задание. Получение бутана1. Реакция Вюрца2. Гидрирование бутина.Первоначально 1-бутин гидрируют до 1-бутена, а затем 1-бутен вторично гидрируют до бутана: CH3-CH2-C СН3—СН2-C 3. Дегидратация бутилового спиртаДегидратацию бутилового спирта проводят в присутствии Al2O3 при температуре 300-400 о C: Затем, полученный 1-бутен гидрируют по водородному радикалу до бутана: 4. Получение из солей карбоновых кислот (реакция Дюма)При сплавлении безводных солей карбоновых кислот с щелочами получаются алканы, содержащие на один атом углерода меньше по сравнению с углеродной цепью исходных карбоновых кислот: 5. Метод Фишера-ТропшаСмесь угарного газа и водорода (синтез-газ) пропускают над катализатором при нагревании, получают: 6. Реакция Гриньяра7. Электролиз соли (реакция Кольбе)CH3-CH2-CH2-COONa + 2Н2О электролиз 8. Получение бутана из спиртаКатализатором служит LiAlH4: 4-е задание. Химические реакции характерные для алканов на примере |
|
При написании уравнений реакций предельных углеводородов, к которым относится исходный углеводород, следует знать, что для этих углеводородов характерными являются реакции замещения, причем в реакции замещения легче всего вступает водород у третичного атома углерода, затем у вторичного и труднее всего у первичного атома углерода. В данном случае, замещение идет у второго атома углерода, так как он третичный.
|
Составляем формулы изомеров для полученного галогенпроизводного углеводорода. Сначала записываем изомеры галогенпроизводных, у которых главная цепь атомов углерода содержит 5 углеродных атомов.
|
|
|
После этого записываем изомеры, содержащие в главной цепи 4 атома углерода.
|
|
|
|
Теперь записываем изомер, содержащий в главной цепи 3 атома углерода.
|
Пример 2.Какие продукты реакции образуется при нитровании 2,4-диметилпентана в условиях реакции Коновалова?
Решение задачи. При нитровании 2,5-диметилгексана в условиях реакции Коновалова (t=140 0 C, 14–20% раствор HNO3, повышенное давление) преимущественно образуется продукт замещения атома водорода при третичных атомах углерода С2 или С4. Поскольку молекула имеет ось симметрии, то продукт будет один – 2-нитро-2,4-диметилпентан. Побочными процессами, сопровождающими реакции нитрования, являются расщепление углеродной цепи (преимущественно рядом с разветвлением) и образование нитропроизводных с меньшим числом атомов углерода. Чем длиннее цепь алкана и выше температура, тем интенсивнее протекает этот процесс. В данной задаче таких продуктов не будет: они образуются при парофазном нитровании алканов (t = 300 о C)
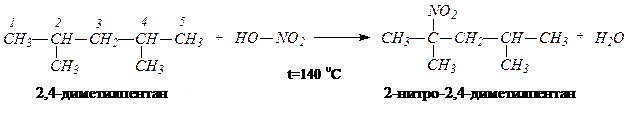 |
Пример 3.Получите 3,4-диметилгексан из галогенпроизводных алканов по реакции Вюрца, без образования побочных продуктов.
Решение задачи. Для синтеза вещества по его формуле необходимо:
а) записать структурную формулу получаемого соединения;
б) обдумать направления синтеза;
в) написать формулы исходных веществ;
г) написать уравнения реакций.
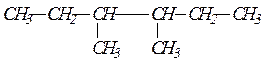 |
По названию вещества записываем формулу получаемого предельного углеводорода:
Получение алканов из галогенопроизводных по реакции Вюрца производится при взаимодействии двух галогенопроизводных с меньшим числом углеродных атомов, чем в синтезируемом соединении, в присутствии металлического натрия. Для выбора подходящих галогенпроизводных нужно разделить формулу алкана на два любых фрагмента, которые в месте разъединения должны соединяться с атомами галогена. В смеси двух галогенпроизводных с металлическим натрием реакция может проходить между двумя различными по строению галогенпроизводными и двумя парами одинаковых галогенпроизводных. В результате в первом случае образуются три алкана — один основной и два побочных. По условию задачи, для получения алкана без образования побочных продуктов, нужно разделить исходный углеводород на два одинаковых фрагмента, которые образуют одно галогенпроизводное. Такое возможно только для симметричных алканов. Искомый углеводород симметричен и мы его делим таким образом:
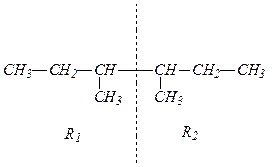 |
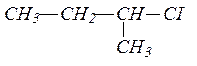
|
Уравнение реакции Вюрца имеет вид:
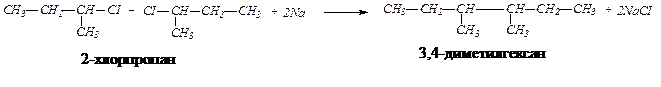 |
Пример 4.Используя необходимые органические и неорганические реагенты, синтезируйте бутин-1 из бутанола-1.
Решение задачи. Запишем структурные формулы исходного соединения и конечного продукта:
|
|
На первой стадии проведем внутримулекулярную дегидратацию спирта:
|
|
|
Далее, получим вицинальное дигалогенпроизводное, действуя на полученный алкен раствором брома в четыреххлористом углероде:
|
Для получения бутина-1 проведем реакцию элиминирования (отщепления двух молекул галогеноводорода — НBr), действуя на 1,2-дибромбутан спиртовым раствором щелочи:
|
|
В этом синтезе на первый взгляд кажется более простым превращение бутена-1 в бутин-1 путем дегидрирования. Однако при осуществлении дегидрирования алкенов всегда образуются алкадиены с сопряженными связями – как термодинамически более стабильные, чем алкины.
Пример 5.Напишите уравнение реакции взаимодействия пентадиена-1,3 с хлором при 40 0 С.

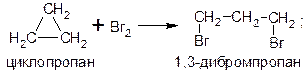
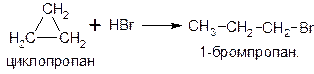






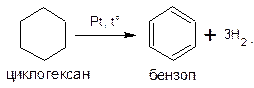
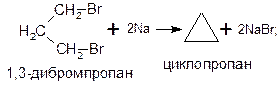
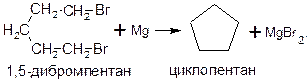



 СН ⇒ CH3-CH2-CH=CH2 ⇒ CH3-CH2-CH2-CH3 (Гидрирование по H2)
СН ⇒ CH3-CH2-CH=CH2 ⇒ CH3-CH2-CH2-CH3 (Гидрирование по H2) CH3-CH2-CH2-CH3 + 2СО2↑ + 2Н2↑ + 2NaOH
CH3-CH2-CH2-CH3 + 2СО2↑ + 2Н2↑ + 2NaOH 

 H3C–CH2–CH3 + CH2=CH2.
H3C–CH2–CH3 + CH2=CH2.