Химия | 10 — 11 классы
Написать уравнение гидролиза : Жира — тристеарата Укажите их биологическую роль.
CHOCOC17H35 + 3H2O = 3C17H35COOH + C3H5(OH)3
биологическую роль играют : запасающую, энергетическую, защитную.
- Гидролиз жиров в организме человека происходит преимуществено?
- Жиры, нейтральные жиры свойства, строение биологическая роль?
- Что образуется при гидролизе жиров?
- 1) основным компонентом некоторго жира является тристеарат, массовая доля которого составляет 80%?
- FeCl3 написать уравнение гидролиза?
- Какую массу жира необходимо взять для получения глицирина массой 250г?
- Помогите пожалуйста?
- Перечислить биологическое значение жиров?
- При гидролизе жиров могут образоваться?
- Написать уравнение гидролиза свиного жира?
- «Карбоновые кислоты» (стр. 3 )
- Напишите уравнение реакции гидролиза жира тристеарата глицерина назовите продукты реакции
Гидролиз жиров в организме человека происходит преимуществено?
Гидролиз жиров в организме человека происходит преимуществено.
Жиры, нейтральные жиры свойства, строение биологическая роль?
Жиры, нейтральные жиры свойства, строение биологическая роль.
Что образуется при гидролизе жиров?
Что образуется при гидролизе жиров.
1) основным компонентом некоторго жира является тристеарат, массовая доля которого составляет 80%?
1) основным компонентом некоторго жира является тристеарат, массовая доля которого составляет 80%.
Какие массы глицерина и стеариновой кислоты могут быть получены при омылении этого жира массой 72, 5 кг?
2)какая масса гидроксида калия и тристеарата потребуется для получения стеарата калия массой 500 кг, если выход продукта сост 80% из за производных потерь?
3) при гидролизе жира массой 222, 5 г получили предельную одноосновную карбоновую кислоту массой 213 г и глицерин.
Определите формулу жира.
FeCl3 написать уравнение гидролиза?
FeCl3 написать уравнение гидролиза.
Какую массу жира необходимо взять для получения глицирина массой 250г?
Какую массу жира необходимо взять для получения глицирина массой 250г.
, если условно принять, что жир представляет собой чистый тристеарат и что омылению подвергалось лишь 85 % жира?
Помогите пожалуйста?
Для всех жиров написать реакцию гидролиза, омыления и гидрирования если это возможно.
Перечислить биологическое значение жиров?
Перечислить биологическое значение жиров.
При гидролизе жиров могут образоваться?
При гидролизе жиров могут образоваться.
Написать уравнение гидролиза свиного жира?
Написать уравнение гидролиза свиного жира.
Назвать продукты гидролиза.
На этой странице вы найдете ответ на вопрос Написать уравнение гидролиза : Жира — тристеарата Укажите их биологическую роль?. Вопрос соответствует категории Химия и уровню подготовки учащихся 10 — 11 классов классов. Если ответ полностью не удовлетворяет критериям поиска, ниже можно ознакомиться с вариантами ответов других посетителей страницы или обсудить с ними интересующую тему. Здесь также можно воспользоваться «умным поиском», который покажет аналогичные вопросы в этой категории. Если ни один из предложенных ответов не подходит, попробуйте самостоятельно сформулировать вопрос иначе, нажав кнопку вверху страницы.
1. Ядро атома образовано положительно заряженными электронами 2. Положительный заряд ядра компенсируется отрицательными электронами. Их число всегда в атоме равно заряду ядра 3. Так как в ядре атома 12 протонов, то заряд ядра + 12 так как атом не ..
Ch4 + br2→ch3br + hbr Ch3br + ch3br→c2h5br + hbr C2h5br + ch3br→c3h7br + hbr.
1) 2 метилпентен 1 2) 3 метилпентен 2 3) 4 метилпентен 2 4) 3, 4 диметилгексен 1 5) 4, 5 диметилгексен 2.
1)3, потому что только это соединение диссоциируется(расворима) в воде с образованием OH 2)3, потому что только эта пара диссоциируется(растворима) в воде с образованием катиона Ba 3)4, потому что только эта пара диссоциируется(растворима) в воде с о..
Это 16 — S и 25 — марганец.
Може молекулярна маса оксиду = 230? Бо такого елементу нема якщо 5 група то формула оксиду R2O5 Ar(R) = (230 — (16 * 5)) / 2 = 75 елемент арсен.
Радуга в небе — — физическое явление (преломление света) мяч падает на землю — физич. — сила тяжести Вода кипит в чайнике — физ явление — туман на озере физ явление — испарение воды и конденсация егов воздухе подъем ртутного столбика в градуснике — ..
Считай по кислороду до реакции и после пред 3hno3 и перед 2no3.
CH3 — C(CH3)2 — C = C(C2H5) — CH2 — CH3 CH3 | CH3 — C — C = C — CH2 — CH3 | | CH3 C2H5.
Газ — иодоводород, HI Прекрасно растворяется в воде, образует сильную кислоту, диссоциирующую на два иона : HI = H( + ) + I( — ).
«Карбоновые кислоты» (стр. 3 )
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 |
а) 1,25, 6)1,5, в) 1,75, г) 2,0.
88***.При обработке смеси эквимолярных количеств предельной одноосновной кислоты и предельного одноатомного спирта, имеющих одинаковое число атомов углерода в молекуле, избытком раствора NaHCO3 выделился газ, объем которого в 4 раза меньше объема оксида углерода (IV), полученного при сжигании такого же количества смеси. Массовые доли кислоты и спирта в смеси составляют соответственно:
а) 54,32 и 45,68%, б) 55,22 и 44,78% ,
в) 56,60 и 43,40% , г) 58,97 и 41,03% .
89.Какие производные карбоновых кислот называются сложными эфирами? Дайте определение жиров. Что общего и в чем различие в строении этих групп органических веществ?
90*.Какие карбоновые кислоты могут входить в состав жиров? Каковы их формулы, названия, классификация по типу углеводородного радикала?
91.Что такое воск? Являются ли природные жиры и воски индивидуальными химическими веществами?
92.Назовите известные вам способы получения сложных эфиров. Приведите примеры реакций. Как называется реакция между карбоновой кислотой и спиртом?
93.Как физические свойства жиров зависят от природы углеводородного радикала, входящего в кислотный остаток?
94.Каким образом из жидких жиров (содержащих остатки непредельных кислот) можно получить твердые жиры? Как этот процесс используется в промышленности?
95.Напишите уравнение реакции гидролиза тристеарата глицерина. Назовите продукты реакции. Является ли эта реакция обратимой?
96. Равновесие в реакции гидролиза жиров можно полностью сместить вправо добавлением щелочи. Напишите уравнение реакции щелочного гидролиза тристеарата глицерина. Почему этот процесс называется омылением? Назовите области его промышленного применения.
97*. Почему мыло теряет свои моющие свойства в жесткой и морской воде? Как можно устранить жесткость воды?
98**. Чем с химической точки зрения отличаются синтетические моющие средства от мыла? Как их получают? Почему CMC не теряют моющих свойств в жесткой воде?
Работа 42. Сложные эфиры. Жиры

99.Укажите формулу сложного эфира:
100. Сколько изомерных карбоновых кислот и сложных эфиров соответствуют общей формуле С4Н8О2?

101.Химическое равновесие в системе
можно сместить вправо:
а) удалением воды, б) введением катализатора,
в) увеличением давления, г) увеличением температуры.
102.Соединение, какой структуры можно отнести к воскам?
а) СН3СООС16Н33, б) С15Н31СООС16Н33,
в) С15Н31СООС2Н5, г) СН2=СН—СООС3Н7.

вещество: формула:
исходные вещества: название реакции:

Допишите уравнения реакций.
105. В состав природных жиров не входит кислота:
а) щавелевая, б) стеариновая,
в) масляная, г) олеиновая.
106. Сколько изомеров имеет молекула жира, содержащая по одному остатку пальмитиновой, стеариновой и масляной кислот?
107.Какую массу триолеата глицерина необходимо подвергнуть гидролизу для получения 42,3 г олеиновой кислоты?
а) 14,7 г, б) 22,1 г, в) 44,2 г, г) 132,6 г.
108.Сколько граммов этилового эфира уксусной кислоты можно получить из 11,5 г
этанола и 30 г уксусной кислоты, если выход реакции составляет 80% от
а) 17,6 г, 6) 27,5 г, в) 35,2 г, г) 55,0 г.
109. Укажите формулу сложного эфира:
110.Сколько изомерных сложных эфиров имеют состав С4Н8О2?
Напишите их структурные формулы и назовите вещества.

можно сместить вправо:
а) увеличением температуры,
б) уменьшением давления,
в) использованием катализатора,
г) удалением воды.
4) сложные эфиры;
а)сложные эфиры глицерина и высших карбоновых кислот,
б)сложные эфиры высших карбоновых кислот и высших спиртов,
в)натриевые и калиевые соли высших карбоновых кислот,
г)производные карбоновых кислот, в которых атом водорода карбоксильной группы замещен на углеводородный радикал.

Укажите названия веществ 1—4:
а) тринитрат глицерина,
б) стеариновая кислота,
в) стеарат натрия,
Напишите уравнения реакций.
Допишите уравнения реакций.
115.Какое из веществ выпадает из общего ряда?
а) триолеат глицерина, б) тринитрат глицерина,
в) тристеарат глицерина, г) трипальмитат глицерина.
116.Сколько изомеров имеет сложный эфир глицерина, содержащий по одному остатку олеиновой, стеариновой и пальмитиновой кислот?
117. Какую массу глицерина можно получить из природного жира массой 17,75кг, содержащего 97% тристеарата глицерина?
а) 1,78 кг, 6) 1,84 кг, в) 1,90 кг, г) 2,26 кг.
118. Какая масса муравьиной кислоты и этилового спирта потребуется для получения 296 г сложного эфира, если выход этого продукта реакции составляет 80% от теоретического?
а) по 184 г, б) по 230 г,
в) по 288 г, г) 300 г кислоты, 230 г спирта
119*. Ананасовый ароматизатор напитков имеет формулу СН3—СН2—СН2—СООС2Н5.
Название этого сложного эфира:
г) верного ответа среди перечисленных нет.
120*. Исключите лишнее вещество:
а) стеарат натрия б) трипальмитат глицерина,
в) триолеат глицерина, г) тристеарат глицерина.
Обоснуйте свой выбор.
121*. Сложные эфиры плохо растворимы в воде и обладают меньшими температурами кипения по сравнению с изомерными им кислотами.
а) меньшая длина углеводородного радикала, связанного с карбоксильным атомом
б) отсутствие межмолекулярных водородных связей;
в) наличие атома углерода в sр2-гибридном состоянии;

122* Название вещества с формулой
в) метиловый эфир уксусной кислоты,
г) уксуснометиловый эфир,
д) все перечисленные ответы верны.
123. В основе процесса переработки жидких растительных масел в твердые жиры лежит реакция:
а) гидрирования, б) гидратации,

124*. В отличие от реакции этерификации
взаимодействие спиртов с ангидридами и
галогенангидридами карбоновых кислот необратима.
Для получения изоамилового эфира уксусной кислоты
(грушевая эссенция) необходимо взять:

д) синтетическое моющее средство.
126*. При сгорании 1 моль сложного эфира образуется по 4 моль оксида углерода (IV) и воды. Сколько изомерных сложных эфиров удовлетворяют условию этой задачи?
а) Один, б) два, в) три, г) четыре.
Напишите формулы изомеров и назовите эти вещества.
127*. Растительное масло (условно чистый триолеат глицерина) массой 1 т подвергли каталитическому гидрированию и получили саломас с выходом 90%. Сколько пачек маргарина по 250 г можно изготовить из этого количества саломаса, если его содержание в маргарине 80% ?
а) 4530, 6)4020, в) 3620, г) 3260.
128*. Органическое стекло получают полимеризацией метилового эфира 2- метилпропеновой кислоты. Элементарное звено полимера имеет относительную молекулярную массу:

129**. Эффективное средство для отпугивания комаров (репеллент) синтезируют по следующей схеме:

130**.Важнейшую роль в промышленности и быту играют полиэфиры — продукты этерификации дикарбоновых кислот двухатомными спиртами. Элементарное звено продукта поликонденсации терефталевой (1,4-бензолдикарбоновой) кислоты и этиленгликоля имеет формулу:
Как называется этот полимер?
131***. К 8,8 г 20%-ного раствора пропанола-2 в этиловом эфире уксусной кислоты добавили 50 мл раствора КОН с концентрацией 8 моль/л. Полученную смесь упарили, сухой остаток прокалили. Массы веществ в остатке после прокаливания составили:
а) 7,84 г СН3СООК; 17,92 г КОН,
б) 11,04 г К2СО3; 13,44 г КОН,
в) 2,87 г С3Н7ОК; 7,84 г СН3СООК; 16,28 г КОН,
г) 2,87 г С3Н7ОК; 7,84 г СН3СООК; 6,72 г С2Н5ОК; 11,80 г КОН.
Резервные задания к теме «Карбоновые кислоты»
Напишите уравнение реакции гидролиза жира тристеарата глицерина назовите продукты реакции
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 1
Какие вещества называют сложными эфирами?
Сложными эфирами называют производные карбоновых кислот, в которых атом водорода карбоксильной группы замещён углеводородным радикалом.
Как можно записать общую формулу жиров? 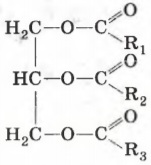
где R1, R2, R3 — радикалы, входящие в состав высших карбоновых кислот: масляной (―С3Н7), пальмитиновой ( ― С15Н31), стеариновой ( ― С17Н35), олеиновой ( ― С17Н33), линолевой ( ― С17Н31) и др.
Можно ли говорить о гомологических рядах жиров?
Нельзя, т.к. в состав жиров могут входить различные остатки как предельных, так и непредельных карбоновых кислот.
Задание 2
Что такое жиры?
Жиры ― это природные соединения, которые представляют собой сложные эфиры глицерина и высших карбоновых кислот.
Являются ли природные жиры индивидуальными химическими веществами?
Не являются, т.к. при выделении жиров получают и другие вещества.
Задание 3
Как физические свойства жиров зависят от природы углеводородного радикала, входящего в кислотный остаток?
В обычных условиях жиры, образованные остатками непредельных кислот, жидкие их называют еще маслами (кроме пальмового масла), а жиры, образованные остатками предельных кислот, твердые (кроме рыбьего жира).
Задание 4
Чему равна масса твёрдого мыла, полученного на основе 400 кг 40%-ного раствора гидроксида натрия и необходимого количества вещества тристеарата? Чему равно это количество?
Дано: m(раствора)=400 кг, ω( NaOH )=40%
Найти: m( C17H35COONa )-?
Решение
1-й способ
1. Рассчитываем массу гидроксида натрия в растворе:
m( NaOH )=ω( NaOH )•m(раствора):100%=40%•400 кг:100%=160 кг
2. Вычисляем к оличество вещества гидроксида натрия массой 160 кг по формуле: n=m/M, где M ― молярная масса.
Mr(NaOH)=40, поэтому M(NaOH)=40 кг/кмоль
n( NaOH )=m( NaOH )/M( NaOH )=160 кг : 40 кг/кмоль=4 кмоль
3. Составим химическое уравнение:
3NaOH + C3H5(C17H35COO)3 = C3H5(OH)3 + 3C17H35COONa
По уравнению реакции n ( NaOH ): n( C3H5(C17H35COO)3 ):n( C17H35COONa )=3:1:3 , поэтому
n( C3H5(C17H35COO)3 )= n( NaOH ):3=4 кмоль:3=1,33 кмоль
n( C17H35COONa )= n( NaOH )=4 кмоль
4. Вычисляем массу мыла к оличеством вещества 4 кмоль по формуле: m= n • M, где M ― молярная масса.
M( C17H35COONa )=306 кг/кмоль
m ( C17H35COONa )= n ( C17H35COONa ) • M( C17H35COONa )=4 кмоль • 306 кг/кмоль=1224 кг
2-й способ
1. Рассчитываем массу гидроксида натрия в растворе:
m( NaOH )=ω( NaOH )•m(раствора):100%=40%•400 кг:100%=160 кг
2. Составим химическое уравнение:
160 кг х кмоль у кг
3NaOH + C3H5(C17H35COO)3 = C3H5(OH)3 + 3C17H35COONa
120 кг 1 кмоль 918 кг
Над формулами соединений NaOH, C3H5(C17H35COO)3 и C17H35COONa записываем вычисленную массу гидроксида натрия (160 кг), неизвестные количество вещества тристеарата и массу мыла(х кмоль и у кг соответственно), а под формулами соединений ― массу соответствующего количества вещества и количество вещества согласно коэффициентам в химическом уравнении. Для этого вычисляем молярную массу веществ и, соответственно, массу 3 кмоль гидроксида натрия и 3 кмоль мыла, т.к. с 3 кмоль NaOH и 1 кмоль C3H5(C17H35COO)3 образуется 3 кмоль C17H35COONa .
M(NaOH)=40 кг/кмоль, масса 1 кмоль=40 кг, а масса 3 кмоль=120 кг
M(C17H35COONa)=306 кг/кмоль, масса 1 кмоль=306 кг, а масса 3 кмоль=918 кг
х=n( C3H5(C17H35COO)3 )=160 кг • 1 кмоль : 120 кг=1,33 кмоль
х= m ( C17H35COONa )=918 кг • 160 кг : 120 кг=1224 кг
Ответ: 1224 кг мыла и 1,33 кмоль тристеарата
Задание 5
Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
этиловый спирт ⟶ ацетальдегид ⟶ уксусная кислота ⟶ метиловый эфир уксусной кислоты ⟶ ацетат калия.
2C2H5OH + CuO ⟶ CH3CHO + Cu + H2O
CH3CHO + Ag2O ⟶ CH3COOH + 2Ag↓
CH3OH + CH3COOH ⇄ CH3COOCH3 + H2O
CH3COOCH3 + KOH ⟶ CH3COOK + CH3OH
Задание 6
У какого из обитателей морей толщина подкожного жира достигает 1 м? В китов.
У кого из морских млекопитающих самое жирное молоко (40% жира)? В дельфинов.
Объясните биологическую целесообразность данных явлений. В случае затруднения используйте Интернет.
Подкожный жировой слой выполняет несколько функций:
― защищает от переохлаждения (терморегуляция);
― создается энергетический запас;
― удерживается вода в организме;
― защита от механического воздействия;
― обеспечение плавучести.
Благодаря жирности молока его поверхностное натяжение в 30 раз больше, чем воды, что особенно важно, учитывая кормление под водой (струя молока не расплывается в воде) .













