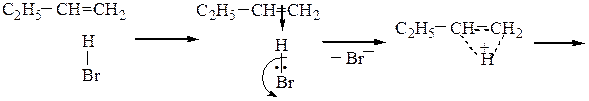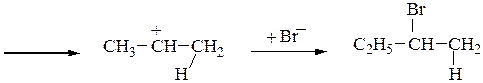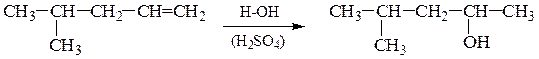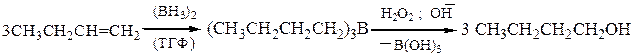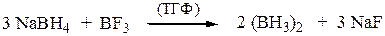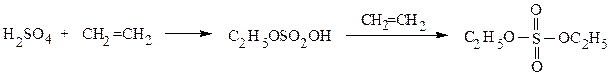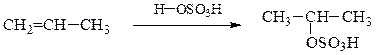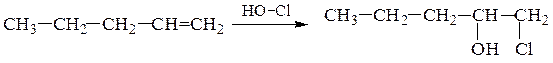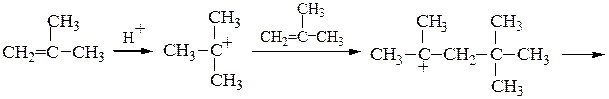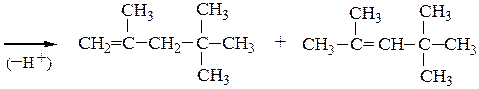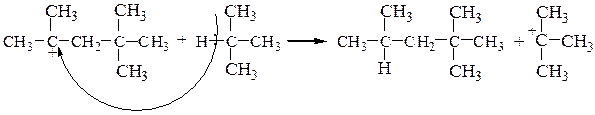Правило Марковникова — при присоединении галогеноводородов или воды к несимметричным алкенам или алкинам атом водорода присоединяется к наиболее гидрогенизированному (гидрированному) углеродному атому (т.е. к атому С, связанному с большим числом атомов Н), а атом галогена (или группа –ОН) – к наименее гидрогенизированному.
Правило, устанавливающее направление реакции присоединения галогеноводородов (гидрогалогенирование) и воды (гидратация), сформулировал русский химик В.В. Марковников в 1869 г.
Правило Марковникова о присоединении по двойной связи объясняется смещением электронной плотности в молекулах несимметричных алкенов.
Механизм присоединения по правилу Марковникова
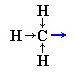
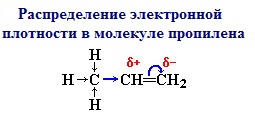
Электронная плотность в молекуле СН3-СН=СН2 до вступления в реакцию распределена неравномерно. Это обусловлено тем, что метильная группа СН3 за счет суммирования небольшой полярности трех С-Н-связей является донором электронов, т.е. проявляет +I-эффект ссылка по отношению к соседним атомам углерода.
Это вызывает смещение подвижности π-электронов двойной связи в сторону более гидрогенизированного атома углерода и появлению на нем частичного отрицательного заряда (δ-).
На другом, менее гидрогенизированном, атоме углерода возникает частичный положительный заряд (δ+). Поэтому атака электрофильной частицы Н+ происходит по более гидрогенизированному углеродному атому, а атом галогена или группа –ОН присоединяются к менее гидрогенизированному атому углерода.
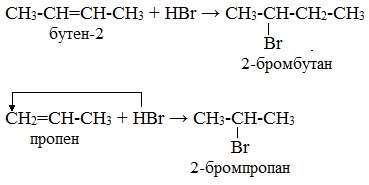
Например, гидробромирование бутена-2 и пропена:
Бутен-2 является симметричным алкеном, оба углеродных атома относительно двойной связи совершенно равноценны. В результате первой реакции образуется один продукт – 2-бромбутан.
Пропен – несимметричный алкен. Один углеродный атом при двойной связи более гидрогенизирован, т.е. содержит большее число атомов водорода. Поэтому продуктом реакции является 2-бромпропан.
Присоединение воды к несимметричным алкенам также происходит по правилу Марковникова.
Например, гидратация пропена и бутена-1:
В результате гидратации пропена образуется пропанол-2, а не пропанол-1. А в результате гидратации бутена-1 – бутанол-2, а не бутанол-1.
Если же в алкене присутствует электроноакцепторный заместитель, т.е. группа, обладающая способностью оттягивать на себя электронную плотность, более стабильным может оказаться первичный катион и реакция пойдет против правила Марковникова, например гидрогалогенирование трифторпропена.
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Электрофильное присоединение (АЕ) несимметричных полярныхреагентов к алкеном с разной степенью замещенности у атомов углерода при двойной связи протекает по правилу Марковникова: катионная часть реагента Х d + (обычно Н + ) присоединяется к более гидрогенизированному атому углерода, а анионная часть Y d — — ко второму, менее гидрогенизированному ненасыщенному С-атому: а) Гидрогалогенирование. Гидрогалогенирование алкенов чаще всего проводят по ионному (электрофильному) механизму. Схема протекания реакции АЕ на примере гидробромирования бутена-1 следующая: вторичный карбкатион устойчивей, Таким образом, правило Марковникова объясняется устойчивостью промежуточно образующихся в результате присоединения протона карбкатионов, которая уменьшается в ряду: третичный, вторичный, первичный. В присутствии пероксидов гидробромирование бутена-2 протекает по механизму радикального присоединения (AR) против правила Марковникова (эффект Хараша): вторичный радикал более устойчив, По механизму AR против правила Марковникова присоединяется только HBr, остальные галогеноводороды не реагируют по пероксидному эффекту:HCl имеет слишком полярную связь и не расщепляется гомолитически, а HI — сильный восстановитель, разрушающий пероксиды. Правило Марковникова также нарушается в случаях, когда электронная плотность двойной связи сильно деформирована за счет соседства с электроноакцепторной группой ( –СF3 , –CN, –COOH, –SO3H, –NO2 и др.). Так, при гидробромировании 3,3,3-трифторпропена-1, благодаря сильному электроноакцепторному влиянию трифторметильной группы образующийся первичный карбкатион CF3СН2СН2 + будет более устойчивым, чем вторичный CF3СH + CH3. Реакционная способность двойной связи будет ослаблена, а продукт не будет соответствовать правилу Марковникова: б) Гидратация (присоединение воды). Протекает по аналогичной схеме электрофильного присоединения (АЕ). В качестве катализаторов применяют H2SO4 , H3PO4 или кислоты Льюиса. Поскольку вода присоединяется по правилу Марковникова, то всегда продуктом реакции будут вторичные или третичные спирты (кроме случая гидратации этилена: CH2=CH2 + H2O ¾® CH3–CH2–OH этанол). Для получения первичных спиртов из алкенов используют метод гидроборирования-окисления, который служит примером присоединения воды по двойной связи, но в отличие от классической гидратации, присоединение к несимметричным алкенам происходит против правила Марковникова: Кроме того, гидроборирование-окисление осуществляется как цис— присоединение. Исходный диборан получают по реакции: в) Сульфатирование (сульфатация, О-сульфирование). Серная кислота присоединяется по двойной связи алкенов согласно правилу Марковникова, образуя моно- и диэфиры серной кислоты: этилсерная кислота диэтилсульфат кислый сульфат изопропилового спирта (изопропилсерная кислота) г)Гипохлорирование – взаимодействие алкенов с хлорноватистой кислотой HOCl, приводящее к хлоргидринам. Реакция также подчиняется правилу Марковникова: электрофильный хлор направляется к более гидрогенизированному атому углерода. Часто для получения хлоргидринов из алкенов в качестве реагентов используют хлор и воду. 4. Димеризация изобутилена протекает в присутствии H2SO4 при 80 0 С и дает смесь 2,4,4-триметилпентена-1 и 2,4,4-триметилпентена-2: 5. Алкилирование изобутилена изобутаном. Первые две стадии механизма реакции изобутилена с изобутаном совпадают со случаем димеризации изобутилена; образовавшийся катион вырывает атом водорода с его парой электронов из молекулы алкана, что приводит к 2,2,4-триметилпентану, а новый карбониевый ион продолжает цепь: Дата добавления: 2017-09-19 ; просмотров: 4271 ; ЗАКАЗАТЬ НАПИСАНИЕ РАБОТЫ |
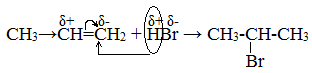
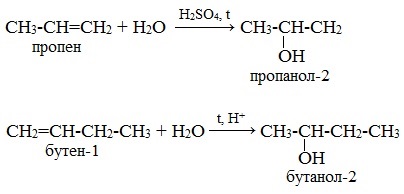
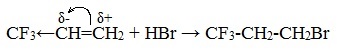

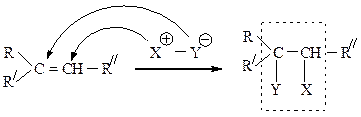
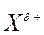 Н Н Н Н С1
Н Н Н Н С1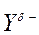 Br C1 ОН OSO3H ОН
Br C1 ОН OSO3H ОН