Задача 946.
Какие равновесия устанавливаются в водном растворе СО2? Как влияет повышение температуры раствора на смещение этих равновесий? Можно ли приготовить 1 н. раствор угольной кислоты?
Решение:
СО2 – кислотный оксид. Однако его кислотообразующие свойства выражены слабо.
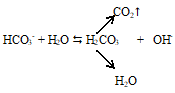
Равновенсие сильно смещено влево, Только одна молекула СО2 из шестисот превращается в угольную кислоту. Основная же масса растворённого в воде СО2 остаётся в молекулярном состоянии. Угольная кислота – очень слабая кислота. В водном растворе она диссоциирует главным образом на ионы Н + и НСО3 – и лишь в ничтожных количествах образуются ионы СО3 2- :
Угольная кислота может существовать только в водном растворе, поэтому приготовить её 1 н раствор просто практически невозможно. При нагревании раствора СО2 улетучивается, равновесие образования Н2СО3 смещается влево и, в конце концов, в растворе СО2 остаётся чистая вода.
Схема равновесия раствора СО2:
Задача 947.
Можно ли получить нейтральный раствор, прибавив к раствору угольной кислоты строго эквивалентное количество щелочи? Ответ мотивировать.
Решение:
При взаимодействии угольной кислоты и едкого натра в строго эквивалентных количествах протекает реакция:
При этом образуется гидрокарбонат натрия, который будет гидролизоваться по аниону:
В растворе будет находиться избыток ионов ОН – , которые будут придавать раствору слабощелочную среду, рН > 7.
Задача 948.
Почему при получении диоксида углерода из мрамора на последний действуют соляной кислотой, а не серной? Какой объем СО2 (условия нормальные) можно получить из 1 кг мрамора, содержащего 96% (масс.) СаСО3?
Решение:
а) При действии на карбонаты растворами кислот выделяется углекислый газ, например, при действии на карбонат кальция соляной или серной кислот:
Эти реакции можно использовать для получения в лабораторных условиях СО2. Обычно на мрамор действуют раствором соляной кислоты, а не серной, так как в первом случае образуется хорошо растворимая соль CaCl2, а во втором случае – малорастворимая СаSO4, пассивирующая действие кислоты на мрамор.
б) Расчет объёма углекислого газа при действии соляной кислоты на 1 кг мрамора:
Находим массу СаСО3 в мраморе:
M(CaCO3) = 1000 . 0,96 = 960 г.
Теперь рассчитаем объём СО2 из пропорции:
100 : 22,4 = 960 : х; х = (22,4 . 960)/100 = 215,04 л.
Лабораторная работа № 3
Читайте также:
|
| Изучите химию на странице ➔ решение заданий и задач по химии. |
| Похожие готовые решения: |
- Закончить уравнения реакций: NaCl+KClO3+H2SO4 → NaCrO2+Br2+NaOH→
- Опишите химическую связь в молекуле декана. Сколько s- и sp3-орбиталей участвуют в образовании σ-связей?
- Дать характеристику окислительно-восстановительных свойств диоксида серы и сернистой кислоты. Ответ подтвердить примерами
- Какой объем аммиака (условия нормальные) можно получить, подействовав двумя литрами 0,5 н. раствора щелочи на соль аммония?
Присылайте задания в любое время дня и ночи в ➔
Официальный сайт Брильёновой Натальи Валерьевны преподавателя кафедры информатики и электроники Екатеринбургского государственного института.
Все авторские права на размещённые материалы сохранены за правообладателями этих материалов. Любое коммерческое и/или иное использование кроме предварительного ознакомления материалов сайта natalibrilenova.ru запрещено. Публикация и распространение размещённых материалов не преследует за собой коммерческой и/или любой другой выгоды.
Сайт предназначен для облегчения образовательного путешествия студентам очникам и заочникам по вопросам обучения . Наталья Брильёнова не предлагает и не оказывает товары и услуги.
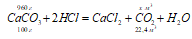
 H2CO3
H2CO3 Готовое решение: Заказ №8716
Готовое решение: Заказ №8716 Тип работы: Задача
Тип работы: Задача Статус: Выполнен (Зачтена преподавателем ВУЗа)
Статус: Выполнен (Зачтена преподавателем ВУЗа) Предмет: Химия
Предмет: Химия Дата выполнения: 22.09.2020
Дата выполнения: 22.09.2020 Цена: 228 руб.
Цена: 228 руб.
