Химия | 10 — 11 классы
Напишите уравнения реакций гидролиза нитрата меди ; хлорида калия ; сульфида натрия в ионном виде.
Укажите реакцию среды в растворах этих солей.
1)Cu(NO3)2 + 2HOH = 2HNO3 + Cu(OH)2
Cu2 + + 2NO3 — + 2H + + 2OH — = 2H + + 2NO3 — + Cu(OH)2
Cu2 + + 2OH — = Cu(OH)2
рН < ; 7 — среда кислая
pH = 7 — среда нейтральная
3)Na2S + 2HOH = 2NaOH + H2S
pH> ; 7 — среда щелочная
2Na + S2 — + 2H + + 2OH = 2Na + + 2OH + H2S
- Из данного перечня солей выберите соли, которые подвергаются в водных растворах гидролизу : сульфид натрия, нитрат цинка, сульфат калия, ацетат натрия?
- 1. С какими из перечисленных веществ взаимодействует (в растворе) карбо нат натрия : хлорид бария, нитрат серебра, гидроксид калия, азотная кислота, нитрат свинца (II)?
- Какую реакцию на индикатор имеют растворы солей : а) хлорида натрия, б) сульфата меди (II), в) сульфата калия, г) силиката натрия?
- С какими из перечисленных веществ взаимодействует хлорид меди 2 : нитрат бария нитрат серебра гидроксид калия серная кислота сульфид натрия?
- Какую среду имеют водный растворы солей : а) сульфата калия, карбоната калия, сульфида калия ; б) хлорида меди (2), нитрата меди(2) , сульфата алюминия?
- 1. Составьте молекулярные и ионные уравнения реакций гидролиза следующих солей : сульфида калия, хлорида цинка, карбоната аммония, сульфата меди (II)?
- С какими из перечисленных веществ взаимодействует хлорид меди 2 : нитрат бария нитрат серебра гидроксид калия серная кислота сульфид натрия?
- Помогите пожалуйста : ) какие из перечисленных солей подвергаются гидролизу при растворении в воде : хлорид калия, нитрат меди(II), сульфат лития, нитрат бария, сульфид натрия, хлорид железа (III)?
- Составьте молекулярные и ионные уравнения реакций гидролиза солей , укажите по возможности среду раствора соли :хлорида железа ||, фосфата калия?
- Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей: нитрат меди (II), сульфид калия
- Задание 1
Из данного перечня солей выберите соли, которые подвергаются в водных растворах гидролизу : сульфид натрия, нитрат цинка, сульфат калия, ацетат натрия?
Из данного перечня солей выберите соли, которые подвергаются в водных растворах гидролизу : сульфид натрия, нитрат цинка, сульфат калия, ацетат натрия.
Определите реакцию среды их водного раствора.
1. С какими из перечисленных веществ взаимодействует (в растворе) карбо нат натрия : хлорид бария, нитрат серебра, гидроксид калия, азотная кислота, нитрат свинца (II)?
1. С какими из перечисленных веществ взаимодействует (в растворе) карбо нат натрия : хлорид бария, нитрат серебра, гидроксид калия, азотная кислота, нитрат свинца (II)?
Напишите уравнения осуществимых реакций, составьте полные и краткие ионные уравнения.
2. Из данного перечня солей выберите соли, которые подвергаются в водных растворах гидролизу : хлорид кальция, нитрат аммония, сульфид аммония, сульфат калия, нитрат бария, хлорид железа(III).
Определите реакцию среды их водного раствора.
3. С какими из перечисленных веществ взаимодействует(в растворе) азотная кислота : сульфид калия, хлорид железа(III), гидроксид натрия, сульфат меди, фторид серебра.
Напишите уравнения практически осуществимых реакций.
Какую реакцию на индикатор имеют растворы солей : а) хлорида натрия, б) сульфата меди (II), в) сульфата калия, г) силиката натрия?
Какую реакцию на индикатор имеют растворы солей : а) хлорида натрия, б) сульфата меди (II), в) сульфата калия, г) силиката натрия?
Составьте ионное уравнение первой стадии гидролиза соли, раствор которой имеет щелочную среду.
С какими из перечисленных веществ взаимодействует хлорид меди 2 : нитрат бария нитрат серебра гидроксид калия серная кислота сульфид натрия?
С какими из перечисленных веществ взаимодействует хлорид меди 2 : нитрат бария нитрат серебра гидроксид калия серная кислота сульфид натрия?
Напишите уравнение реакций составьте ионные уравнения.
Какую среду имеют водный растворы солей : а) сульфата калия, карбоната калия, сульфида калия ; б) хлорида меди (2), нитрата меди(2) , сульфата алюминия?
Какую среду имеют водный растворы солей : а) сульфата калия, карбоната калия, сульфида калия ; б) хлорида меди (2), нитрата меди(2) , сульфата алюминия?
Напишите уравнение гидролиза.
1. Составьте молекулярные и ионные уравнения реакций гидролиза следующих солей : сульфида калия, хлорида цинка, карбоната аммония, сульфата меди (II)?
1. Составьте молекулярные и ионные уравнения реакций гидролиза следующих солей : сульфида калия, хлорида цинка, карбоната аммония, сульфата меди (II).
Укажите реакцию среды в растворах этих солей.
ПОМОГИТЕ С ХИМИЕЙ!
Из данного перечня солей выберите соли, которые подвергаются в водных растворах гидролизу и определите реакцию среды их водного раствора : а) нитрат натрия, карбонат калия, хлорид алюминия, сульфид калия.
Б) нитрат свинца(II), хлорид бария, фосфат калия, сульфат цинка.
С какими из перечисленных веществ взаимодействует хлорид меди 2 : нитрат бария нитрат серебра гидроксид калия серная кислота сульфид натрия?
С какими из перечисленных веществ взаимодействует хлорид меди 2 : нитрат бария нитрат серебра гидроксид калия серная кислота сульфид натрия?
Напишите уравнение реакций составьте ионные уравнения.
Помогите пожалуйста : ) какие из перечисленных солей подвергаются гидролизу при растворении в воде : хлорид калия, нитрат меди(II), сульфат лития, нитрат бария, сульфид натрия, хлорид железа (III)?
Помогите пожалуйста : ) какие из перечисленных солей подвергаются гидролизу при растворении в воде : хлорид калия, нитрат меди(II), сульфат лития, нитрат бария, сульфид натрия, хлорид железа (III)?
Какую реакцию среды будут иметь растворы этих солей?
Запишите необходимые для ответа молекулярные и ионные уравнения.
Срочно нужно, помогите пожалуйста.
Составьте молекулярные и ионные уравнения реакций гидролиза солей , укажите по возможности среду раствора соли :хлорида железа ||, фосфата калия?
Составьте молекулярные и ионные уравнения реакций гидролиза солей , укажите по возможности среду раствора соли :
хлорида железа ||, фосфата калия.
Вы перешли к вопросу Напишите уравнения реакций гидролиза нитрата меди ; хлорида калия ; сульфида натрия в ионном виде?. Он относится к категории Химия, для 10 — 11 классов. Здесь размещен ответ по заданным параметрам. Если этот вариант ответа не полностью вас удовлетворяет, то с помощью автоматического умного поиска можно найти другие вопросы по этой же теме, в категории Химия. В случае если ответы на похожие вопросы не раскрывают в полном объеме необходимую информацию, то воспользуйтесь кнопкой в верхней части сайта и сформулируйте свой вопрос иначе. Также на этой странице вы сможете ознакомиться с вариантами ответов пользователей.
Амфотерные — АL(OH)3, Zn(OH)2, Fe(OH)3. Основные — Ca(OH)2. Кислоты — H3SO4, HNO3. СТАВЬ СПАСИБО.
[Ca(NH₃)₃(H₂O)]Cl₂ хлорид акватриамминкальция.
Плюсовий, його заряд завжди такий.
Дано m(ppa NaOH) = 200 g W(NaOH) = 2% m(ppa HCL) = 100 g W(HCL) = 4% — — — — — — — — — — — — — — — — — — — — — — — — — — — m(NaCL) — ? M(NaOH) = 200 * 2% / 100% = 4 g m(HCL) = 100 * 4% / 100% = 4g M(NaOH) = 40 g / mol n(NaOH) = m / M = 4 / 40 = 0. ..
Решение находится на фото.
Да, потому что Ca является металлом , а к. О SO4 не металл.
36 + 10 = 56 г 55 разделить 5 = 11.
А) 3 молекулы воды б) 2 молекулы диоксида углерода в) 5 молекул карбоната кальция г) 3 молекулы серной кислоты д) 4 молекулы хлорида натрия.
Ответ навариант 1, задание первое находится на фото.
Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей: нитрат меди (II), сульфид калия
Решение:
Нитрат меди (II) Cu(NO3)2– соль слабого двухкислотного основания и сильной кислоты. Катионы слабого основания Cu 2+ связывают гидроксид ионы из воды. Гидролиз такой соли идет по катиону:
Сокращенное ионно-молекулярное уравнение гидролиза:
Cu 2+ + H2O 
полное ионно-молекулярное уравнение:
Cu 2+ + 2NO3 — + H2O 
Cu(NO3)2+ H2O 
В растворе накапливаются катионы водорода, которые создают кислую реакцию среды (pH 2– связывают ионы водорода из воды, образуя анионы кислой соли HS – . Соль гидролизуется по аниону.
Сокращенное ионно-молекулярное уравнение:
S 2– + H2O 
полное ионно-молекулярное уравнение:
2К + + S 2– + H2O 
К2S + H2O 
Появление избыточного количества ионов OH – обусловливает щелочную реакцию среды (pH > 7).
22. Какие из солей Al2(SO4)3, K2S, Pb(NO3)2, KCl подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей.
Решение:
Сульфат алюминия Al2(SO4)3– соль слабого трехкислотного основания и сильной кислоты. Гидролиз такой соли идет по катиону слабого основания с образованием катионов основной соли AlOH 2+ .
Сокращенное ионно-молекулярное уравнение гидролиза:
Al 3+ + H2O 
полное ионно-молекулярное уравнение:
2Al 3+ + 3SO4 2- + 2H2O 
Al2(SO4)3 + 2H2O 
В растворе накапливаются катионы водорода, которые создают кислую реакцию среды (pH 2– связывают ионы водорода из воды, образуя анионы кислой соли HS – . Соль гидролизуется по аниону.
Сокращенное ионно-молекулярное уравнение:
S 2– + H2O 
полное ионно-молекулярное уравнение:
2К + + S 2– + H2O 
К2S + H2O 
Появление избыточного количества ионов OH – обусловливает щелочную реакцию среды (pH > 7).
Нитрат свинца (II) Pb(NO3)2– соль слабого двухкислотного основания и сильной кислоты. Катионы слабого основания Pb 2+ связывают гидроксид ионы из воды. Гидролиз такой соли идет по катиону:
Сокращенное ионно-молекулярное уравнение гидролиза:
Pb 2+ + H2O 
полное ионно-молекулярное уравнение:
Pb 2+ + 2NO3 — + H2O 
Pb(NO3)2+ H2O 
В растворе накапливаются катионы водорода, которые создают кислую реакцию среды (pH + и анионы Cl – . Катионы K + не могут связывать анионы OH – , так как KOH – сильный электролит. Анионы Cl – не могут связывать катионы Н + , так как НCl – сильный электролит. Таким образом, можно сделать вывод, что хлорид калия не гидролизуется. Равновесие между ионами и молекулами воды не нарушается, и раствор остается нейтральным, рН равен 7.
Как изменится цвет лакмуса в растворах солей: хлорида натрия, карбоната натрия, хлорида меди (II)? Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей.
Решение:
Хлорид натрия NaCl —соль сильной кислоты и сильного основания. При растворении в воде хлорид натрия диссоциирует на ионы Na + и анионы Cl – . Катионы Na + не могут связывать анионы OH – , так как NaOH – сильный электролит. Анионы Cl – не могут связывать катионы Н + , так как НCl – сильный электролит. Таким образом, можно сделать вывод, что хлорид натрия не гидролизуется. Равновесие между ионами и молекулами воды не нарушается, и раствор остается нейтральным, рН равен 7. Цвет лакмуса не изменяется.
Карбонат натрия Na2CO3 – соль двухосновной слабой кислоты и сильного основания. Анионы слабой кислоты CO3 2– связывают ионы водорода из воды, образуя анионы кислой соли HCO3 — . Соль гидролизуется по аниону.
Сокращенное ионно-молекулярное уравнение:
CO3 2– + H2O 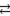
полное ионно-молекулярное уравнение:
2Na + + CO3 2– + H2O 
Na2CO3 + H2O 
Появление избыточного количества ионов OH – обусловливает щелочную реакцию среды (pH > 7). Цвет лакмуса меняется с фиолетового на синий.
Хлорид меди (II) CuCl2– соль слабого двукислотного основания и сильной кислоты. Гидролиз такой соли идет по катиону слабого основания с образованием катионов основной соли CoOH + .
Сокращенное ионно-молекулярное уравнение гидролиза:
Cu 2+ + H2O 
полное ионно-молекулярное уравнение:
Cu 2+ + 2Cl — + H2O 
CuCl2+ 2H2O 
В растворе накапливаются катионы водорода, которые создают кислую реакцию среды (pH .
Задание 1
Какие соли подвергаются гидролизу и почему? Объясните это на примерах нитрата цинка, сульфата калия и сульфида натрия.
Гидролизу подвергаются соли образованные или слабым основанием и сильной кислотой, или сильным основанием и слабой кислотой.
Нитрат цинка образован слабым основанием (Zn(OH)2) и сильной кислотой (HNO3), поэтому он подвергается гидролизу:
Zn(NO3)2 + HOH ⇄ ZnOHNO3 + HNO3
Zn 2+ + 2NO3 — + HOH ⇄ ZnOH + + NO3 — + H + + NO3 —
Zn 2+ + HOH ⇄ ZnOH + + H +
Сульфат калия образован сильным основанием (KOH) и сильной кислотой (H2SO4), поэтому он не подвергается гидролизу:
K2SO4 + HOH ⇄ KOH + KHSO4
2K + + SO4 2- + HOH ⇄ K + + OH — + K + + H + + SO4 2-
HOH ⇄ H + + OH —
Сульфид натрия образован сильным основанием (NaOH) и слабой кислотой (H2S), поэтому он подвергается гидролизу:
Na2S + HOH ⇄ NaOH + NaHS
2Na + + S 2- + HOH ⇄ Na + + OH — + Na + + HS —
S 2- + HOH ⇄ OH — + HS —









