(соль образованна слабым многокислотным основанием и слабой многоосновной кислотой)
Если продукты гидролиза выводятся из сферы реакции (в виде осадка или газа), то процесс может протекать до конца:
Al2S3 + 6 H2O = 2 Al(OH)3 + 3 H2S
ионно-молекулярное уравнение: 2 Al 3+ + 3S 2- + 6H2O = 2Al(OH)3 + 3 H2S
В этом случае гидролиз протекает необратимо.
Полностью гидролизуются соли (карбонаты, сульфиды алюминия, хрома(III), железа(III)).
Гидролиз осложняет протекание многих других реакций обмена. Так, при взаимодействии карбоната натрия с сульфатом меди в осадок обычно выпадает основной карбонат меди (CuOH)2CO3.
Бинарные соединения: нитриды, фосфиды, карбиды, ацетилениды, бориды:
Гидролиз солей
Водные растворы солей имеют разные значения рН и показывают различную реакцию среды — кислую, щелочную, нейтральную.
Например, водный раствор хлорида алюминия AlCl3 имеет кислую среду (рН 7), растворы хлорида натрия NaCl и нитрита свинца Pb(NO2)2 — нейтральную среду (pН = 7). Эти соли не содержат в своем составе ионы водорода Н + или гидроксид-ионы ОН — , которые определяют среду раствора. Чем же можно объяснить различные среды водных растворов солей? Это объясняется тем, что в водных растворах соли подвергаются гидролизу.
Слово «гидролиз» означает разложение водой («гидро» — вода, «лизис» — разложение).
Гидролиз — одно из важнейших химических свойств солей.
Гидролизом соли называется взаимодействие ионов соли с водой, в результате которого образуются слабые электролиты.
Сущность гидролиза сводится к химическому взаимодействию катионов или анионов соли с гидроксид-ионами ОН — или ионами водорода Н + из молекул воды. В результате этого взаимодействия образуется малодиссоциирующее соединение (слабый электролит). Химическое равновесие процесса диссоциации воды смещается вправо.
Поэтому в водном растворе соли появляется избыток свободных ионов Н + или ОН — , и раствор соли показывает кислую или щелочную среду.
Гидролиз — процесс обратимый для большинства солей. В состоянии равновесия только небольшая часть ионов соли гидролизуется.
Любую соль можно представить как продукт взаимодействия кислоты с основанием. Например, соль NaClO образована слабой кислотой HClO и сильным основанием NaOH.
В зависимости от силы исходной кислоты и исходного основания соли можно разделить на 4 типа:
Соли I, II, III типов подвергаются гидролизу, соли IV типа не подвергаются гидролизу
Рассмотрим примеры гидролиза различных типов солей.
I. Соли, образованные сильным основанием и слабой кислотой, подвергаются гидролизу по аниону. Эти соли образованы катионом сильного основания и анионом слабой кислоты, который связывает катион водорода Н + молекулы воды, образуя слабый электролит (кислоту).
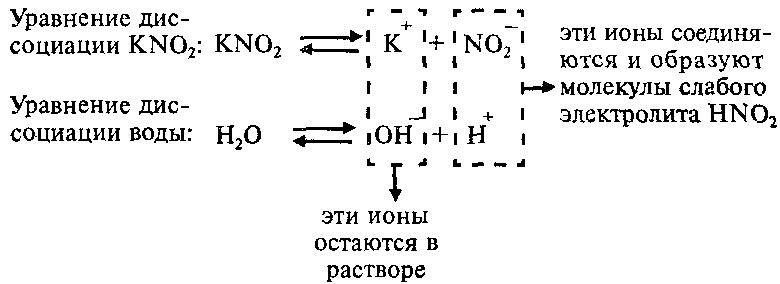
Пример: Составим молекулярное и ионные уравнения гидролиза нитрита калия KNO2.
Соль KNO2 образована слабой одноосновной кислотой HNO2 и сильным основанием KОН, что можно изобразить схематически так:
Напишем уравнение гидролиза соли KNO2:
Каков механизм гидролиза этой соли?
Так как ионы Н + соединяются в молекулы слабого электролита HNО2, их концентрация уменьшается и равновесие процесса диссоциации воды по принципу Ле-Шателье смещается вправо. В растворе увеличивается концентрация свободных гидроксид-ионов ОН — . Поэтому раствор соли KNO2 имеет щелочную реакцию (pН > 7).
Вывод: Соли, образованные сильным основанием и слабой кислотой, при растворении в воде показывают щелочную реакцию среды, pН > 7.
II. Соли, образованные слабым основанием и сильной кислотой, гидролизуются по катиону. Эти соли образованы катионом слабого основания и анионом сильной кислоты. Катион соли связывает гидроксид-ион ОН — воды, образуя слабый электролит (основание).
Пример: Составим молекулярное и ионное уравнения гидролиза йодида аммония NH4I.
Соль NH4I образована слабым однокислотным основанием NH4OH и сильной кислотой НI:
При растворении в воде соли NH4I катионы аммония NH4 + связываются с гидроксид-ионами ОН — воды, образуя слабый электролит – гидроксид аммония NH4OH. В растворе появляется избыток ионов водорода Н + . Среда раствора соли NH4I – кислая, рН — из молекулы воды и образует слабое основание, и анионом слабой кислоты, который связывает ионы Н + из молекулы воды и образует слабую кислоту. Реакция растворов этих солей может быть нейтральной, слабокислой или слабощелочной. Это зависит от констант диссоциации слабой кислоты и слабого основания, которые образуются в результате гидролиза.
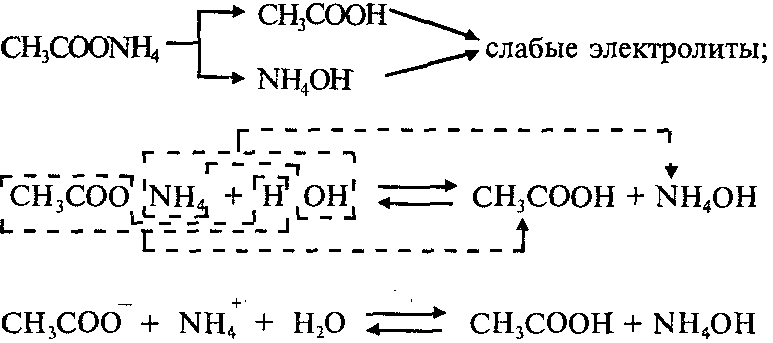
Пример 1: Составим уравнения гидролиза ацетата аммония CH3COONH4. Эта соль образована слабой уксусной кислотой СН3СООН и слабым основанием NH4ОH:
Реакция раствора соли CH3COONH4 – нейтральная (рН=7), потому что Kд(СН3СООН)=Kд(NH4ОH).
Пример 2: Составим уравнения гидролиза цианида аммония NH4CN. Эта соль образована слабой кислотой HCN и слабым основанием NH4ОH:
Реакция раствора соли NH4CN — слабощелочная (pН > 7), потому что Kд(NH4ОH)> Kд(HCN).
Как уже было отмечено, для большинства солей гидролиз является обратимым процессом. В состоянии равновесия гидролизуется только небольшая часть соли. Однако некоторые соли полностью разлагаются водой, т. е. для них гидролиз является необратимым.
Необратимому (полному) гидролизу подвергаются соли, которые образованы слабым нерастворимым или летучим основанием и слабой летучей или нерастворимой кислотой. Такие соли не могут существовать в водных растворах, К ним, например, относятся:
Пример: Составим уравнение гидролиза сульфида алюминия Al2S3:
Гидролиз сульфида алюминия протекает практически полностью до образования гидроксида алюминия Al(OH)3 и сероводорода H2S.
Поэтому в результате обменных реакций между водными растворами некоторых солей не всегда образуются две новые соли. Одна из этих солей может подвергаться необратимому гидролизу с образованием соответствующего нерастворимого основания и слабой летучей (нераствориой) кислоты. Например:
Суммируя эти уравнения, получаем:
или в ионном виде:
IV. Соли, образованные сильной кислотой и сильным основанием, не гидролизуются, потому что катионы и анионы этих солей не связываются с ионами Н + или ОН — воды, т. е. не образуют с ними молекул слабых электролитов. Равновесие диссоциации воды не смещается. Среда растворов этих солей — нейтральная (рН = 7,0), так как концентрации ионов Н + и ОН — в их растворах равны, как в чистой воде.
Вывод: Соли, образованные сильной кислотой и сильным основанием, при растворении в воде гидролизу не подвергаются и показывают нейтральную реакцию среды (рН = 7,0).
Ступенчатый гидролиз
Гидролиз солей может протекать ступенчато. Рассмотрим случаи ступенчатого гидролиза.
Если соль образована слабой многоосновной кислотой и сильным основанием, число ступеней гидролиза зависит от основности слабой кислоты. В водном растворе таких солей на первых ступенях гидролиза образуются кислая соль вместо кислоты и сильное основание. Ступенчато гидролизуюгся соли Na2SO3, Rb2CО3, K2SiO3, Li3PO4 и др.
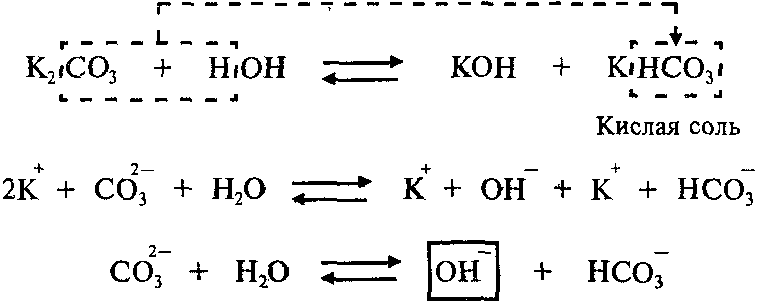
Пример: Составим молекулярное и ионное уравнения гидролиза карбоната калия K2СО3.
Гидролиз соли K2СО3 протекает по аниону, потому что соль карбонат калия образована слабой кислотой Н2СО3 и сильным основанием KОН:
Так как Н2СО3 – двухосновная кислота, гидролиз K2СО3 протекает по двум ступеням.
Продуктами первой ступени гидролиза K2СО3 являются кислая соль KHCO3 и гидроксид калия KОН.
Вторая ступень (гидролиз кислой соли, которая образовалась в результате первой ступени):
Продуктами второй ступени гидролиза K2СО3 являются гидроксид калия и слабая угольная кислота Н2СО3. Гидролиз по второй ступени протекает в значительно меньшей степени, чем по первой ступени.
Среда раствора соли K2СО3 — щелочная (рН > 7), потому что в растворе увеличивается концентрация ионов ОН — .
Если соль образована слабым многокислотным основанием и сильной кислотой, то число ступеней гидролиза зависит от кислотности слабого основания. В водных растворах таких солей на первых ступенях образуется основная соль вместо основания и сильная кислота. Ступенчато гидролизуются соли MgSО4, CoI2, Al2(SO4)3, ZnBr2 и др.
Пример: Составим молекулярное и ионное уравнения гидролиза хлорида никеля (II) NiCl2.
Гидролиз соли NiCl2 протекает по катиону, так как соль образована слабым основанием Ni(OH)2 и сильной кислотой НСl. Катион Ni 2+ связывает гидроксид-ионы ОН — воды. Ni(OH)2 — двухкислотное основание, поэтому гидролиз протекает по двум ступеням.
Продуктами первой ступени гидролиза NiCl2 являются основная соль NiOHCl и сильная кислота HCl.
Вторая ступень (гидролиз основной соли, которая образовалась в результате первой ступени гидролиза):
Продуктами второй ступени гидролиза являются слабое основание гидроксид никеля (II) и сильная хлороводородная кислота НCl. Однако степень гидролиза по второй ступени намного меньше, чем по первой ступени.
Среда раствора NiCl2 — кислая, рН + .
Гидролизу подвергаются не только соли, но и другие неорганические соединения. Гидролизуются также жиры, углеводы, белки и другие вещества, свойства которых изучаются в курсе органической химии. Поэтому можно дать более общее определение процесса гидролиза:
Гидролиз — это реакция обменного разложения веществ водой.
Составление ионно-молекулярных и молекулярных уравнений гидролиза солей
Решение задач на составление уравнений гидролиза солей
Задание 201.
Составьте ионно-молекулярное и молекулярное уравнения гидролиза, происходящего при смешивании растворов К2S и СгС13. Каждая из взятых солей гидролизуется необратимо до конца с образованием соответствующих основания и кислоты.
Решение:
Гидролиз соли K2S и CrCl3
K2S – соль сильного основания и слабой кислоты гидролизуется по аниону, а CrCl3 – соль слабого основания и сильной кислоты гидролизуется по катиону:
K2S ⇔ 2K + + S 2- ; CrCl3 ⇔ Cr 3+ + 3Cl — ;
а) S 2- + H2O ⇔ HS — + OH — ;
б) Cr 3+ + H2O ⇔ CrOH 2+ + H + .
Если растворы этих солей находятся в одном сосуде, то идёт взаимное усиление гидролиза каждой из них, ибо ионы Н+ и ОН-, связываясь друг с другом, образуют молекулы слабого электролита Н2О (Н + + ОН — ⇔ Н2О). При образовании дополнительного количества воды гидролитическое равновесие обеих солей сдвигается вправо, и гидролиз каждой соли идёт до конца с образованием осадка и газа:
3S 2- + 2Cr 3+ + 6H2O ⇔ 2Cr(OH)3↓ + 3H2S↑ (ионно-молекулярная форма);
3K2S + 2CrCl3 + 6Н2О ⇔ 2Cr(OH)3↓ + 3H2S↑ + 6KCl (молекулярная форма).
Задание 202.
К раствору FeCl3 добавили следующие вещества: a) HCl; б) КОН; в) ZnCl2; г) Na2СО3. В каких случаях гидролиз хлорида железа (III) усилится? Почему? Составьте ионно-молекулярные уравнения гидролиза соответствующих солей.
Решение:
Гидролиз соли FeCl3
а) Соль FeCl3 гидролизуется по катиону, а HCl диссоциирует в водном растворе:
FeCl3 ⇔ Fe 3+ + 3Cl — ;
Fe 3+ + H2O ⇔ FeOH 2+ + H + ;
HCl ⇔ H + + Cl —
Если растворы этих веществ находятся в одном сосуде, то идёт угнетение гидролиза соли FeCl3, ибо образуется избыток ионов водорода Н + и равновесие гидролиза сдвигается влево:
б) Соль FeCl3 гидролизуется по катиону, а KOH диссоциирует в водном растворе с образованием ОН — :
FeCl3 ⇔ Fe 3+ + 3Cl — ;
Fe 3+ + H2O ⇔ FeOH 2+ + H + ;
KOH ⇔ K + + OH —
Если растворы этих веществ находятся в одном сосуде, то идёт гидролиза соли FeCl3 и диссоциации КОН, ибо ионы Н + и ОН — , связываясь друг с другом, образуют молекулы слабого электролита Н2О (Н + + ОН — ⇔ Н2О). При этом гидролитическое равновесие соли FeCl3 и диссоциация КОН сдвигаются вправо и гидролиз соли и диссоциация основания идут до конца с образованием осадка Fe(OH)3. По сути, при смешивании FeCl3 и КОН протекает реакция обмена. Ионно-молекулярное уравнение процесса:
Молекулярное уравнение процесса:
в) Соль FeCl3 и соль ZnCl2 гидролизуется по катиону:
Fe 3+ + H2O ⇔ FeOH 2+ + H + ;
Zn 2+ + H2O ⇔ ZnOH + + H +
Если растворы этих солей находятся в одном сосуде, то идёт взаимное угнетение гидролиза каждой из них, ибо избыточное количество ионов Н + вызывает смещение гидролитического равновесие влево, в сторону уменьшения концентрации ионов водорода Н + .
г) Соль FeCl3 гидролизуется по катиону, а соль Na2СO3 – по аниону:
Если растворы этих солей находятся в одном сосуде, то идёт взаимное усиление гидролиза каждой из них, ибо ионы Н + и ОН — , связываясь друг с другом, образуют молекулы слабого электролита Н2О (Н + + ОН — ⇔ Н2О). При образовании дополнительного количества воды гидролитическое равновесие обеих солей сдвигается вправо, и гидролиз каждой соли идёт до конца с образованием осадка Fe(OH)3↓, слабого электролита H2CО3:
Задание 203.
Какие из солей Al2(SO4)3, K2S, Pb(NO3)2, КСl подвергаются гидролизу? Составьте ионно-молекулярные и молекулярные уравнения гидролиза соответствующих солей. Какое значение рН (> 7
а) Al2(SO4)3 — соль слабого основания и сильной кислоты. В этом случае катионы Al 3+ связывают ионы ОН — воды, образуя катионы основной соли AlOH 2+ . Образование Al(OH) 2+ и Al(OH)3 не происходит, потому что ионы AlOH 2+ диссоциируют гораздо труднее, чем ионы Al(OH) 2+ и молекулы Al(OH)3. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
или в молекулярной форме:
В растворе появляется избыток ионов водорода, которые придают раствору Al2(SO4)3 кислую среду, рН
б) K2S – соль сильного однокислотного основания KOH и слабой многоосновной кислоты H2S. В этом случае анионы S 2- связывают ионы водорода Н+ воды, образуя анионы кислой соли НS-. Образование H2S не происходит, так как ионы НS — диссоциируют гораздо труднее, чем молекулы H2S. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза:
K2S ⇔ 2К + + S 2- ;
S 2- + H2O ⇔Н S- + ОH —
или в молекулярной форме:
В растворе появляется избыток гидроксид-ионов, которые придают раствору K2S щелочную среду, рН > 7.
в) Pb(NO3)2 — соль слабого основания и сильной кислоты. В этом случае катионы Pb 2+ связывают ионы ОН- воды, образуя катионы основной соли PbOH + . Образование Pb(OH)2 не происходит, потому что ионы PbOH + диссоциируют гораздо труднее, чем молекулы Pb(OH)2. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
или в молекулярной форме:
В растворе появляется избыток ионов водорода, которые придают раствору Pb(NO3)2 кислую среду, рН
г) КCl – соль сильного основания и сильной кислоты гидролизу не подвергается, так как ионы К + , Cl — не связываются ионами воды H + и OH — . Ионы К + , Cl — , H + и OH — останутся в растворе. Так как в растворе соли присутствуют равные количества ионов H + и OH — , то раствор имеет нейтральную среду, рН = 0.
Задание 204.
При смешивании растворов FeCl3 и Na2СО3 каждая из взятых солей гидролизуется необратимо до конца с образованием соответствующих основания и кислоты. Выразите этот совместный гидролиз ионно-молекулярным и молекулярным уравнениями.
Решение:
Гидролиз соли FeCl3
FeCl3 — соль слабого основания и сильной кислоты. В этом случае катионы Fe 3+ связывают ионы ОН — воды, образуя катионы основной соли FeOH 2+ . Образование Fe(OH) 2+ и Fe(OH)3 не происходит, потому что ионы FeOH 2+ диссоциируют гораздо труднее, чем ионы Fe(OH) 2+ и молекулы Fe(OH)3. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
FeCl3 ⇔ Fe 3+ + 3Cl —
Fe 3+ + H2O ⇔ FeOH 2+ + H +
Na2CO3 — соль сильного основания и слабой кислоты. В этом случае анионы CO3 2- связывают ионы водорода Н + воды, образуя анионы кислой соли HCO3 — . Образование H2CO3 не происходит, так как ионы HCO3 — диссоциируют гораздо труднее, чем молекулы H2CO3. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза:
Если растворы этих солей находятся в одном сосуде, то идёт взаимное усиление гидролиза каждой из них, ибо ионы Н + и ОН — , связываясь друг с другом, образуют молекулы слабого электролита Н2О (Н + + ОН — ⇔ Н2О). При образовании дополнительного количества воды гидролитическое равновесие обеих солей сдвигается вправо, и гидролиз каждой соли идёт до конца с образованием осадка и газа:
Задание 205.
К раствору Nа2СО3 добавили следующие вещества: a)HCl; б)NaOH; в) Cu(NО3)2; г)K2S. В каких случаях гидролиз карбоната натрия усилится? Почему? Составьте ионно-молекулярные уравнения гидролиза соответствующих солей.
Решение:
Гидролиз соли Na2CO3
а) Соль Na2CO3 гидролизуется по аниону, а HCl диссоциирует в водном растворе:
Если растворы этих веществ находятся в одном сосуде, то идёт взаимное усиление гидролиза каждой из них, ибо ионы Н + и ОН — , связываясь друг с другом, образуют молекулы слабого электролита Н2О (Н + + ОН — ⇔ Н2О). При этом гидролитическое равновесие соли Na2CO3 и диссоциация HCl сдвигаются вправо и гидролиз соли и диссоциация кислоты идут до конца с образованием газообразного углекислого газа. Ионно-молекулярное уравнение процесса:
Молекулярное уравнение процесса:
б) Соль Na2CO3 гидролизуется по аниону, а NaOH диссоциирует в водном растворе:
Если растворы этих веществ смешать, то образуется избыток ионов ОН — , что сдвигает равновесие гидролиза Na2CO3 влево и гидролиз соли будет угнетаться.
в) Соль Na2CO3 гидролизуется по аниону, а соль Cu(NO3)2 – по катиону:
Если растворы этих солей находятся в одном сосуде, то идёт взаимное усиление гидролиза каждой из них, ибо ионы Н + и ОН — , связываясь друг с другом, образуют молекулы слабого электролита Н2О (Н + + ОН — ⇔ Н2О). При образовании дополнительного количества воды гидролитическое равновесие обеих солей сдвигается вправо, и гидролиз каждой соли идёт до конца с образованием осадка и газа:
г) Na2CO3 и К2S — соли сильного основания и слабой кислоты, поэтому обе гидролизуются по аниону:
Если растворы этих солей находятся в одном сосуде, то идёт взаимное угнетение гидролиза каждой из них, ибо избыток ионов ОН — , согласно принципу Ле Шателье, смещает равновесие гидролиза обеих солей влево, в сторону уменьшения концентрации ионов ОН — , т. е. гидролиз обеих солей будет угнетаться.
Задание 206.
Какое значение рН (> 7
а) Na2S – соль сильного однокислотного основания NaOH и слабой многоосновной кислоты H2S. В этом случае анионы S 2- связывают ионы водорода Н+ воды, образуя анионы кислой соли НS-. Образование H2S не происходит, так как ионы НS — диссоциируют гораздо труднее, чем молекулы H2S. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза:
Na2S ⇔ 2Na + + S 2- ;
S 2- + H2O ⇔ НS — + ОH —
или в молекулярной форме:
В растворе появляется избыток гидроксид-ионов, которые придают раствору Na2S щелочную среду, рН > 7.
б) AlCl3 — соль слабого основания и сильной кислоты. В этом случае катионы Al3+ связывают ионы ОН — воды, образуя катионы основной соли AlOH 2+ . Образование Al(OH) 2+ и Al(OH)3 не происходит, потому что ионы AlOH 2+ диссоциируют гораздо труднее, чем ионы Al(OH) 2+ и молекулы Al(OH)3. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
AlCl3 ⇔ Al 3+ + 3Cl — ;
Al 3+ + H2O ⇔ AlOH 2+ + H +
или в молекулярной форме:
В растворе появляется избыток ионов водорода, которые придают раствору Al2(SO4)3 кислую среду, рН
в) NiSO4 — соль слабого многокислотного основания Ni(OH)2 и сильной двуходноосновной кислоты H2SO4. В этом случае катионы Ni 2+ связывают ионы ОН — воды, образуя катионы основной соли NiOH + . Образование Ni(OH)2 не происходит, потому что ионы NiOH + диссоциируют гораздо труднее, чем молекулы Ni(OH)2. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
или в молекулярной форме:
В растворе появляется избыток ионов водорода, которые придают раствору NiSO4 кислую среду, рН
Задание 207.
Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей Pb(NO3)2, Na2CO3, Fe2(SO4)3. Какое значение рН (> 7
а) Pb(NO3)2 — соль слабого основания и сильной кислоты. В этом случае катионы Pb 2+ связывают ионы ОН — воды, образуя катионы основной соли PbOH + . Образование Pb(OH)2 не происходит, потому что ионы PbOH + диссоциируют гораздо труднее, чем молекулы Pb(OH)2. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
или в молекулярной форме:
В растворе появляется избыток ионов водорода, которые придают раствору Pb(NO3)2 кислую среду, рН
б) Na2CO3 — соль сильного основания и слабой кислоты. В этом случае анионы CO3 2- связывают ионы водорода Н + воды, образуя анионы кислой соли HCO3 — . Образование H2CO3 не происходит, так как ионы HCO3 — диссоциируют гораздо труднее, чем молекулы H2CO3. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза:
или в молекулярной форме:
В растворе появляется избыток гидроксид-ионов, которые придают раствору Na2CO3 щелочную среду, рН > 7.
в) Fe2(SO4)3 — соль слабого основания и сильной кислоты. В этом случае катионы Fe 3+ связывают ионы ОН — воды, образуя катионы основной соли FeOH 2+ . Образование Fe(OH) 2+ и Fe(OH)3 не происходит, потому что ионы FeOH 2+ диссоциируют гораздо труднее, чем ионы Fe(OH) 2+ и молекулы Fe(OH)3. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
Молекулярная форма процесса:
В растворе появляется избыток ионов водорода, которые придают раствору Fe2(SO4)3 кислую среду, рН
Задание 208.
Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей НСООК, ZnSО4, Аl(NO3)3. Какое значение рН (> 7
а) НСООК – соль сильного однокислотного основания KOH и слабой одноосновной кислоты НСООН. В этом случае анионы НСОО — связывают ионы водорода Н + воды, образуя слабый электролит НСООН. Ионно-молекулярное уравнение гидролиза:
НСООК ⇔ К + + НСОО — ;
НСОО — + H2O ⇔ НСООН + ОH —
или в молекулярной форме:
НСООК + Н2О = НСООН + КОН
В растворе появляется избыток гидроксид-ионов, которые придают раствору НСООК щелочную среду, рН > 7.
б) ZnSО4 — соль слабого многокислотного основания Zn(OH)2 и сильной многосновной кислоты. В этом случае катионы Zn 2+ связывают ионы ОН — воды, образуя катионы основной соли ZnOH + . Образование Zn(OH)2 не происходит, потому что ионы СоOH + диссоциируют гораздо труднее, чем молекулы Zn(OH)2. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
или в молекулярной форме:
В растворе появляется избыток ионов водорода, которые придают раствору ZnSО4 кислую среду, рН
в) Аl(NO3)3 — соль слабого многокислотного основания Al(OH)3 и сильной одноосновной кислоты HNO3. В этом случае катионы Al 3+ связывают ионы ОН — воды, образуя катионы основной соли AlOH 2+ . Образование Al(OH) 2+ и Al(OH)3 не происходит, потому что ионы AlOH 2+ диссоциируют гораздо труднее, чем ионы Al(OH) 2+ и молекулы Al(OH)3. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
Молекулярное уравнение реакции:
В растворе появляется избыток ионов водорода, которые придают раствору Cr(NO3)3 кислую среду, рН
Задание 209.
Какое значение рН (> 7
а) Ортофосфат натрия Na3PO4 – соль слабой многоосновной кислоты Н3РО4 и сильного однокислотного основания. В этом случае анионы РО4 3- связывают ионы водорода Н+ воды, образуя анионы кислой соли HРО4 2- . Образование H2РО4 — и Н3РО4 не происходит, так как ионы HРО4 2 — диссоциируют гораздо труднее, чем ионы H2РО4 — и молекулы Н3РО4. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза:
или в молекулярной форме:
В растворе появляется избыток гидроксид-ионов, которые придают раствору Na3PO4 щелочную среду, рН > 7.
б) K2S – соль сильного однокислотного основания KOH и слабой многоосновной кислоты H2S. В этом случае анионы S 2- связывают ионы водорода Н + воды, образуя анионы кислой соли НS — . Образование H2S не происходит, так как ионы НS — диссоциируют гораздо труднее, чем молекулы H2S. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза:
K2S ⇔ 2К + + S 2- ;
S 2- + H2O ⇔ НS — + ОH —
или в молекулярной форме:
В растворе появляется избыток гидроксид-ионов, которые придают раствору K2S щелочную среду, рН > 7.
в) CuSO4 — соль слабого основания и сильной кислоты. В этом случае катионы Cu 2+ связывают ионы ОН — воды, образуя катионы основной соли CuOH + . Образование Cu(OH)2 не происходит, потому что ионы CuOH + диссоциируют гораздо труднее, чем молекулы Cu(OH)2. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
или в молекулярной форме:
В растворе появляется избыток ионов водорода, которые придают раствору CuSO4 кислую среду, рН
Задание 210.
Составьте ионно-молекулярные и молекулярные уравнения гидролиза солей CuCl2, Сs2СО3, Сr(NО3)3. Какое значение рН (> 7
а) CuCl2 — соль слабого многокислотного основания Сu(OH)2 и сильной одноосновной кислоты HCl. В этом случае катионы Cu 2+ связывают ионы ОН — воды, образуя катионы основной соли CuOH + . Образование Cu(OH)2 не происходит, потому что ионы CuOH + диссоциируют гораздо труднее, чем молекулы Cu(OH)2. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
CuCl2 ⇔ Cu 2+ + 2Cl — ;
Cu 2+ + H2O ⇔ CuOH + + H +
или в молекулярной форме:
В растворе появляется избыток ионов водорода H+, которые придают раствору CuCl2 кислую среду, рН
б) Сs2CO3 — соль сильного однокислотного основания CsOH и слабой двухосновной кислоты Н2СО3. В этом случае анионы CO3 2- связывают ионы водорода Н + воды, образуя анионы кислой соли HCO3 — . Образование H2CO3 не происходит, так как ионы HCO3 — диссоциируют гораздо труднее, чем молекулы H2CO3. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по аниону. Ионно-молекулярное уравнение гидролиза:
или в молекулярной форме:
В растворе появляется избыток гидроксид-ионов, которые придают раствору Сs2CO3 щелочную среду, рН > 7.
в) Cr(NO3)3 — соль слабого многокислотного основания Cr(OH)3 и сильной одноосновной кислоты HNO3. В этом случае катионы Cr 3+ связывают ионы ОН — воды, образуя катионы основной соли CrOH 2+ . Образование Cr(OH)2 + и Cr(OH)3 не происходит, потому что ионы CrOH 2+ диссоциируют гораздо труднее, чем ионы Cr(OH)2 + и молекулы Cr(OH)3. В обычных условиях гидролиз идёт по первой ступени. Соль гидролизуется по катиону. Ионно-молекулярное уравнение гидролиза:
Молекулярное уравнение реакции:
В растворе появляется избыток ионов водорода, которые придают раствору Cr(NO3)3 кислую среду, рН