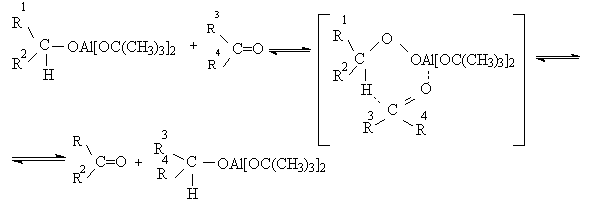
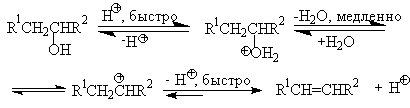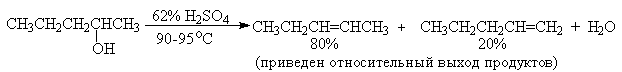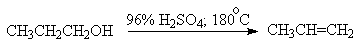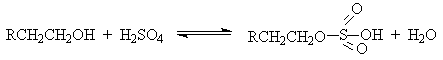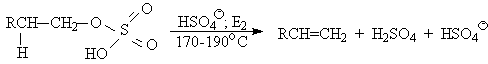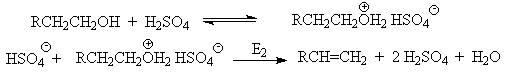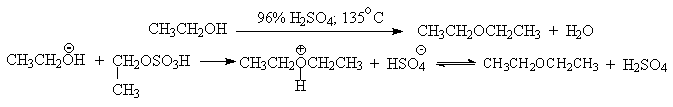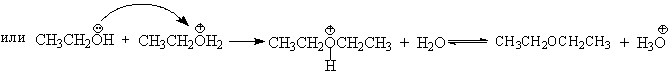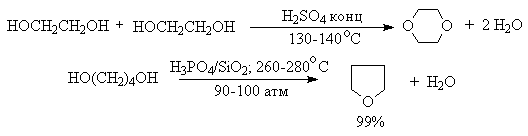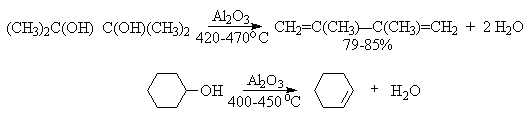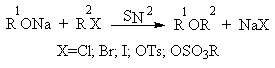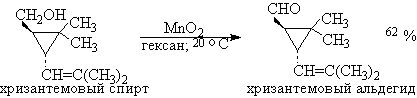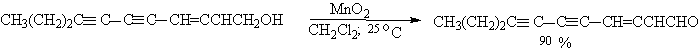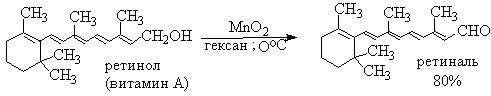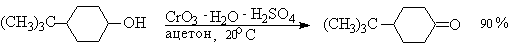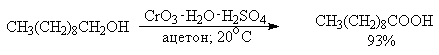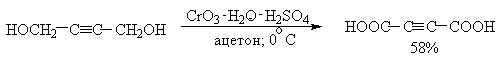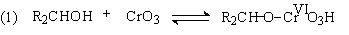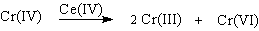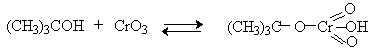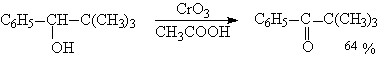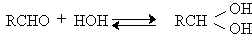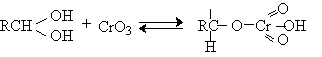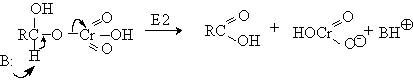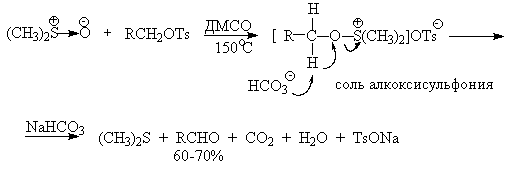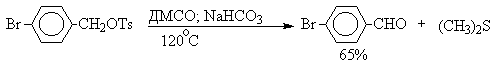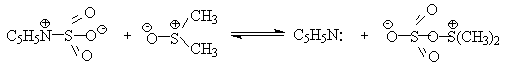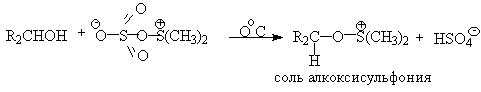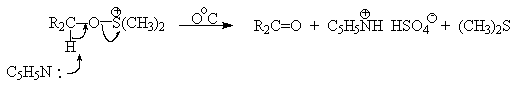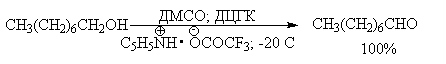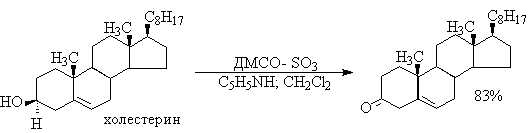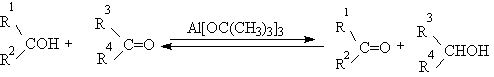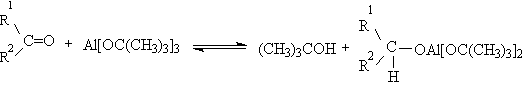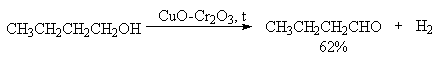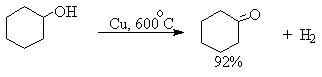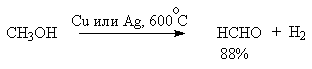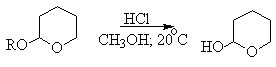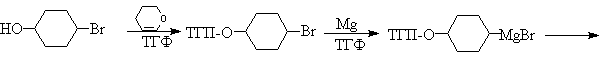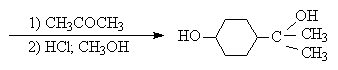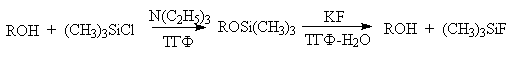Протонирование спиртов в ненуклеофильной среде приводит к дегидратации, котоая происходит при нагревании спирта в концентрированной серной, фосфорной кислотах или в суперкислой среде — смеси пятифтористой сурьмы и фторсульфоновой кислоты. Катион алкоксония, отщепляя воду, образует нестабильный интемедиат- карбокатион, который теряет протон с образованием алкена. Наиболее медленная стадия всего процесса — превращение катиона алкоксония в карбокатион. Концентрированная H2SO4 или H3PO4 связывают выделяющуюся воду, что делает весь процесс необратимым.
Приведенная последовательность превращений типична для реакций мономолекулярного элиминирования Е1, продукты которого определяются правилом Зайцева, т.е. преобладает наиболее разветвленный при двойной связи алкен. Вторичные спирты подвергаются дегидратациии при нагревании с 85%-ной
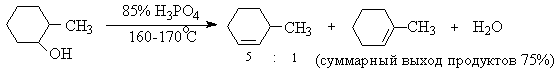
Фосфорной кислотой при 160-170 о С или с 60-70%-ной серной кислотой при 90-100 о С и направление дегидратации соответствует правилу Зайцева.
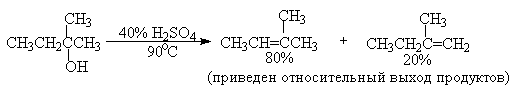
Дегидратацию третичных спиртов можно проводить уже в 20-50%-ной серной кислоте при 85-100 o С.
Третичные спирты дегидратируются так легко, что возможна избирательная дегидратация диола, содержащего третичную и первичную гидроксильные группы.
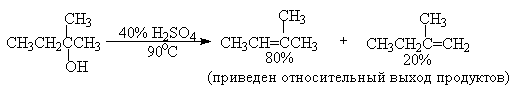
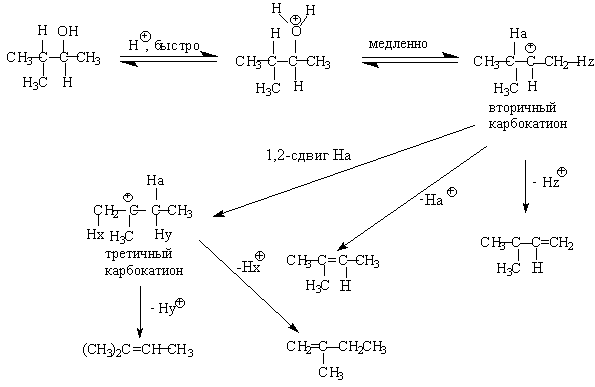
Для El-элиминирования, также как и для других процессов с образованием карбокатиона в качестве интермедиата, характерны перегруппировки, включающие анионотропную 1,2-миграцию гидрид-иона или алкильной группы. В качестве примера можно привести кислотно-катализируемую дегидратацию 3-метилбутанола-2 в 80%-ной серной кислоте.
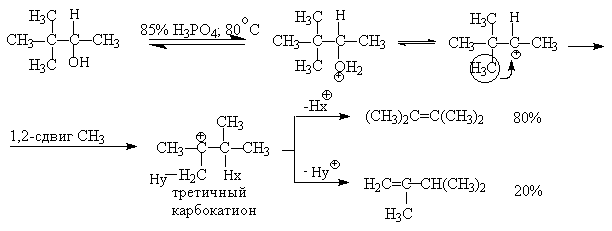
Примером скелетной изомеризации карбокатиона в Е1-элиминировании может служить дегидратация 3,3-диметилбутанола-2.
Для первичных спиртов, вероятно, реализуется иной, Е2 механизм дегидратации в концентрированной серной кислоте, они дегидратируются в гораздо более жестких условиях. Так, пропан ол-1 дает пропилен при нагревании с 96%-ной серной кислотой при 170-190 o С, этанол в этих же условиях дает этилен.
Первичные спирты при взаимодействии с серной кислотой легко образуют полуэфиры серной кислоты. Е2-Элиминированию в этом случае, по-видимому, подвергается полуэфир, а роль основания выполняет гидросульфат-ион или вода.
Возможен и другой механизм дегидратации первичных спиртов, в котором субстратом является катион алкоксония, а основанием гидросульфат-ион.
В более мягких условиях при нагревании простейших первичных спиртов с 96%-ной серной кислотой при 130-140 o С преимущественно получаются простые эфиры. При этом первичный спирт алкилируется либо под действием полуэфира серной кислоты, либо при взаимодействии с катионом алкоксония.
Этим способом получают простейшие простые эфиры — диэтиловый, дипропиловый и дибутиловый эфиры и циклические простые эфиры, например, тетрагидрофуран и диоксан. Вторичные и третичные спирты в этих условиях дегидратируются с образованием алкенов.
Этот способ неприемлем для получение несимметричных эфиров из двух спиртов, так как при этом образуется смесь трех возможных продуктов ROR, R’OR, R’OR’.
В промышленности для внутри- или межмолекулярной дегидратации вместо серной кислоты в качестве дегидратирующего средства используют безводную окись алюминия. Гетерогенная каталитическая дегидратация первичных, вторичных и третичных спиртов над окисью алюминия при 350-450 o С приводит к алкенам.
4. Получение простых эфиров по Вильямсону
Наиболее простым методом получения простых эфиров является реакция алкоголятов щелочных металлов с алкилгалогенидами или алкилсульфонатами (реакция Вильямсона, 1852 г.).
В отличие от межмолекулярной дегидратации спиртов реакция Вильямсона пригодна для синтеза как симметричных, так и несимметричных простых эфиров.
Получение простых эфиров по Вильямсону представляет собой обычную реакцию бимолекулярного нуклеофильного замещения у насыщенного атома углерода с помощью алкоксид- или феноксид-ионов. Если простой эфир содержит вторичную или третичную алкильные группы, ее следует вводить с помощью алкоголята, но не алкилгалогенида или алкилсульфоната, поскольку в противном случае преимущественно или исключительно будет происходить Е2-элиминирование.
Наилучшие результаты достигаются в том случае, когда в качестве алкилирующего агента используются первичные алкил-, аллил- и бензилгалогениды и сульфонаты.
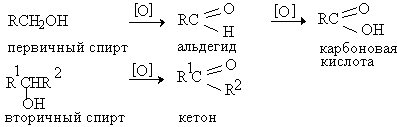
Окисление первичных спиртов в альдегиды и вторичных спиртов в кетоны является одним из важнейших превращений функциональных групп и оценкой избирательного действия реагента, используемого в качестве окислителя.
Третичные спирты не окисляются, а в жестких условиях окисление сопровождается деструкцией углеродного скелета. Наиболее широкое применение для окисления спиртов нашли реагенты на основе переходных металлов — хрома (VI), марганца (VII), марганца (IV).
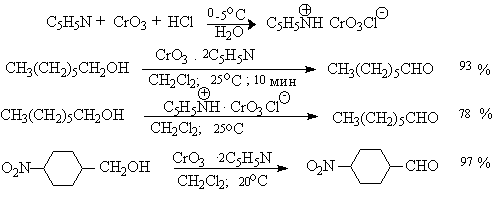
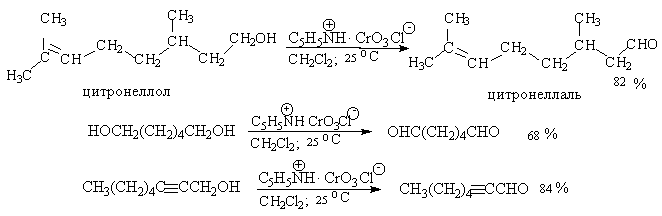
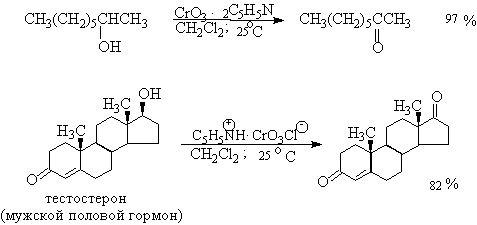
Самостоятельную и наиболее сложную проблему при окислении первичных спиртов до альдегидов составляет дальнейшее окисление альдегидов до карбоновых кислот. Для предотвращения окисления альдегидов в карбоновые кислоты в качестве окислителя используют комплексы хромового ангидрида с третичными аминами, которые уменьшают окислительную способность окислителя и делают окисление более селективным. Лучшими реагентами для окисления первичных спиртов в альдегиды являются комплекс CrO3 с двумя молями пиридина (реагент Саррета-Коллинза) и хлорхромат пиридиния C5H5N + H . CrO3 . Cl — (реагент Кори) в хлористом метилене. Реагент Саррета-Коллинза получается при медленном введении оксида хрома (VI) к пиридину при 10-15 о С. Оранжевый комплекс CrO3 c пиридином и HСl получается при добавлении пиридина к раствору CrO3 в 20%-ной соляной кислоте. Оба эти реагента растворимы в CH2Cl2 или CHCl3.
Ниже приведены некоторые наиболее типичные примеры окисления первичных спиртов до альгедигов комплексами оксида хрома VI.
Оба окислителя обеспечивают очень высокие выходы альдегидов, однако хлорхромат пиридиния имеет важное преимущество, так как он не затрагивает двойную и тройную связи и может быть использован для получения ненасыщенных альдегидов.
Для получения a,b-ненасыщенных альдегидов окислением замещенных аллиловых спиртов универсальным окислителем является оксид марганца (IV) MnO2. Этот реагент окисляет в петролейном эфире или хлористом метилене ненасыщенные спирты с одной или несколькими двойными или тройными связями без изомеризации и перегруппировки, что с успехом используется в синтезе природных соединений.
Комплексы хромового ангидрида с пиридином окисляют и вторичные спирты до кетонов с почти количественными выходами.
Однако чаще всего для окисления вторичных спиртов используют реактив Джонса — раствор строго рассчитанного количества CrO3 в водной серной кислоте. Важное достоинство реагента Джонса состоит в том, что вторичные спирты, содержащие двойную или тройную связь, быстро окисляются до кетонов без затрагивания кратных связей.
Первичные спирты окисляются реактивом Джонса до карбоновых кислот.
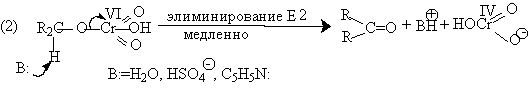
Механизм оксиления спиртов под действием хромового ангидрида подробно изучен. Эта реакция включает несколько стадий. Сначала из спирта и CrO3 образуется сложный эфир хромовой кислоты. Во второй, ключевой, стадии имеет место окислительно-восстановительное элиминирование, приводящее к образованию альдегида или кетона и частицы, содержащей Cr(IV). При окислении дейтерированного CH3CD(OH)CH3 и недейтерированного пропанола-2 наблюдается кинетический изотопный эффект КН/KD=7. Столь значительный первичный кинетический изотопный эффект показывает, что элиминирование является наиболее медленной стадией, определяющей скорость всего процесса.
Установлено, что частицы, содержащие хром (IV), также принимают участие в окислении спирта.
Окисление под действием соединений Cr (IV) можно полностью подавить с помощью солей, содержащих ионы Mn (II) или Ce (III), которые окисляются Cr (IV). Каталитические количества Ce (IV) также подавляют эту побочную реакцию, поскольку Ce (IV) катализируют диспропорционирование Cr(IV) на Cr(III) и Cr (VI).
Для третичных спиртов, не содержащих атомов водорода при карбонильном углероде, эфиры хромовой кислоты могут быть выделены.
Раствор хромового ангидрида в трет-бутиловом спирте также используется для окисления первичных и вторичных спиртов. Раствор хромового ангидрида в уксусной кислоте нередко употребляется в качестве окислителя вторичных спиртов до кетонов.
Механизм дальнейшего окисления альдегидов до карбоновых кислот по существу аналогичен механизму окисления спиртов. В водной среде альдегид находится в равновесии с геминальным 1,1-диолом, который образует сложный эфир с хромовым ангидридом. При элиминировании НCrO3 — из этого сложного эфира получается карбоновая кислота.
Поэтому для того, чтобы избежать дальнейшего окисления альдегида, окисление первичных спиртов следует проводить в апротонной среде при полном отсутствии влаги. Этому условию в полной мере удовлетворяют реагенты Коллинза и Кори, для которых в качестве растворителей используют тщательно обезвоженный хлористый метилен.
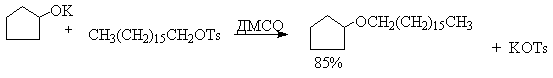
В последние тридцать лет разработано несколько эффективных способов окисления первичных и вторичных спиртов с помощью ДМСО или комплексов ДМСО с электрофильными агентами. Тозилаты первичных спиртов, также как и бензилтозилаты, окисляются в альдегиды при нагревании в ДМСО в течение 10-30 минут при 120-150 о С в присутствии гидрокарбоната натрия как слабого основания.
ДМСО в этой реакции выполняет роль нуклеофильного агента, который замещает тозилоксигруппу по обычному SN2 механизму с образованием алкоксисульфониевой соли. Катион алкоксисульфониевой соли далее подвергается окислительно-восстановительному элиминированию по механизму, аналогичному для окислительно-восстановительного элиминирования из сложных эфиров хромовой кислоты. Гидрокарбонат-ион является основанием в этой Е2 реакции элиминирования, приводящей к диметилсульфиду и альдегиду. В качестве примера приведем получение гептаналя и и-бромбензальдегида.
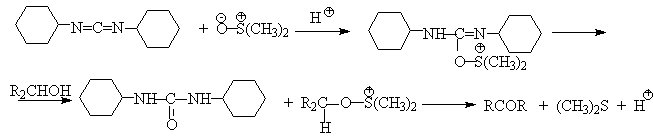
Слабый нуклеофильный агент ДМСО легко превращается в сильный электрофильный агент, который реагирует со спиртами уже ниже 0 o С в мягких условиях. Необходимую активацию ДМСО проводят с помощью серного ангидрида, трифторуксусного ангидрида, N-хлорсукцинимиджа или N,N-дициклогексилкарбодиимида C6H11N=C=NC6H11 (ДЦГК). Во всех случаях в качестве реакционноспособного интермедиата образуется активированная алкоксисульфониевая соль, которая далее подвергается внутримолекулярной окислительно-восстановительной фрагментации.
Для окисления первичных и вторичных спиртов до альдегидов и кетонов в мягких условиях эффективен комплекс ДМСО с SOs, образующийся при взаимодействии пиридинсульфотриоксида с ДМСО.
SO3 в качестве электрофильной частицы может быть заменен трифторуксусным ангидридом или ДЦГК (реактив Пфитцера-Моффата). Этот реагент в настоящее время употребляется наиболее часто.
Приведем для иллюстрации два примера окисления спиртов комплексами ДМСО.
Эти методы окисления вытеснили старый громоздкий способ окисления вторичных спиртов по Оппенауэру, который заключается в нагревании спирта с алкоголятом алюминия в присутствии карбонильного соединения в качестве акцептора гидрид-ионов. Этот процесс обратим (обратная реакция называется восстановлением по Меервейну-Понндорфу-Верлею). Равновесие можно сместить вправо, если выбрать сильный акцептор гидрид-иона — п-хинон, бензофенон, хлоранил (2,3,5,6-тетрахлор-1,4-бензохинон).
Окисление спиртов по Оппенауэру в теоретическом отношении представляет собой пример окислительного процесса с переносом гидрид-иона от восстановителя к окислителю в одну стадию, в то время, как в выше описанных процессах окисление спиртов осуществляется в несколько стадий с последовательным переносом одного или нескольких электронов.
Для получения альдегидов и кетонов из первичных и вторичных спиртов можно пользоваться реакцией каталитического дегидрирования. Так в промышленности из метанола получают формальдегид, из бутилового спирта -масляный альдегид и из циклогексанола — циклогексанон. В качестве катализатора используется медь, серебро, хромит меди.
6. Защитные группы для гидроксильной группы
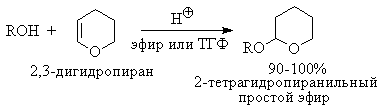
При осуществлении многостадийных синтезов сложных органических молекул часто необходимо защитить гидроксильную группу, чтобы провести требуемую реакцию по другой функциональной группе. Введение «защиты» включает три стадии: 1) образование инертного производного; 2) выполнение требуемого превращения с другой функциональной группой и 3) снятие защитной группы. Для гидроксильной группы хорошо зарекомендовавшим себя методом является образование ацеталя в результате кислотно-катализируемого присоединения спирта к 2,3-дигидропирану.
Подобно простым эфирам, тетрагидропиральные (ТГП) эфиры инертны по отношению к нуклеофильным агентам, сильным основаниям (RMgX, RLi, NaH, NaNHz, RONa и др.), а также окислителям и восстановителям. Однако ТГП-группа чувствительна к кислотному расщеплению и легко удаляется в растворе хлористого водорода в метаноле.
Ниже приведен типичный пример использования защитной ТГП-группы.
Другой защитной группой является триметилсилильная группа, которая вводится с помощью (СНз)зSiС1. Эта группа легко удаляется под действием фторид-иона.
Однако триметилсилильная защитная группа малоустойчива по отношению как к кислотным, так и основным агентам и она легко снимается даже при хроматографии на силикагеле. Значительно более устойчива трет-бутилдиметилсилильная группа, которая вводится с помощью [(СНз)зС](СНз)281С1 и удаляется обработкой KF или (C4H9)4NF. Две другие защитные группы -бензильная и трифенилметильная (тритильная) вводятся с помощью бензилбромида и трифенилхлорметана в присутствии основания — третичного амина, а синаются или каталитическим гидрогенолизом или действием раствора HBr в ледяной уксусной кислоте.
Нагревание спирта с концентрированной серной кислотой уравнение
Наиболее доступный и распространенный лабораторный способ получения этилена — нагревание смеси этилового спирта с концентрированной серной кислотой. Однако первоначально взаимодействие спирта с кислотой приводит к образованию сложного эфира, который затем при нагревании распадается на этилен и серную кислоту:
Таким образом, серная кислота выходит из реакции, т.е. выполняет роль катализатора.
Уравнение реакции получения этилена дается учащимся лишь в суммарном виде:
Чтобы увеличить выход этилена и тем самым обеспечить проведение всех опытов с ним при экономном расходовании спирта, необходимо учесть следующее.
Этилен, как было показано выше, образуется из кислого этилового эфира серной кислоты (этилсерной кислоты). Если в реакцию этерификации вступит не весь спирт, то при нагревании смеси он будет отгоняться вместе с этиленом, т.е. будет потерян для реакции. Реакция этерификации, как известно, обратима, и при эквимолекулярном соотношении спирта и серной кислоты, кроме эфира, в смеси будет содержаться известное количество спирта и кислоты. Чтобы сдвинуть равновесие в сторону образования эфира и полнее использовать спирт, следует увеличить содержание серной кислоты. Опыт показывает, что при увеличении количества кислоты количество этерифицируюшегося спирта в начале заметно возрастает, а после того как соотношение количеств кислоты и спирта достигнет примерно 3:1, оно возрастает уже незначительно. Поэтому практически наилучшие результаты получаются, если на 1 моль (46 г) спирта брать 3 моля (3 o 98 = 294 г) серной кислоты или на 1 объем спирта брать примерно тройной объем концентрированной серной кислоты. В таком случае спирт будет этерифицирован в значительной своей части, потери его будут очень невелики и выход этилена возрастет.
По мере разложения эфира концентрация кислоты будет увеличиваться, и условия для более полного использования спирта будут улучшаться. Чтобы реакция шла без обильного пенообразования и сильных толчков, к смеси добавляют битое стекло или фарфоровую крошку, обеспечивающие равномерное кипение.
Демонстрационный опыт проводят следующим образом. В колбу емкостью 300-500 мл наливают 20 мл этилового спирта и постепенно добавляют 60 мл концентрированной серной кислоты. Смесь взбалтывают и охлаждают в струе воды. Затем насыпают фарфоровую крошку, закрывают колбу плотно пробкой с отводной трубкой и присоединяют промывные склянки (лучше склянки Тищенко) с концентрированной серной кислотой и с 10-процентным раствором щелочи. К склянке со щелочью присоединяют стеклянную трубку, опущенную в ванночку с водой для собирания газа:
Колбу укрепляют в штативе на асбестированной сетке или на песочной бане и нагревают тем или иным способом, предварительно проверив прибор, как обычно, на герметичность. Вначале нагревание ведут довольно интенсивно, чтобы быстро перейти «порог» образования этилового эфира (140°С), затем, когда начнет выделяться этилен, нагревают медленно, поддерживая равномерный ток газа и по возможности не допуская вспенивания.
Когда проба газа в пробирке покажет, что воздух полностью вытеснен из прибора, этилен собирают в цилиндры и газометр, как было описано выше, или непосредственно используют для опытов: поджигают у отводной трубки, пропускают и бромную воду и т.п. Для прекращения реакции удаляют газоотводную трубку из ванны, отделяют промывные склянки от колбы и только после этого прекращают нагревание. При получении больших количеств этилена (например, при наполнении газометра для опытов, проводимых в нескольких классах) следует взять больше исходной смеси веществ.
Для постановки в качестве лабораторного опыта эксперимент можно значительно упростить. В пробирку, закрепленную в штативе, наливают 1 мл этилового спирта и осторожно прилипают 3 мл концентрированной серной кислоты. Добавляют несколько фарфоровых крупинок и закрывают пробирку пробкой, в которую вставлен узкий конец хлоркальциевой трубки, содержащей патронную известь (для улавливания оксидов серы и углерода). Широкий конец хлоркальциевой трубки закрывают пробкой с газоотводной трубкой, на конец которой надет резиновый шланг. Содержимое пробирки осторожно нагревают. Выждав некоторое время, необходимое для вытеснения из пробирки воздуха, этилен собирают в другую пробирку по принципу вытеснения или пропускают в реакционный раствор брома или перманганата калия:
Нагревание спирта с концентрированной серной кислотой уравнение
В одну пробирку налейте 2-3 мл этилового спирта и осторожно добавьте 6-9 мл концентрированной серной кислоты. Затем всыпьте немного предварительно прокалённого песка, чтобы избежать толчков жидкости при кипении. Закройте пробирку пробкой с газоотводной трубкой, закрепите её в штативе (рис. 18) и осторожно нагрейте.
- Какой газ выделяется при нагревании смеси этилового спирта с серной кислотой?
При нагревании смеси этилового спирта с серной кислотой образуется газ этилен:
C2H5OH t, H₂SO₄ ⟶ CH2=CH2↑ + H2O