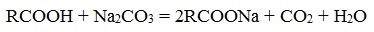Известно несколько способов получения мыл.
- Нейтрализация кислот углекислым натрием (кальцинированной содой)
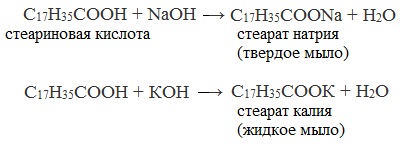
- Нейтрализация кислот гидроксидом натрия (каустической содой)
Жидкие калиевые мыла и твердые натриевые мыла получают растворением высших алифатических кислот в водных растворах едких щелочей:
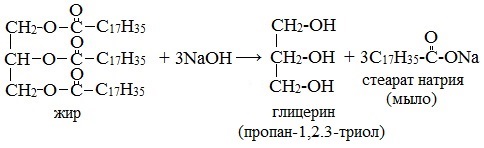
- Омыление триглицеридов гидроксидом натрия
Получение мыла основано на реакции омыления — кипячением животного сала либо растительного масла с гидроксидом натрия или калия (гидролиз сложных эфиров жирных кислот (т.е. жиров) в присутствии щелочей), в результате которого образуется трехатомный спирт глицерин и соли высших карбоновых кислот (мыло):
Прямой способ. В специальных емкостях (варочных котлах) нагретые жиры омыляют едкой щёлочью (обычно гидроксидом натрия). Для гидролиза жира в щелочной среде берется немного топленого свиного сала, около 10 мл этилового спирта и 10 мл раствора щелочи.
В результате реакции в варочных котлах образуется однородная вязкая жидкость, густеющая при охлаждении — мыльный клей, состоящий из мыла и глицерина. Содержание жирных кислот в мыле, полученном непосредственно из мыльного клея обычно 40—60 %. Такой продукт имеет название «клеевого мыла».
Косвенный способ заключается в дальнейшей обработке мыльного клея.
Варку мыла заканчивают обработкой мыльного раствора (мыльного клея) избытком щелочи или раствором хлорида натрия. В результате этого на поверхность раствора всплывает концентрированный слой мыла, называемый ядром.
Он содержит не менее 60 % жирных кислот; нижний слой — подмыльный щёлок, раствор электролита с большим содержанием глицерина. (также содержит загрязняющие компоненты, содержавшиеся в исходном сырье).
Полученное мыло называют ядровым, а процесс его выделения из раствора – отсолкой или высаливанием.
Производство хозяйственного мыла заканчивают на стадии высаливания, при этом происходит очистка мыла от белковых, красящих и механических примесей. Производство туалетного мыла проходит все стадии механической обработки. Наиболее важной из них является шлифовка, т.е. переведение ядрового мыла в раствор кипячением с горячей водой и повторным высаливанием. При этом мыло получается особо чистым и светлым.
Для улучшения некоторых характеристик хозяйственного мыла, а также для удешевления в него вводят наполнители: некоторые натриевые соли, которые при растворении в воде приводят к подщелачиванию; клеи и крахмал – способствуют пенообразованию мыльного раствора и стойкости пены, однако моющей способностью не обладают.
Особое место среди наполнителей занимает сапонин, получаемый выщелачиванием некоторых растений и прежде всего мыльного корня. Он хорошо растворяется в воде и его растворы сильно пенятся. Сапонин применяют для дорогих сортов мыла.
При использовании в качестве щёлочи каустической соды получают твердое натриевое мыло. Мягкое или даже жидкое калиевое мыло образуется, когда применяется каустический поташ.
Главное условие красящих веществ, употребляемых для подкраски туалетного мыла, — это хорошее смешивание их с мылом и отсутствие вредного влияния на кожу.
Красный цвет для прозрачного мыла получают при помощи фуксина и эозина, для непрозрачного мыла используют киноварь и сурик. Желтый цвет мылу придает экстракт куркумы и пикриновая кислота. Для получения мыла зеленого цвета применяют зеленый анилин или хромовую зеленую краску. Коричневый цвет мыла образуется из светлой или темной коричневой анилиновой краски или жженого сахара.
В промышленности вместо щелочи применяют соду, а так как жиры являются одной из главных составляющих пищи человека, то за основу берут не животные жиры, а углеводороды, входящие в состав парафинов (нефти).
Мыла полученные из синтетических кислот аналогичны по своей химической природе обычным мылам.
Мыла: классификация, получение, свойства
С химической точки зрения мыла представляют собой соли высших жирных (C8–C18), нафтеновых или смоляных кислот.
В бытовом смысле — это технические продукты, обладающие моющим действием.
Классификация мыла
Существует несколько классификаций мыл.
По растворимости мыла делят на:
- Растворимые щелочные мыла — калиевые, натриевые, аммониевые соли жирных кислот. В зависимости от природы катиона мыла растворимость в воде увеличивается в ряду: Li + — Na + — K + — NH4 +
- нерастворимые металлические мыла — соли поливалентных металлов (Ca, Mg, Ni, Mn, Al, Co, Pb).
По консистенции:
- Жидкие мыла – соли калия, аммония
- Твердые мыла – соли натрия, лития, поливалентных металлов
По назначению:
По способу получения:
Химические способы получения мыла
Производство мыла (мыловарение) довольно длительный и сложный процесс, состоящий из нескольких стадий.
Если рассматривать только химические реакции, лежащие в основе получения мыла, то как уже было рассмотрено мыла можно получить при щелочном гидролизе жиров, при этом образуются глицерин и соли высших карбоновых кислот – мыла. Кроме этого мыла получаются при нейтрализации высших карбоновых кислот гидроксидом натрия или калия или углекислым натрием:
- Омыление триглицеридов гидроксидами натрия или калия
- Нейтрализация высших карбоновых кислот гидроксидом натрия (каустической содой) или гидроксидом калия
Твердые мыла получают при растворении высших карбоновых кислот в водном растворе гидроксида натрия, жидкие мыла — при растворении высших карбоновых кислот в водном растворе гидроксида калия.
- Нейтрализация высших карбоновых кислот углекислым натрием (кальцинированной содой):
Промышленное получение мыла (варка мыла)
Для производства мыла в промышленности используют как синтетические жирные (высшие) кислоты, так и животные жиры, растительные масла, канифоль.
Для получения хозяйственных мыл применяют саломас с температурой плавления 46–60°С, для туалетного мыла — с температурой плавления 39–43°С.
Салома́с — это твёрдый жир, получаемый в промышленности путём гидрогенизации жидких жиров, в основном растительных масел.
Все жиры, используемые при варке мыла, не должны содержать воду и механические примеси.
Жидкие растительные масла применяют в мыловарении всех видов жидких хозяйственных и туалетных мыл. Наиболее ценным из является хлопковое масло, содержащее до 30 % насыщенных высших кислот, в основном пальмитиновой. Также используют и другие масла, такие как подсолнечное, соевое, кокосовое, пальмовое.
Введение небольших количеств жидких растительных масел в рецептуру хозяйственных мыл способствует снижению температуры их застывания.
Внесение 10–15 % канифоли увеличивает растворимость и пластичность мыла.
Основные стадии варки мыла
В промышленности мыла получают в две стадии – первая стадия химическая, вторая — механическая:
- Химическая стадия – варка мыла. Вначале проводят карбонатное омыление, при котором нейтрализуется около 70 % свободных жирных кислот. Затем проводят каустическое доомыление – нейтрализация оставшихся кислот гидроксидом натрия.
- Механическая стадия – охлаждение, сушка, шлифовка, отделка и упаковка готового продукта
Способы варки мыла
Варку мыла (химическая стадия) можно осуществить прямым и косвенным способом.
Для варки мыла прямым способом исходная жировая смесь должна быть хорошо очищена. Этим способом проводят нейтрализацию жировой смеси растворами содопродуктов и получают мыльный клей, содержащий 67–70 % жирных кислот. Далее его подвергают механической очистке — охлаждению, сушке, шлифовке, отделке. Прямой способ используется при варке хозяйственного мыла.
При варке мыла косвенным способом полученный прямым способом мыльный клей, подвергают дальнейшей обработке растворами электролитов, т.е. проводят высаливание. При этом происходит разделение мыльной массы на фазы: ядро и подмыльный щелок или ядро, подмыльный клей, подмыльный щелок. Полученное мыльное ядро в этом случае содержит 60–63 % жирных кислот. Далее полученное мыльное ядро обрабатывают подобно мылу, сваренному прямым способом. В качестве электролитов используют NaCl, NaOH. Косвенный способ применим для варки мыла из неочищенного жирового сырья. Варка мыла косвенным способом позволяет получить мыло высокой степени чистоты.
Жидкое мыло готовят из растительных масел, канифоли, таллового масли и др. прямым или косвенным способом. В качестве основания применяют соединения калия (KOH, K2CO3).
Если при варке мыла использовалось сырье из животных или растительных жиров, то после отделения ядра выделяют образующийся побочный продукт – глицерин. Глицерин широко применяют в различных отраслях производства.
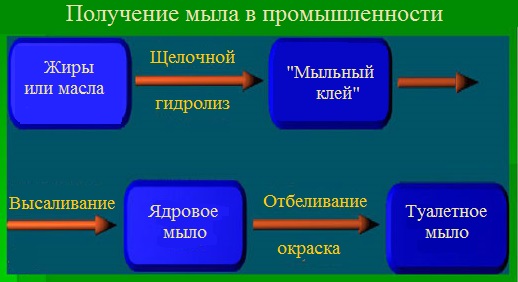
Кратко схему производства мыла можно представить следующим образом:
Моющие свойства мыла
Итак, мыла – соли высших жирных кислот – состоят из аниона жирной кислоты и катиона металла (чаще всего натрия или калия).
В водных растворах щелочные мыла подвергаются гидролизу, т.к. образованы слабыми кислотами и сильными основаниями. Их растворы имеют щелочную реакцию (рН>7). В сильно разбавленных растворах мыла полностью диссоциируют на ионы:
Способность мыла пениться, отмывать загрязнения связана с образованием мицелл и высокой поверхностной активности. Водорастворимые щелочные мыла являются анионными поверхностно-активными веществами.
Углеводородный остаток жирной кислоты является гидрофобной частью мыла, кабоксильный ион – гидрофильной частью.
Этапы растворения грязи под действием мыла:
- При соприкосновении мыла с грязью, гидрофобная часть мыла окружает гидрофобное загрязняющее вещество и проникает внутрь, а поверхность загрязнения покрывается оболочкой гидрофильных групп.
- Гидрофильная часть мыла взаимодействуют с полярными молекулами воды.
- Ионы мыла «захватывают» загрязнение и отрываются от поверхности, переходя в воду.
- Плавающие частицы удерживаются в растворе до его смены.
В домашних условиях тоже можно приготовить мыло. Имея под рукой необходимые ингредиенты, самостоятельное производство мыла не составит большого труда.
Глицериновое мыло с нуля на NaOH — новое прочтение старой идеи 2 🙂
Сейчас давайте проведём эксперимент по созданию мыла по такому же рецепту, но на гидроксиде натрия.
Мыло это непрозрачное, но назвать его иначе как глицериновым, я никак не могу 🙂
Рецепт я взяла такой же, как у калийного мыла с начала недели, но теперь мы используем щёлочь NaOH — гидроксид натрия, потому что будем делать твёрдое мыло.
Правда, пришлось внести некоторые изменения, а именно — совсем без воды обойтись не удалось 🙂
Итак, чтобы сделать глицериновое мыло с нуля своими руками, вам понадобится:
8% касторовое масло
15% кокосовое масло
62% оливковое масло
пережир на калькуляторе установлен на 5%
процентное соотношение воды к маслам на калькуляторе 38%
щелочь гидроксид натрия (NaOH) — по калькулятору щелочи
глицерин = значение воды, рассчитанной на калькуляторе щелочи
вода + 5-10% к весу масел
Рецепт может быть любым, просто вместо воды, положенной по калькулятору щелочи, вы берете глицерин.
Почему я использую здесь воду?
Если в глицериновом мыле на гидроксиде калия при реакции глицерина и щелочи образовывалось достаточно воды для растворения гидроксида калия, то гидроксид натрия реагирует с глицерином в меньшем количестве, соответственно воды выделяется тоже меньше, и её недостаточно для полного растворения гидроксида натрия.
Порядок приготовления мыла с нуля:
Во-первых, помните о мерах безопасности — на вас должны быть очки и перчатки.
Взвешиваем глицерин и греем его до температуры 100-110 градусов.
Высокая температура очень важна, т.к. она запускает реакцию. На этот раз я грела глицерин в микроволновке.
Добавляем щёлочь в горячий глицерин.
Не бойтесь. Также не бойтесь температуры — она высокая — 130-140 градусов
Нерастворённый гидроксид натрия процедите через ситечко
И добавьте к нему горячую воду до полного растворения крупинок.
Смешайте масла и щелочной раствор — и глицериновый, и водный!
Смешайте смесь погружным блендером
След очень интересный — как гель! Может быть, это и есть гель ? 🙂
Можете добавить на этом этапе отдушку, если вы делаете мыло холодным способом.
И разлейте его в формы.
Я сделала 2 партии:
Холодный способ приготовления глицеринового мыла с нуля:
Могу только поделиться наблюдениями, т.к. зреть ему ещё 4 недели.
Мыло оставалось полужидким (консистенция мёда) ещё часа 4.
Никакие «пики» на его поверхности не сохранялись.
Это автоматически делает его необыкновенной находкой для изготовления мыла со свирлами!
Через сутки мыло было полумягким. Через 3-4 дня оно стало достаточно плотным, чтобы вынуть его из формы и порезать.
Мыло плотное, но пружинистое — очень интересное.
И цвет совершенно белый — восхитительно!
Горячий способ приготовления глицеринового мыла с нуля:
Конечно, я бы не выдержала ждать 4 недели, чтобы попробовать новое мыло.
Часть я отделила и сразу же сварила горяим способом на водяной бане.
Мыло постепенно проходило все стадии готовности
И через пару часов оно готово! Сразу в форму!
Застывает оно моментально!
Обмылки пробуем: пена есть!
Кусок достала из формы на следующий день:
Обычно горячий способ не бывает таким ровным, но тут получилось!
Мыло пружинистое, но твёрдое, не проминается.
И очень-очень приятное по свойствам 🙂
Добавить комментарий через Vkontakte
17 комментариев
Красота какая! У меня сразу пара вопросов. 1. а нельзя ли на стадии растворения щёлочи просто добавить воды к глицерину сразу или уже когда видно, что не всё растворилось? Хотя понимаю, что ты такое мыло первый раз делала и можешь не знать ответа 🙂 2. какую отдушку добавляла? как она себя в ХС повела в этом мыле? меня в основном загущение мыла интересует. мечтаю о том, чтоб добавил отдушку, а на мыльной массе это никак не отразилось. читала, что есть американские отдушки специальные для ХС, но пока до них не добралась.
А вообще, я тобой восхищаюсь как мыловаром 🙂 сама уже с начала лета ничего не варила, но в ближайшее время планирую возобновлять, ибо НГ близится.
viollanka,
1) делала первый раз, мастер-классов таких не видела, так что не знаю 🙂
Думаю, можно. Только водичку погорячей возьми.
2) не добавляла. Но вообще вести должна как в обычном мыле хс, т.к. химически мыло отличается лишь наличием неагрессивного глицерина.
С загущением не знаю, буду ещё экспериментировать в этом направлении, т.к. мыло без отдушки восхитительно долго не густело, а потом — рраз и схватилось!
Наташа, спасибо!у тебя столько идей! МОЛОДЕЦ! обязательно попробую такое мыло!
Наталья,здравствуйте! а гель ваше мыло холодным способом проходило? или просто залили в форму и все?
Галина,
у меня ощущение, что гель мыло проходило, когда я его до следа доводила.
Специально я его не нагревала, потому что рабочие температуры и температура смешивания были очень высокие.
Скажите, пожалуйста! А Вы воду в остаток щёлочи добавляли, или как требует ОБЖ — щёлочь в воду?
АРТА,
конечно, следуем ОБЖ.
Но строго говоря, тут уже не чистая щёлочь, а смесь щелочи и глицерина, на фото как раз видно, какая она мокрая 🙂
В любом случае, я всегда за соблюдение техники безопасности.
Наталья, вода для растворения непрореагирующей щелочи, я если она вся прореагировала?
Литовка, тогда не нужна 🙂
Наталья, большое спасибо за великолепную идею!
Хотела уточнить, возможно ли поставить мелкие порционные формочки с мылом в морозилку во избежание геля?
Упор идет именно на то, чтобы кусочки были фигурные, порционные.
Варю принципиально ХС. Духовка без термометра, а на водяной бане однажды варила уже калийное мыло, и неудачно, пришлось еще 2 недели вызревать ему.
Благодарю за ответ.
Маш-Маш,
тут гель может пройти без вашего ведома, мы глицерин обязательно греем до высокой температуры.
А вот красивую фигурную форму это мыло легко принимает, и гс и хс, так что нет необходимости в холодильнике.
Я сегодня сделала это мыло! Аж два раза! 🙂 Первый раз — первый блин 🙁 Щелочь в глицерине совсем не хотела расходится, масса была похожа на манную кашу. Я ее и перетирала, она на меня слегка шипела, и грела, и снова перетирала, потом добавила кипятка, но бОльшая часть щелочи так и осталась шариками.
Т.к. масла я уже отмеряла и прогрела, то оставлять их «на завтра» было невозможно, поскольку завтра начинаются каникулы, и все мои мужики будут дома, а это — рейды на кухню каждые 5-10 минут. Короче, решилась я на второй заход, но по упрощенной схеме.
Я взяла пополам глицерина и воды. Сначала растворили щелочь в воды. Полностью она, конечно не разошлась, т.к. воды для нее было мало. Попутно я нагрела глицерин до 130 градусов. Пока мешала щелочь, глиц остыл до 110, вот тут-то я их и соединила — щелочной раствор в глиц. Реацию щелочь продолжила — раствор стал снова мутным, ну и градусник показывал несколько минут повышение температуры. Часть щелочи все равно осталась мусорными хлопьями, но они остались в ситечке. 🙂 Потом все как написано — щелочь+масла, гелевый след (очень красивый!), отдушки Манго и Сандал, форма, пики (пока держатся), сверху притрусила бордовой перламутровой микой. Ждем-с. Спасибо большое за вдохновение!
irike, рада, что получилось, хоть и не с первого раза 🙂
Наталья, спасибо за рецепт и за то, что радуете нас Вашими экспериментами. Постоянно читаю и загораюсь мотивацией.
Делала 2 варианта. По Вашему рецепту и как сделала irike. И второй вариант получился лучше, проще, комфортнее, как хотите.
Воду брала 1:1 со щелочью, остальное глицерин. В глицерин вливать щелочнлй раствор желательно частями, повышение температуры происходит на 10 — 17 градусов.
И пережир я выставила на 8%. В Вашем варианте щелочь остается немного на сите и 5% вполне обоснованы. Во втором случае щелочь реагирует вся и даже большая дозировка глицерина не дает спасения. Возможно что у меня глицерин растительный? Специально пробовала в разные формы 5%, 7% и 8% для чтстлты эксперимента. Для моей жирной кожи 8% — для тела самое оно. 5% можно лишь для лица, подсушивает.
Буду рада, если эти эксперименты кому — то пригодятся )
Спасибо за ваш опыт 🙂
щёлочь, которая осталась на сите была растворена доп. водой, я её не выкинула, если что 🙂
Наталья, да, я прочитала о том, что щелочь, оставшаяся на сите была растворена :-), но у меня есть догадка, что когда щелочь растворяется в глицерине, или реакция идет по — другому, или оставшаяся щелочь теряет свои свойства немного. В смысле, что она уже прореагировала с глицерином и не такая концентрированная.
Поэтому, опять таки догадка, что процент нужно повысить для людей с сухой кожей, т.к. в случае растворения каустика в воде, раствор становится более концентрированный. И мне комфортнее мыться с 7%, ну а с 8% это сказка. И это при моей жирной коже.
Я это имела ввиду 🙂
Вообще глицерин ооочень мало реагирует со щелочью, так что этим значением можно пренебречь. зато при реакции выделяет воду, которой почти достаточно, чтобы щелочь растворить.
А пережир — это дело индивидуальное, вы правы 🙂
Оставить комментарий Отменить ответ
Этот сайт использует Akismet для борьбы со спамом. Узнайте, как обрабатываются ваши данные комментариев.