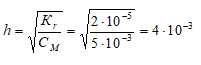Алгоритм написания уравнений гидролиза
Гидролиз по катиону
1. Определяем тип гидролиза. Необходимо написать уравнение диссоциации соли.
Гидролиз сульфата меди(II): CuSO4 = Cu 2+ + SO4 2–
Соль образована катионом слабого основания и анионом сильной кислоты. Гидролиз по катиону.
2. Записываем ионное уравнение гидролиза, определяем среду:
Cu 2+ + HOH CuOH + + H + ;
образуется катион гидроксомеди(II) и ион водорода, среда кислая
3. Составляем молекулярное уравнение. Из положительных и отрицательных частиц находящихся в растворе, записываются нейтральные частицы, существующие только на бумаге. В данном случае из CuOH + SO4 2– составляем (CuOH)2SO4. Для уравнивания числа ионов меди необходимо перед сульфатом меди поставить коэффициент два. Получаем:
Продукт реакции относится к группе основных солей: сульфат гидроксомеди(II).
- Ступенчатый гидролиз аниона — Cus?
- Молекулярное и ионно молекулярное уравнение гидролиза Al2(SO4)3 + H2O ступенчато?
- Как определить, по катиону или по аниону идёт гидролиз?
- Написать ступенчатый гидролиз CaC2 AL4C3 NiCl2?
- Установите, по какому типу проходит гидролиз сульфида аммония : Выберите один ответ : А?
- Установите соответствие между названием соли и ее отношением к гидролизу?
- Установите соответствие между названием соли и ее способностью к гидролизу?
- Как зависит гидролиз солей от природы катиона и аниона, образующих соль?
- Установите, по какому типу проходит гидролиз ацетата калия : Выберите один ответ : А?
- Будьте добры, объясните что означает гидролиз по аниону и катиону?
- Составить уравнение гидролиза соли?
- Как правильно написать уравнения гидролиза и рассчитать константу и степень гидролиза соли
- Молекулярная и ионная формы уравнений реакций гидролиза
- а) Гидролиз сульфида калия:
- б) Гидролиз сульфата меди (ⅠⅠ):
- в) Совместный гидролиз хлорида алюминия и ацетата калия:
- Определение степени гидролиза и рН раствора цианида калия
Ступенчатый гидролиз аниона — Cus?
Химия | 10 — 11 классы
Ступенчатый гидролиз аниона — Cus.
S(2 — ) + H2O — — > ; HS( — ) + OH( — )
HS( — ) + H2O — — > ; OH( — ) + H2S ↑.
Молекулярное и ионно молекулярное уравнение гидролиза Al2(SO4)3 + H2O ступенчато?
Молекулярное и ионно молекулярное уравнение гидролиза Al2(SO4)3 + H2O ступенчато.
Как определить, по катиону или по аниону идёт гидролиз?
Как определить, по катиону или по аниону идёт гидролиз?
Не могу разобраться : ( Напишите подробно, пожалуйста!
Написать ступенчатый гидролиз CaC2 AL4C3 NiCl2?
Написать ступенчатый гидролиз CaC2 AL4C3 NiCl2.
Установите, по какому типу проходит гидролиз сульфида аммония : Выберите один ответ : А?
Установите, по какому типу проходит гидролиз сульфида аммония : Выберите один ответ : А.
Гидролиз по катиону B.
Гидролиз по аниону С.
Гидролизу не подвергается Д.
Гидролиз по катиону и аниону.
Установите соответствие между названием соли и ее отношением к гидролизу?
Установите соответствие между названием соли и ее отношением к гидролизу.
В)нитрат свинца 2
1) гидролиз по катиону
2) гидролиз по аниону
3) гидролиз по катиону и аниону
4) гидролизу не подвергается.
Установите соответствие между названием соли и ее способностью к гидролизу?
Установите соответствие между названием соли и ее способностью к гидролизу.
А) бромид аммония Б) бромид калия В) сульфид хрома Г) сульфат хрома 1) не гидролизуется 2) гидролиз по катиону 3) гидролиз по аниону 4) полный гидролиз(по катиону и аниону).
Как зависит гидролиз солей от природы катиона и аниона, образующих соль?
Как зависит гидролиз солей от природы катиона и аниона, образующих соль.
Установите, по какому типу проходит гидролиз ацетата калия : Выберите один ответ : А?
Установите, по какому типу проходит гидролиз ацетата калия : Выберите один ответ : А.
Гидролиз по катиону B.
Гидролиз по аниону С.
Гидролизу не подвергается Д.
Гидролиз по катиону и аниону.
Будьте добры, объясните что означает гидролиз по аниону и катиону?
Будьте добры, объясните что означает гидролиз по аниону и катиону?
Составить уравнение гидролиза соли?
Составить уравнение гидролиза соли.
Указать значение pH.
По какому типу гидролизуется соль а) по катиону ; б) по аниону ; в) и по катиону и по аниону : CoCl2.
На этой странице сайта размещен вопрос Ступенчатый гидролиз аниона — Cus? из категории Химия с правильным ответом на него. Уровень сложности вопроса соответствует знаниям учеников 10 — 11 классов. Здесь же находятся ответы по заданному поиску, которые вы найдете с помощью автоматической системы. Одновременно с ответом на ваш вопрос показаны другие, похожие варианты по заданной теме. На этой странице можно обсудить все варианты ответов с другими пользователями сайта и получить от них наиболее полную подсказку.
Ar(Na) = 23 Ar(Mg) = 24 Ar(C) = 12 Ar(S) = 32 Ar(Cr) = 52 Ar(Se) = 79 Ar(Sn) = 119 Ar(Hg) = 201.
V(C₃H₆) = 50 л v — объем воздуха объемная доля кислорода в воздухе w(O) = 0, 2095 2C₃H₆ + 9O₂ = 6CO₂ + 6H₂O по уравнению реакции v(O₂) / 9 = v(C₃H₆) / 2 объем кислорода в воздухе v(O₂) = vw(O) v(O₂) = 9v(C₃H₆) / 2 = vw(O) объем воздуха v = 9v(C₃H₈) /..
2Al + 6H2O + Ba(OH)2 = Ba3 [Al (OH)6]2 + 3H2 реакция идет таким образом. А остальные части решения просто пропорция.
1. а) 4 метил пропин — 2 б) 2, 3 диметил бутен — 1 в) бутин — 1 г) 1, 4 дихлор бутен — 2 д) тетраметилметан е) 1, 2, 3, 4 тетрабром бутан 2. Дано W(C) = 90% = 0. 9 D(N2) = 1. 25 — — — — — — — — — — — — — — — — — — — — — — — — — M(CxHy) — ? M(CxHy..
Это лёгкая задача : ).
А). 3 — метил пентан б). Бутен — 2 в). Гексин — 2 г). 3, 4 — диметилгептанол — 4 д). 2 — метилуксусная кислота(или 2 — метилбутановая кислота).
Формула 1 моль железа является Fe, в ней 1 атом. Вычислим число атомов на 1 моль . Число Авагадро = 6. 02•10 ^ 23 N = 1•Na = 1•6, 02•10 ^ 23 = 6, 02•10 ^ 23 Значит в 1 моль 6, 02•10 ^ 23 атомов А в 5 моль получится х Составим пропорцию Получим х =..
Для того чтобы была ионная связь разница межде электроотрицательносями дожна быть 2. 1 и более мы можем частично сказать что это ионная связь но правильней если ковалентная N берет у Li 3 электрона.
Ответ есть на фотографии.
(140 — 110) / 10 = 3 Значит берем кубический корень из 27 и получаем 3 — коэффициент Вант — Гоффа.
Как правильно написать уравнения гидролиза и рассчитать константу и степень гидролиза соли
Молекулярная и ионная формы уравнений реакций гидролиза
Задача 21.
Напишите в молекулярной и ионной форме уравнения реакций гидролиза следующих солей: а) сульфида калия; б) сульфата меди (ⅠⅠ); в) совместного гидролиза хлорида алюминия и ацетата калия. Константа гидролиза соли.
Решение:
а) Гидролиз сульфида калия:
K2S + H2O = KHS + KOH — (молекулярная форма);
S 2– + HOH = HS – + OH – — (ионная форма).
б) Гидролиз сульфата меди (ⅠⅠ):
Cu 2+ + HOH = CuOH + + H + — (ионная форма).
в) Совместный гидролиз хлорида алюминия и ацетата калия:
AlCl3 + 3CH3COOK + 3H2O = Al(OH)3↓ + 3CH3COOH + 3KCl — (молекулярная форма);
Al 3+ + 3CH3COO – + 3HOH = Al(OH)3↓ + 3CH3COOH — (ионная форма).
Определение степени гидролиза и рН раствора цианида калия
Задача 22.
Определите степень гидролиза и pH раствора цианида калия с молярной концентрацией 0,005 моль/л.
Решение:
Цианид калия – соль, образованная сильным основанием КОН и слабой кислотой HCN, которая в водном растворе гидролизуется по аниону.
KCN + HOH ⇔ KOH + HCN
CN – + HOH ⇔ HCN + OH –
Таким образом, при гидролизе этой соли в растворе ее будет избыток ионов OH-, что придает раствору щелочную реакцию
(pH > 7 – среда щелочная).
Константа гидролиза соли, образованной слабой кислотой и сильным основанием определяется по формуле:
Kw = 1 . 10 -14 – ионное произведение воды.
KD(HCN) = 5 . 10 -10 – константа диссоциации циановодородной кислоты
Константа гидролиза цианида калия равна:
Kr(KCN) = Kw/KD(HCN) = (1 . 10 -14 )/(5 . 10 -10 ) = 2 . 10 -5 .
Находим степень гидролиза цианида калия, получим:
Рассчитаем молярную концентрацию ионов OH? в растворе, получим:
[OH – ] = h . СM(KCN) = (4 . 10 -3 ) . 0,005 = 2 . 10 -5 моль/л.
Находим гидроксильный показатель, получим:
рОН = — lg[OH – ] = – lg2 . 10 -5 = 5 — lg2 = 5 — 0,30 = 4,7.
Находим водородный показатель, получим