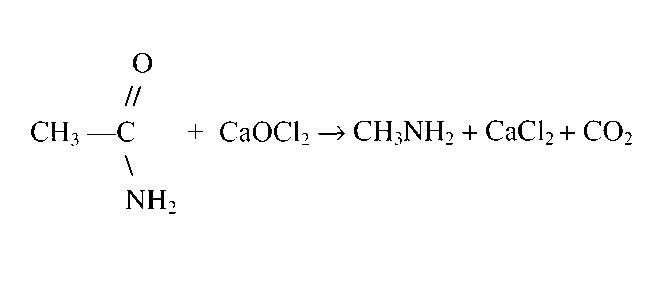Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Содержание
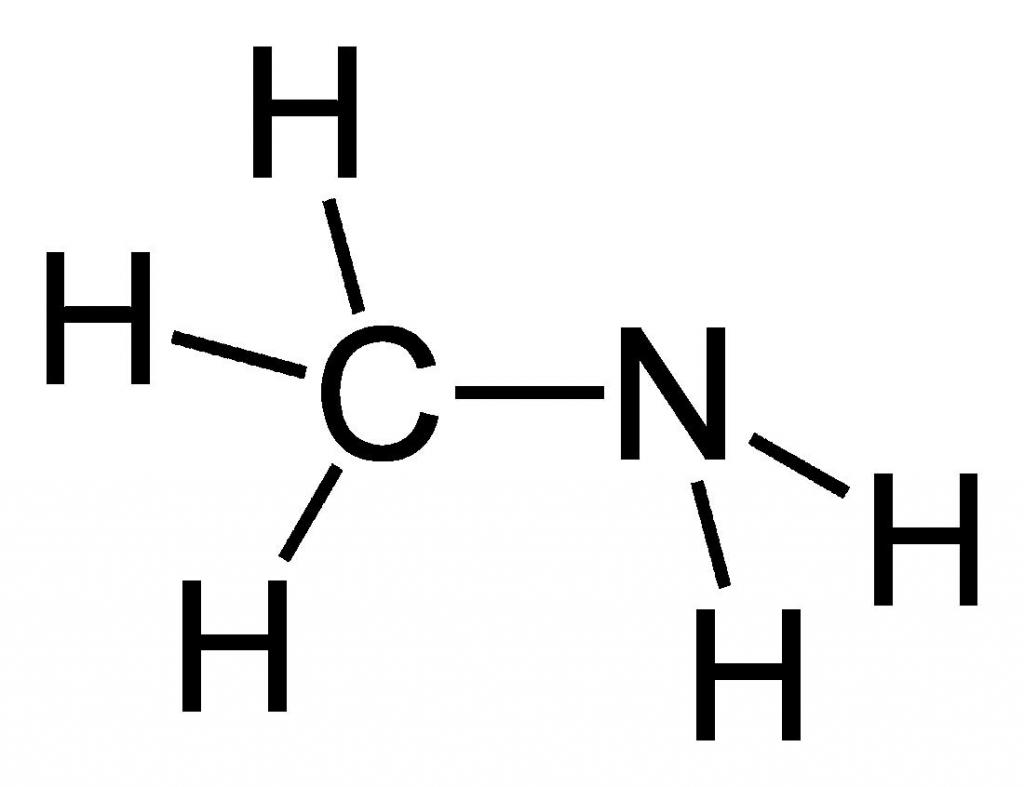
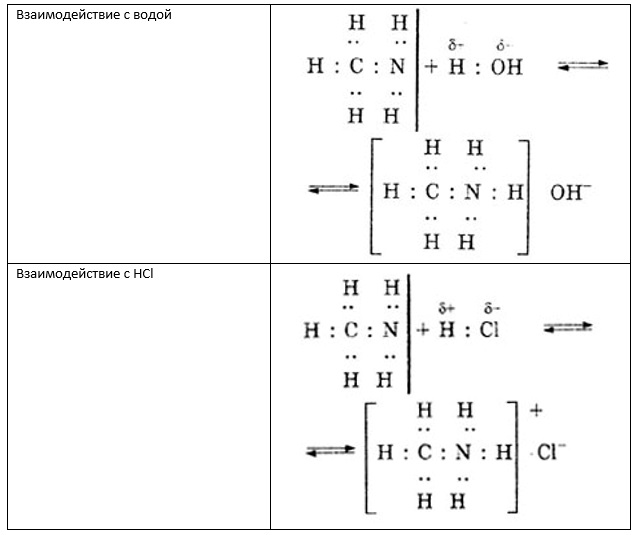
Метиламин: получение, свойства, использованиеФормула метиламина в химии считается почти примитивной. Однако для простых смертных одно название данного соединения является устрашающим, не говоря о том, что о структуре или формуле и вовсе ничего не известно. Многим неизвестно о специфичном запахе данного соединения или о его удивительно широких возможностях применения в различных производствах. Это вполне очевидно, ведь всего знать невозможно, и это факт. Но разве не интересно открывать для себя что-то ранее неизвестное? Что такое метиламин?Метиламин — органическое соединение с формулой CH3NH2. Он является одним из производных аммиака, принадлежит к алифатическим органическим веществам. Его относят к крайне огнеопасным соединениям, так как этот газ легко смешивается с воздухом, образуя при этом взрывчатые смеси. Структура данного вещества представлена на рисунке ниже. Из названия очевидно, что данное вещество относится к такому классу органических соединений, как амины (а именно — первичные амины), и оно является простейшим его представителем. При нормальных условиях метиламин — это газ (как и упоминалось ранее), без цвета, но с ярко выраженным запахом аммиака. Ингаляция данным веществом чревата сильным раздражением кожи, глаз, верхних дыхательных путей. Способен оказывать негативное влияние на почки и печень организма. А вдыхание его ведет к возбуждению и последующему угнетению центральной нервной системы. Возможно наступление смерти из-за остановки дыхания. Способы синтеза метиламинаОдин из промышленных способов получения метиламина опирается на реакцию метанола с аммиаком. Условиями проведения данного химического взаимодействия является высокая температура (370-430 °С), а также давление 20-30 бар. Реакция осуществляется в газовой фазе, но на гетерогенном катализаторе, основанном на цеолите. В смеси с метиламином образуются побочные вещества, такие как диметиламин и триметиламин. Поэтому данный способ получения нуждается в очистке метиламина (например, путем неоднократной перегонки). Иной способ получения метиламина заключается в проведении реакции формалина с хлоридом аммония при нагревании. Но и это не последний возможный вариант синтеза данного амина! Также известен способ получения метиламина посредством перегруппировки ацетамида по Гофману. На рисунке ниже представлено уравнение данной реакции. Химические свойства метиламинаКак правильно знакомиться с новым химическим соединением? Для начала нужно узнать, каково его название, особенности структуры. Затем важно понять, как его можно получить, поэтому сначала было рассказано о методах получения метиламина. А теперь нужно изучить его химические свойства. Данному органическому соединению присущи все типичные свойства первичных аминов, так как оно является стандартным представителем данного класса. Если в качестве вещества, вступающего в реакцию с метиламином, выступает вода или минеральная кислота, то происходит образование, соответственно, гидроксида метиламмония или кристаллической соли. Данные реакции представлены на рисунке ниже. Если проводить сравнение метиламина с анилином или аммиаком, то можно прийти к выводу, что метиламин проявляет более сильные основные свойства. Это объясняется тем, что атом азота в составе молекул метиламина более электроотрицателен. Если в качестве вещества, вступающего в реакцию с метиламином, выступает NaOCl, то происходит хлорирование — замещение атома водорода в аминогруппе на атом хлора. Так же как и другие первичные амины, метиламин образует спирт при взаимодействии с азотистой кислотой (HNO2). Применение метиламина и условия храненияCH3NH2 имеет очень широкую область применения. Он используется для синтеза красителей, фармацевтических препаратов (например, неофиллина, теофиллина, промедола), пестицидов, гербицидов, инсектицидов (севин, шрадан), фунгицидов, стерилизаторов земли в сельской промышленности, а также применяется в ветеринарной медицине. Используется метиламин и при изготовлении сильных взрывоопасных веществ (таких как, например, тетрил), различных материалов для фото (метол), растворителей (например, ДМФА, диметилацетамид), ускорителей вулканизации, ингибиторов коррозии, дубильных веществ, ракетных топлив (N,N-диметилгидразин). Также встречается метиламин в природе как второстепенный экскрет у костных рыб. Чаще всего используют данное соединение в виде 40-процентного раствора в воде, метаноле, этаноле или тетрагидрофуране. Чтобы применять метиламин в производстве или в процессе изготовления чего-либо, необходимо правильно его хранить. Оптимальные условия хранения: в сжиженном виде в объеме 10-250 м 3 , в цилиндрических резервуарах, расположенных горизонтально, при комнатной температуре, но вдали от солнечных лучей, в местах, недоступных для детей и животных. Разумеется, при работе с метиламином, как и с любым другим химическим веществом, необходимо использовать специальную одежду, перчатки и очки для индивидуальной защиты. Особое внимание нужно уделить защите слизистых оболочек и органов дыхания. Амины: способы получения, строение и свойстваАмины – это органические производные аммиака NH3, в молекуле которого один, два или три атома водорода замещены на углеводородные радикалы. Строение аминовАтом азота находится в состоянии sp 3 -гибридизации, поэтому молекула имеет форму тетраэдра. Также атом азота в аминах имеет неподелённую электронную пару, поэтому амины проявляют свойства органических оснований. Классификация аминовПо количеству углеводородных радикалов, связанных с атомом азота, различают первичные, вторичные и третичные амины. По типу радикалов амины делят на алифатические, ароматические и смешанные.
Номенклатура аминов
При наличии одинаковых радикалов используют приставки ди и три.
В этом случае аминогруппа указывается в названии приставкой амино-:
Например, N-метиланилин: Символ N- ставится перед названием алкильного радикала, чтобы показать, что этот радикал связан с атомом азота, а не является заместителем в бензольном кольце. Изомерия аминовДля аминов характерна изомерия углеродного скелета, изомерия положения аминогруппы и изомерия различных типов аминов. Изомерия углеродного скелетаДля аминов характерна изомерия углеродного скелета (начиная с С4H9NH2).
Изомерия положения аминогруппыДля аминов характерна изомерия положения аминогруппы (начиная с С3H9N).
Изомерия между типами аминов
Физические свойства аминовПри обычной температуре низшие алифатические амины CH3NH2, (CH3)2NH и (CH3)3N – газы (с запахом аммиака), средние гомологи – жидкости (с резким рыбным запахом), высшие – твердые вещества без запаха. Ароматические амины – бесцветные жидкости с высокой температурой кипения или твердые вещества. Первичные и вторичные амины образуют слабые межмолекулярные водородные связи: Это объясняет относительно более высокую температуру кипения аминов по сравнению с алканами с близкой молекулярной массой. Амины также способны к образованию водородных связей с водой: Поэтому низшие амины хорошо растворимы в воде. С увеличением числа и размеров углеводородных радикалов растворимость аминов в воде уменьшается. Ароматические амины в воде не растворяются. Химические свойства аминов
Как в аммиаке, так и в аминах атом азота имеет неподеленную пару электронов: |


| Поэтому амины и аммиак обладают свойствами оснований. |
1. Основные свойства аминов
| Алифатические амины являются более сильными основаниями, чем аммиак, а ароматические — более слабыми. |
Это объясняется тем, что радикалы СН3–, С2Н5– увеличивают электронную плотность на атоме азота:
Это приводит к усилению основных свойств.
| Основные свойства аминов возрастают в ряду: |
1.1. Взаимодействие с водой
В водном растворе амины обратимо реагируют с водой. Среда водного раствора аминов — слабощелочная:
1.2. Взаимодействие с кислотами
Амины реагируют с кислотами, как минеральными, так и карбоновыми, и аминокислотами, образуя соли (или амиды в случае карбоновых кислот):
При взаимодействии аминов с многоосновными кислотами возможно образование кислых солей:
1.3. Взаимодействие с солями
Амины способны осаждать гидроксиды тяжелых металлов из водных растворов.
| Например, при взаимодействии с хлоридом железа (II) образуется осадок гидроксида железа (II): |
2. Окисление аминов
Амины сгорают в кислороде, образуя азот, углекислый газ и воду. Например, уравнение сгорания этиламина:
3. Взаимодействие с азотистой кислотой
Первичные алифатические амины при действии азотистой кислоты превращаются в спирты:
| Это качественная реакция на первичные амины – выделение азота. |
Вторичные амины (алифатические и ароматические) образуют нитрозосоединения — вещества желтого цвета:
4. Алкилирование аминов
Первичные амины способны взаимодействовать с галогеналканами с образованием соли вторичного амина:
Из полученной соли щелочью выделяют вторичный амин, который можно далее алкилировать до третичного амина.
Особенности анилина
Анилин С6H5-NH2 – это ароматический амин.
| Анилин – бесцветная маслянистая жидкость с характерным запахом. На воздухе окисляется и приобретает красно-бурую окраску. Ядовит. В воде практически не растворяется. |
При 18 о С в 100 мл воды растворяется 3,6г анилина. Раствор анилина не изменяет окраску индикаторов.
| Для анилина характерны реакции как по аминогруппе, так и по бензольному кольцу. |
- Бензольное кольцо уменьшает основные свойства аминогруппы по сравнению алифатическими аминами и даже с аммиаком:
Анилин не реагирует с водой, но реагирует с сильными кислотами, образуя соли:
- Бензольное кольцо в анилине становится более активным в реакциях замещения, чем у бензола.
Реакция с галогенами идёт без катализатора во все три орто- и пара- положения.
| Качественная реакция на анилин: реагирует с бромной водой с образованием 2,4,6-триброманилина (белый осадок ↓). |
Получение аминов
Восстановление нитросоединений
Первичные амины можно получить восстановлением нитросоединений.
- Гидрирование водородом:
- Восстановление сульфидом аммония:
- Алюминий в щелочнойсреде.
Алюминий реагирует с щелочами с образованием гидроксокомплексов.
В щелочной и нейтральной среде получаются амины.
Восстановлением нитробензола получают анилин.
- Металлами в кислой среде – железом, оловом или цинком в соляной кислоте.
При этом образуются не сами амины, а соли аминов:
Амины из раствора соли выделяют с помощью щелочи:
Алкилирование аммиака и аминов
При взаимодействии аммиака с галогеналканами происходит образование соли первичного амина, из которой действием щелочи можно выделить сам первичный амин.
Если проводить реакцию с избытком аммиака, то сразу получится амин, а галогеноводород образует соль с аммиаком:
Гидрирование нитрилов
Таким образом получают первичные амины. Возможно восстановление нитрилов водородом на катализаторе:
.
Соли аминов
- Соли аминов — это твердые вещества без запаха, хорошо растворимые в воде, но не растворимые в органических растворителях (в отличие от аминов).
- При действии щелочей на соли аминов выделяются свободные амины:
- Соли аминов вступают в обменные реакции в растворе:
- Взаимодействие с аминами.
Соль амина с более слабыми основными свойствами может реагировать с другим амином, образуя новую соль (более сильные амины вытесняют менее сильные из солей):
15 комментариев
Добавить ваш
Где получение аминов , там 2) Реакция Зинина слева написано R как радикал, а справа (после равно) уже метиламин, почему метиламин справа, а слева просто R? Разве Зинин не анилин получил этим способом?
Да, спасибо, поправил. В узком смысле реакцией Зинина называют получение именно ароматических аминов, в широком смысле так называют восстановление любых нитросоединений сульфидом аммония.
Здравствуйте! Скажите, пожалуйста, реагируют ли третичные амины с галогеналканами? Если да, то как идет реакция и что получается? Например,при взаимодействии триметиламина с хлорметаном?
Здравствуйте! Реагируют, но дальнейшее замещение по связям N-H не идет.
Здравствуйте! Не показано взаимодействие аминов со спиртами.
Третичные амины с алкилгалогенидами реагируют. Получаются четвертичные аммониевые соли. Говорить, что они вообще не реагируют, неправильно. Они не вступают в реакцию алкилирования.
R3N + RCl = R4N(+)Cl(-)
По такой схеме за счет пары электронов на азоте реагируют алифатические амины, ароматические амины, пиридин с получением N-алкилпиридинийхлорида (иодида) и пр.
Да, спасибо за комментарий. Я имел в виду, что не идет дальнейшее замещение.
спасибо, отличная идея!
для полноты информации я бы добавил оптическую изомерию и примеры этой изомерии ко всем классам органических веществ, потому что на егэ это есть
На ЕГЭ пока оптической изомерии нет.
Admin>Здравствуйте! Реагируют, но дальнейшее замещение по связям N-H не идет.
что значит «дальнейшее»? у триметиламина — и так уже нет N-H связей, может вы имели в виду протонированный триметил-амин (скажем) солянокислый, что в форме соли он останется третичным амином например до момента щелочного депротонирования(высвобождения основания амина)
—
а что кстати, есть способ галоидным алкилом моноалкилирование первичного ароматического амина до вторичного осуществить, избежав образования третичного амина — диалкилированного уже
на этилировании уже проще, а вот метиллирование нейромедиаторов не удавалось остановить на стадии N,N-ДиМет.(например в ацетоне с карбонатом калия, или с DIPEA), выход третичного целевого амина всегда оказывался либо самым низким из продуктов реакции, либо просто очень низким(10% в сложной смеси аминов с преобладанием четвертичной соли триметиламмония метилиодида, а сейчас подумал — если при N-метилировании первичного ароматического амина метилиодидом, образуется гидроиодид N-метил…исх.пер.амина, он же даже во второе метиллирование уже не должен входить, усиленным основанием став (скажем адреналином, основнее норадреналина исходного как я понимаю за счет появившегося электроннодонороного метила) и так будет выведен из реакционной среды(например выпав осадком соли, не солватированной в неполярной РС)
получается в отсутствие основного катализа алкилирование первичных аминов ограничивается моно-алкилированием — не далее чем до вторичного амина? или на практике соли не так надёжны как в оптимистичных прогнозах теоретизирующего учащегося?