Определенпие, конструкция и история создания литий-ионных аккумуляторов
Литий — наиболее легкий металл, он вдвое легче воды и всплывает даже в керосине. Одновременно с этим, литий обладает огромным электрохимическим потенциалом, что делает его одним из самых активных металлов (E0(Li + /Li 0 ) =
-3.04 В). Это свойство лития дает возможность создавать на его основе батареи и аккумуляторы с очень высокой плотностью энергии при минимальных размерах и массе.
Литий-ионный аккумулятор — источник тока многоразового действия, состоящий из отрицательного электрода, способного обратимо внедрять ионы лития и положительного электрода, также способного к обратимому внедрению ионов лития. Эти два электрода разделены электролитом, проводящим по ионам лития.
Первые литиевые аккумуляторы использовали анод из металлического лития и катод из оксидов различных металлов. К сожалению, эта схема проявила себя как весьма ненадежная – аккумуляторы регулярно вспыхивали или взрывались. Обеспечить большое количество циклов заряд/разряд для анода из металлического лития оказалось проблематично: при заряде аккумулятора металлический литий, восстанавливающийся на аноде, может образовывать дендриты (игольчатые кристаллы), пронизывающие слой электролита и создающие риск короткого замыкания.
В попытках решить проблему циклируемости анода из металлического лития при температурах окружающей среды группа исследователей из Оксфорда предложила заменить металлический литий на матрицу из углеродных материалов (графита или кокса), способную обратимо интеркалировать катионы лития до состава LiC6 при минимальном (не более 10%) изменении объема.
Эта идея оказалась очень плодотворной. Такой тип аккумуляторов получил название литий-ионных. Первый литиево-ионный аккумулятор разработала корпорация Sony в 1991 году.
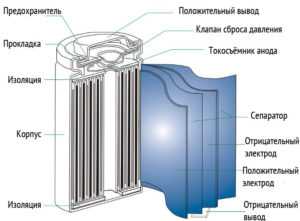
Конструктивно Li-ion аккумуляторы производятся в цилиндрическом и призматическом вариантах. (рис. 1.1). (рис. 1.2).
Материалы для литий-ионных аккумуляторов: анодные, катодные материалы и электролиты.
Анодные материалы
Графит является наиболее предпочтительным анодным материалом для коммерческих литиевых источников тока (ЛИТ). Графит имеет явно выраженную слоистую структуру (рис 1.3), и при внедрении лития в межслоевые пространства его удельный объем увеличивается незначительно.
Известны многие материалы, способные образовывать бинарные соединения с литием, так что их емкость значительно превышает 372 мАч/г. В частности, литий способен образовывать концентрированные сплавы с алюминием, а также интерметаллические соединения с оловом, кремнием и другими элементами. Максимальная удельная емкость электродов из алюминия, олова и кремния при образовании Li9Al14, Li17Sn4 и Li22Si5 составляет, соответственно, 2235, 959 и 4211 мАч/г. Тем не менее, все указанные материалы очень сильно увеличивают свой объем при внедрении лития, и изменения удельного объема при образовании упомянутых соединений составляет более 300%. Увеличение удельного объема сопряжено с возникновением гигантских внутренних напряжений, приводящих к разрушению (растрескиванию, превращению в порошок) активных материалов.
Катодные материалы
В качестве активных материалов положительных электродов в настоящее время используют литированные оксиды металлов переменной валентности, чаще всего слоистый кобальтит лития LiCoO2, а также его аналог слоистый никелат лития LiNiO2 или литий-марганцевую шпинель LiMn2O4.
В структуре LiCoO2 октаэдры СoO6 связаны попарно ребрами и образуют отрицательно заряженные слои CoO2, которые стабилизированы и экранированы слоями октаэдрически координированных ионов лития (рис.1.4). При этом ионы лития могут свободно перемещаться в плоскости слоя, обратимо интеркалировать и деинтеркалировать в данную структуру в значительных количествах с одновременным изменением формальной степени окисления кобальта Co +3 Co +4 .
И кобальтит, и никелат лития, а также и литий-марганцевые шпинели не обладают достаточно высокой электронной проводимостью. Поэтому в активную массу положительных электродов всегда вводят некоторое количество электропроводной добавки, обычно углеродного материала (сажи или графита). Как правило, в современных литиевых аккумуляторах катод состоит преимущественно (на 80%) из порошкообразного активного материала, 10% сажи или графита и 10% связующего вещества (фторсодержащие органические полимеры).
Предпринимались неоднократные попытки усовершенствовать активные материалы электродов литий-ионных аккумуляторов. Что касается усовершенствования материалов положительных электродов, то первым шагом было создание целого ряда замещенных оксидов. Самый простой пример — это материалы общей формулы LiNiyCo1−yO2 где 0 0 С до 130 0 С) в течение долгого времени,
-высокие значения ионной проводимости при комнатной температуре,
-малую электронную проводимость,
-новые возможности в дизайне батарей (т.к. полимерному электролиту легко придать нужную форму),
-отсутствие опасности утечки электролита
Электрохимические процессы на литий-ионных аккумуляторах.
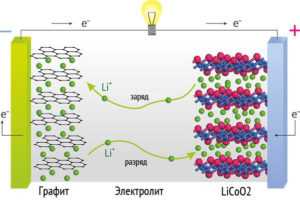
При разряде Li-ion аккумулятора происходят деинтеркаляция лития из углеродного материала (на отрицательном электроде) и интеркаляция лития в оксид (на положительном электроде). При заряде аккумулятора процессы идут в обратном направлении,т.е. происходит внедрение иона лития в активный материал отрицательного электрода и одновременная экстракция иона лития из активного материала положительного электрода. Суммарная реакция в элементе показана на рис. 1.6. Таким образом, во всей системе отсутствует металлический (нуль-валентный) литий, а процессы разряда и заряда сводятся к переносу ионов лития с одного электрода на другой. Поэтому такие аккумуляторы получили название «литий-ионных», или аккумуляторов типа кресла-качалки.
- Химические процессы Li-ion аккумуляторов
- Устройство, эксплуатация и характеристики литий─ионных аккумуляторов
- Как появились литий─ионные батареи?
- Реакции, происходящие в Li─Ion аккумуляторе
- Реакции на отрицательном электроде
- Реакции на положительном электроде
- Устройство литий─ионных аккумуляторов
- Параметры Li-Ion аккумуляторов
- Эксплуатация литий─ионных батарей
- Зарядка Li─Ion аккумуляторов
- Хранение и разрядные характеристики литий─ионных АКБ
- Безопасность
- Защита литий─ионных батарей
- Как функционирует защита АКБ?
- Деградация Li─Ion аккумуляторов
- Перспективы развития литий─ионных аккумуляторных батарей
Химические процессы Li-ion аккумуляторов

Революцию в развитии перезаряжаемых литиевых аккумуляторов произвело сообщение о том, что в Японии разработаны аккумуляторы с отрицательным электродом из углеродных материалов. Углерод оказался весьма удобной матрицей для интеркаляции лития.
Для того чтобы напряжение аккумулятора было достаточно большим, японские исследователи использовали в качестве активного материала положительного электрода оксиды кобальта. Литерованный оксид кобальта имеет потенциал около 4 В относительно литиевого электрода, поэтому рабочее напряжение Li-ion аккумулятора имеет характерное значение 3 В и выше.
При разряде Li-ion аккумулятора происходят деинтеркаляция лития из углеродного материала (на отрицательном электроде) и интеркаляция лития в оксид (на положительном электроде). При заряде аккумулятора процессы идут в обратном направлении. Следовательно, во всей системе отсутствует металлический (нуль-валентный) литий, а процессы разряда и заряда сводятся к переносу ионов лития с одного электрода на другой. Поэтому такие аккумуляторы получили название «литий-ионных», или аккумуляторов типа кресла-качалки.
Процессы на отрицательном электроде Li-ion аккумулятора. Во всех Li-ion аккумуляторах, доведенных до коммерциализации, отрицательный электрод изготавливается из углеродных материалов. Интеркаляция лития в углеродные материалы представляет собой сложный процесс, механизм и кинетика которого в существенной степени зависят от природы углеродного материала и природы электролита.
Углеродная матрица, применяемая в качестве анода, может иметь упорядоченную слоистую структуру, как у природного или синтетического графита, неупорядоченную аморфную или частично упорядоченную (кокс, пиролизный или мезофазный углерод, сажа и др.). Ионы лития при внедрении раздвигают слои углеродной матрицы и располагаются между ними, образуя интеркалаты разнообразных структур. Удельный объем углеродных материалов в процессе интеркаляции-деинтеркаляции ионов лития меняется незначительно.
Кроме углеродных материалов в качестве матрицы отрицательного электрода изучаются структуры на основе олова, серебра и их сплавов, сульфиды олова, фосфориды кобальта, композиты углерода с наночастицами кремния.
Процессы на положительном электроде Li-ion аккумулятора. Если в первичных литиевых элементах применяются разнообразные активные материалы для положительного электрода, то в литиевых аккумуляторах выбор материала положительного электрода ограничен. Положительные электроды литий-ионных аккумуляторов создаются исключительно из литированных оксидов кобальта или никеля и из литий-марганцевых шпинелей.
В настоящее время в качестве катодных материалов все чаще применяются материалы на основе смешанных оксидов или фосфатов. Показано, что с катодами из смешанных оксидов достигаются наилучшие характеристики аккумулятора. Осваиваются и технологии покрытий поверхности катодов тонкодисперсными оксидами.
При заряде Li-ion аккумулятора происходят реакции:
на положительных пластинах:
LiCoO2 > Li1-xCoO2 + xLi+ + xe-
на отрицательных пластинах:
С + xLi+ + xe- > CLix
При разряде происходят обратные реакции. Процесс заряда демонстрируется рисунком.
Процесс заряда литий-ионного (Li-ion) аккумулятора
Рис.1. Процесс заряда литий-ионного (Li-ion) аккумулятора
Устройство, эксплуатация и характеристики литий─ионных аккумуляторов
В современных мобильных телефонах, ноутбуках, планшетах используются литий─ионные аккумуляторы. Постепенно они вытеснили щелочные аккумуляторы с рынка портативной электроники. Раньше во всех этих устройствах использовались никель─кадмиевые и никель─металлгидридные аккумуляторные батареи. Но их времена прошли, поскольку Li─Ion батареи имеют лучшие характеристики. Правда, они могут заменить щелочные не по всем параметрам. Например, для них недостижимы токи, которые могут отдавать никель─кадмиевые АКБ. Для питания смартфонов и планшетов это некритично. Однако в области портативного электроинструмента, который потребляет большой ток, щелочные аккумуляторы по-прежнему в ходу. Тем менее, работы по разработке аккумуляторов с высокими токами разряда без кадмия продолжаются. Сегодня мы поговорим о литий─ионных аккумуляторных батареях, их устройстве, эксплуатации и перспективах развития.
Как появились литий─ионные батареи?
Самые первые аккумуляторные элементы с анодом из лития были выпущены в семидесятых годах прошлого столетия. У них была высокая удельная энергоёмкость, что сразу сделало их востребованными. Специалисты давно стремились разработать источник на основе щелочного металла, который имеет высокую активность. Благодаря этому было достигнуто высокое напряжение этого типа батарей и удельная энергия. При этом сама разработка конструкции таких элементов была выполнена довольно быстро, а вот их практическое использование вызвало сложности. С ними удалось справиться только в 90-е годы прошлого века.
Это случилось после ряда несчастных случаев. В момент разговора ток, потребляемый от аккумулятора, выходил на максимум и началась вентиляция с выбросом пламени. В результате произошло много случаев получения пользователями ожогов лица. Поэтому учёным пришлось дорабатывать конструкцию литий─ионных аккумуляторов.
Металлический литий крайне нестабилен, особенно проявляется при зарядке и разрядке. Поэтому исследователи стали создавать аккумуляторную батарею литиевого типа без использования лития. Стали использоваться ионы этого щелочного металла. Отсюда и пошло их название.
Литий─ионные батареи имеют меньшую удельную энергию, чем литиевые аккумуляторы.
Но они безопасны при соблюдении норм заряда и разряда.
Вернуться к содержанию
Реакции, происходящие в Li─Ion аккумуляторе
Рывком в направлении внедрения литий─ионных аккумуляторных батарей в бытовую электронику стала разработка АКБ, у которых минусовой электрод был выполнен из углеродного материала. Кристаллическая решётка углерода очень хорошо подошла в качестве матрицы для интеркаляции ионов лития. Чтобы увеличить напряжение аккумулятора, положительный электрод был выполнен из оксида кобальта. Потенциал литерованного оксида кобальта составляет примерно 4 вольта.
Величина рабочего напряжения большинства литий─ионных аккумуляторов составляет 3 вольта и более. В процессе разряда на минусовом электроде происходит деинтеркаляция лития из углерода и его интеркаляция в оксид кобальта плюсового электрода. В процесс зарядки процессы происходят наоборот. Получается, что металлического лития в системе нет, а работают его ионы, которые перемещаются с одного электрода на другой, создавая электрический ток.
Вернуться к содержанию
Реакции на отрицательном электроде
Все современные коммерческие модели литий─ионных аккумуляторов имеют минусовой электрод из углеродосодержащего материала. От природы этого материала, а также вещества электролита во многом зависит сложный процесс интеркаляции лития в углерод. Матрица углерод на аноде имеет слоистую структуру. Структура может быть упорядоченной (натуральный или синтетический графит) или частично упорядоченной (кокс, сажа и т. п.).
При интеркаляции ионы лития раздвигают слои углерода, внедряясь между них. Получаются различные интеркалаты. При интеркаляции и деинтеркаляции удельный объем матрицы углерода меняется несущественно. В отрицательный электрод, помимо углеродного материала, могут использоваться серебро, олово и их сплавы. Также пробуют использовать композитные материалы с кремнием, сульфидами олова, соединениями кобальта и т. п.
Реакции на положительном электроде
В первичных литиевых элементах (батарейках) для изготовления плюсового электрода часто используются самые разные материалы. В аккумуляторах этого сделать не получается и выбор материала ограничен. Поэтому плюсовой электрод Li─Ion аккумулятора выполняется из литированного оксида никеля или кобальта. Также могут применяться литий─марганцевые шпинели.
Сегодня ведутся исследования материалов из смешанных фосфатов или оксидов для катода. Как удалось доказать специалистам, такие материалы улучшают электрические характеристики литий─ионных АКБ. Также разрабатываются способы нанесения оксидов на поверхность катода.
Реакции, протекающие в литий─ионном аккумуляторе при заряде, можно описать следующими уравнениями:
С + xLi + + xe — → CLix
В процессе разряда реакции идут в обратном направлении.
На рисунке ниже схематично показаны процессы, протекающие в литий─ионном аккумуляторе при заряде и разряде.
Реакции, протекающие в Li-Ion аккумуляторе
Устройство литий─ионных аккумуляторов
По своему исполнению Li─Ion аккумуляторы выполняются в цилиндрическом и призматическом исполнении. Цилиндрическая конструкция представляет рулон электродов с сепараторным материалом для разделения электродов. Этот рулон помещён в корпус из алюминия или стали. С ним соединён минусовой электрод.
Положительный контакт выводится в виде контактной площадки на торец аккумулятора.
Цилиндрический литий─ионный аккумулятор
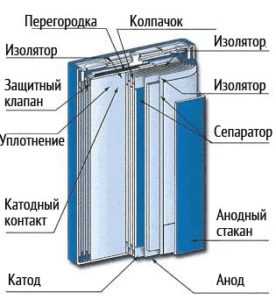
Li─Ion аккумуляторы призматической конструкции делаются с помощью укладывания пластин прямоугольной формы друг на друга. Такие батареи дают возможность сделать упаковку более плотной. Сложность заключается в поддержке сжимающего усилия на электродах. Есть призматические АКБ с рулонной сборкой электродов, скручиваемых в спираль.
Призматический литий─ионный аккумулятор
Кроме того, для увеличения безопасности эксплуатации в Li-Ion аккумуляторах в обязательном порядке используется электронная плата. Её назначение – это контроль за процессами заряда и разряда, исключение перегрева и короткого замыкания.
Сейчас выпускается много призматических литий─ионных аккумуляторов. Они находят применение в смартфонах и планшетах. Конструкция призматических батарей часто может отличаться у различных производителей, поскольку не имеет единой унификации. Электроды противоположной полярности разделяются сепаратором. Для его производства используется пористый полипропилен.
Конструкция Li-Ion и прочих разновидностей литиевых АКБ всегда выполняется герметичной. Это обязательное требование, поскольку вытекания электролита не допустимо. Если он вытечет, то электроника будет повреждена. Кроме того, герметичное исполнение не допускает попадания внутрь АКБ воды и кислорода. Если они попадут внутрь, то в результате реакции с электролитом и электродами разрушат аккумулятор. Производство комплектующих для литиевых аккумуляторов и их сборка находится в специальных сухих боксах в атмосфере аргона. При этом используются сложные приёмы сваривания, герметизации и т. п.
Ао – активная масса отрицательного электрода;
Ап — активная масса положительного электрода.
Такой баланс не допускает образование лития (чистого металла) и исключает возгорание.
Вернуться к содержанию
Параметры Li-Ion аккумуляторов
Выпускаемые сегодня литий─ионные аккумуляторы имеют высокую удельную энергоёмкость и рабочее напряжение. Последнее в большинстве случаев составляет от 3,5 до 3,7 вольта. Энергоёмкость составляет от 100 до 180 ватт-час на килограмм или от 250 до 400 на литр. Некоторое время назад производители не могли выпустить АКБ с ёмкостью выше нескольких ампер-час. Сейчас проблемы, сдерживающие развитие в этом направлении, устранены. Так, что в продаже стали встречаться аккумуляторы литиевого типа с ёмкостью в несколько сотен ампер-час.
Саморазряд этого типа батарей равен 4─6 процента в течение первого месяца. Далее он уменьшается и в год составляет до процентов. Это значительно меньше, чем у никель─кадмиевых и никель─металлогидридных батарей. Срок службы примерно 400─500 циклов заряд-разряд.
Теперь поговорим об особенностях эксплуатации литий─ионных аккумуляторов.
Вернуться к содержанию
Эксплуатация литий─ионных батарей
Зарядка Li─Ion аккумуляторов
Заряд литий─ионных АКБ обычно комбинированный. Сначала они заряжаются при постоянном токе величиной 0,2─1С пока не наберут напряжение 4,1─4,2 вольта. А затем зарядка ведётся при постоянном напряжении. Первая ступень продолжается примерно около часа, а вторая около двух. Чтобы зарядить аккумулятор быстрее, используется импульсный режим. Первоначально выпускались Li─Ion аккумуляторы с графитом и для них устанавливалось ограничение напряжения 4,1 вольта на одну банку. Дело в том, что при более высоком напряжении в элементе начинались побочные реакции, сокращающие срок эксплуатации этих аккумуляторов.
Постепенно эти минусы удалось устранить за счёт легирования графита различными добавками. Современные литий─ионные элементы без проблем заряжают до 4,2 вольта. Погрешность составляет 0,05 вольта на элемент. Существуют группы Li─Ion аккумуляторных батарей для военной и промышленной сферы, где требуется повышенная надёжность и длительный срок службы. Для таких АКБ выдерживают максимальное напряжение на элемент 3,90 вольта. У них несколько ниже энергетическая плотность, но увеличенный срок службы.
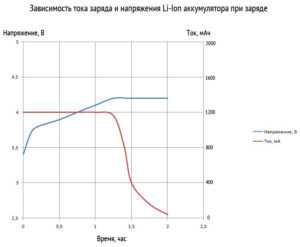
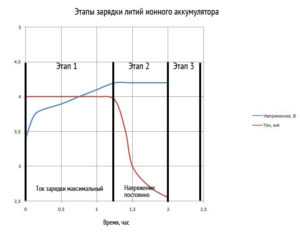
Зависимость тока заряда и напряжения Li─Ion аккумулятора при заряде
На графике ниже представлены этапы зарядки Li─Ion батареи.
Этапы зарядки литий─ионного аккумулятора
- Этап 1. На этой стадии через аккумуляторную батарею течёт максимальный ток заряда. Он продолжается до момента достижения порогового напряжения;
- Этап 2. При постоянном напряжении на АКБ ток зарядки постепенно уменьшается. Этот этап прекращается, когда величина тока уменьшается до 3 процентов от начального значения;
- Этап 3. Если аккумулятор ставится на хранение, то на этом этапе идёт периодический заряд для компенсации саморазряда. Делается ориентировочно через каждые 500 часов.
Из практики известно, что увеличение тока заряда не сокращает время зарядки батареи. При повышении тока напряжение растёт быстрее до порогового значения. Но тогда потом второй этап зарядки длится дольше. Некоторые зарядные устройства (ЗУ) могут зарядить Li─Ion аккумулятор за час. В таких ЗУ отсутствует второй этап, но реально аккумулятор в этой точке заряжается где-то на 70 процентов.
Что касается струйной подзарядки, то для литий─ионных батарей она неприменима. Это объясняется тем, что этот тип АКБ не может при перезарядке поглощать избыточную энергию. Струйная подзарядка может привести к переходу части ионов лития в металлическое состояние (валентность 0).
А непродолжительный заряд хорошо компенсирует саморазряд и потери электрической энергии. Зарядка на третьем этапе может делаться каждые 500 часов. Как правило, выполняется при снижении напряжения АКБ до 4,05 вольта на одном элементе. Заряд ведётся до поднятия напряжения до 4,2 вольта.
Стоит отметить слабую стойкость литий─ионных аккумуляторов к перезаряду. В результате подачи лишнего заряда на углеродной матрице (минусовой электрод) может начаться осаждение металлического лития. Он имеет очень высокую химическую активность и взаимодействует с электролитом. В результате на катоде начинается выделение кислорода, что грозит ростом давления в корпусе и разгерметизацией. Поэтому если вы заряжаете Li─Ion элемент в обход контроллера, не допускайте подъёма напряжения при заряде выше, чем рекомендует производитель батареи. Если постоянно перезаряжать аккумулятор, срок его службы сокращается.
Безопасности Li-Ion АКБ производители уделяют серьёзное внимание. Заряд прекращается при увеличении напряжения выше допустимого уровня. Также установлен механизм выключения заряда при увеличении температуры батареи выше 90 Цельсия. Некоторые современные модели батарей имеют в своей конструкции выключатель механического типа. Он срабатывает при росте давления внутри корпуса АКБ. Механизм контроля напряжения электронной платы отключает банку от внешнего мира по минимальному и максимальному напряжению.
Существуют литий─ионные батареи без защиты. Это модели, содержащие в своём составе марганец. Этот элемент при перезаряде способствует торможению металлизации лития и выделению кислорода. Поэтому в таких аккумуляторах защита становится не нужна.
Хранение и разрядные характеристики литий─ионных АКБ
Аккумуляторы литиевого типа хранятся достаточно хорошо и саморазряд в год составляет всего 10─20% в зависимости от условий хранения. Но при этом деградация элементов батареи продолжается даже, если она не используется. Вообще, все электрические параметры литий─ионного аккумулятора могут отличаться для каждого конкретного экземпляра.
К примеру, напряжение при разряде меняется в зависимости от степени зарядки, тока, температуры окружающей среды и т. п. На срок эксплуатации АКБ оказывают влияние токи и режимы цикла разряд-заряд, температура. Один из главных недостатков Li-Ion батарей ─ это чувствительность к режиму заряд-разряд, из-за чего в них и предусматривается много разных видов защит.
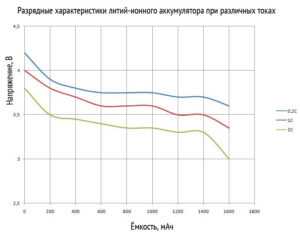
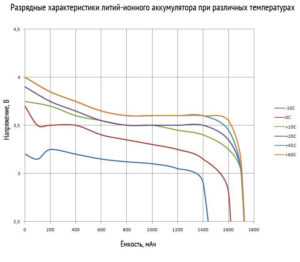
На графиках ниже представлены разрядные характеристики литий─ионных аккумуляторов. На них рассмотрена зависимость напряжения от тока разряда и температуры окружающей среды.
Разрядные характеристики литий-ионного аккумулятора при разных разрядных токах
Разрядные характеристики литий-ионного аккумулятора при различных температурах
Безопасность
В целом к настоящему времени проблема защиты литий─ионных аккумуляторов уже решена. Электронная защита держит под контролем процесс заряда и разряда. К тому же постоянно дорабатывается материал катода, в том числе, в направлении термической стабильности.
Li-Ion аккумуляторы имеют встроенную защиту от внутреннего короткого замыкания. Некоторые категории АКБ также оснащают защитой от внешнего короткого замыкания. Внутренняя защита реализована в виде двухслойного сепаратора. Один слой выполнен из полипропилена, а второй из аналога полиэтилена. Если в результате появления литиевых дендритов происходит короткое замыкание, то этот второй слой из-за разогрева оплавляется. В результате он становится непроницаемым, что предотвращает дальнейший рост дендритов лития к положительному электроду.
Вернуться к содержанию
Защита литий─ионных батарей
Выше мы несколько раз упоминали о защите Li─Ion аккумуляторов. Давайте, суммируем всю информацию.
В аккумуляторных батареях литиевого типа применяется полевой транзистор для размыкания цепи, когда напряжение банки возрастает до 4,3 вольта. Термическая защита разъединяет цепь при нагреве АКБ выше 90 градусов Цельсия. Ещё в литий─ионных батареях можно встретить предохранитель, срабатывающий при увеличении давления в корпусе до 1034 кПа. Также устанавливаются схемы, предохраняющие элемент от глубокого разряда. Их назначение – разорвать цепь при снижении напряжения элемента до 2,5 вольта.
Как функционирует защита АКБ?
Схема защиты литий─ионной аккумуляторной батареи при включённом телефоне имеет сопротивление 0,05─0,1 Ом. Это два ключа, которые соединены последовательно. Первый предназначен для срабатывания на верхнем, а второй ─ на нижнем значении напряжения АКБ. Сопротивление увеличивает в 2 раза внутреннее сопротивление АКБ. Аккумулятор отдаёт максимальный ток при низком внутреннем сопротивлении. Схема защиты сделана, как препятствие для бесконтрольного роста тока (как зарядки, так и разрядки) аккумулятора.
Также схема защиты может быть реализована с помощью химических добавок. Для этого используется марганец. В таких АКБ вместо схемы защиты ставится только предохранитель. И всё это не сказывается на безопасности. Марганец не даёт аккумулятору перегреться и воспламениться. В результате отказа от электронной схемы снижается цена литий─ионных батарей, но это порождает другую проблему. Такую АКБ пользователь может заряжать «неродной» зарядкой. И в этом случае может случиться так, что ЗУ не остановит процесс при полной зарядке. Тогда без схемы пойдёт перезаряд и выход аккумулятора из строя. Такие вещи заканчиваются вздутием корпуса.
Вернуться к содержанию
Деградация Li─Ion аккумуляторов
Из-за чего происходит деградация Li-Ion аккумуляторов и какие факторы приводят к снижению ёмкости? Это:
- расслоение графитовой матрицы;
- разрушение структуры катода;
- образование частиц металлического лития;
- появление пассивирующей плёнки на электродах. Она снижает поверхностную активность;
- разрушение механической структуры электрода из-за изменений объёма электродов при заряде-разряде.
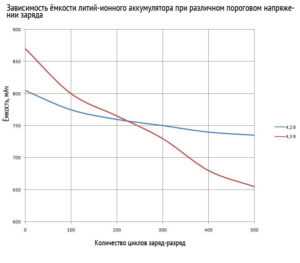
Зависимость ёмкости литий-ионного аккумулятора при различном пороговом напряжении заряда
Стоит отметить, что при уменьшении «амплитуды циклирования» увеличивается срок эксплуатации. Что это значит? То есть, не нужно разряжать телефон до выключения и заряжать его до 100%. Благодаря этому уменьшается механическая нагрузка на электроды, которая вызвана изменением объёма из-за внедрения ионов лития. Чем глубже разряд и полнее заряд, тем большие механические напряжения испытывают электроды.
Вернуться к содержанию
Перспективы развития литий─ионных аккумуляторных батарей
Литий─ионные аккумуляторы уже превратились в полноценное семейство батарей, как щелочные или автомобильные. От остальных групп АКБ они выделяются своей высокой энергоёмкостью, режимами заряд-разряд и рядом других характеристик. Их эксплуатация требует использования электронных схем контроля заряда-разряда и некоторых других средств защиты.
В случае с литиевыми аккумуляторами задача их безопасного использования усложняется требованиями к габаритам. Они должны быть максимально компактными, поскольку используются в портативной электронике. Из-за близкого расположения электродов и стремления добиться максимальной удельной ёмкости литий─ионные аккумуляторы долго не могли вывести на рынок для коммерческого использования.
Сейчас активно ведутся разработки новых материалов для электродов. Причём при использовании нового материала проходит долгое время до того момента, как его удаётся внедрить в серийное производство.
На рынке наблюдается довольно большой разброс литиевых батарей по электрическим характеристикам, габаритам и т. п. Отчасти это происходит из-за того, что пока нет единых стандартов в этом направлении. Кроме того, рынок наводнила продукция из Китая и других стран азиатского региона. Эти производители зачастую не придерживаются никаких норм, стараясь выпустить максимально доступные аккумуляторы.
Кроме того, усовершенствование литий─ионных аккумуляторов будет вестись в направлении уменьшения размеров, увеличения энергоёмкости, более гибкие решения в плане формы и т. п. Также работы ведутся в направлении разработки материалов для катода на базе соединений лития. Их цель – создание моделей литиевых АКБ, способных заменить никель─кадмиевые аккумуляторы в устройствах, потребляющих большой ток (портативный электроинструмент).
Вернуться к содержанию