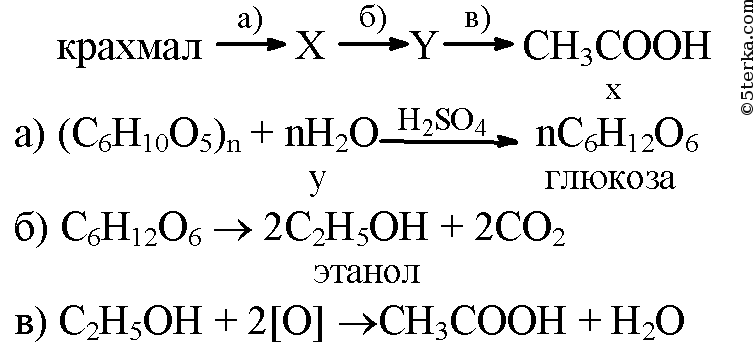- 1. Напишите уравнения реакций, при помощи которых можно осуществить следующие превращения: крахмал → X → Y → уксусная кислота. Укажите названия веществ X и Y.
- Напишите уравнения реакций, при помощи которых можно осуществить следующие превращения: крахмал → X → Y → уксусная кислота. Укажите названия веществ X и Y
- Ваш ответ
- решение вопроса
- Похожие вопросы
- Методические указания к выполнению лабораторных и практических работ «Органическая химия» (стр. 5 )
1. Напишите уравнения реакций, при помощи которых можно осуществить следующие превращения: крахмал → X → Y → уксусная кислота. Укажите названия веществ X и Y.

задача №1
к главе «Тема IX. Углеводы. Работа 2 Крахмал, целлюлоза. Вариант 3».
Выделите её мышкой и нажмите CTRL + ENTER
Большое спасибо всем, кто помогает делать сайт лучше! =)
Нажмите на значок глаза возле рекламного блока, и блоки станут менее заметны. Работает до перезагрузки страницы.
Напишите уравнения реакций, при помощи которых можно осуществить следующие превращения: крахмал → X → Y → уксусная кислота. Укажите названия веществ X и Y
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,289
- гуманитарные 33,621
- юридические 17,900
- школьный раздел 607,151
- разное 16,830
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Методические указания к выполнению лабораторных и практических работ «Органическая химия» (стр. 5 )
 | Из за большого объема этот материал размещен на нескольких страницах: 1 2 3 4 5 |
8. Напишите уравнения реакций получения уксусной кислоты из этилена.
9. Написать формулы всех изомерных карбоновых кислот и сложных эфиров с молекулярной формулой С5Н10О2.
10. Напишите реакции этерификации между глицерином и масляной кислотой;
глицерином и стеариновой кислотой.
Лабораторная работа №13
Цель работы: 1. Закрепление теоретических знаний по свойствам глюкозы.
2. Приобретение практических навыков лабораторного эксперимента.
Приборы и реактивы: раствор глюкозы – С6Н12О6,, CuSO4– сульфат меди, K2Cr2O7 –бихромат калия, NaOН– гидроксид натрия, Н2SO4– серная кислота, метиловый оранжевый, фенолфталеин, штатив с пробирками, спиртовки.
Глюкоза – органическое соединение, является альдегидоспиртом. Глюкоза сладкая на вкус, содержится в плодах, ягодах. Общая формула С6Н12О6,
структурная формула СН2(ОН)– СН(ОН)– СН(ОН)– –СН(ОН)– СН(ОН)– СОН
Опыт №1. Взаимодействие глюкозы с сернокислой медью.
В сухую пробирку приливают насыщенный раствор сульфата меди и добавляют по каплям немного едкого натра. Прилить такое же по объему количество раствора глюкозы.
Смесь нагревают и наблюдают протекание реакции.
Записать наблюдения, указать изменение цвета, сделать вывод.
Опыт №2. Взаимодействие глюкозы с серной кислотой.
В сухую пробирку приливают 1 N раствор серной кислоты и добавляют по каплям немного раствора глюкозы.
Смесь нагревают и наблюдают протекание реакции.
Записать наблюдения, указать изменение цвета, сделать вывод.
Опыт №3. Взаимодействие глюкозы с аммиачным раствором оксида серебра.
В сухую пробирку приливают насыщенный аммиачный раствор оксида серебра и добавляют такое же по объему количество раствора глюкозы.
Смесь нагревают и наблюдают протекание реакции.
Записать наблюдения, указать изменение цвета, сделать вывод.
1. Что называется глюкозой?
2. Что является изомером глюкозы?
3. Назовите область применения глюкозы.
4. Как можно получить глюкозу?
5. Каким соединением можно заменить глюкозу?
Лабораторная работа №14
Цель работы: 1. Закрепление теоретических знаний о свойствах крахмала.
2. Приобретение практических навыков лабораторного эксперимента.
Приборы и реактивы:
Крахмал –(С6Н10О5)n, крахмальный клейстер, иод, гидроксид меди– Cu(OH)2, Н2SO4– серная кислота, уксусная кислота – СН3СООН, метиловый оранжевый, фенолфталеин, синий лакмус, штатив с пробирками, спиртовки.
Крахмал является природным альдегидом. Молекулярная формула крахмала (С6Н10О5)n – имеет сложную структуру разветвленной формы. Крахмал является питательным веществом для человека.
Опыт №1. Получение крахмального клейстера.
В пробирку насыпать немного сухого крахмала, добавить несколько капель воды и все
хорошо взболтать; содержимое нагреть или добавить горячей воды и немного серной
кислоты, в результате чего наблюдается образование клейстера, который представляет
собой вязкую массу.
Образовался белый цвет. Масса вязкая.
Опыт №2. Взаимодействие крахмала с йодом.
Часть крахмального клейстера из 1-го опыта перенести в другую пробирку и добавить несколько капель йода. Указать, что наблюдается.
C6H10O5 + J2→ Цвет темно-синий.
Опыт №3. Взаимодействие крахмала с гидроксидом меди.
В пробирку с крахмальным клейстером прилить немного гидроксида меди Cu(OH)2. Наблюдать ход реакции.
C6H10O5 + Cu(OH)2 → Образуется красный цвет.
Опыт №4: Взаимодействие крахмала с уксусной кислотой.
К крахмальному клейстеру прилить немного уксусной кислоты. Содержимое
взболтать и немного нагреть. Образуется ацетат крахмала.
Цвет изменится на коричневый. Видны границы. Сделать вывод.
C6H10O5 + СН3СООН → Образуется коричневый цвет.
1. Написать процесс фотосинтеза крахмала в растениях.
2. Как объяснить клеящее действие вареного картофеля?
3. Сок зеленого яблока дает реакцию с иодом, сок спелого яблока дает реакцию с аммиачным раствором оксида серебра. Как это объяснить?
4. Область применения крахмала.
Лабораторная работа №15
Цель работы: 1. Закрепление теоретических знаний о свойствах нитросоединений.
2. Приобретение практических навыков лабораторного эксперимента.
Приборы и реактивы:
Нитрометан, нитроэтан, газ – водород, хлор, бромная вода, азотистокислое серебро, штатив с пробирками, спиртовки.
Нитросоединениями называются азотсодержащие органические соединения, имеющие нитро – группу – NО2 вместо атома водорода в своем молекулярном составе.
Например: СН3– NО2 нитрометан, С2Н5–NО2 нитроэтан, С3Н7–NО2 нитропропан
Нитросоединения – яды. Они плохо действуют на центральную нервную систему.
Нитросоединения применяются в качестве лаков, красок, красителей, растворителей.
Опыт №1. Реакция восстановления – реакция гидрирования.
Опыт проводить в вытяжном шкафу. В колбу с нитрометаном пропускают водород. Реакция протекает в кислой среде, катализатором являются металлические стружки, например, железные.
Такой же опыт можно провести с нитроэтаном.
Написать химическую реакцию, записать наблюдения.
Опыт №2. Реакция хлорирования.
Опыт проводить в вытяжном шкафу. В колбу с нитрометаном пропускают хлор.
Происходит изменение цвета и запаха.
Такой же опыт можно провести с нитроэтаном.
Написать химическую реакцию, записать свои наблюдения.
Опыт №3. Реакция бромирования.
Опыт проводить в вытяжном шкафу. В колбу с нитрометаном пропускают бромную воду. Реакция протекает в щелочной среде, в присутствии щелочи калия.
Такой же опыт можно провести с нитроэтаном.
Написать химическую реакцию, записать свои наблюдения.
Опыт №4. Получение нитросоединений в лабораторных условиях.
Опыт проводить в вытяжном шкафу. В колбу с бром–метаном приливают немного раствора азотистокислого серебра. Происходят изменения. Такой же опыт можно провести с бром–этаном.
Написать химическую реакцию, записать свои наблюдения.
1. Какую функциональную группу имеют нитросоединения?
2. Напишите гомологический ряд нитросоединений.
3. Где используют нитробензол, нитроциклогексан, тринитротолуол?
Лабораторная работа №16
Цель работы: 1. Закрепление теоретических знаний о свойствах белковых тел.
2. Приобретение практических навыков лабораторного эксперимента.
3. Изучение качественных цветных реакций на белки.
Приборы и реактивы:
Гидроксид меди – Cu(OH)2, Н2SO4– серная кислота, CuS04 –сульфат меди, Н NО3–
азотная кислота, метиловый оранжевый, фенолфталеин, синий лакмус, штатив с пробирками, спиртовки.
Белки составляют основу живой материи. Белки – это высокомолекулярные органические соединения или биополимеры. Белки состоят из многих амонокислот, связанных между собой сложным разветвленным строением. Наиболее главными элементами в строении белков являются водород – Н, углерод – С. кислород – О,
фосфор – Р, азот – N, сера –S.
Белок клейковины выделен из пшеничной муки, белок казеин – из молока, в 18 веке был выделен белок крови – это белок самой сложной конфигурации.
Опыт №1. Цветная реакция с гидроксидом меди.
В пробирку поместить 2 мл яичного белка и прилить свежеприготовленный раствор гидроксида меди, используя медный купорос и щелочь натрия. В ходе реакции белок должен окраситься в красно – фиолетовый цвет.
Напишите подробные наблюдения, сделайте вывод.
Опыт №2. Цветная реакция с азотной кислотой.
На светлую шерстяную или хлопчато – бумажную ткань капнуть небольшим количеством азотной кислоты – Н NО3. Образуется оранжевое пятно.
Что происходит, сделайте вывод.
Опыт №3. Горение тканей на основе белковых нитей.
Подожгите несколько нитей различных тканей на белковой основе: шерстяные, льняные, хлопчато – бумажные. По запаху определите какой ткани эти нити принадлежат. Сделайте сравнение и напишите свой вывод.
Опыт №4. Определение белка из группы веществ.
В пробирку налить немного молока – продукта с белковым материалом. В молоко входят белки, жиры, углеводы. Выделить из молока жир и затем действием кислоты – белок.
Сравните, как ведет себя при нагревании кислое молоко с добавкой соды и без соды.
Объясните это явление.
1. Какие органические соединения называются белковыми?
2. Из каких аминокислот состоят белки? Приведите примеры.
3. Напишите общую структурную формулу белков и укажите пептидную связь.
4. Что называется ферментом?
5. Какие ученые начинали изучать структуру белков.
6. Напишите: как выглядит первичная структура белка,
вторичная структура белка,
третичная структура белка,
четвертичная структура белка.
7. Напишите область нахождения белковых тел в природе.
«Гетерофункциональные органические соединения».
Решение экспериментальных задач.
Цель работы: 1.Закрепить знания о гетерофункциональных органических соединениях с
помощью экспериментальных задач.
1.Составьте уравнения реакций а) окисления глюкозы гидроксидом меди
б) восстановления глюкозы в шестиатомный спирт.
2.Распознайте растворы глюкозы и сахарозы, находящихся в разных пробирках.
3. Проверьте, подвергается ли гидролизу сахароза в стакане сладкого чая.
4. Определите формулу вещества, если известно, что оно содержит 6,25% Р, 12,5% N,
56,25% Н, 25% О (по молям). Рассчитайте молекулярную формулу и назовите это
5.Составьте уравнения реакций получения этилового спирта из крахмала:
6.Используя химический способ, разделите смесь этилового спирта и уксусной кислоты.
7.Составьте структурные формулы всех изомерных аминомасляной и
8.В пробирку налить немного молока.
В молоко входят белки, жиры, углеводы. Выделить из молока жир и затем действием
Сравните, как ведет себя при нагревании кислое молоко с добавкой соды и без соды.
Объясните это явление.
9.Определите молекулярную массу стеариновой кислоты.
10.Определите плотность по кислороду пальмитиновой кислоты.
1. Ким, химия. [ Текст]: учеб. пособие для сред. спец. Образования / – Новосибирск: Сибирское университетское издательство, 2010. – 814 с.
2. Березин, Б. Д., Березин, современной органической химии. [Текст]: учебник для сред. спец. учеб. заведений / , – 2-е изд., перераб. и доп. – М.: Высшая школа, 2011. – 768 с.
3. Нейланд, химия [Текст]: учебник для сред. спец. учеб. заведений / – 2-е изд., перераб. и доп. – М.: Высшая школа, 2010. – 750 .
4. Петров, А. А., Бальян, Х. В., Трощенко, химия [Текст]: учебник для студентов сред. проф. учеб. заведений / Под ред. – 6-е изд., стер. – М. : Издательский центр «Академия», 2010. – 624 с.
1. Артеменко, А. И., Тикунова, И. В., Ануфриев по органической химии. [Текст] / Артеменко, А. И., Тикунова, И. В., Ануфриев, Е. К.–М.:Высшая школа, 2010-187с.
2. Березин, Б. Д., Березин, современной органической химии. . [Текст] Учебное пособие для вузов. / Березин, Б. Д., Березин, Д. Б –М.: Высшая школа,2010.-768с.
3. Градберг, работы и семинарские занятия по органической химии. . [Текст] / Градберг, И. И – М.: Дрофа, 2009.-352с.