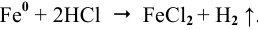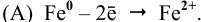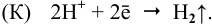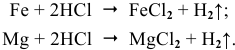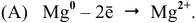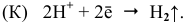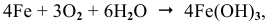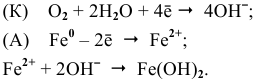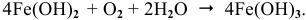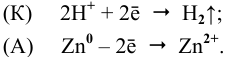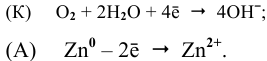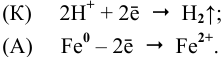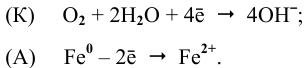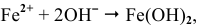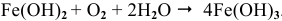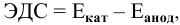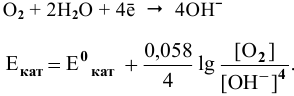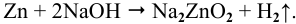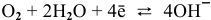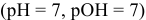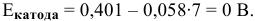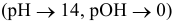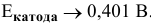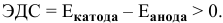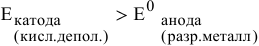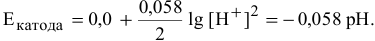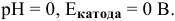Коррозия металлов. Методы защиты металлов от коррозии
Задача 74
Железная пластинка погружается в разбавленный раствор 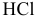
Решение:
При погружении железной пластинки в раствор 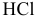
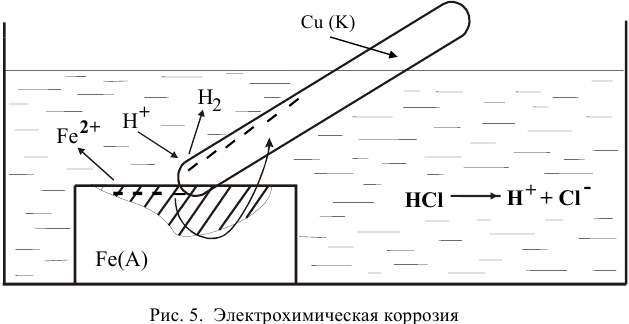
При касании железа медью образуется короткозамкнутый гальванический элемент, состоящий из железного и медного электродов, загруженных в раствор электролита. Медный электрод играет роль катода, так как он имеет более высокий электродный потенциал. На катоде должен протекать процесс восстановления, а на аноде — железной пластине — процесс окисления:
Таким образом, железо продолжает растворяться, причем скорость электрохимического процесса выше, чем скорость обычного окислительно-восстановительного процесса.
На катоде происходит деполяризация, т.е. процесс восстановления каких-либо частиц, называемых деполяризатором, избытком электронов.
В кислой среде роль деполяризатора играют катионы водорода:
Таким образом, водород выделяется с поверхности меди, несмотря на отсутствие взаимодействия 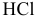
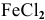
Задача 75
Две пластинки — одна железная, а другая магниевая -погружены раздельно в разбавленную соляную кислоту. Что изменится, если соединить обе пластинки?
Решение:
Обе пластинки, находящиеся раздельно в разбавленной 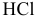
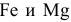
При объединении пластин образуется короткозамкнутый гальванический элемент, и протекает электрохимическая коррозия. Магний, будучи более активным металлом, играет роль анода. На аноде происходит процесс окисления:
На катоде — железной пластинке — будет происходить водородная деполяризация:
Таким образом, при соприкосновении двух пластин наблюдается усиление выделения водорода с поверхности железа, хотя разрушение железа резко уменьшается, а активизируется процесс разрушения магниевой пластины. Выделение водорода с поверхности магния резко сокращается.
Задача 76
Кладут в один стакан, содержащий солевой раствор, кусочек чистого железа, а в другой стакан, содержащий такой же солевой раствор, — кусочек железа, соединенный с кусочком свинца. В оба стакана есть доступ кислороду воздуха. Через несколько дней определяют содержание ионов железа в обоих стаканах. В каком из стаканов концентрация ионов железа будет больше ?
Решение:
Кислород растворяется в водном растворе. Железо, погруженное в солевой раствор, в присутствии растворенного кислорода будет подвергаться коррозии, хотя и медленно, так как оно чистое, а чистые металлы медленно корродируют (обычно присутствие примесей в железе (чугуне) резко увеличивает скорость коррозии).
Процесс коррозии чистого железа может быть представлен следующей схемой:
где 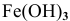
Железо в контакте с менее активным свинцом играет роль анода и подвергается электрохимической коррозии с кислородной деполяризацией на свинцовом катоде:
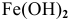
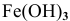
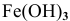
Скорость электрохимической коррозии намного выше скорости химической коррозии, поэтому в стакане, содержащем железо, соединенное со свинцом, концентрация ионов железа 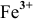
Задача 77
Описать процессы электрохимической коррозии, протекающие на оцинкованном железе при наличии трещин в защитном слое:
а) в кислой среде;
б) в нейтральной среде в присутствии кислорода.
Решение:
Покрытие железа цинком относится к анодным покрытиям, так как металл покрытия более активный, чем защищаемый металл, а значит, в случае протекания электрохимической коррозии он играет роль анода.
В кислой среде на поверхности катода, т.е. на поверхности железа, протекает водородная деполяризация (рис.6):
В нейтральной среде в присутствии кислорода на поверхности катода (железа) протекает кислородная деполяризация (рис.7):
Продукт коррозии, образующийся по реакции
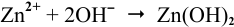
Задача 78
Описать процессы электрохимической коррозии,
протекающей на хромированном железе при наличии трещин в защитном слое:
а) в кислой среде;
б) в нейтральной среде в присутствии кислорода.
Решение:
Покрытие железа хромом относится к катодным покрытиям, так как металл покрытия менее активный, чем защищаемый металл, а значит, в случае протекания электрохимической коррозии он играет роль катода.
Защищаемый металл играет роль анода, т.е. подвергается разрушению.
В кислой среде на поверхности катода, т.е. на поверхности хрома, протекает водородная деполяризация (рис.8):
В нейтральной среде в присутствии кислорода на поверхности катода (хрома) протекает кислородная деполяризация (рис.9):
Продукт коррозии, образующийся по реакции
на воздухе окисляется:
Задача 79
Объяснить, почему в стальном сосуде застойная зона подвергается интенсивной коррозии (нейтральная среда в присутствии кислорода воздуха), тогда как в цинковом сосуде, наоборот, застойная зона подвергается коррозии в незначительной степени.
Решение:
Интенсивность (скорость) электрохимической коррозии зависит от ЭДС образующегося короткозамкнутого элемента: чем больше величина ЭДС, тем интенсивнее электрохимическая коррозия.
Для электрохимической коррозии ЭДС рассчитывается аналогично расчету ЭДС гальванического элемента:
где 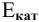
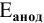
Для электродной полуреакции кислородной деполяризации
В зоне, подверженной воздействию кислорода, электродный потенциал катодных участков будет выше, чем в застойной зоне (концентрация кислорода в растворе находится в числителе). Таким образом, в начальный момент ЭДС микрогальваноэлементов в зоне, подверженной воздействию кислорода, будет выше, чем ЭДС микрогальваноэлементов в застойной зоне, а значит, коррозия анодных участков в зонах, подверженных воздействию кислорода, будет значительной. Эта коррозия в начальный момент приводит к накоплению анионов 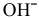
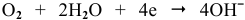
В сосуде из цинка коррозия зон, подверженных воздействию кислорода, всегда будет очень интенсивной, так как щелочная среда не пассивирует цинк, а наоборот, способствует его разрушению:
Поэтому застойная зона меньше подвергается коррозии, чем аэрируемая.
Задача 80
Показать необходимыми расчетами, что платина в контакте с золотом никогда не подвергается электрохимической коррозии, тогда как медь в контакте в золотом подвергается электрохимической коррозии только в присутствии кислорода в щелочной среде.
Решение:
Для процесса кислородной деполяризации
электродный потенциал определяется по формуле Нернста:
В нейтральной среде
В щелочной среде
Для того, чтобы протекала электрохимическая коррозия, необходимо следующее:
Таким образом, электродный потенциал металла (анода) должен быть ниже 0 В в нейтральной среде или ниже 0,401 В в сильно щелочной среде (рН=14). Если находятся в контакте золото и платина, платина играет роль анода, но ее стандартный электродный потенциал 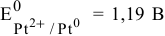
Медь в контакте с золотом может подвергаться электрохимической коррозии с кислородной деполяризацией, особенно в щелочной среде, так как 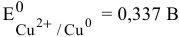
Остается показать отсутствие электрохимической коррозии с водородной деполяризацией для обоих случаев.
Электродный потенциал водородной деполяризации выражается уравнением:
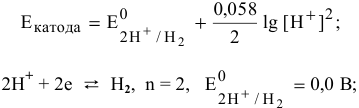
В кислой среде
В слабокислой среде
Таким образом, металлы, имеющие электродный потенциал выше 0 В, в кислой среде не подвергаются электрохимической коррозии с водородной деполяризацией.
Эти задачи взяты со страницы решения задач по неорганической химии:
Возможно эти страницы вам будут полезны:




















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Задачи к разделу Коррозия металлов
В данном разделе вы найдете задачи по теме Коррозия металлов. Приведены уравнения реакций, протекающих при электрохимической коррозии металлов, а также примеры задач на определение защитных свойств оксидных пленок, определение коррозионной стойкости металлов.
Задача 1. В каком случае цинк корродирует быстрее: в контакте с никелем, железом или с висмутом? Ответ поясните. Напишите для всех случаев уравнение электрохимической коррозии в серной кислоте. Будет ли оксидная пленка, образующаяся на кальции, обладать защитными свойствами?
Решение.
В месте контакта двух металлов корродирует более активный металл. Происходит отток электронов от более активного металла к менее активному. Металл тем активнее, чем более отрицателен его электродный потенциал. В таблице электродных потенциалов найдем:
В данном случае, цинк корродирует быстрее в контакте с висмутом, так как из перечисленных металлов, Bi является самым неактивным. В образовавшейся паре роль анода выполняет цинк.
Запишем уравнения электрохимической коррозии в серной кислоте:
Zn—Bi
К: 2H + +2e — = H2
А : Zn — 2e — = Zn 2+
Zn + 2H + = Zn 2+ + H2
Fe-Bi
К: 2H + +2e — = H2
А : Fe — 3e — = Fe 3+
2Fe + 6H + = Fe 3+ + 3H2
Ni-Bi
К: 2H + +2e — = H2
А : Ni — 2e — = Ni 2+
Ni + 2H + = Ni 2+ + H2
Будет ли оксидная пленка, образующаяся на кальции, обладать защитными свойствами?
Защитные свойства пленки оценивают величине фактора Пиллинга—Бэдвордса: (α = Vок/VМе), значения которого вы найдете в таблице, приведенной в теоретической части данного раздела. Мы рассчитаем значение α по формуле:
т.е α Решение.
Протекторная защита заключается в присоединении к защищаемому металлическому изделию, металла с более отрицательным значением стандартного электродного потенциала E 0 , т.е. более активного металла. Для защиты железа подойдут, например, цинк и бериллий:
Запишем уравнения электрохимической коррозии во влажной среде, насыщенной кислородом:
Fe—Zn
К: O2 + 2H2O + 4e — = 4OH —
А: Zn — 2 e — = Zn 2+
Fe-Be
К: O2 + 2H2O + 4e — = 4OH —
А : Be — 2e — = Be 2+
Будет ли оксидная пленка, образующаяся на алюминии, обладать защитными свойствами?
Защитные свойства пленки оценивают величине фактора Пиллинга—Бэдвордса: (α = Vок/VМе), значения которого вы найдете в таблице, приведенной в теоретической части данного раздела. Мы рассчитаем значение α по формуле:
Мок = 27·2+16·3 = 102 г/моль
т.е 2,5>α>1, а это значит, что оксидная пленка, образующаяся на Al, является сплошной и обладает защитными свойствами.
Задача 3. Деталь сделана из сплава, в состав которого входит магний и марганец. Какой из компонентов сплава будет разрушаться при электрохимической коррозии? Ответ подтвердите уравнениями анодного и катодного процесса коррозии: а) в кислой среде; б) в кислой среде, насыщенной кислородом. Будет ли оксидная пленка, образующаяся на олове, обладать защитными свойствами?
Решение.
При электрохимической коррозии сплава, в первую очередь будет разрушаться более активный металл, т.е. металл, имеющий более отрицательное значение стандартного электродного потенциала. В таблице электродных потенциалов найдем:
По значениям E видно, что магний является более активным металлом, чем марганец, вследствие чего при коррозии Mg будет разрушаться в первую очередь.
Запишем уравнения электрохимической коррозии магния а) в кислой среде; б) в кислой среде, насыщенной кислородом:
а) в кислой среде
А: Mg — 2 e — = Mg 2+
Mg + 2H + = Mg 2+ + H2
б) в кислой среде, насыщенной кислородом
К: O2 + 2H2O + 4e — = 4OH —
А : Mg — 2e — =Mg +
Будет ли оксидная пленка, образующаяся на олове, обладать защитными свойствами?
Защитные свойства пленки оценивают величине фактора Пиллинга—Бэдвордса: (α = Vок/VМе), значения которого вы найдете в таблице, приведенной в теоретической части данного раздела. Мы рассчитаем значение α по формуле:
Олово может образовать два оксида SnO и SnO2, поэтому рассчитаем значение α для каждого случая
МSnO = 119+16 = 135 г/моль
т.е для всех оксидных пленок α лежит в интервале 2,5>α>1, т.е. они являются сплошными и обладают защитными свойствами.
Задача 4. С целью защиты от коррозии цинковое изделие покрыли оловом. Какое это покрытие: анодное или катодное? Напишите уравнение атмосферной коррозии данного изделия при нарушении целостности покрытия. Оценить коррозионную стойкость алюминия в серной кислоте, если убыль массы алюминиевой пластины размером 70х20х1 мм составила после 8 суток испытания 0,0348 г.
Решение.
Если металлическое покрытие изготовлено из металла с более отрицательным потенциалом (более активный), чем защищаемый, то оно называется анодным покрытием. Если металлическое покрытие изготовлено из металла с более положительным потенциалом (менее активный), чем защищаемый, то оно называется катодным покрытием.
В таблице электродных потенциалов найдем:
Олово будет выполнять роль катода и покрытие из него – катодное. При нарушении целостности покрытия, корродировать будет цинк, как более активный металл. При атмосферной коррозии протекают следующие уравнения реакций:
К: O2 + 2H2O + 4e — = 4OH —
А: Zn — 2 e — = Zn 2+
Оценить коррозионную стойкость алюминия в серной кислоте, если убыль массы алюминиевой пластины плотностью ρ = 2,7 г/см 3 , размером 70х20х1 мм составила после 8 суток испытания 0,0348 г.
Оценить коррозионную стойкость металла можно по формуле:
Kн = 365·h/τ
h = Δm/(S·ρ)
Найдем площадь поверхности металла:
S = 2·(7·2) + 2·(7·0,1) + 2·(2·0,1) = 29,8 см 2
h = 0,0348/(29,8·2,7) = 0,00043см = 0,0043 мм
Kн = 365·0,0043/8 = 0,02 мм/год
По десятибалльной шкале коррозионной стойкости металлов, алюминий соответствует 4 баллам и относится к стойким металлам.
Задача 5. Если на стальной предмет нанести каплю воды, то коррозии подвергается средняя, а не внешняя часть смоченного металла. Чем это можно объяснить? Какой участок металла, находящийся под влиянием капли, является анодным, а какой катодным? Составьте электронные уравнения соответствующих процессов. Будет ли оксидная пленка, образующаяся на никеле, обладать защитными свойствами?
Решение .
При нанесении на стальной предмет капли воды, наибольший доступ воздуха будет по краям капли, где протекает процесс восстановления кислорода. Т.е. края капли выступают в качестве катода. Для окисления железа остается центр капли, где доступ воздуха минимален. Здесь центр капли является анодом. В этом случае протекают следующие реакции:
А: Fe – 2e — = Fe 2+
Будет ли оксидная пленка, образующаяся на никеле, обладать защитными свойствами?
Защитные свойства пленки оценивают величине фактора Пиллинга—Бэдвордса: (α = Vок/VМе), значения которого вы найдете в таблице, приведенной в теоретической части данного раздела. Мы рассчитаем значение α по формуле:
Мок = 59+16 = 75 г/моль
Подставим значения в формулу:
α = 75·8,9/(59·1·6,7) = 1,7
т.е α лежит в интервале 2,5>α>1, т.е. оксидная пленка является сплошной и обладает защитными свойствами.
Задача 7. Сплав содержит железо и никель. Какой из названных компонентов будет разрушаться при атмосферной коррозии? Приведите уравнение анодного и катодного процессов. Оценить коррозионную стойкость цинка на воздухе при высоких температурах. Образец цинка размером 50х30х1 мм после 180 часов окисления и снятия продуктов коррозии весил 10,6032 г.
Решение.
Исходя из положения металлов в электрохимическом ряду напряжения металлов, находим, что железо более активный металл, чем никель:
Поэтому в первую очередь при атмосферной коррозии будет разрушаться железо. В этом случае протекают следующие реакции:
А: Fe – 2e — = Fe 2+
Далее Fe(OH)2 переходит в Fe(OH)3
Оценить коррозионную стойкость цинка на воздухе при высоких температурах. Образец цинка плотностью ρ = 7,14 г/см 3 , размером 50х30х1 мм после 180 часов окисления и снятия продуктов коррозии весил 10,6032 г.
Оценить коррозионную стойкость металла можно по формуле:
Kн = 365·h/τ
h = Δm/(S·ρ)
Найдем площадь поверхности металла:
S = 2·(5·3) + 2·(5·0,1) + 2·(3·0,1) = 31,6 см 2
Масса металла до коррозии равна:
Убыль массы:
Δm = m1 – m2 = 10,71 — 10,6032 = 0,1068
h = 0,1068/(31,6·7,14) = 0,00047 см = 0,0047 мм
Kн = 365·0,0047/7,5 = 0,23 мм/год
По десятибалльной шкале коррозионной стойкости металлов, цинк соответствует 6 баллам и относится к пониженностойким металлам.
Задача 8. Почему химически чистое железо является более стойким против коррозии, чем техническое железо? Составьте уравнения анодного и катодного процессов, происходящих при коррозии технического железа во влажном воздухе и в азотной кислоте. Будет ли оксидная пленка, образующаяся на свинце, обладать защитными свойствами?
Решение.
Техническое железо содержит примеси, которые, как правило, выполняют роль катода. Либо, если это углерод, который не передает в раствор положительно заряженных ионов и не имеет заградительного барьера от ионов водорода в кислой среде. Само железо будет служить анодом и подвергаться разрушению.
В химически чистом железе нет примесей, которые образовали бы гальванопару с железом, где бы оно окислялось.
При коррозии технического железа протекают следующие реакции:
Во влажном воздухе
А: Fe – 2e — = Fe 2+
Далее Fe(OH)2 переходит в Fe(OH)3
В азотной кислоте
А: Fe – 2e — = Fe 2+
Будет ли оксидная пленка, образующаяся на свинце, обладать защитными свойствами?
Защитные свойства пленки оценивают величине фактора Пиллинга—Бэдвордса: (α = Vок/VМе), значения которого вы найдете в таблице, приведенной в теоретической части данного раздела. Мы рассчитаем значение α по формуле:
Свинец может образовать оксиды состава PbO и PbO2, поэтому рассчитаем значение α для каждого случая
МPbO = 207+16 = 223 г/моль
т.е для всех оксидных пленок α лежит в интервале 2,5>α>1, т.е. они являются сплошными и обладают защитными свойствами.
Задача 9. Приведите примеры двух металлов, пригодных для протекторной защиты никеля. Для обоих случаев напишите уравнение электрохимической коррозии в среде азотной кислоты. Оценить коррозионную стойкость кадмия на воздухе при высоких температурах. Образец кадмия плотностью ρ = 8,65 г/см 3 , размером 45х25х1 мм после 150 часов окисления и снятия продуктов коррозии весил 10,0031 г.
Решение.
Протекторная защита – один из видов электрохимической защиты – заключается в следующем.
К защищаемому сооружению присоединяют пластины более активного металла, который называется протектором. Протектор – металл с более отрицательным потенциалом – является анодом, а защищаемое сооружение – катодом. Соединение протектора и защищаемого сооружения проводником тока, приводит к разрушению протектора.
Для протекторной защиты никеля подойдут, например, железо и цинк:
При электрохимической коррозии в среде азотной кислоты протекают следующие реакции:
Ni — Fe
А: Fe – 2e — = Fe 2+
Ni — Zn
Оценить коррозионную стойкость кадмия на воздухе при высоких температурах. Образец кадмия плотностью ρ = 8,65 г/см 3 , размером 45х25х1 мм после 150 часов окисления и снятия продуктов коррозии весил 10,0031 г.
Оценить коррозионную стойкость металла можно по формуле:
Kн = 365·h/τ
h = Δm/(S·ρ)
Найдем площадь поверхности металла:
S = 2·(4,5·2,5) + 2·(4,5·0,1) + 2·(2,5·0,1) = 23,9 см 2
Масса металла до начала коррозии равна:
m1 = V·ρ = 4,5·2,5·0,1·8,65 = 9,7313 г
Убыль массы:
Δm = m1 – m2 = 10,0031 – 9,7313 = 0,2718
h = 0,2718/(23,9·8,65) = 0,0013 см = 0,013 мм
Kн = 365·0,013·24/150 = 0,76 мм/год
По десятибалльной шкале коррозионной стойкости металлов, определяем, что в данных условиях, кадмий соответствует 7 баллам и относится к пониженностойким металлам.
Коррозия металла уравнение и задачи
8.4 РЕШЕНИЕ ТИПОВЫХ ЗАДАЧ ПО ТЕМЕ “КОРРОЗИЯ МЕТАЛЛОВ И МЕТОДЫ ЗАЩИТЫ МЕТАЛЛОВ ОТ КОРРОЗИИ”
(для нехимических специальностей)
1. Склепаны два металла. Укажите, какой из металлов подвергается коррозии:
а) Mn – Al ; б) Sn – Bi .
а) Al в ряду напряжений находится перед марганцем и имеет более отрицательное значение стандартного электродного потенциала, поэтому при контакте этих двух металлов Al будет анодом, а Mn — катодом. Окисляться, т.е. подвергаться коррозии, будет алюминий.
б) В этом случае корродировать будет олово, т.к. в ряду напряжений оно расположено впереди висмута и, следовательно, является электрохимически более активным.
2. Какие из нижеперечисленных металлов выполняют для свинца роль анодного покрытия: Pt , Al , Cu , Hg ?
Анодное покрытие – это нанесение на защищаемое изделие электрохимически более активного металла. Из перечисленных металлов электрохимически более активным (по сравнению со свинцом) является алюминий (см. ряд напряжений металлов).
3. Какие из нижеперечисленных металлов выполняют для свинца роль катодного покрытия: Ti , Mn , Ag , Cr ?
Катодное покрытие – это нанесение на защищаемое изделие электрохимически менее активного металла. Из перечисленных металлов электрохимически менее активным (по сравнению со свинцом) является серебро (см. ряд напряжений металлов).
4. Укажите продукт коррозии при контакте Zn – Ni в нейтральной среде.
При контакте двух металлов различной электрохимической активности возникает гальванический элемент. В нейтральной среде его схема выглядит следующим образом:
Так как цинк электрохимически более активен (см. ряд напряжений металлов), он будет окисляться ( корродировать ). На никеле будет протекать восстановительный процесс (в нейтральной среде – кислородная деполяризация):
А (–): Zn – 2e — = Zn 2+
Продукт коррозии – Zn (OH)2.
5. Укажите продукт коррозии при контакте Zn – Ni в кислой среде ( HCl ).
При контакте двух металлов различной электрохимической активности возникает гальванический элемент. Его схема для кислой среды раствора:
Так как цинк электрохимически более активен (см. ряд напряжений металлов), он будет окисляться ( корродировать ). На никеле будет протекать восстановительный процесс (в кислой среде – водородная деполяризация):