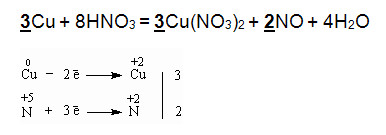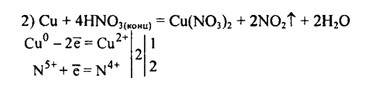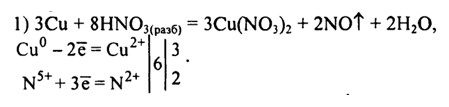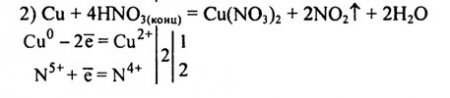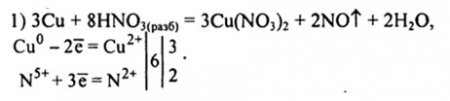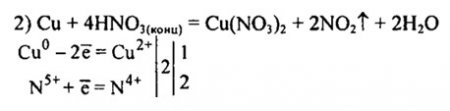тест по химии (9 класс) по теме
Контрольная работа по теме «Неметаллы» составлена в двух вариантах для 9 класса по программе О.С Габриеляна
- Скачать:
- Предварительный просмотр:
- По теме: методические разработки, презентации и конспекты
- Ответы на контрольную работу по теме «Неметаллы»(Габриелян)
- Основные разделы
- Контрольные работы
- Ответы на контрольную работу по теме «Неметаллы»(Габриелян)
- Контрольная работа по теме «Неметаллы»
- Просмотр содержимого документа «Контрольная работа по теме «Неметаллы»»
Скачать:
| Вложение | Размер |
|---|---|
| kontrolnaya_rabota_nemetally_9_kl.odt | 24.44 КБ |
Предварительный просмотр:
Контрольная работа по теме «Неметаллы»
При выполнении заданий с выбором ответа (А1 — А8) запишите в тетрадь номер правильного ответа.
А1. Заряд ядра атома +17 имеют атомы химического элемента:
1) азота 2)кислорода 3)серы 4)хлора
А2. Число общих электронных пар в молекуле водорода:
А3. Ковалентная неполярная связь имеется в молекуле вещества, формула которого :
1) N 2 2)CH 4 3)HCI 4)Na 2 S
А4. Степень окисления фосфора в ряду веществ, формулы которых
Са 3 Р 2 — Р — Р 2 О 3 — Р 2 О 5
- повышается от 0 до +5
- повышается от -3 до +5
- понижается от +6 до -2
- повышается от -4 до +4
А5. Реактивом на карбонат-анион является катион:
А6.Химическая реакция возможна между веществами , формулы которых:
- SiO 2 и Н 2 О 3) Р 2 О 5 и NaОН
- SO 2 и СO 2 4) Н 2 SiO 3 и Mg
А7. Оксид серы (IV) не образуется при взаимодействии веществ, формулы которых :
- S и O 2 3) Hg и Н 2 SO 4(конц)
- Н 2 SO 4(конц) и Сu 4) СаСО 3 и Н 2 SO 4
А8. Массовая доля азота в сульфате аммония равна
В 1. В ряду химических элементов Ge —► Si—► C
1) увеличивается радиус атомов
2) усиливаются неметаллические свойства соответствующих им простых веществ
3) ослабевает основный характер их высших оксидов
4) увеличивается чило электронов во внешнем слое
5) увеличивается заряд ядра атомов
В2. Установите соответствие между исходными веществами и продуктами реакции.
Исходные вещества Продукты реакции
A) CuSO 4 + NaОН 1) Н 2 O + CuSO 4
Б) Сu(OH) 2 + Н 2 SO 4 2) CuCI 2 + BaSO 4
В) CuSO 4 + BaCI 2 3) Na 2 SO 4 + Сu(OH) 2
4) CuCI 2 + BaSO 4
5) CuCI 2 + SO 2 + Н 2 О
С 1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
С—► СO 2 —►Na 2 СO 3 —► NaСI
С 2. К 27 г раствора с массовой долей хлорида меди 10% добавили избыток раствора сульфида натрия. Определите массу выпавшего осадка.
Контрольная работа по теме «Неметаллы»
При выполнении заданий с выбором ответа (А1 — А8) запишите в тетрадь номер правильного ответа.
А1. Заряд ядра атома +14 имеют атомы химического элемента:
1) азота 2) кислорода 3) кремния 4) углерода
А2. Число общих электронных пар в молекуле азота:
А3. Ковалентная полярная связь имеется в молекуле вещества, формула которого :
1) N 2 2)O 2 3) NaCI 4)H 2 S
А4. Степень окисления серы в ряду веществ, формулы которых
SO 3 — SO 2 — S — H 2 S
- повышается от 0 до +5
- понижается от +5 до 0
- повышается от -4 до +4
- понижается от +6 до -2
А5. Реактивом на сульфат -анион является катион:
А6. Химическая реакция возможна между веществами , формулы которых:
- СO 2 и NaОН 3) SO 2 и N 2 О 5
- Cu и Н 2 SO 4(разб) 4) Р 2 О 5 и HCI
А7. Оксид углерода (IV) образуется при взаимодействии веществ, формулы которых :
- Na 2 CO 3 и KСI 3) СO и Н 2 O 4
- СаСО 3 и HCI 4) СаСО 3 и K 2 SO 4
А8. Массовая доля кислорода в нитрате меди (II) равна
В 1. В ряду химических элементов As —► P—► N
1) увеличивается электроотрицательность
2) возрастают радиусы атомов
3) усиливаются металические свойства
4) увеличивается чило электронов во внешнем слое
5)уменьшается радиус атомов элементов
В2. Установите соответствие между исходными веществами и продуктами реакции.
Исходные вещества Продукты реакции
A) FeSO 4 + KОН 1) Fe(OH) 2 + K 2 SO 4
Б) K 2 O + Н 2 SO 4 2)K 2 O + Fe(OH) 2
В) KОН + SO 2 3) K 2 SO 4 + H 2 O
4) K 2 SO 3 + H 2 O
5) K 2 SO 4 + H 2
С 1. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
СI 2 —► HСI—►NaСI —► AgСI
С 2. На 300 г. известняка, содержащего 75% карбоната кальция , подействовали избытком соляной кислоты. Вычислите объем (н.у) выделившегося газа.
Время выполнения работы 45 мин.
Часть 1-8 баллов, часть 2 — 4 балла(2+2), часть 3 — 10 баллов (3+4). Итого: 19 баллов.
менее 7 баллов — «2»
СO 2 + Na 2 O = Na 2 CO 3
Na 2 CO 3 + 2HCI = 2NaCI +СO 2 +H 2 O
HCI+ NaОН = NaCI+ H 2 O
NaCI+AgNО 3 =NaNО 3 + AgCI
По теме: методические разработки, презентации и конспекты
Контрольная работа по природоведению 5 класс; контрольная работа по географии 6 класс «Гидросфера»
Контрольные работы составлены с учётом материалов учебников «Природоведение 5 класс» авторы: Т.С. Сухова, В.И.Строганов и «Землеведение 6 класс» авторы :В.П.Дронов,Л.Е.Савельева.Данные работы ап.
Комплексные числа.Контрольная работа №1 и контрольная работа №2
Контрольная работа №1 и №2 по теме » Комплексные числа» на курсах «Учитель профильной школы».
Методические указания и контрольные задания для домашней контрольной работы по ПМ 04. Управление работами по производству и переработке продукции растениеводства МДК. 04.03Организация малого бизнеса для студентов заочной формы обучения Специальность
Методические указания и контрольные задания для домашней контрольной работы поПМ 04. Управление работами по производству и переработке продукции растениеводства МДК. 04.03Организация малого.
Методические указания и контрольные задания для домашней контрольной работы по ПМ 04. Управление работами по производству и переработке продукции растениеводства МДК.04.02. Учет и анализ хозяйственной деятельности для студентов заочной формы обучения
Методические указания и контрольные задания для домашней контрольной работы по ПМ 04. Управление работами по производству и переработке продукции растениеводстваМДК.04.02. Учет и анализ хо.
Методические указания и контрольные задания для домашней контрольной работы по ПМ 04. Управление работами по производству и переработке продукции животноводства МДК.04.01. Управление структурным подразделением организации для студентов заочной формы
Методические указания и контрольные задания для домашней контрольной работы по ПМ 04. Управление работами по производству и переработке продукции животноводства МДК.04.01. Управление .
Контрольная работа по русскому языку по теме «Наречие» 7 класс, контрольная работа по русскому языку по теме «Частицы» 7 класс
Контрольная работа по теме «Наречие», контрольная работа по теме «Частицы».
Контрольная работа №8 Итоговая контрольная работа
Контрольная работа №8Итоговая контрольная работа.
Ответы на контрольную работу по теме «Неметаллы»(Габриелян)
Основные разделы
Контрольные работы
Ответы на контрольную работу по теме «Неметаллы»(Габриелян)
- Post category:Контрольные работы по химии 9 класс
- Reading time: 12 минут чтения
ЗАДАНИЕ 1
Напишите уравнения реакций для следующих переходов:
С →С02 →СаС03 →СаС12 →СаС03.
Превращение 1 рассмотрите в свете ОВР, 4 — в свете ТЭД.
С→СО2→ СаСО3→ CaCl2 → СаСО3
C+O2 → CO2
C0 -4e= C+4 восстановитель
O2 + 4e= 2O-2 окислитель
CO2+ CaO→CaCO3
CaCO3+2HCl→ CaCl2 +H2O + CO2
CaCl2+Na2CO3=CaCO3+2NaCl
Ca2++CO32-=CaCO3
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
N2 + ЗН2 2NH3 + Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
3H2 + N2 2NH3 + Q
N20 +2*3е→2N-3 окислитель
H20 -2*1е→2H+1 восстановитель
Исходные вещества: 1 моль азота (молекула из 2 атомов азота), 3 моль водорода (молекула из 2 атомов водорода). Продукт реакции – аммиак, 2 моль. Молекула из 1 атома азота и 2 атомов водорода. Исходные вещества продукты реакции – газы.
Реакция:
Экзотермическая.
Окислительно-восстановительная.
Прямая.
Каталитическая.
Обратимая.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + HN03(paз6) → CU(N03)2 + NO + Н20.
ЗАДАНИЕ 4
К раствору, содержащему 16 г сульфата меди (II), прибавили избыток железных опилок. Какая масса меди выделилась при этом?
CuSO4 + Fe = FeSO4 + Cu
n (CuSO4) = 16/160 = 0,1моль
n (CuSO4) = n (Cu) =0,1моль
m(Cu) = 0,1*64= 6,4 г
ЗАДАНИЕ 1
Напишите уравнения реакций для следующих переходов:
N2 → NO → N02 →HN03 →CU(N03)2.
Превращение 1 рассмотрите в свете ОВР, 4 — в свете ТЭД.
N2 + O2 = 2NO
N20 -4e= 2N+2 восстановитель
O20 +4e= 2O-2 окислитель
2NO + O2 = 2NO2
4NO2 + O2 + 2H2O = 4HNO3
3Cu + 8HNO3 = 3Cu(NO3)2 + 2NO + 4H2O
3Cu0 + 8H++8NO3- = 3Cu2+ +6NO3- + 2NO + 4H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
2N0 + 02 2N02 + Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
2NO + O2 = 2NO2 + Q
N+2 -2e = N+4 восстановитель
O2 +4e = 2O-2 окислитель
Исходные вещества: 2 моль оксида азота 2 (молекула из 1 атома азота и 1 атома кислорода), 1 моль кислорода (молекула из 2 атомов кислорода). Продукт реакции – оксид азота 4, 2 моль (1 атом азота и 2 атома кислорода в молекуле). Исходные вещества продукты реакции – газы.
Реакция:
Экзотермическая.
Окислительно-восстановительная.
Прямая.
Некаталитическая.
Обратимая.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + НNO3(КОНЦ) → Cu(N03)2 + N02 + Н20.
ЗАДАНИЕ 4
6,5 г цинка обработали достаточным количеством разбавленного раствора серной кислоты. Определите объем выделившегося водорода.
H2SO4 + Zn = Zn SO4 + H2 ↑
n(Zn) = 6,5/65 = 0,1 моль
n(H2) = n(Zn) = 0,1 моль
V(H2) = 0,1*22,4 = 2,24 л
ЗАДАНИЕ 1
Напишите уравнения реакций для следующих переходов:
S → S02 →S03 H2S04 →BaS04.
Превращение 1 рассмотрите в свете ОВР, 4 — в свете ТЭД.
S+O2→ SO2
S0 -4e = S+4
O02 + 4e = 2O-2
2SO2+O2→2SO3
SO3+H2O→H2SO4
H2SO4+ BaCl2 = BaSO4↓ + 2HCl
SO42-+ Ba2+ = BaSO4↓
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
С02 + С 2СО — Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
СО2 + С = 2СО– Q
С+4 +2е = С+2 окислитель
С0 -2е =С+2 восстановитель
Исходные вещества: 1 моль оксида углерода 4 (1 атом углерода, 2 атома кислорода) – газ, 1 моль углерода (1 атом углерода) -тв. Продукт реакции – 2 моль оксида углерода 2 (1 атом углерода, 1 атома кислорода) – газ.
Эндотермическая
ОВР
Прямая
ЗАДАНИЕ 3
В схеме реакции расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Zn + H2S04(KOHц) → ZnS04 + H2S↑ + H20.
Zn + H2SO4(конц.) → ZnSO4 + H2S↑ + H2O
уравнения полуреакций:
Zn0 – 2e– → Zn+2| 2 | 8 | 4 | – восстановитель
S+6 + 8e– → S–2 | 8 | 8 | 1 | – окислитель
4Zn0 + S+6 = 4Zn+2 + S–2
4Zn + 5H2SO4(конц.) = 4ZnSO4 + H2S↑ + 4H2O
ЗАДАНИЕ 4
Определите количество вещества сульфата калия, полученного при сливании избытка раствора гидроксида натрия с раствором, содержащим 2 моль серной кислоты.
2KOH + H2SO4 = K2SO4 + H2O
n(H2SO4) = n(K2SO4) = 2 моль
ЗАДАНИЕ 1
Напишите уравнения реакций для следующих переходов:
Si → Si02 →Na2Si03 →H2Si03 →Si02.
Превращение 1 рассмотрите в свете ОВР, 3 — в свете ТЭД.
1) Si + O2 = SiO2
Si0 -4е = Si+4 восстановитель
O20 +4е = 2O2- окислитель
2) SiO2 + Na2O = Na2SiO3
3) Na2SiO3 + 2HCl = H2SiO3 ↓+ 2NaCl
2H+ +SiO3 2- = H2SiO3 ↓
4) H2SiO3 = SiO2 + Н2О
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
Н20(пар) + СО Н2 + С02 — Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
Н+12О + С+2О = Н02 + С+4О2 – Q
2Н+1 +2е = Н02 окислитель
С+2 -2е =С+4 восстановитель
Исходные вещества: 1 моль воды (2 атома водорода, 1 атом кислорода) – газ, 1 моль оксида углерода 2 (1 атом углерода, 1 атом кислорода) -газ. Продукты реакции – 1 моль водорода (2 атома водорода в молекуле) – газ, 1 моль оксида углерода 4 (1 атом углерода, 2 атома кислорода) – газ.
Эндотермическая
ОВР
Прямая
Обратимая
Некаталитическая.
ЗАДАНИЕ 3
В схеме реакции расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
NH3 + CuO→ N2 + Сu + Н20.
2NH3 + 3CuO -> 3Cu + N2 + 3H2O
N-3 -6е = N20 восстановитель
Cu+2 +2е =Cu0 окислитель
ЗАДАНИЕ 4
10 г оксида магния обработали раствором азотной кислоты. Какая масса соли образовалась?
MgO + 2HNO3 = Mg(NO3)2 + H2O
n (MgO) = 10/40 =0,25 моль
n (MgO) = n (Mg(NO3)2) = 0,25 моль
m(Mg(NO3)2) = 0,25*148= 37 г
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
С → СН4 →С02 →СаС03 →… →СаС03.
Превращение 2 рассмотрите в свете ОВР, 5 — в свете ТЭД.
С + 2Н2 = СН4
СН4 + 2О2 = СО2 + 2Н2О
С-4 — 8е=С+4 восстановитель
О2 о +4е = 2О-2 окислитель
СО2 + СаО = СаСО3
CaCO3 + CO2 + H2O ↔ Ca(HCO3)2
Ca(HCO3)2 = CaCO3↓ + CO2 + H2O
Ca2+ + 2HCO3- = CaCO3↓ + CO2 + H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
2Fe + ЗС12 = 2FeCl3 + Q,
по всем изученным признакам классификации.
Определите окислитель и восстановитель, процессы окисления и восстановления.
ЗАДАНИЕ 3
В схеме реакции расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + HN03(paз6) →Cu(NO3)2 + … + Н20.
ЗАДАНИЕ 4
К 160 кг 10%-го раствора сульфата меди (II) прибавили железные опилки. Какая масса меди выделилась?
CuSO4 + Fe = FeSO4 + Cu
m (CuSO4) = 160*0,1= 16 г
n(CuSO4) = 16/160 = 0,1 моль
m (Cu) =0,1 * 64 = 6,4 г
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
N2 → Li3N →NO →N02 … →…→ Cu(NO3)2.
Превращение 2 рассмотрите в свете ОВР, 5 — в свете ТЭД.
1)N2+6Li->t,кат. ->2Li3N
2) 4Li3N + 5O2->t->4NO+6Li2O
N-3 -5e =N+2 восстановитель
O20 +4е= 2O-2 окислитель
3)2NO+O2->2NO2
4)4NO2+2H2O+O2->4HNO3
5) Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O
Cu0 + 4H+ +2NO3 -= Cu2+ + 2NO2 + 2H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
2А1 + 3S = A12S3 + Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
2Al + 3S = Al2S3 + Q
Al – 3e– = Al +III восстановитель
S+ 2e– = S –Il окислитель
Экзотермическая
ОВР
Прямая
Необратимая
Некаталитическая
Исходные вещества: 2 моль алюминия – тв., 3 моль серы тв.
Продукт: 1 моль сульфида алюминия (из 2 атомов алюминия, 3 атомов серы) – тв.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + HN03(KOHЦ) → Cu(N03)2 + … + Н20.
ЗАДАНИЕ 4
Достаточное количество цинка обработали 120 кг 10%-го раствора серной кислоты. Определите объем выделившегося газа.
Zn + H2SO4 = ZnSO4 + H2
m (H2SO4) = 120*0,1= 12кг= 12000 г
n(H2SO4) = 12000/98 = 122 моль
n(H2) = n(H2SO4) = 122 моль
V(H2) = 122*22,4 = 2742 л
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
S →FeS →S02 →S03 →…→ BaS04.
Превращение 2 рассмотрите в свете ОВР, 5 — в свете ТЭД.
Fe + S = FeS
2FeS + 3O2 = 2FeO + 2SO2
S-2 -6e = S+4 восстановитель
O20 +4е= 2O-2 окислитель
2SO2 + O2 = 2SO3
SO3 + H2O = H2SO4
BaCl2 + H2SO4 → BaSO4↓ + 2HCl
Ba2+ + SO42- → BaSO4↓
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
ЗСа + 2Р = Са3Р2 — Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
3Са + 2Р = Са3Р2 — Q
Са – 2e– = Са +II восстановитель
Р + 3e– = Р –IlI окислитель
Эндотермическая
ОВР
Прямая
Необратимая
Некаталитическая
Исходные вещества: 2 моль фосфора – тв., 3 моль кальция тв.
Продукт: 1 моль фосфида кальция (из 2 атомов фосфора, 3 атомов кальция) – тв.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Zn + H2S04(KOH4) → ZnS04 + … + Н20.
2H2SO4 + Zn = SO2↑ +ZnSO4 + 2H2O
Zn – 2e– = Zn +II восстановитель
S+6 + 2e– = S +4 окислитель
ЗАДАНИЕ 4
Какой объем водорода выделится при взаимодействии достаточного количества цинка с 200 г 10% -го раствора серной кислоты?
H2SO4 + Zn = Zn SO4 + H2 ↑
m (H2SO4) = 200*0,1= 20 г
n(H2SO4) = 20/98 = 0,2 моль
n(H2) = n(H2SO4) = 0,2 моль
V(H2) = 0,2*22,4 = 4,57л
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
Si → Si02 →Na2Si03 →…→ Si02.
Превращение 1 рассмотрите в свете ОВР, 3 — в свете ТЭД.
Si + O2 = SiO2
Si0 -4е = Si+4
O20 +4е= 2O-2 окислитель
SiO2 + Na2O = Na2SiO3
Na2SiO3 + 2HCl = H2SiO3 + 2NaCl
2Н+ +SiO3 2- = H2SiO3 ↓
H2SiO3 = SiO2+ H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
Fe203 + 2А1 = 2Fe + А1203 + Q,
по всем известным признакам классификации.
Рассмотрите данную реакцию с точки зрения ОВР.
Fe2O3 + 2Al = 2Fe + Al2O3 + Q
Al0 – 3e– = Al +III восстановитель
Fe+3 + 3e– = Fe 0 окислитель
Экзотермическая
ОВР
Прямая
Необратимая
Некаталитическая
Исходные вещества: 2 моль алюминия – тв., 1 моль оксида железа 3 (2 атома железа и 3 атома кислорода в ФЕ) тв.
Продукты: 2 моль железа, 1 моль оксида алюминия (из 2 атомов алюминия, 3 атомов кислорода в ФЕ) – тв.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
NH3 + CuO→N2 + Сu + … .
3CuO + 2NH3 = 3Cu + N2 + 3H2O
Cu+2 + 2е = Cu0 окислитель
2N-3 -6е = N20 восстановитель
ЗАДАНИЕ 4
Достаточное количество оксида магния обработали 40 кг 10%-го раствора азотной кислоты. Какая масса соли образовалась?
2HNO3 + MgO = Mg(NO3)2 + H2O
m (HNO3) = 40000*0,1= 4000 г
n(HNO3) = 4000/63 = 63,5 моль
n(Mg(NO3)2) = n(HNO3)/2 = 31,7 моль
m (Mg(NO3)2) = 31,7*148 = 4698 г = 4,698 кг
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
С →СН4 → … →CaCO3→ … → CaCO3.
Рассмотрите все реакции в свете ОВР и ТЭД везде, где это имеет место.
С + 2Н2 = СН4
С0 +4е = С-4 окислитель
Н20 -2е = 2Н+1 восстановитель
СН4 + О2 = СО2 + Н2О
С-4 -8е = С+4 восстановитель
О20 +4е = 2О-2 окислитель
СО2 + СаО = СаСОз
CaCO3+2HCl→ CaCl2 +H2O + CO2
CaCO3+2H+→ Ca2+ +H2O + CO2↑
CaCl2+Na2CO3=CaCO3+2NaCl
Ca2++CO32-=CaCO3
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
Zn + 2НС1 = ZnCl2 + H2↑ + Q,
по всем изученным признакам классификации.
Рассмотрите реакцию с точки зрения ТЭД.
Zn+2HCl=ZnCl2+H2 + Q
Исходные вещества: 1 моль цинк, 2 моль соляной кислоты (1 атом водорода, 1 атом хлора в молекуле). Продукты реакции: 1 моль хлорида цинка (1 атом цинка, 2 атома хлора в ФЕ), 1 моль водорода (2 атома водорода).
Экзотермическая реакция
Цинк – тв., соляная кислота – ж., хлорид цинка тв. (раствор), водород – г.
Без катализатора
С изменением степеней окисления
Необратимая
2H++2Cl-+Zn0=Zn2++2Cl-+H20
2H++Zn0=Zn2++H20
ЗАДАНИЕ 3
Закончите уравнение ОВР, расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
Сu + HN03(paз6) →.
ЗАДАНИЕ 4
К 160 кг 10%-го раствора сульфата меди (II) прибавили избыток железных опилок. Какая масса меди выделилась, если выход продукта составил 90% от теоретически возможного?
Fe + CuSO4 = FeSO4 + Cu
m (CuSO4) = 160000*0,1= 16000 г
n (CuSO4) = 16000/160= 100 моль
n (CuSO4)= n (Cu) по уравнению (теор.) = 100 моль
n (Cu) = 100/0,9 = 90 моль (пр.)
m (Cu) = 90*64= 5760 г
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
N2 →… →NO →N02 →… →Cu(N03)2.
Рассмотрите все реакции в свете ОВР и ТЭД везде, где это имеет место.
1)N2+3H2->t,кат. ->2NH3
N20 +2*3е→2N-3 окислитель
H20 -2*1е→2H+1 восстановитель
2)4NH3+5O2->t,кат. ->4NO+6H2O
N-3 — 5е→N+2 восстановитель
O20 +4e→2O-2 окислитель
3)2NO+O2->2NO2
N+2 — 2е→N+4 восстановитель
O20 +4e→2O-2 окислитель
4)4NO2+2H2O+O2->4HNO3
N+4 — 1е→N+5 восстановитель
O20 +4e→2O-2 окислитель
5)Cu + 4HNO3 = Cu(NO3)2 + 2NO2 + 2H2O
Cu0 + 4H+ +2NO3 -= Cu2+ + 2NO2 + 2H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
2NO + 02 2N02 + Q,
по всем изученным признакам классификации. Рассмотрите данную реакцию в свете ОВР.
2NO + O2 = 2NO2 + Q
N+2 -2e = N+4 восстановитель
O2 +4e = 2O-2 окислитель
Исходные вещества: 2 моль оксида азота 2 (молекула из 1 атома азота и 1 атома кислорода), 1 моль кислорода (молекула из 2 атомов кислорода). Продукт реакции – оксид азота 4, 2 моль (1 атом азота и 2 атома кислорода в молекуле). Исходные вещества продукты реакции – газы.
Реакция:
Экзотермическая.
Окислительно-восстановительная.
Прямая.
Некаталитическая.
Обратимая.
ЗАДАНИЕ 3
Закончите уравнение ОВР и расставьте коэффициенты в нем методом электронного баланса, укажите окислитель и восстановитель:
Сu + НNОз(конц.> →.
ЗАДАНИЕ 4
ЦИНК массой 6,5 кг обработали избытком раствора серной кислоты. Определите объем выделившегося газа, если выход продукта реакции составил 80% от теоретически возможного.
H2SO4 + Zn = Zn SO4 + H2 ↑
n(Zn) = 65000/65 = 1000 моль
n(H2) = n(Zn) = 1000 моль (теор.)
n(H2)практ. = 1000*0,8 = 800моль
V(H2) = 800*22,4 = 17920л
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
S →FeS →S02 →… →H2S04 →… .
Рассмотрите все реакции в свете ОВР и ТЭД везде, где это имеет место.
S+ Fe = FeS
S0 + 2e = S-2 окислитель
Fe0 -2e= Fe+2 восстановитель
4FeS + 7O2 → 2Fe2O3 + 4SO2↑
S-2 -6e = S+4 восстановитель
O2 +4e = 2O-2 окислитель
2SO2 + O2 = 2SO3
S +4 — 2е→ S +6 восстановитель
O20 +4e→2O-2 окислитель
SO3 + H2O = H2SO4
SO3 + H2O = 2H+ +SO42-
H2SO4 + 2NaOH = Na2SO4 + H2O
2H+ +2OH- = H2O
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
С02 + С 2СО — Q,
по всем изученным признакам классификации. Рассмотрите данную реакцию в свете ОВР.
СО2 + С = 2СО– Q
С+4 +2е = С+2 окислитель
С0 -2е =С+2 восстановитель
Исходные вещества: 1 моль оксида углерода 4 (1 атом углерода, 2 атома кислорода) – газ, 1 моль углерода (1 атом углерода) -тв. Продукт реакции – 2 моль оксида углерода 2 (1 атом углерода, 1 атома кислорода) – газ.
Эндотермическая
ОВР
ЗАДАНИЕ 3
Закончите уравнение ОВР и расставьте коэффициенты в нем методом электронного баланса, укажите окислитель и восстановитель:
Zn + H2S04(KOHЦ) →.
Zn + H2SO4(конц.) → ZnSO4 + H2S↑ + H2O
уравнения полуреакций:
Zn0 – 2e– → Zn+2| 2 | 8 | 4 | – восстановитель
S+6 + 8e– → S–2 | 8 | 8 | 1 | – окислитель
4Zn0 + S+6 = 4Zn+2 + S–2
4Zn + 5H2SO4(конц.) = 4ZnSO4 + H2S↑ + 4H2O
ЗАДАНИЕ 4
Какой объем водорода выделится при взаимодействии 13 г цинка с избытком раствора серной кислоты? Объемная доля выхода водорода составляет 90% от теоретически возможного.
H2SO4 + Zn = Zn SO4 + H2 ↑
n(Zn) = 13/65 = 0,2 моль
n(H2) = n(Zn) = 0,2 моль (теор.)
n(H2)практ. = 0,2*0,9 = 0,18 моль
V(H2) = 0,18*22,4 = 4,032 л
ЗАДАНИЕ 1
Напишите уравнения реакций для переходов:
Si →…→ Na2Si03 →…→ Si02.
Рассмотрите все реакции в свете ОВР и ТЭД везде, где это имеет место.
Si + O2 = SiO2
S0 -4e = S+4 восстановитель
O2 +4e = 2O-2 окислитель
SiO2 + Na2O = Na2SiO3
SiO2 + Na2O = 2Na+ +SiO32-
Na2SiO3 + 2HCl = H2SiO3 ↓+ 2NaCl
2Н+ + SiO32- = H2SiO3 ↓
H2SiO3 = SiO2 + Н2О
ЗАДАНИЕ 2
Дайте характеристику реакции, уравнение которой
H20(nap) + C0H2 + C02-Q,
по всем изученным признакам классификации.
Рассмотрите данную реакцию в свете ОВР.
Н+12О + С+2О = Н02 + С+4О2 – Q
2Н+1 +2е = Н02 окислитель
С+2 -2е =С+4 восстановитель
Исходные вещества: 1 моль воды (2 атома водорода, 1 атом кислорода) – газ, 1 моль оксида углерода 2 (1 атом углерода, 1 атом кислорода) -газ. Продукты реакции – 1 моль водорода (2 атома водорода в молекуле) – газ, 1 моль оксида углерода 4 (1 атом углерода, 2 атома кислорода) – газ.
Эндотермическая
ОВР
Прямая
Обратимая
Некаталитическая.
ЗАДАНИЕ 3
В схеме ОВР расставьте коэффициенты методом электронного баланса, укажите окислитель и восстановитель:
NH3 + CuO→N2 + … + … .
3CuO + 2NH3 = 3Cu + N2 + 3H2O
Cu+2 + 2е = Cu0 окислитель
2N-3 -6е = N20 восстановитель
ЗАДАНИЕ 4
10 кг оксида магния обработали избытком раствора азотной кислоты. Какая масса соли образовалась, если выход соли составил 80% от теоретически возможного?
2HNO3 + MgO = Mg(NO3)2 + H2O
n(MgO) = 1000/40 = 250 моль
n(Mg(NO3)2) = n(MgO) = 250 моль (теор.)
n(Mg(NO3)2)практ. = 250*0,8 = 200 моль
m (Mg(NO3)2) 200*148 = 29600 г
Контрольная работа по теме «Неметаллы»
Данная разработка предназначена для контроля и учёта знаний по теме «Неметаллы» в тестовой форме. С кадификатором и спецификацией.
Просмотр содержимого документа
«Контрольная работа по теме «Неметаллы»»
Муниципальное общеобразовательное учреждение
средняя общеобразовательная школа №1
Контрольная работа по теме
Сольвар Татьяна Александровна
элементов содержания и требований к уровню подготовки обучающихся
для проведения тематической контрольной работы
Учебник: Габриелян О.С. Химия. 9 класс
Вид контроля: тематический
Перечень элементов предметного содержания, проверяемых на контрольной работе
Описание элементов предметного содержания
Периодический закон и Периодическая система химических элементов Д.И.Менделеева
Закономерности изменения свойств элементов и их соединений в связи с положением в Периодической системе химических элементов Д.И. Менделеева
Строение атома. Строение электронных оболочек атомов первых 20 элементов Периодической системы Д.И. Менделеева
Атомы и молекулы. Химический элемент. Простые и сложные вещества. Основные классы неорганических веществ. Номенклатура неорганических соединений
Строение веществ. Химическая связь: ковалентная (полярная и неполярная), ионная, металлическая
Классификация химических реакций по различным признакам: числу и составу исходных и полученных веществ, изменению степеней окисления химических элементов, поглощению и выделению энергии.
Окислительно-восстановительные реакции. Степень окисления. Окислитель и восстановитель
Химические свойства простых веществ-неметаллов: водорода, кислорода, галогенов, серы, азота, фосфора, углерода, кремния. Химические свойства основных классов неорганических веществ.
Химические свойства кислот, солей, щелочей.
Проведение расчетов на основе формул и уравнений реакций. Вычисление количества вещества, массы или объема вещества по количеству вещества, массе или объему одного из реагентов или продуктов реакции
Взаимосвязь различных классов неорганических веществ
Химическая реакция. Условия и признаки протекания химических реакций. Химические уравнения. Сохранение массы веществ при химических реакциях.
Перечень требований к уровню подготовки обучающихся, освоивших
Описание требований к уровню подготовки обучающихся
Знать/понимать химическую символику: знаки химических элементов, формулы химических веществ, уравнения химических реакций;
Знать/понимать: важнейшие химические понятия: вещество, химический элемент, атом, молекула, относительные атомная и молекулярная массы, ион, катион, анион, электроотрицательность, валентность, степень окисления, моль, молярная масса, молярный объем, растворы, окислитель и восстановитель, окисление и восстановление, тепловой эффект реакции
Характеризовать химические элементы (от водорода до кальция) на основе их положения в Периодической системе химических элементов Д.И. Менделеева и особенностей строения их атомов;
Составлять: схемы строения атомов первых 20 элементов Периодической системы Д.И. Менделеева;
Объяснять закономерности изменения строения атомов, свойств элементов в пределах малых периодов и главных подгрупп, а также свойства образуемых ими высших оксидов;
Знать/понимать Периодический закон Д.И. Менделеева
Составлять формулы неорганических соединений изученных классов; уравнения химических реакций.
Уметь называть: соединения изученных классов неорганических веществ.
Определять/классифицировать вид химической связи в соединениях; принадлежность веществ к определенному классу соединений.
Определять/классифицировать типы химических реакций.
Характеризовать взаимосвязь между составом, строением и свойствами неорганических веществ;
химические свойства основных классов неорганических веществ (оксидов, кислот, оснований и солей)
Определять/классифицировать возможность протекания реакций ионного обмена;
Вычислять количество вещества, объем или массу вещества по количеству вещества, объему или массе реагентов или продуктов реакции массовую долю вещества в растворе
для проведения тематической контрольной работы
Вид контроля: тематический
Назначение контрольной работы: оценить уровень освоения каждым учащимся класса содержания учебного материала . по теме «Неметаллы» по предмету химия.
Содержание контрольных измерительных заданий определяется содержанием рабочей программы по теме «Неметаллы» учебного предмета химия, а также содержанием темы «Неметаллы» учебника для общеобразовательных учреждений под редакцией Габриеляна О.С..
Контрольная работа состоит из 12 заданий: 8 заданий базового уровня, 2 — повышенного, 2- высокого уровня сложности.
Распределение заданий по уровням сложности, проверяемым элементам предметного, метапредметного содержания, уровню подготовки, типам заданий и времени выполнения представлено в таблице 1