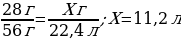Контрольная работа № 2 по темам: Кислород.Водород, Растворы.Вода»,
Химия 8 класс, 1-2 вариант, с ответами
- Просмотр содержимого документа «Контрольная работа № 2 по темам: «Кислород.Водород,Растворы.Воды»»
- Методические материалы контрольной работы по химии в 8 классе по теме: «Кислород, водород, вода, растворы.»
- Дистанционное обучение как современный формат преподавания
- Педагогическая деятельность в контексте профессионального стандарта педагога и ФГОС
- Химия: теория и методика преподавания в образовательной организации
- Дистанционные курсы для педагогов
- Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
- Материал подходит для УМК
- Другие материалы
- Вам будут интересны эти курсы:
- Оставьте свой комментарий
- Автор материала
- Дистанционные курсы для педагогов
- Подарочные сертификаты
- Контрольная работа по теме «Водород. Кислород. Вода. Растворы» учебно-методический материал по химии (8 класс)
- Скачать:
- Предварительный просмотр:
- По теме: методические разработки, презентации и конспекты
- 🔥 Видео
Просмотр содержимого документа
«Контрольная работа № 2 по темам: «Кислород.Водород,Растворы.Воды»»
Контрольная работа № 2
по теме: « Кислород. Водород. Растворы. Вода»
Напишите уравнения реакций горения в кислороде:
А) угля; б) лития; в) сероводорода H2S.Назовите продукты реакций.
Напишите уравнения реакций взаимодействия:
А) магния с соляной кислотой; б) натрия с водой; в)водорода с серой; г) водорода с оксидом меди.
Напишите уравнения реакций, позволяющих осуществить следующие превращения:FeO——Fe——-FeSO4. и укажите к какому типу реакций относится каждая из них.
Вычислите, какую массу кислорода можно получить при разложении 43,4 г оксида ртути.
Рассчитайте, какой объем водорода (н.у.) образуется при взаимодействии 28 г железа с соляной кислотой.
Вычислите массовую долю растворенного вещества в растворе, полученном при растворении 15 г соли в 45 г воды.
Рассчитайте, какую массу воды необходимо взять для приготовления раствора с массовой долей вещества 20%, если нужно растворить 100 г соли.
Контрольная работа № 2
по теме: « Кислород. Водород. Растворы. Вода»
1. Напишите уравнения реакций горения в кислороде:
Назовите продукты реакций.
Напишите уравнения реакций взаимодействия:
А) железа с раствором серной кислоты; б) бария с водой; в)водорода с кислородом; г) водорода с оксидом железа Fe2O3.
Напишите уравнения реакций, позволяющих осуществить следующие превращения:Cu——CuO——-Cu(NO3)2, и укажите к какому типу реакций относится каждая из них.
Рассчитайте, какую массу кислорода можно получить при разложении 24,5 г хлората калия KClO3.
Рассчитайте, какой объем водорода (н.у.) который вступит в реакцию с 25 г оксида кобальта CoO.
Выпарили 50 г раствора, при этом получили 5 г хлорида натрия. Вычислите массовую долю соли в растворе.
Рассчитайте, какую массу сахара и воды нужно взять для приготовления 250 г раствора с массовой долей сахара 15%.







1.А) 2. Mg + O₂ = 2MgO.







m р. в. (соль) = 5 г
Массовая доля растворённого вещества соли:
ω . (соль) = m . (соль) / m р-ра (соль) = 5 г / 50 г = 0,1 (10%)
Ответ: ω р. в. (соль) = 10%
Решение: m(сах)= m (раствора)* ω (сах)=0,15*250 г= 37,5г.
m (H₂O) = m(р-ра)- m (сах)=250 г-37,5 г=212,5 г.
Ответ: m (H₂O)= 212,5 г
Видео:Водород и кислород. 1 часть. 8 класс.Скачать

Методические материалы контрольной работы по химии в 8 классе по теме: «Кислород, водород, вода, растворы.»
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Рабочие листы и материалы для учителей и воспитателей
Более 300 дидактических материалов для школьного и домашнего обучения
Контрольная работа № 2 по темам:
«Кислород», «Водород», «Вода. Растворы»
1. Тест (выберите один правильный вариант ответа)
1. Элемент, наиболее распространенный на Земле, — это
1) кислород 2) азот 3) водород 4) кремний
2. В промышленности кислород получают из
1) хлората калия 2) воды 3) воздуха 4) перманганата калия
3. Катализатором разложения пероксида водорода является
1) оксид кальция 2) оксид серы(IV) 3) оксид магния 4) оксид марганца(IV)
4. Кислород выделяется в ходе
1) гниения 2) дыхания 3) горения 4) фотосинтеза
5. Укажите газ, который не относиться к благородным
1) азот 2) гелий 3) аргон 4)неон
6. Сложные вещества, состоящие из двух элементов, один из которых кислород это:
а) оксиды б) соли в) кислоты г) основания
7. Укажите правильное суждение
1) водород очень мало растворяется в воде
2) водород имеет высокую температуру сжижения
3) водород может быть получен при взаимодействии серебра с водой
4) водород не реагирует с кислородом
8. Взвеси, в которых мелкие частицы твердого вещества равномерно распределены между молекулами воды, называются:
1) суспензиями 2)эмульсиями 3) дымами 4)аэрозолями
9.Вода реагирует с активными металлами, такими как натрий и кальций, с образованием
1) гидроксидов 2)оксидов и водорода 3)кислот 4)гидроксидов и водорода
10. Вода реагирует почти со всеми оксидами неметаллов с образованием
1) гидроксидов и водорода 2)оксидов и водорода 3)кислот 4)гидроксидов
2. Задания со свободным ответом
1. Закончите уравнения реакций горения, расставьте коэффициенты, назовите получившиеся вещества.
2. Допишите уравнения реакций, характеризующих химические свойства водорода:
3.Рассчитайте, какую массу сахара и воды нужно взять для приготовления 250г раствора с массовой долей сахара 15%.
4.Составьте уравнения реакций взаимодействия с водой следующих веществ: калия, кальция.
Укажите названия веществ, образующихся в результате реакции.
Контрольная работа № 2 по темам:
«Кислород», «Водород», «Вода. Растворы»
1. Тест (выберите один правильный вариант ответа)
1. Укажите объемную долю кислорода в воздухе
1) 0,009 2) 0,209 3) 0,409 4) 0,781
2. В лаборатории кислород можно получить при разложении
1) хлората калия 2) перманганата калия 3) пероксида водорода 4) любого из перечисленных веществ
3. Молекулярный кислород не реагирует с
1) алюминием 2) золотом 3) медью 4) цинком
4. Газ, который поддерживает горение, — это
1) кислород 2) водород 3) азот 4) углекислый газ
а) водород б) кислород в) углекислый газ г) аргон
а) сернистый б) кислород в) углекислый г) водород
7. Вещества, ускоряющие химические реакции это:
а) растворы б) смеси в) воздух г) катализаторы
8. Взвеси, в которых мелкие капельки жидкого вещества равномерно распределены между молекулами воды, называются
1) суспензиями 2) эмульсиями 3) дымами 4) аэрозолями
9. При нагревании вода реагирует с менее активными металлами, такими как железо и цинк, с образованием
1) гидроксидов 2) оксидов и водорода 3) кислот 4) гидроксидов и водорода
10. Вода реагирует с оксидами активных металлов, таких как натрий и кальций, с образованием
1) гидроксидов и водорода 2) оксидов и водорода 3) кислот 4) гидроксидов
2. Задания со свободным ответом.
1. Закончите уравнения реакций горения, расставьте коэффициенты, назовите получившиеся вещества.
2.Допишите уравнения реакций, характеризующих химические свойства водорода:
3. Рассчитайте, какую массу сахара и воды нужно взять для приготовления 500г раствора с массовой долей сахара 5%.
4.Составьте уравнения реакций взаимодействия с водой следующих веществ: бария, лития.
Укажите названия сложных веществ, образующихся в результате реакции.
Контрольная работа № 2 по темам:
«Кислород», «Водород», «Вода. Растворы»
Ответы. Критерии оценивания.
За каждый правильный ответ 1 балл. Всего – 10 баллов.
а) 4P + 5O2 → 2P2O5 — оксид фосфора(V) б) C + O2 → CO2 – оксид углерода(IV)
в) 2Zn + O2 → 2ZnO — оксид цинка г) 2C2H6 + 7O2 → 4CO2 +6 H2O – оксид углерода(IV), вода
За каждое правильно написанное уравнение 1балл, за каждое правильно названное вещество 0,5 балла. Всего 6 баллов.
Водород в этих реакциях окисляется.
За каждое правильно написанное уравнение 1балл. За определение процесса 1 балл. Всего 3 балла.
3.1) m(сахара) = m(раствора) x W(сахара) : 100% = (250х15% ): 100% =37,5г
2) m(воды) = m(раствора) — m(сахара) = 250 — 37,5 =212,5г
За каждое правильное действие 1 балл, всего 2 балла
KOH – гидроксид калия
Ca(OH) 2 – гидроксид кальция
LiOH– гидроксид лития
За каждое правильно написанное уравнение 1балл, за каждое правильно названное вещество 0,5 балла. Всего 4,5 балла.
Всего за работу – 25,5 баллов
«2» — от 0 — 13 баллов, «3» — от13,5 до 18,5 баллов, «4» -от 19 до 21 баллов, «5» от 21,5 баллов.
Ответы. Критерии оценивания.
За каждый правильный ответ 1 балл. Всего – 10 баллов.
а) 3Fe + 2O2 → FeO Fe2O3 (Fe3O4) — железная окалина б) 2Ca + O2 →2CaO – оксид кальция
в) 4Li + O2 → 2Li2O — оксид лития г) 2C2H2 + 5O2 → 4CO2 + 2H2O – оксид углерода(IV), вода
За каждое правильно написанное уравнение 1балл, за каждое правильно названное вещество 0,5 балла. Всего 6 баллов.
Водород в этих реакциях окисляется.
За каждое правильно написанное уравнение 1балл. за определение процесса 1 балл. Всего 3 балла.
3.1) m(сахара) = m(раствора) x W(сахара) : 100% = (500х 5% ): 100% = 25г
2) m(воды) = m(раствора) — m(сахара) = 500 — 25 = 475г
За каждое правильное действие 1 балл, всего 2 балла
2 Li + 2 H 2 O = 2 LiOH + H 2
В a ( OH )2 – гидроксид бария
LiOH – гидроксид лития
NaOH – гидроксид натрия
За каждое правильно написанное уравнение 1балл, за каждое правильно названное вещество 0,5 балла. Всего 4,5 балла.
Всего за работу – 25,5 баллов
«2» — от 0 — 13 баллов, «3» — от13,5 до 18,5 баллов, «4» -от 19 до 21 баллов, «5» от 21,5 баллов.
Курс повышения квалификации
Дистанционное обучение как современный формат преподавания
- Сейчас обучается 859 человек из 78 регионов
Курс повышения квалификации
Педагогическая деятельность в контексте профессионального стандарта педагога и ФГОС
- Сейчас обучается 49 человек из 21 региона
Курс профессиональной переподготовки
Химия: теория и методика преподавания в образовательной организации
- Сейчас обучается 376 человек из 64 регионов
«Мотивация здорового образа жизни. Организация секций»
Свидетельство и скидка на обучение каждому участнику
- Для всех учеников 1-11 классов
и дошкольников - Интересные задания
по 16 предметам
«Как закрыть гештальт: практики и упражнения»
Свидетельство и скидка на обучение каждому участнику
Видео:Реакции металлов с кислородом и водой. 8 класс.Скачать

Дистанционные курсы для педагогов
Самые массовые международные дистанционные
Школьные Инфоконкурсы 2022
33 конкурса для учеников 1–11 классов и дошкольников от проекта «Инфоурок»
Найдите материал к любому уроку, указав свой предмет (категорию), класс, учебник и тему:
5 842 167 материалов в базе
Материал подходит для УМК
«Химия», Рудзитис Г.Е., Фельдман Ф.Г.
Глава 4. Вода. Растворы
Ищем педагогов в команду «Инфоурок»
Другие материалы
- 04.11.2020
- 368
- 6
- 04.11.2020
- 707
- 17
- 04.11.2020
- 1472
- 177
- 04.11.2020
- 280
- 3
- 04.11.2020
- 112
- 0
- 03.11.2020
- 1352
- 143
- 03.11.2020
- 284
- 6
- 02.11.2020
- 990
- 72
«Учись, играя: эффективное обучение иностранным языкам дошкольников»
Свидетельство и скидка на обучение
каждому участнику
Вам будут интересны эти курсы:
Оставьте свой комментарий
Авторизуйтесь, чтобы задавать вопросы.
Добавить в избранное
- 05.11.2020 2735
- DOCX 23.2 кбайт
- 113 скачиваний
- Оцените материал:
Настоящий материал опубликован пользователем Кузнецова Инна Владимировна. Инфоурок является информационным посредником и предоставляет пользователям возможность размещать на сайте методические материалы. Всю ответственность за опубликованные материалы, содержащиеся в них сведения, а также за соблюдение авторских прав несут пользователи, загрузившие материал на сайт
Если Вы считаете, что материал нарушает авторские права либо по каким-то другим причинам должен быть удален с сайта, Вы можете оставить жалобу на материал.
Автор материала
- На сайте: 6 лет и 4 месяца
- Подписчики: 0
- Всего просмотров: 6252
- Всего материалов: 6
Московский институт профессиональной
переподготовки и повышения
квалификации педагогов
Видео:контрольная работа 8 класс рудзитис параграфы 22-35 кислород водород вода растворыСкачать

Дистанционные курсы
для педагогов
663 курса от 690 рублей
Выбрать курс со скидкой
Выдаём документы
установленного образца!
Учителя о ЕГЭ: секреты успешной подготовки
Время чтения: 11 минут
Минпросвещения проведет Всероссийский конкурс для органов опеки и попечительства
Время чтения: 1 минута
Минпросвещения рекомендует школьникам сдавать телефоны перед входом в школу
Время чтения: 1 минута
С 1 сентября в российских школах будут исполнять гимн России
Время чтения: 1 минута
Минобрнауки отменило плановые и внеплановые проверки вузов в 2022 году
Время чтения: 1 минута
Около 20% детей до 15 лет не воспринимают прочитанную информацию
Время чтения: 1 минута
Российские школьники начнут изучать историю с первого класса
Время чтения: 1 минута
Подарочные сертификаты
Ответственность за разрешение любых спорных моментов, касающихся самих материалов и их содержания, берут на себя пользователи, разместившие материал на сайте. Однако администрация сайта готова оказать всяческую поддержку в решении любых вопросов, связанных с работой и содержанием сайта. Если Вы заметили, что на данном сайте незаконно используются материалы, сообщите об этом администрации сайта через форму обратной связи.
Все материалы, размещенные на сайте, созданы авторами сайта либо размещены пользователями сайта и представлены на сайте исключительно для ознакомления. Авторские права на материалы принадлежат их законным авторам. Частичное или полное копирование материалов сайта без письменного разрешения администрации сайта запрещено! Мнение администрации может не совпадать с точкой зрения авторов.
Видео:Как Решать Задачи по Химии // Задачи с Уравнением Химической Реакции // Подготовка к ЕГЭ по ХимииСкачать

Контрольная работа по теме «Водород. Кислород. Вода. Растворы»
учебно-методический материал по химии (8 класс)
4 варианта контрольной работы с заданиями с развернутым ответом (2 вопроса и задача на массовую долю вещества в растворе)
Видео:Химические уравнения // Как Составлять Уравнения Реакций // Химия 9 классСкачать

Скачать:
| Вложение | Размер |
|---|---|
| kontrolnaya_rabota_vodorod._kislorod._voda.docx | 15.64 КБ |
Видео:Составление уравнений химических реакций. 1 часть. 8 класс.Скачать

Предварительный просмотр:
- Почему водород называют экологичным топливом? Свой ответ обоснуйте уравнением реакции.
- Как получают водород в промышленности? Напишите уравнение реакции. Почему водород в промышленности не получают тем же способом, что и в лаборатории?
- К 500 г раствора с массовой долей вещества 15% прилили 200 г воды. Найдите массовую долю получившегося раствора.
- Как получают кислород в промышленности и в лаборатории? Напишите уравнения реакций.
- Какими способами можно собрать полученный водород? На каких физических свойствах основаны данные методы?
- Рассчитайте массовую долю сахара в чае, который Вы пьете. Масса сахара в одной чайной ложке – 2 г. Кружка вмещает, в среднем, 300 мл воды. Сколько сахара нужно положить в стакан чая (объем стакана – 200 мл), чтобы получить одинаково сладкий чай?
- Напишите реакцию горения природного газа (метан СН 4 ), если известно, что при этом процессе образуются углекислый газ и вода.
- Почему в случае пожара, во избежание отравления угарным газом (формула – СО), рекомендуют лечь на пол и ползком пробираться к выходу?
- К 500 г раствора с массовой долей вещества 15% добавили 40 г соли. Найдите массовую долю получившегося раствора.
- Как получают водород в лаборатории? Напишите уравнение реакции. Почему водород в промышленности получают другим способом?
- Какими способами можно собрать полученный кислород? На каких физических свойствах основаны данные методы?
- К 300 г раствора с массовой долей вещества 20% добавили 30 г соли. Найдите массовую долю получившегося раствора.
Видео:Водород. 8 класс.Скачать

По теме: методические разработки, презентации и конспекты
Контрольная работа по теме «Внутренние воды России»
Контрольная работа состоит из трёх частей в первой части работы проверяется знание терминологии по теме, вторая часть работы тест в форме «закончить предложение», третья часть ответы на вопросы. Кажда.
Разноуровневые варианты контрольных работ по темам: «Кислород. Водород. Вода, растворы, основные классы неорганических соединений»
Дифференцированные задания для работы с учащимися различными способностями.
Контрольная работа по теме «Внутренние воды России»
Контрольная работа составлена в тествой форме. Проверяется уровень знаний терминологии и умений соотнести объекты и работать с контурной картой по данной теме. В работу включены критериями оцени.
Контрольная работа по теме «Кислород. Газообразное состояние веществ»
Контрольная работа по теме «Кислород. Газообразное состояние веществ» (8 класс).
8 класс, Контрольная работа по темам «Кислород», «Водород», «Вода»
Материал для самоподготовки, 8 класс.
Контрольная работа по теме «Кислород. Оксиды. Горение»
Контрольная работа по теме: «Кислород. Оксиды. Горение», 8 класс.
Контрольная работа по теме: «Кислород и сера»
Проверочная работа по теме: «Кислород и сера», выявить затруднения в условии учебного материала и определить пути их преодоления.Тема: «Кислород и сера»»Цель: определить .
🔥 Видео
Химия 8 класс (Урок№11 - Кислород: получение, физические и химические свойства,применение. Оксиды.)Скачать

Как расставлять коэффициенты в уравнении реакции? Химия с нуля 7-8 класс | TutorOnlineСкачать

Химия | КислородСкачать

Химия 8 класс (Урок№14 - Вода в природе и способы её очистки.Физические и химические свойства воды.)Скачать

Контрольная 1 химия 8 класс Вариант 1 стр 4 Повторение основных вопросов курса химии 7 классаСкачать

Как ЛЕГКО понять Химию с нуля — Массовая доля вещества // ХимияСкачать

8 класс. Массовая доля растворенного вещества. Решение задач.Скачать

Типы Химических Реакций — Химия // Урок Химии 8 КлассСкачать

Ошибка! смотри коммент. Контрольная #2 Вариант 2 Химия 8 класс. Классы неорганических соединенийСкачать

Контрольная работа №1 по химии 8 класса | Повторение основных вопросов курса химии 7 классаСкачать

Кислород. 8 класс.Скачать

Химические Цепочки — Решение Цепочек Химических Превращений // Химия 8 классСкачать

Химические уравнения. СЕКРЕТНЫЙ СПОСОБ: Как составлять химические уравнения? Химия 8 классСкачать