Уравнение Марка—Куна—Хаувинка — уравнение, связывающее характеристическую вязкость полимера в растворе и его молекулярную массу.
Уравнение записывается как [ η ] = K η M a <displaystyle [eta ]=K_,M^> ,
где [ η ] — характеристическая вязкость полимерной цепи с молекулярной массой M , a и K — константы, величина которых зависит от природы полимера и растворителя и температуры. Как правило,
Также иногда соотношением Марка—Куна—Хаувинка называется зависимость между коэффициентом поступательного трения f и молекулярной массой полимера:
где K f <displaystyle K_> и b — некоторые константы, зависящие от природы полимера, растворителя и температуры.
Уравнения Марка—Куна—Хаувинка применяются для быстрой оценки молекулярной массы и размера макромолекул. Соотношения справедливы для разбавленных растворов.
История
Соотношение (первое из приведенных в этой статье) получено экспериментально в 1938 году Г. Ф. Марком и независимо от него Р. Хаувинком (Roelof Martinus Frederik Houwink) в 1940. В зарубежной литературе уравнение носит имена Mark-Houwink. Так как Х. Кун и И. Сакурада также внесли вклад, нередко встречается и название Kuhn-Mark-Houwink-Sakurada.
Константы для уравнения марка куна хаувинка
1.3.1. Гидродинамические методы
В соответствии с законом Ньютона сила, необходимая для сдвига двух соседних гипотетических слоев жидкости, отнесенная к единице площади их соприкосновения (так называемое напряжение сдвига τ), пропорциональна скорости сдвига (или градиенту скорости сдвига 
Коэффициент пропорциональности η в этом уравнении называется коэффициентом вязкости (или вязкостью). Жидкости, вязкости которых в изотермических условиях остаются постоянными при любых значениях τ и 
Перечень используемых в лабораторно-технологической практике вискозиметрических терминов приведен в табл. 1.1.
Значения [η] оцениваются экстраполяцией значений приведенной или приведенной логарифмической вязкости к «нулевой» концентрации полимера (рис. 1.8), т.е.
Таблица 1.1. Вискозиметрические характеристики
Величину M v высокомолекулярных соединений определяют обычно по вязкости разбавленных растворов, концентрация которых не превышает 1/[η]. Эту величину называют средневязкостной молекулярной массой.
Для измерения вязкости разбавленных растворов применяют капиллярные вискозиметры. Схема одного из них приведена на рис. 1.9. Исследуемую жидкость заливают в вискозиметр и тщательно термостатируют. Закрыв патрубок 3, раствор из баллона 4 переводят в баллон 1. Для обеспечения постоянства перепада давления в вискозиметре создают «висящий» слой, для чего открывают патрубок 3. Контролируют время истечения жидкости через калиброванный капилляр между метками измерительного баллона 1.
В соответствии с законом Гагена — Пуазейля
где r — радиус капилляра; l — длина капилляра; ΔР — давление, действующее на жидкость; Q — объем жидкости, вытекающей за время t.
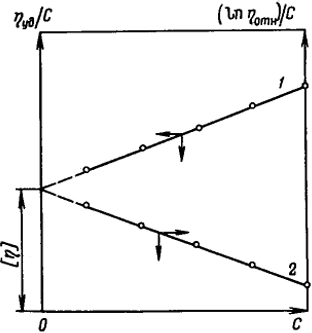
Рис. 1.8. Зависимость приведенной (1) и приведенной логарифмической (2) вязкости от концентрации полимера
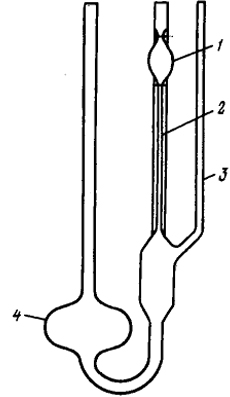
Рис. 1.9. Схема вискозиметра с «висящим» уровнем:
1 — измерительный баллон; 2 — калиброванный капилляр; 3 — патрубок; 4 — приемный баллон
Очевидно, что ΔР = Δhр, где Δh — высота столба жидкости, а ρ — плотность жидкости. Следовательно,
где К‘ = πr 4 Δh/(8 Ql) [K‘ — величина, постоянная для данного вискозиметра].
Так как плотность разбавленного раствора ρ и плотность растворителя ρ0 практически одинаковы, то η = K‘t. Тогда ηотн = t/t0, где t и t0 — время истечения раствора и растворителя.
Вискозиметрическим методом обычно определяется средневязкостная молекулярная масса M v.
Значение [η] связано с величиной молекулярной массы следующей зависимостью (уравнение Марка-Хаувинка-Флори):
где Kη и α — константы, определяемые экспериментально для данной системы полимер-растворитель при выбранной температуре.
Значение α зависит от конформации макромолекул, термодинамического качества растворителя и температуры (см. гл. 2). Оно может изменяться от 0,5 для статистического молекулярного клубка в θ-растворителе до 2,0 для абсолютно жесткой молекулы. Величина Кη имеет размерность дл/г, изменяется обычно в пределах от 10 -2 до 10 -5 и зависит от выбора системы полимер — растворитель, полидисперсности, разветвленности, тактичности полимера, температуры и других факторов. В этом отношении выбор значений Kη и α для вычисления M v условен.
Значения Кη и α для ряда волокнообразующих полимеров приведены в Приложении 6.
Для получения сопоставимых результатов по M v целесообразно для каждого полимера использовать регламентированные условия определения [η] (температура, растворитель) и постоянные значения Кη и α.
Вопрос. Для сополимеров переменного состава, характеризующихся случайным статистическим распределением звеньев вдоль цепи, а также химической неоднородностью фракций (карбоцепные сополимеры, не полностью замещенные эфиры целлюлозы), определение Кη и α не имеет смысла. Объясните причину этого утверждения.
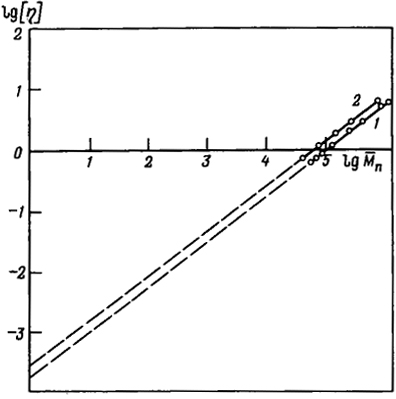
Рис. 1.10. Зависимость lg[η] = f(lg Mn) для полиакрилонитрила в диметилформамиде при 25°С:
1 — фракционированный; 2 — нефракционированный полимер
Ответ. Статистические сополимеры не являются соединениями постоянного химического строения и состава. Поэтому при определении значения M v можно подобрать значения Kη и α лишь для данного препарата в данном растворителе. Другой образец этого сополимера, отличающийся хотя бы особенностями чередования звеньев полимерной цепи, а тем более химическим строением их, характеризуется иными гидродинамическими показателями, другими значениями Кη и α при изотермических условиях.
Вместе с тем при одинаковом составе сополимеров, синтезированных в идентичных условиях, возможна оценка молекулярных масс вискозиметрическим способом на основании значений Kη и α, определенных независимым способом. Например, для волокнообразующего сополимера акрилонитрила (40%), винилхлорида (58%) и n-стиролсульфокислоты (2%) Kη = 1,21·10 и α = 0,82 в ацетоне при 25°С.
Задача. Для вычисления значений Kη и α для полиакрилонитрила, синтезированного полимеризацией в присутствии персульфата калия, полимер был подвергнут фракционированию. Получено 8 фракций, различающихся по величине [η]. Осмометрическим методом при 25°С в диметилформамидных растворах были определены значения М для каждой фракции. В тех же условиях были определены [η] и М n пяти образцов нефракционированного, полиакрилонитрила. Результаты измерений приведены на рис. 1.10. Определить значения Кη и α.
Решение. Логарифмируя уравнение (1.32), получаем
Очевидно, что тангенс угла наклона прямой к оси абсцисс равен α. В данном случае он одинаков для прямых 1 и 2 (рис. 1.10) и составляет
Значения Кη определяют, экстраполируя прямые 1 и 2 до пересечения с осью ординат (lg M v = 0). Для нефракционированного полиакрилонитрила Kη = 2,37·10 -4 , для фракционированного Кη = 17,5·10 -4 .
Задача. Для установления значений Кη и α для растворов поливинилацетата в ацетоне были выделены узкие фракции, определены их молекулярные массы М п (осмометрически) и характеристические вязкости [η]. Оказалось, что для фракции с М п = 22500 [η] = 0,194, а для фракции с М n = 40000 [η] = 0,289. Вычислить значения Kη и α.
Решение. Составляем систему уравнений:
Решая эту систему уравнений, находим Кη и α:
0,289/0,194 = (40000/22500) α ; α = 0,686;
В некоторых случаях значение [η] может быть оценено по результатам определения Луд при одной концентрации. Этот способ является применимым и достаточно точным только для тех систем полимер — растворитель, для которых график ηуд/С от С — прямая, а угол ее наклона — постоянный. Этот способ оценки [η] может быть использован для определения молекулярных характеристик волокнообразующих полимеров, синтезированных в одинаковых условиях. Для таких расчетов используют формулу Соломона-Сьюта:
Задача. Рассчитать средневязкостную молекулярную массу и степень полимеризации полиэтилентерефталата, если относительная вязкость ηотн полимера в о-хлорфеноле при концентрации 0,50 г/100 см 3 равна 1,340.
Решение. В соответствии с формулой (1.33) имеем
[η] = 2(0,34 — ln1,34) 0,5 0,5 -1 = 0,87.
Элементарное звено полиэтилентерефталата
имеет молекулярную массу M0 = 192. Для о-хлорфенола, являющегося растворителем этого полимера, при 25°С значения Кη = 6,56·10 -4 , α = 0,73.
Молекулярная масса, определяемая вискозиметрическим способом и называемая средневязкостной молекулярной массой M v, существенно зависит от наличия в полимере высокомолекулярных фракций:
Средневязкостная молекулярная масса эквивалентна истинной молекулярной массе гипотетической однородной фракции с тем же значением [η], что и у данного полимера.
Для относительно гибких макромолекул, когда 0,5 ≤ α ≤ 1, М п ≤ M v ≤ M w. Для жестких молекул, когда α > 1, M v > М w. Отличия в значениях M v и M w иногда достигают 40%.
Задача. Рассчитать средневязкостную молекулярную массу М v и степень полимеризации Р поливинилового спирта (раствор в воде при 25°С), если известны значения приведенных логарифмических вязкостей растворов:
| С, г/100 см 3 | 0,1 | 0,2 | 0,3 | 0,4 |
| ln ηотн/С | 2,1 | 1,6 | 1,0 | 0,2 |
Решение. Графическая зависимость ln ηотн/С — С для водных растворов поливинилового спирта дает [η] = 2,8. Аналитическое решение этой зависимости позволяет получить уравнение прямой линии: ln ηотн/С = 2,8 — 6,3С (при этом σ 2 = 5,75·10 -3 ). При С → 0 ln ηотн/С = [η] = 2,8. Согласно уравнению (1.32) в соответствии с Приложением 6 имеем
Kη = 5,95·10 -4 ; α = 0,63; М
| α |
| v |
= [η]/Кη;
M
| 0,63 |
| v |
= 2,8/(5,95·10 -4 ); M v = 6,7·10 5 ; М0 = 44; P n = 15350.
Вискозиметрическое определение средней молекулярной массы M v является наиболее удобным способом оценки этой важнейшей характеристики волокнообразующих полимеров и поэтому применяется как в лабораторных исследованиях, так и при оценке характеристик качества полимерного сырья. Значения Kη и α в уравнении Марка-Хаувинка-Флори (1.32) для ряда волокнообразующих полимеров приведены в Приложении 6.
Гидродинамические свойства макромолекул в разбавленных растворах
Метод вискозиметрии один из самых простых в аппаратурном оформлении. В то же время он позволяет получить такие важные характеристики макромолекул, как молекулярная масса, размеры, коэффициент набухания макромолекулярного клубка, степень полидисперсности макромолекул и др.
Вязкость (внутреннее трение жидкости) обусловлена взаимодействием молекул жидкости и проявляется при ее течении. Течение жидкости в капилляре диаметром х, характеризуется градиентом скорости 
Коэффициент пропорциональности h называется коэффициентом вязкости просто вязкостью.
Вязкость можно рассматривать как меру энергии, рассеиваемой в форме теплоты в процессе течения жидкости. Растворы полимеров обладают более высокой вязкостью по сравнению с низкомолекулярными жидкостями. Даже в разбавленном растворе макромолекула, находясь в ламинарном потоке растворителя, разными своими частями оказывается в слоях, движущихся с разными скоростями. В результате этого молекулярный клубок испытывает действие момента сил, который заставляет его вращаться в потоке, что приводит к дополнительной затрате энергии.
Ламинáрный – [

где t и t0 – времена истечения соответственно раствора и чистого растворителя.
Отношение 

Вязкость разбавленного раствора непроницаемых сплошных невзаимодействующих сферических частиц описывается формулой Эйнштейна:
где j – объемная доля растворенного вещества;
2,5 – коэффициент, учитывающий гидродинамическое взаимодействие жесткой сферической частицы со средой.
Эту формулу можно записать в виде

где r2 – плотность растворенного вещества.
Уравнение Эйнштейна означает, что характеристическая вязкость раствора сплошных невзаимодействующих частиц (не обязательно сферических, тогда коэффициент 2,5 будет другим) определяется только плотностью вещества и не зависит от молекулярной массы и размеров частиц. Это происходит вследствие того, что масса таких частиц строго пропорциональна их объему. При этом hпр постоянна в широком интервале концентраций, поскольку частицы предполагаются невзаимодействующими. Уравнению Эйнштейна (в первом приближении) подчиняются разбавленные растворы глобулярных белков разных молекулярных масс. Для всех этих систем [h] »0,04 дл/г независимо от молекулярной массы полимера.
Гибкие линейные макромолекулы в растворе представляют собой рыхлые клубки, в которых лишь 2–5 % объема занято самим полимером, а 95–98 % – растворителем. Тем не менее такие рыхлые клубки, перемещаясь в потоке, вращаются вместе с включенным в них растворителем. Поэтому при рассмотрении процесса течения их можно принять условно непроницаемыми для растворителя.
Допустим для простоты, что макромолекулярный клубок в q-растворителе имеет форму шара радиуса Re (радиус эквивалентной сферы), который примем равным Rg(среднему радиусу инерции). Считая эти частицы непроницаемыми для растворителя в потоке, можно применить к ним уравнение Эйнштейна, причем объемная доля вещества в этом случае учитывает не собственный объем макромолекул, а их эффективный объем в растворе вместе с включенным в них растворителем. Тогда, учитывая, что в q-условиях 

Это формула Флори – Фокса для вязкости полимера в q-растворителе. Здесь Ф – постоянная Флори, в первом приближении не зависящая от свойств полимера. Формула (16) обычно используется для определения невозмущенных размеров макромолекулы 
В условиях, отличных от q-условий, например в хороших растворителях, как уже отмечалось, молекулярный клубок дополнительно набухает. Принимая, что формула Флори – Фокса справедлива также для раствора полимер в хорошем растворителе и подставляя значение (h 2 ) 1/2 из выражения (10) в уравнение (16), получим:
Сопоставляя это уравнение с уравнением (16) и пренебрегая зависимостью Ф от качества растворителя (что, вообще говоря, не вполне справедливо), можно оценить коэффициент набухания макромолекулы:

Большинство полимеров в растворах ведут себя отлично от эйнштейновских частиц (твердые сферические частицы), и для них наблюдается зависимость характеристической вязкости от молекулярной массы полимера. Эта зависимость обусловлена тем, что либо эффективный объем макромолекулярного клубка в растворе растет быстрее, чем его молекулярная масса, либо тем, что клубок имеет несферическую форму и частично проницаем для потока растворителя.
Выражая 

Это уравнение связывает характеристическую вязкость с молекулярной массой полимера в q-условиях.
Для раствора полимера в любом растворителе имеем:

Уравнение (18) носит название уравнения Марка – Куна – Хаувинка. Первоначально оно было получено эмпирически. Уравнение (18) справедливо для большого числа полимерных веществ и является основным уравнением вискозиметрии разбавленных растворов полимеров.
Постоянная K = 10 –2 ¸ 10 –5 зависит от температуры и природы полимера и растворителя. Показатель асвязан с конформацией макромолекулы в растворе и зависит от всех факторов, влияющих на конформацию цепи: для очень компактных частиц типа эйнштейновских а = 0; для гауссовых клубков в q-условиях а = 0,5; для гибких макромолекул в хороших растворителях а = 0,6–0,8; для жестких макромолекул, т. е. протекаемых клубков а = 1,0–1,5; для палочкообразных частиц а = 2,0. Таким образом, в общем случае постоянная а изменяется в пределах: 0 £ а £ 2,0.
Очевидно, что для расчета молекулярной массы полимера по формуле (18) необходимо предварительное определение констант K и а. Поэтому вискозиметрический метод определения молекулярной массы полимера является лишь относительным. Константы K и а находят, представив уравнение Марка – Куна – Хаувинка в логарифмической форме:
lg[h] = lgK + algM (19)
Молекулярные массы серии узких фракций полимера определяют с помощью какого-либо абсолютного метода (осмометрии, светорассеяния и др.). Из прямолинейной зависимости lg[h] от lgM находят K и а.
Зависимость приведенной вязкости от концентрации раствора полимера (рисунок 12) описывается уравнением Хаггинса:
где K¢– константа Хаггинса, характеризующая взаимодействие макромолекул в данном растворителе.
Рисунок 12 – Зависимость приведенной вязкости от концентрации раствора полимера.
В хороших растворителях K¢= 0,2 – 0,3, в плохих – K¢ ³ 0,5.
Характеристическая вязкость определяет поведение изолированных макромолекул. Она представляет собой меру потерь энергии на трение изолированных макромолекул о растворитель при их вращении в результате поступательного движения в потоке с градиентом скорости, отличным от нуля. Характеристическая вязкость зависит от размеров макромолекул в растворе, от природы растворителя и температуры раствора. В хорошем растворителе макромолекулярный клубок набухает и вязкость увеличивается. Для систем с ВКТР повышение температуры приводит к улучшению качества растворителя, вязкость возрастает; в системах с НКТР с повышением температуры качество растворителя ухудшается и вязкость раствора полимера уменьшается.
Характеристическая вязкость может быть использована в качестве критерия перехода от разбавленного к умеренно концентрированному раствору. Значение [h] пропорционально объему макромолекулярного клубка, поэтому раствор можно считать разбавленным, если для него С > 1/[h].
В случае полидисперсного полимера молекулярная масса, определяемая по уравнению (18), является средневязкостной. Учитывая, что вязкость разбавленного раствора является аддитивным свойством и что константы K и а не зависят от молекулярной массы, для вязкости раствора полидисперсного полимера можно написать:
можно заключить, что 

Характеристические вязкости и молекулярные массы для одного и того же полимера, измеренные в двух разных растворителях, для которых константы а уравнения Марка – Куна – Хаувинка различны (например, в хорошем и плохом растворителях), различаются:

Это обусловлено тем, что в хорошем растворителе макромолекулярные клубки находятся в относительно набухшем состоянии и средняя молекулярная масса более чувствительна к присутствию высокомолекулярной фракции, тогда как в плохом растворителе макромолекулы имеют более компактные конформации и вклады макромолекул разной длины различаются в меньшей степени. Отношение 



Справочные данные
Значения констант K и а в уравнении Марка – Хаувинка [h] =KM а














