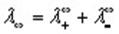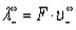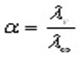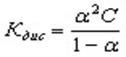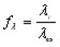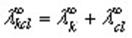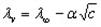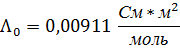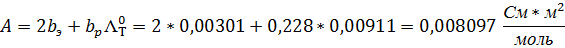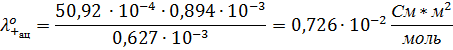Эквивалентная электропроводность при бесконечном разбавлении как для сильных, так и для слабых электролитов может быть вычислена с помощью закона Кольрауша.
Согласно закону Кольрауша эквивалентная электропроводность раствора электролита при бесконечном разбавлении определяется выражением:
где 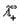
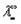
Эквивалентные электропроводности ионов называются также подвижностями. Они равны произведению абсолютной скорости ионов на число Фарадея, т.е.
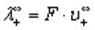
где 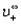
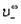
По измеренным сопротивлениям для каждой из концентраций вычисляют удельную электропроводность, эквивалентную электропроводность, а затем вычисляют степень диссоциации по уравнению:
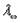
Константу равновесия процесса диссоциации слабого электролита вычисляют по уравнению (закон разбавления Оствальда):
где ? – степень диссоциации,
С – концентрация раствора.
При работе с раствором сильного электролита необходимо вычислить коэффициент электропроводности по уравнению:
Подвижности ионов К’ и Cl’ взять из приложения ( в конце работы).
Для сильных электролитов зависимость эквивалентной электропроводности от концентрации выражается эмпирическим уравнением Кольрауша
где а – постоянная, зависящая от природы электролита, растворителя и температуры.
Видео:Константа нестойкости и диссоциация комплексных соединенийСкачать

ИЗМЕРЕНИЕ УДЕЛЬНОЙ ЭЛЕКТРОПРОВОДНОСТИ РАСТВОРОВ СЛАБЫХ ЭЛЕКТРОЛИТОВ
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Измерения электрической проводимости растворов производят с помощью приборов, называемых кондуктометрами. Методика выполнения измерений описана в инструкции, прилагаемой к используемому прибору.
Любые исследования, основанные на измерении электрической проводимости, объединяются под названием кондуктометрии. Кондуктометрические методы применяются для изучения свойств как сильных, так и слабых электролитов.
РАБОТА № 1
ИЗМЕРЕНИЕ УДЕЛЬНОЙ ЭЛЕКТРОПРОВОДНОСТИ РАСТВОРОВ СИЛЬНЫХ ЭЛЕКТРОЛИТОВ
Цель работы:определение предельной молярной проводимости и коэффициентов проводимости сильных электролитов.
Электролит: CH3COONa
| Молярная концентрация раствора C, моль/м 3 | 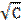 | Удельная проводимость σ* 10 4 ,См/м | Эквивалентная проводимость Λ*10 4 , См*м 2 /моль | Λ0 |  | A |
| 0,196 | ||||||
| 0,01 | 0,1 | 0,5535 | 55,35 | 0,00911 | 0,6076 | 0,0358 |
| 0,1 | 0,3162 | 1,439 | 14,39 | 0,1580 | 0,0243 | |
| 8,059 | 8,059 | 0,0885 | 0,0083 | |||
| 3,1623 | 51,65 | 5,165 | 0,0567 | 0,0027 | ||
| 270,5 | 2,705 | 0,0297 | 0,0009 |
1. Постройте график 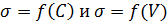
2. Рассчитайте эквивалентную электрическую проводимость каждого раствора:
3. Постройте график 

4. Рассчитайте значение 
5. Сравните Λ0 найденное графически, с теоретическим.
6. Рассчитайте коэффициент проводимости для каждого раствора fΛ=Λ/Λ0
7. Сделайте вывод о влиянии концентрации на взаимодействие между ионами.
В растворах слабых электролитов, чем выше концентрация, тем ниже коэффициент проводимости.
По теории Дебая — Онзагера снижение эквивалентной электрической проводимости при переходе от бесконечно разбавленного раствора к растворам конечных концентраций связано с уменьшением скоростей движения ионов. Это объясняется появлением эффектов торможения движения ионов, возникающих за счет сил электростатического взаимодействия между ионом и его ионной атмосферой.
8. Установите область концентрации, для которой применимо уравнение Кольрауша.
Уравнение Кольрауша, в соответствии с графиком, применимо к области концентраций от 0,01 моль/м 3 до 0,1 моль/м 3
9. Найдите значение предельной электропроводности электролита и коэффициента А по уравнению Кольрауша.
y = -0,0005x + 0,0079

10. Результаты измерений занесите в таблицу.
11. Рассчитайте значение углового коэффициента в уравнении Дебая-Хюккеля-Онзагера, если ε=78,25; η=0,894*10 -3 Па*с;
Уравнение Дебая-Хюккеля-Онзагера (1,1 – электролит)
Подставив значения, получим (q = 1/2, так как электролит симметричен):
12. Сравните значения полученных угловых коэффициентов:
A (графическая) = 0,0005
А (аналитическая) = 0,008097
13. Определите подвижность катиона и аниона, если число переноса аниона дано в таблице.
14. Предельную электрическую подвижность катиона в водном растворе.
15. Скорость движения катиона при градиенте поля 100 В/м.
16. Стоксов радиус иона (для воды η = 0,894 * 
17. Подвижность катиона при бесконечном разведении в ацетоне и нитрометане, вязкости которых при этой температуре соответственно равны 0,310∙ 

Работа №2
ИЗМЕРЕНИЕ УДЕЛЬНОЙ ЭЛЕКТРОПРОВОДНОСТИ РАСТВОРОВ СЛАБЫХ ЭЛЕКТРОЛИТОВ
Цель работы:определение степени диссоциации слабых электролитов при разных концентрациях и константы диссоциации.
Электролит: CH3COOH
| Молярная концентрация раствора C, моль/м 3 | 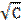 | Удельная проводимость σ*10 4 ,См/м | Эквивалентная проводимость Λ*10 4 , См*м 2 /моль | Степень диссоциации α | Ка |
| 1,61 | 1,6116 | 0,004125 | 1,7086*10 -5 | ||
| 2,2361 | 3,56 | 0,7119 | 0,001822 | 1,6629*10 -5 | |
| 3,1623 | 5,13 | 0,5130 | 0,001313 | 1,7262*10 -5 | |
| 4,4721 | 7,2 | 0,3602 | 0,000922 | 1,7017*10 -5 | |
| 7,0711 | 11,37 | 0,2273 | 0,000582 | 1,6946*10 -5 |
1. Рассчитать эквивалентную проводимость растворов.
2. Построить графики зависимости 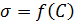

3. Пользуясь величинами предельных подвижностей ионов, по закону независимого движения ионов рассчитайте предельную молярную проводимость электролита.
4. Рассчитайте степень диссоциации слабого электролита в каждом исследуемом растворе.
5. Постройте график зависимости α от концентрации раствора.
6. По закону разбавления Оствальда рассчитайте константу диссоциации для каждого раствора и найдите ее среднее значение.
7. По графикам в координатах 

8. Сравните найденное значение константы диссоциации с табличным значением.
К(найденное) = 2,24*10 -7
К(табличное) = 1,8*10 -5
9. Сделайте вывод о влиянии концентрации раствора на величины α и Ка
У слабых электролитов степень и константа диссоциации понижаются с повышением концентрации раствора.
Видео:Электрическая проводимость растворов электролитов. Кондуктометрия.Скачать

КО́ЛЬРАУША ЗАКО́Н
В книжной версии
Том 14. Москва, 2009, стр. 580
Скопировать библиографическую ссылку:
КО́ЛЬРАУША ЗАКО́Н, закон независимости движения ионов, или закон аддитивности электропроводности электролитов при бесконечном разведении растворов. Закон установлен экспериментально Ф. Кольраушем в 1879. Физич. сущность К. з. состоит в том, что в бесконечно разбавленном растворе электролита перенос электрич. тока осуществляется всеми ионами независимо друг от друга. Вследствие этого общая молярная электропроводность раствора электролита при бесконечном разведении $Lambda^0$ равна сумме предельных электропроводностей отдельных ионов, а разность молярных электропроводностей двух растворов солей с общим катионом не зависит от природы этого катиона, напр.
💡 Видео
Химическое равновесие. Константа равновесия. 10 класс.Скачать

сильные и слабые электролиты РАСЧЕТ рНСкачать

Сильные и слабые электролиты. Константа диссоциации. Водородный показатель.Скачать

Степень электролитической диссоциации. Сильные и слабые электролиты. 9 класс.Скачать

Электропроводность сильных и слабых электролитовСкачать

Электролитическая диссоциация кислот, оснований и солей. 9 класс.Скачать

Урок 194. Уравнение Ван-дер-ВаальсаСкачать

5. Решение волнового уравнения на отрезке методом ФурьеСкачать

Теории кислот, оснований и растворов. Теория Аррениуса-Оствальда. 11 класс.Скачать

Якута А. А. - Механика - Волновое уравнение. Механические волны. Скорость распространения волнСкачать

Диссоциация. Сильные и слабые электролиты. Проводник второго рода. Химия – ПростоСкачать

Свободные электромагнитные колебания. 11 класс.Скачать

СЛОЖИТЕ ДВА КОРНЯСкачать

Коллигативные свойства растворов. Законы РауляСкачать

Лекция 28 Эквивалентная электропроводностьСкачать

Якута А. А. - Механика - Вынужденные колебания. АЧХ. ФЧХСкачать
Уравнение Лагранжа 2-го рода для механизма с одной степенью свободыСкачать

Закон ОствальдаСкачать