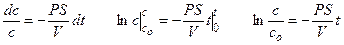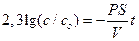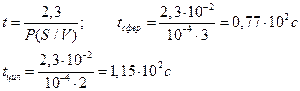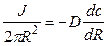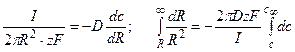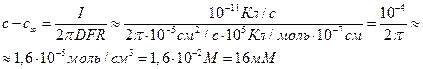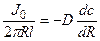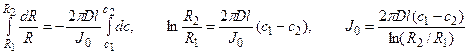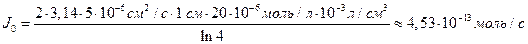Диффузия представляет собой спонтанное движение растворенного вещества в сторону понижения концентрации. Диффузионные законы определяют движение незаряженных веществ в объеме (на любых расстояниях при отсутствии конвекции), перенос ионов в неперемешиваемых слоях у поверхности мембран, а также движение ионов на малых расстояниях.
Формула Стокса–Эйнштейна связывает коэффициент диффузии D с температурой T, вязкостью среды η и радиусом диффундирующих частиц r (k – константа Больцмана). Например, вязкость воды при 20°С составляет ηH2O= 10 –3 Па∙с (1 Па = 1 Н/м 2 ).
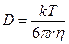
Пользуясь (4.1), можно оценить коэффициент диффузии в воде для малых молекул с радиусом
0,2 нм (10 –5 см 2 /с) или для молекул другого размера. На движение ионов в растворе влияет электрическое поле. Коэффициент диффузии иона зависит от его заряда (z):
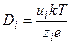
где u – подвижность иона, имеющая размерность м 2 ·с –1 ·В –1 (см 2 ·с –1 ·В –1 ), е – заряд электрона. Например, подвижности ионов K + и Na + равны 7,6·10 –4 и 5,2·10 –4 см 2 ·с –1 ·В –1 , соответственно. Из (4.1) и (4.2) получаем уравнение для расчета подвижности иона по его радиусу и заряду.
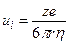
Подвижность численно равна скорости движения ионов (см/с) при напряженности поля 1 В/см.
Законы Фика описывают скорость диффузии вещества, а также пространственное распределение концентрации диффундирующего вещества в различные моменты времени.
Первый закон Фика связывает поток вещества J с коэффициентом диффузии D и градиентом концентрации (dc/dx). Размерность потока – моль∙см –2 ∙с –1 ).
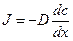
В случае диффузии через тонкую мембрану
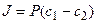
где P=Dg/h – проницаемость, h – толщина мембраны, g – коэффициент распределения вещества между водной и липидной фазами, а 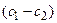
Второй закон Фика описывает направление изменений концентрации вещества во времени (dc/dt) в зависимости от знака второй производной (d 2 c/dx 2 ), определяющей вогнутость или выпуклость профиля концентрации по координате x:
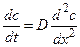
Из (4.6) в частности следует, что в случае одномерной стационарной диффузии (т.е. при dc/dt=0) профиль концентрации линеен: 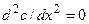
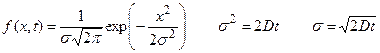
где x – координата, f(x,t) – функция распределения, σ – среднеквадратичное отклонение для нормального распределения вещества относительно исходной точки при x = 0, σ 2 – дисперсия, а t – время. Область, расположенная между координатами ±σ, содержит более 68% от общего количества диффундирующего вещества. Согласно уравнению Эйнштейна, величина σ, обозначаемая также 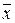
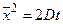
где 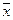
Пример 4.1. После инъекции в клетку некоторого вещества до концентрации co, клетку отмывают средой, не содержащей этого вещества. Какое время инкубации необходимо, чтобы внутренняя концентрация вещества понизилась в 10 раз, если проницаемость мембраны для этого вещества составляет 10 –4 см/с? Решить задачу для клетки сферической формы с диаметром 200 мкм и для цилиндрической клетки с диаметром 200 мкм и длиной 1 см.
Решение: При записи первого закона Фика учтем, что диффузия происходит через тонкую мембрану и, что концентрация во внешнем растворе равна нулю.
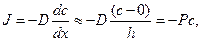
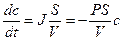
Решение этого дифференциального уравнения описывает кинетику изменения концентрации вещества внутри клетки:
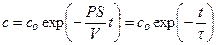
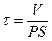
Уравнение решают методом разделения переменных и интегрирования по времени от нуля до t при соответствующем изменении концентрации от co до c.
Для ответа на вопрос задачи удобно перейти к десятичным логарифмам:
Отношение S/V определяется геометрией клетки. Для сферы и цилиндра оно составляет соответственно

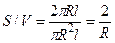
С учетом условия задачи c/co = 0,1 и R = 0,01 см, находим искомое время t:
Аналогичный подход используется для случаев, когда в момент времени t = 0 в наружный раствор добавляют проникающее вещество, которое начинает поступать внутрь клетки, причем наружная концентрация остается постоянной (co = const) из-за большого объема среды по сравнению с объемом клеток. В таком опыте моменту времени t = 0 соответствует внутренняя концентрация с = 0, а произвольному моменту времени t соответствует внутренняя концентрация с. В этом случае интегрирование дифференциального уравнения приводит к следующему решению:
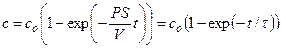
Пример 4.2. Предположим, что через калиевый канал с устьем R = 10 Å протекает ток I силой 10 пА (рис. 4.1.). При этом концентрация К + в устье повышается по сравнению с объемом раствора. Найти концентрацию в области устья канала, если концентрация К + в объеме составляет 10 мМ. При расчете принять, что коэффициент диффузии К + в воде
Решение: На выходе из канала суммарный поток переносимых ионов диффундирует во всех направлениях, ограничиваемых полусферой. Выделим элемент поверхности полусферы и запишем поток через единицу поверхности, пользуясь первым законом Фика.
Суммарный поток вещества J связан с электрическим током I соотношением 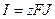
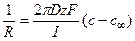
Следовательно, перепад концентрацией между устьем канала и объемом раствора составит
Соответственно, концентрация в устье канала cx составит 26 мМ.
Пример 4.3. Концентрация Са 2+ в питательном растворе на расстоянии 300 мкм от поверхности корня составляет 100 мкМ, а у поверхности корня с диаметром 200 мкм – 80 мкМ. Оценить диффузионный поток Са 2+ к поверхности корня на 1 см его длины (моль·с –1 ), а также поток Са 2+ на единицу поверхности корня (моль·см –2 ·с –1 ) в предположении, что коэффициент диффузии D = 5·10 –6 см 2 /с.
Решение: Обозначим суммарный диффузионный поток для сегмента корня длиной l символом J0. Поток Са 2+ направлен радиально из объема среды к центру корня. Поток через единичный участок цилиндрической поверхности неперемешиваемого слоя на расстоянии R от центра корня составит J0/(2πRl). Запишем уравнение первого закона Фика в радиальных координатах:
Решая уравнение, находим формулу для расчета потока по концентрациям на разном удалении от центра корня (концентрации с1 и с2 для радиальных расстояний R1 и R2).
В расчете на единицу поверхности корня поток составит
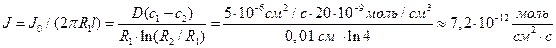
Пассивный транспорт (диффузия)
Поскольку при данном виде транспорта энергия транспортируемого вещества уменьшается, то его перенос идёт только в одном направлении по концентрационному или электрохимическому градиенту. В соответствии с законом Фика диффузия прямо пропорциональная градиенту концентрации вещества, площади диффузионной мембраны, коэффициенту распределения и обратно пропорциональной толщине мембраны.
Основная количественная характеристика, используемая при описании переноса ионов или незаряженных частиц (неэлектролитов) через мембраны- это поток.
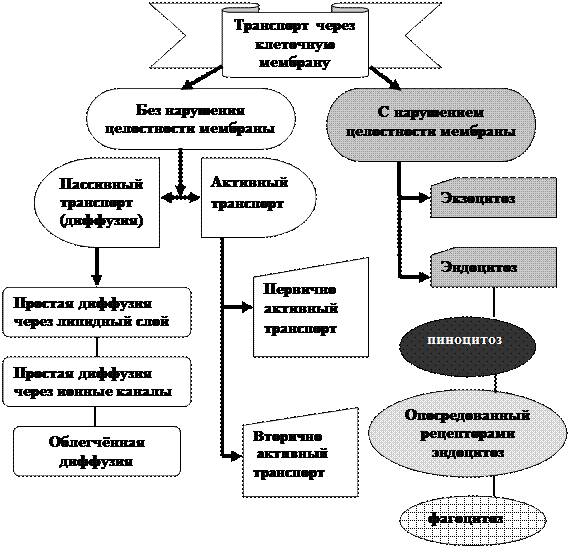 |
Рис.3.15. Виды транспорта веществ через клеточную мембрану
Поток вещества Ф измеряют не в числе частиц, а в числе молей данного вещества . Трансмембранные потоки ионов имеют направление нормальное к поверхности мембраны. Плотность потока (J, моль/с▪м 2 ) – это количество вещества, переносимого в секунду через единицу площади, расположенной нормально потока ( к поверхности мембраны). Положительным считается направление потока из замкнутого пространства наружу. Поэтому поток из клетки в окружающую среду имеет знак «+», а поток в клетку имеет знак «-» . Величина J зависит от концентрации переносимых веществ по обе стороны мембраны (С1 и С2) , а в случае ионов – так же от разности потенциалов между водными фазами, омывающими мембрану φ1 и φ2: ∆φ= φ2: — φ21. В конечном счёте обе характеристики (потенциал и концентрация) влияют на поток потому, что от них зависит энергия ионов (молекул) в данном растворе. Энергия моля ионов данного вида в среде носит название электрохимического потенциала иона и равна: μ=μ о + RTlnC+zFφ, где μ о – стандартный химический потенциал, определяемый энергией взаимодействия иона с молекулой среды;R- газовая постоянная; Т- абсолютная температура; С- молярная концентрация, z- безразмерный заряд иона, F- число Фарадея; φ – потенциал в данной области среды.
|
Простая диффузия через липидный слой (рис. 3.6.) обеспечивает трансмембранный перенос веществ, которые имеют достаточно высокий коэффициент распределения между водной и липидными фазами. К таким веществам относятся: жирорастворимые вещества и незаряженные полярные молекулы (ряд гормонов, алкоголь, мочевина, О2, СО2 и др.). Большое значение для растворения в липидном слое и перенос через него молекул и ионов играет
 |
Проницаемость клеточной мембраны для многих веществ ограничена не только липидным бислоем, но и прилегающими к мембране неперемешивающимися слоями воды, которые вместе с клеточной мембраной в совокупности ведут себя как последовательно соединённые электрические соединения. В свою очередь движение жидкости в клетке и вне её зависит от тканевого метаболизма. Если жидкость внутри клетки и в межклеточной среде интенсивно движется, то толщина примембранного слоя воды может превышать толщину самой клеточной мембраны в 100-300 раз. В то же время вязкость клеточной мембраны (благодаря липидам) в 10-100 раз выше вязкости воды. Следовательно, коэффициенты диффузии иона в воде и мембране относятся друг к другу как 30-100 к единице. Отсюда следует, что в коэффициенте распределения вещества в системе мембрана/вода решающую роль играет липофильность молекулы (иона). Если для К + , Na + , Cа 2+ примембранные слои воды практически не влияют на общую проницаемость: основная барьерная функция принадлежит липидному бислою мембраны, то для нейтральных молекул (например кислорода) роль примембранных слоёв воды для его трансмембранного проникновения в клетку становится заметной.
Простая диффузия через ионные каналы мембраны(рис. 3.17.) даёт возможность проходить через клеточную мембрану веществам, обладающим низким коэффициентом распределения между липидной и водной фазами, следовательно, не растворяющихся в липидах. Например, вода, которая проходит сквозь мембрану клетки, благодаря наличию в ней специальных каналов (аквапоринов), расположенные в бислое липидов. При этом вода переходит из менее концентрированного раствора в более концентрированный. Через ионные каналы могут диффундировать малые незаряженные молекулы, в том числе, и способные одновременно проходить через липидный бислой (этанол, мочевина, О2, СО2 и др). Следует отметить избирательность ионных каналов для незаряженных катионов и анионов.
Ионные каналы клеточной мембраныпредставлены интегральными белками, которые образуют поры в липидном бислое клеточной мембран.
 |
Селективность (избирательность) канала определяется диаметром поры и энергией дегидратации иона. Диаметр поры несколько больше диаметра иона в кристаллическом состоянии. Малые размеры поры делают необходимым снятие с проходящего через мембрану иона его «водной шубы», т.е. осуществлять его временную дегидратацию.
Проницаемость канала регулируется а) изменением мембранного потенциала (потенциалуправляемые каналы); б) влиянием биологически активного вещества (гормоны, медиаторы, Са 2+ ) на канальный белок (рецепторуправляемые каналы).
Для ионного канала характерны три физиологических состояния: покой (потенциальной активен), открыт ( активирован) и закрыт (инактивирован).
|
Облегчённая диффузия (рис. 3.18.) характерна для большинства полярных молекул (сахара, аминокислоты, нуклеотиды и т.д.), для которых липидный бислой мембраны плохо проницаем. Поэтому в процессе эволюции сформировался особый транспорт таких веществ через клеточную мембрану, осуществляемый с участием специфических мембранных белков переносчиков, которые и помогают (облегчают проникновение) этим веществам прохождение через мембрану клетки. Облегчённую диффузию отличает от простой следующие особенности:
 |
3. Наличие специфических стимуляторов и ингибиторов облегчённой диффузии. Например, инсулин активирует облегчённую диффузию глюкозы в жировые и мышечные клетки.
Активный транспорт
Данный вид переноса вещества через клеточную мембрану сопряжён с затратой энергии, благодаря чему он даёт возможность переносить вещества против градиента их концентрации, т.е. из зоны меньшей в зону большей концентрации. В качестве источника энергии в клетки используются : энергия связей аденозинтрифосфорной кислоты (АТФ) и энергия трансмембранных ионных градиентов. В зависимости от вида используемой энергии различают два вида активного транспорта: первично активный транспорт (используется энергия АТФ) и вторично активный транспорт(используется энергия электрохимического градиента Na + ).
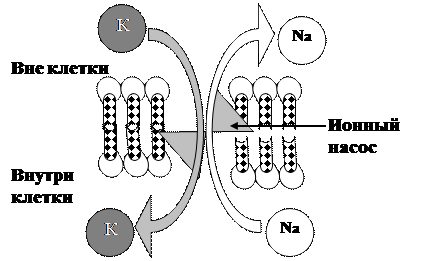
Первично активный транспортосуществляется в результате деятельности ионных насосов, белковый комплекс которых обладает свойствами переносчика (для транспортируемого вещества) и фермента, расщепляющего АТФ, энергия которого используется насосом для транспорта (рис.3.19.).
Рис.3.19. Схема первично активного транспорта через клеточную мембрану
В настоящее время в клетке обнаружены следующие насосы, использующие энергию АТФ: Na + ,К + -насос (Na + ,К + -АТФаза) имеется в плазматической мембране всех клеток организма человека. Энергия АТФ затрачивается на удаление из клетки Na + и возвращения туда К + , проникших путём простой диффузии. Са 2+ -насос (Са 2+ -АТФаза)как в плазматической мембране, так и мембранах клеточных органелл (например, цистерны в миоцитах). Насос откачивает кальций из цитозоля клетки либо во внеклеточную среду, либо в его внутриклеточные депо. Наличие данного насоса обусловлено той важной ролью, которую играет кальций в жизнедеятельности клеток. Протонный насос (Н + -АТФаза)имеется как в плазматической мембране, так и мембранах некоторых клеточных органелл.
Вторично активный транспорт(рис.3.20.) использует энергию градиента концентрации Na + созданного К + ,Na + -насосом. Ионы натрия и транспортируемые вещества связываются с молекулой белка переносчика мембраны. Натрий, перемещением внутрь клетки по электрохимическому градиенту «тащит» за собой вещества (например моносахара и аминокислоты), которые могут переносится против градиента концентрации. Внутриклеточный натрий откачивается Na + ,К + — насосом, благодаря чему восстанавливается электрохимический градиент натрия и цикл повторяется снова.
 | |
 |  |
 |




|
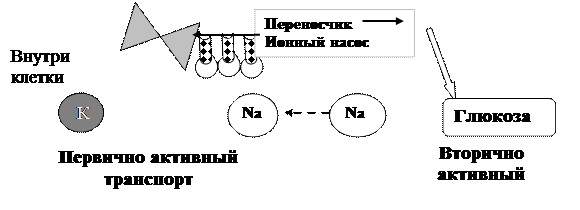 |
Рис. 3.20. Схема вторично активного транспорта через клеточную мембрану
Эндоцитоз и экзоцитоз
Данные виды трансмембранного переноса веществ в клетку и из неё сформировались в процессе эволюции и предназначены для крупномолекулярных веществ не способных перемещаться через клеточную мембрану разобранными выше способами.
Эндоцитоззаключается в поступлении вещества из внеклеточной среды в клетку в составе мелких или крупных пузырьков, образовавшихся из участков плазматической мембраны, в которых и заключено транспортируемое вещество. Эти пузырьки либо сливаются в клетках с органеллами (лизосомами), где происходит переваривание поступивших путём эндоцитоза веществ, либо они транспортируются на противоположный полюс клетки и выделяют воё содержимое во внеклеточную среду путём экзоцитоза.
Различают три вида эндоцитоза:
1. пиноцитоз (неспецифических захват внеклеточной жидкости и растворённых в ней веществ)
2. опосредованный рецепторами эндоцитоз (связывание веществ со специфическими рецепторами на клеточной мембране с образованием окаймлённых пузырьков ( эндосом).
3. фагоцитоз(захват крупных частиц «профессиональными клетками» фагоцитами- нейтрофилы, моноциты, макрофаги)
Экзоцитоз –процесс выделения клеткой веществ во неклеточную среду. Он существует во всех клетках, но особенно он важен для нервных клеток (выделение медиаторов), клеток эндокринной системы (выделение гормонов) и клеток желёз внешней секреции (выделение пищеварительных соков). Выделение вещества из клетки происходит в составе экзоцитозных пузырьков, образующихся в специальной клеточной органелле (аппарат Гольджи). Пузырьки транспортируются с помощью микрофиламентов и микротрубочек к клеточной мембране, сливаются с ней, а их содержимое выделяется во внеклеточную среду.
Жизненный путь клетки
Клеточный цикл неполовых клеток состоит из интерфазы и митоза. Интерфаза включает в себя последовательно протекающие периоды G1, (G0)S, и G2. Период G1 следует за митозом. Длительность от нескольких часов до суток. После периода G1 наступает либо период G0, либо S. В период G0 клетка может выйти из цикла и либо: 1. Быть длительно неактивной (например, клетки иммунной памяти); 2.Функционировать как обычная дифференцированная клетка (например, гепатоцит) в обычных условиях; 3) Достигать необратимой дифференцировки (например, нейроны и кардиомиоциты). Если клетка переходит из периода G1 в период S (синтетический период), то через 8-12 часов переходит в премитотический период G2. который длится 2-4 часа и затем переходит в митоз. Митоз состоит из следующих фаз: профаза, метафаза, анафаза и телофаза. В ходе митоза из материнской клетки образуются две дочерние клетки, идентичные материнской.
Физиологическая гибель клетки (апопотоз) -это активный, генетически запрограммированный процесс. Пусковыми факторами апоптоза являются: нарушение рецепторного аппарата клетки, активные формы кислорода, этанол, низкокалорийную диету и т.д.. Существуют два пути его активации.
Первый путь реализуется через активацию специального гена, который запускает апоптоз путём остановки клеточного цикла и торможения ферментов, отвечающих за репарацию повреждённого участка ДНК. При этом актируются гены, кодирующие синтез белков-стимуляторов апопотоза, которые активируют ферменты, повреждающие структуры клетку и приводящие тем самым её к гибели. В клетке существуют и «гены-спасатели», кодирующие белки, тормозящие апоптоз.
Второй путь реализации апоптоза заключается в появлении на мембране стареющих клеток специального белка, к которому вырабатываются антитела, адсорбирующиеся на мембранах клеток с образованием комплекса белок-апоптоза + антитело. При его контакте с фагоцитом стареющая клетка, несущая данный комплекс, прикрепляется к мембране фагоцитирующей клетки и поглощается ею. Данный процесс получил название аутофагоцитоза.
Физиологическое значение апоптоза:
1) регуляция развития тканей и органов в период внутриутробного развития;
2) инволюция зрелых органов и тканей,
3)регуляция популяции клеток: уничтожения старых и генетически изменённых клеток в зрелых тканях.
Уменьшение способности к апоптозу ниже физиологического уровня –путь к аутоиммунным заболеваниям и злокачественному перерождению клеток.
Транспорт неэлектролитов через клеточные мембраны. Простая диффузия. Уравнение Фика. Облегченная диффузия: механизмы, транспорта (подвижные, фиксированные переносчики), отличия от простой диффузии
Живые системы на всех уровнях организации — открытые системы, поэтому транспорт веществ через биологические мембраны — необходимое условие жизни. Большое значение для описания транспорта веществ имеет понятие электрохимического потенциала.
Химическим потенциалом данного вещества называется величина, численно равная энергии Гиббса, приходящаяся на 1 моль этого в-ва.
Математически химический потенциал определяется как частная производная от энергии Гиббса G по количеству k-го вещества, при постоянстве температуры Т, давления Р и количеств всех других веществ m1:
м (мю) = (dG/dmk)Р,Т,m1
Для разбавленного раствора:
м = м0 +RTlnC, где м0 — стандартный химический потенциал, численно равный химическому потенциалу данного вещества при его концентрации 1 моль/л в растворе.
Электрохимический потенциал — величина, численно равная энергии Гиббса G на 1 моль данного вещества, помещенного в электрическое поле.
Для разбавленных растворов
м (мю с черточкой) = м0 + RTlnC + zFф(фи), где F = 96500 Кл/моль — число Фарадея, z — заряд иона электролита.
Транспорт веществ через биологические мембраны можно разделить на 2 основных типа: пассивный и активный.
Пассивный транспорт — это перенос вещества из мест с большим значением электрохимического потенциала к местам с его меньшим значением. Пассивный транспорт идет с уменьшением энергии Гиббса, и поэтому данный процесс может идти самопроизвольно без затраты энергии.
Диффузия — самопроизвольное перемещение вещества из мест с большей концентрацией в места с меньшей концентрацией вещества вследствие хаотического теплового движения молекул. Диффузия вещества через липидный бислой вызывается градиентом концентрации в мембране. Плотность потока вещества по закону Фика:
Jm = -DdC/dx = -D(Cm2 — Cm1)/1 = D(Cm1 — Cm2)/1,
где Cm — концентрация вещества в мембране около каждой поверхности, 1 — толщина мембраны.
В биологических мембранах был обнаружен еще один вид диффузии — облегченная диффузия. Облегченная диффузия происходит при участии молекул-переносчиков. Облегченная диффузия происходит от мест с большей концентрацией переносимого вещества к местам меньшей концентрацией. По-видимому, облегченной диффузией объясняется также перенос через биологические мембраны аминокислот, сахаров и других биологически важных веществ.
Отличия облегченной диффузии от простой:
перенос вещества с участием переносчика происходит значительно быстрее;
облегченная диффузия обладает свойством насыщения: при увеличении концентрации с одной стороны мембраны плотность потока вещества возрастает лишь до некоторого предела, когда все молекулы переносчика уже заняты;
при облегченной диффузии наблюдается конкуренция переносимых веществ в тех случаях, когда переносчиком переносятся разные вещества; при этом одни вещества переносятся лучше, чем другие, и добавление одних веществ затрудняет транспорт других;
есть вещества, блокирующие облегченную диффузию — они образуют прочный комплекс с молекулами переносчика.
Разновидностью облегченной диффузии является транспорт с помощью неподвижных молекул-переносчиков, фиксированных определенным образом поперек мембраны. При этом молекула переносимого вещества передается от одной молекулы переносчика к другой, как по эстафете.