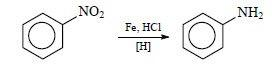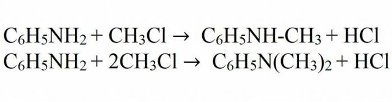1. Вещество CH 3 -NH-CH(CH 3 ) 2 относится к ряду …
Ответ 1 : амидов
Ответ 2 : ароматических аминов
Ответ 3 : алифатических аминов
Ответ 4 : нитросоединений
2. Вещество, формула которого имеет вид C 6 H 5 -N(CH 3 ) 2 , называется …
Ответ 1 : анилин
Ответ 2 : диметилфениламин
Ответ 3 : диметилфенол
Ответ 4 : диметилнитробензол
3. Какую реакцию на индикатор показывают амины жирного ряда?
Ответ 1 : кислотную
Ответ 2 : нейтральную
Ответ 3 : щелочную
Ответ 4 : не действуют на индикатор
4. Характерной химической реакцией аминов, обусловленной наличием в их молекулах аминогруппы, является …
Ответ 1 : радикальное замещение
Ответ 2 : взаимодействие с кислотами с образованием солей
Ответ 3 : электрофильное присоединение
Ответ 4 : нуклеофильное присоединение
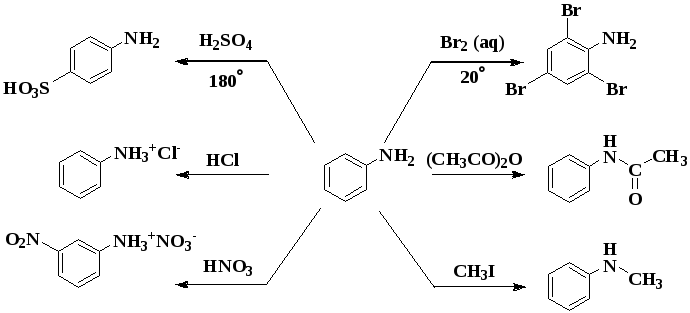
5. Какие реакции характерны для анилина?
- а) C 6 H 5 NH 2 + Br 2
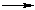
б) C 6 H 5 NH 2 + NaOH
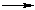
в) C 6 H 5 NH 2 + HCl
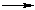
г) C 6 H 5 NH 2 + C 6 H 6
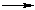
Ответ 1 : в
Ответ 2 : а, в
Ответ 3 : б, г
Ответ 4 : г
6. В приведенной схеме превращений соединением, относящимся к классу аминов,

Ответ 2 : Б
Ответ 3 : В
Ответ 4 : Г
7. Определите массу хлорида фениламмония, если к анилину массой 13,95 г добавили хлороводород, выделившийся на первой стадии хлорирования метана объемом Калькулятор
- Предмет: химия. Класс: 10. Тема: Азотсодержащие органические соединения и их природные источники
- Анилин. Свойства анилина.
- Строение анилина.
- Физические свойства анилина.
- Получение анилина.
- Химические свойства анилина.
- Применение анилина.
- Анилин — структурная формула и свойства органического соединения
- Анилин (фениламин) — понятие, строение, физические свойства
- Получение анилина
- Химические свойства анилина
- Применение анилина
Предмет: химия. Класс: 10. Тема: Азотсодержащие органические соединения и их природные источники
Тема: Азотсодержащие органические соединения и их природные источники
Форма контроля: тест.
Количество учащихся в классе –
1. Пояснительная записка.
Основой разработки КИМа является Федеральный компонент государственного стандарта основного общего образования и программа курса химии для 8-11 классов общеобразовательных учреждений .
Цель контроля: выявить уровень образовательных результатов учащихся по разделу «Азотсодержащие органические соединения и их природные источники»
— понятия: амины, денатурация, функциональная группа, поликонденсация
— классификация и номенклатура органических веществ
— особенности строения молекул и химических свойств веществ
— применение веществ в народном хозяйстве
— давать определения понятиям
— узнавать формулы аминов
— устанавливать соответствие веществами и их свойствами
— объяснять основные свойства аминов
— определять качественные реакции на вещества
— составлять уравнения реакций, расставлять в них коэффициенты
— осуществлять расчеты по химическому уравнению
— вычислять массовую долю вещества и концентрацию раствора
Краткая характеристика КИМа:
— Форма контроля: тест. Структура теста аналогична структуре тестов в форме ГИА и ЕГЭ, что позволит постепенно подготовить учащихся к работе с подобным материалом.
— Количество вариантов: 1
Характеристика заданий, с помощью которых выявляются предметные результаты:
— понятия – А1, А4, В3, С1
— особенности химических свойств веществ: А1, А3, А5, А6, А10, С2, С3
— классификация и номенклатура веществ: А2, В3
— роль веществ в организме человека: А9, В1
— качественные реакции: А8
— строение молекул веществ: В3, В2,
— применение веществ в народном хозяйстве: А7
— типы реакций и их признаки: А4, А8
Инструкция по выполнению работы для учащихся.
На выполнение контрольного тестирования по химии отводится 40 минут. Работа состоит из 16 заданий, которые разделены на задания:
Тестовые задания с выбором одного правильного ответа. Букву правильного ответа обведи кружком.
Тестовые задания на соотнесение и с множественным выбором. Буквы правильных ответов обведи кружком или установи соответствие (соедини линиями) предлагаемые категории.
Задания с развёрнутым ответом. Впиши ответ после задания.
Внимательно прочитай каждое задание и предлагаемые варианты ответа. Отвечай только после того, как ты понял вопрос и проанализировал все варианты ответа.
Выполняй задания в том порядке, в котором они даны. Если какое-то задание вызывает у тебя затруднение, пропусти его и постарайся выполнить, в ответах, на которые ты уверен. К пропущенным заданиям ты можешь вернуться, если у тебя останется время.
За выполнение различных по сложности заданий даётся от одного до 6 баллов. Баллы, полученные тобой за выполненные задания, суммируются. Постарайся выполнить как можно больше заданий и набрать наибольшее количество баллов. Ответы записывай чётко и разборчиво. Удачи!
Содержание контрольного тестирования
Задания с развёрнутым ответом. Впиши ответ после задания.
С1. (2б) Как называется необратимое разрушение белка под действием кислот, спиртов,
солей тяжёлых металлов, при нагревании? Запиши название процесса в именительном
С2. (6б) Составь уравнения реакций по приведенной ниже схеме:
С2Н2 → С6Н6 → С6Н5NO2 → С6Н5NH2
Дай названия продуктам реакции (органическим веществам).
Названия продуктов реакций
С3. (6б) Вычисли массу бромной воды с массовой долей брома 2%, которая потребуется
для полного взаимодействия со 186 г 1%-го раствора анилина.
Дано по уравнению реакции
Итого: 34 балла
31-34 баллов — «5»
24-30 баллов — «4»
15-23 баллов — «3»
0-14 баллов — «2»
Контрольная работа №3
Азотсодержащие органические вещества
и их природные источники
Баллов ___________ Оценка ____
Тестовые задания с выбором одного правильного ответа.
Обведи кружком букву одного правильного ответа:
А1. (1б) Амины — это органические производные:
А6. (1б) Нуклеотид аденин в ДНК комплементарен нуклеотиду:
А) гуанину
Б) тимину
В) цитозину
Г) гуанину
А7. (1б) Анилин не используется для получения:
А) лекарств
Б) красителей
Г) пищевых добавок
А3. (1б) Аминокислоты могут иметь свойства:
А) только основные
Б) только кислотные
В) и основные, и кислотные
Г) не имеют ни основных, ни кислотных свойств
А8. (1б) Признак реакции взаимодействия
анилина с бромной водой:
A) выделение газа
Б) выделение тепла и света
B) образование осадка
Г) обесцвечивание окраски
А4. (1б) Тип химической реакции, к которому относится взаимодействие аминокислот друг с другом
А) полимеризация
Б) поликонденсация
В) дегидрирование
Г) этерификация
А9. (1б) Основная функция ДНК:
А) перенос аминокислот
Б) хранение наследственной информации
В) структурная
Г) синтез белка
А5. (1б) Для аминов характерны свойства:
А) кислот
Б) оснований
В) амфотерных соединений
Г) солей
А10. (1б) Какая из данных схем уравнений реакций не характерна для анилина?
Б) С6Н5NН2 + C2H5OH →
Тестовые задания на соотнесение и с множественным выбором.
В1. (4б) Установи соответствие (соедини линиями) между структурой молекулы белка и её характеристикой:
1) выделяют энергию для жизни
2) строит тела всех живых организмов
3) входят в состав белков-антител уничтожающих чужеродные
4) участники многих химических реакций в организме
В2. (4б) Установи истинность или ложность утверждений: Обведи кружком Да или Нет
А) Да/Нет. Нуклеиновые кислоты состоят из аминокислот.
Б) Да/Нет. Белки состоят из нуклеотидов.
В) Да/Нет. При денатурации белка сохраняется первичная структура белка.
Г) Да/Нет. Ферменты состоят из белков.
В3. (2б) Функциональные группы, обязательно входящие в состав аминокислоты:
Обведи кружками буквы нескольких правильных ответов:
Химическая связь, образующая первичную структуру белка:
Ответы по выполнению контрольного тестирования
За верное выполнение каждого задания 1 балл.
Анилин. Свойства анилина.
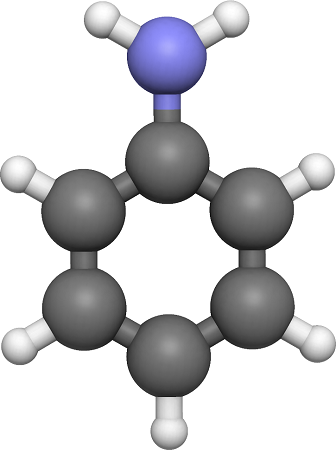
Анилин (фениламин) C5H5NH2 – представитель класса ароматических аминов, в которых аминогруппа связана напрямую с бензольным кольцом.
Строение анилина.
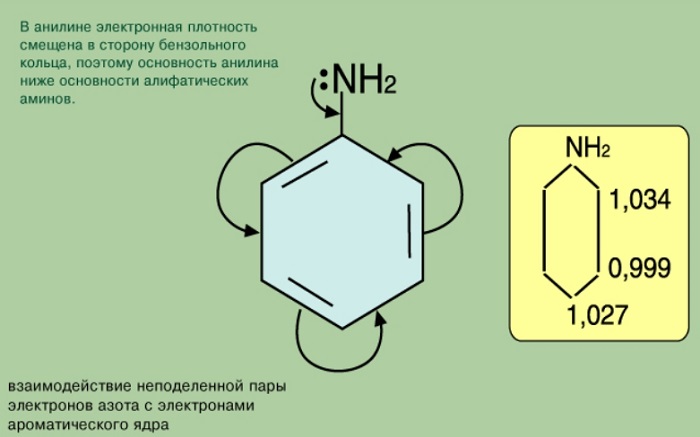
Неподеленная пара атома азота реагирует с π-системой бензольного кольца. Взаимодействие можно представить так:
На атоме азота появляется частично положительный заряд, и основные свойства понижаются. А в бензольном кольце, наоборот, электронная плототность повышается, и наиболее сильно в орто- и пара- положениях:
Физические свойства анилина.
Анилин – бесцветная маслянистая жидкость, немного тяжелее воды, мало растворимы в воде, но хорошо – в этиловом спирте и в бензоле.
Получение анилина.
1. Основным способом получения анилина является процесс восстановления нитробензола. Для этого используют никелевый или медный катализатор при 250-350 °С:
В лаборатории используют восстановления цинка в кислой среде или алюминия в щелочной:
Химические свойства анилина.
Анилин является более слабым основанием, чем алифатические амины, т.к. электронная пара азота частично смещена в бензольное кольцо.
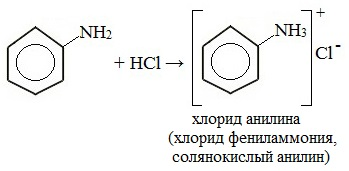
Анилин вступает в реакцию с сильными кислотами, образуя соли фениламмония, которые растворимы в воде, но нерастворимы в неполярных органических растворителях:
2. Анилин вступает в реакции электрофильного замещения в безольном кольце. Аминогруппа направляет замещение в орто- и пара- положения. Анилин легко бромируется, при этом выпадает белый осадок:
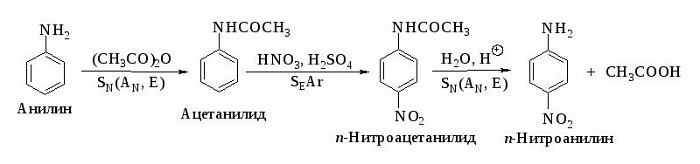
3. С концентрированной азотной кислотой анилин взаимодействует со взрывом. На время реакции можно защитить аминогруппу (превратить ее в амидную перед нитрованием), а после нитрования гидролизовать амид с образованием исходной аминогруппы:
3. При взаимодействии с азотистой кислотой образуются соли диазония:
4. Анилин легко подвергается окислению, темнее при хранении. Если на анилин действовать хлорной известью, то водный раствор анилин окрашивается в интенсивный фиолетовый цвет. Это реакция является качественной.
Применение анилина.
Анилин используют преимущественно для синтеза лекарственных средств и красителей:
Анилин — структурная формула и свойства органического соединения
Анилин – это соединение, которое относят к органическим веществам. Принадлежит к классу аминов. Чтобы понять, что такое амины, можно представить формулу аммиака, затем один атом водорода или все заменить углеводородным радикалом.
Анилин (фениламин) — понятие, строение, физические свойства
Если в формуле аммиака только один водородный атом заменить фенил радикалом, получится анилин (фениламин). Поэтому его можно считать производным аммиака. Вещество называют также аминобензол.
Можно иначе представить это соединение. Если в формуле бензола вместо одного водорода поставить аминогруппу, получается анилин. Значит это производная бензола, где атом водорода замещается на аминогруппу.
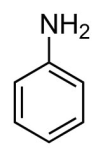
Эмпирическая (молекулярная) формула фениламина C6H5 NH2. Его записывают с помощью структурной формулы:
Аминобензол содержит две группы атомов: аминогруппу и фенил радикал. Они оказывают влияние на свойства вещества.
Аминогруппа NH2– состоит из атома азота и двух атомов водорода. У азота на внешнем энергетическом уровне содержится 5 электронов. Два электрона образуют химическую связь с атомами углерода, один электрон образует связь с углеродом фенил радикала. У него еще остаётся два электрона. Они образуют свободную пару электронов.
Аминогруппа в составе анилина может присоединять протон водорода. Поэтому соединение проявляет свойства оснований. Так как по определению, вещества, присоединяющие протон водорода, принято считать основаниями.
Фенил радикал C6H5 – имеет в своём составе бензольное кольцо. Благодаря этому фениламин должен вступать в реакции, характерные для бензола.
Так как 2 группы атомов находятся в одном соединении, они оказывают влияние друг на друга.
Фенил радикал, влияя на функциональную группу, вовлекает свободную пару электронов в π — электронную систему. Такое смещение плотности влияет на проявление свойств соединения как основания. В результате фениламин не вступает во взаимодействие с водой. Аммиак, таким образом, более сильное основание.
Функциональная группа влияет на π — систему. Нарушается равномерное распределение электронной плотности. Она повышается у атомов 2,4,6 (в орто — и пара — положениях). Именно здесь будет идти замена водорода на другие атомы в химических реакциях.
Фениламин — это жидкость, маслянистая и ограниченно растворяющаяся в воде. Растворяется в органических соединениях.
Кипит при температуре 184 0 С, замерзает при температуре –6 0 С. При окислении окрашивается в красно-бурый цвет. Молярная масса 93 г/моль. Плотность вещества при 20 0 С составляет 1,02173 г/см 3 .
Вещество ядовито. Его относят ко второму классу опасности. При контакте с кожей может вызвать аллергию. При попадании в организм вызывает отравление. Есть информация о том, что оно может вызвать генетические мутации, возникает риск возникновения раковых заболеваний. Его называют ядом крови, так как вызывает кислородное голодание.
Получение анилина
Фениламин получают из нитробензола. Данный способ был предложен русским учёным Н. Н. Зининым. Поэтому получил название «реакция Зинина».
Проводят взаимодействие железа с нитробензолом в присутствии соляной кислоты.
Идёт восстановление нитробензола до анилина. Синтез можно представить уравнениями реакций:
Fe + 2HCl = FeCl2 + 2H
При взаимодействии анилина с галогеналканами и спиртами получают смесь вторичных, а также третичных аминов. Такое превращение носит название алкилирование.
Химические свойства анилина
Для вещества характерны две группы свойств.
Реакции, идущие за счет функциональной группы.
Фениламин взаимодействует с кислотами. В результате образуются соли. При взаимодействии анилина с хлороводородной кислотой получается хлорид фениламмония, или анилин солянокислый:
Свойства, идущие за счёт фенил радикала.
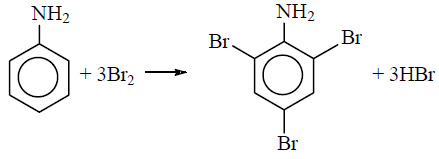
Для фениламина характерна реакция замещения, например бромирование. В результате получают 2,4,6 триброманилин. Образуется осадок белого цвета, поэтому реакцию считают качественной на обнаружение данного вещества.
Уравнение реакции с бромом выглядит следующим образом:
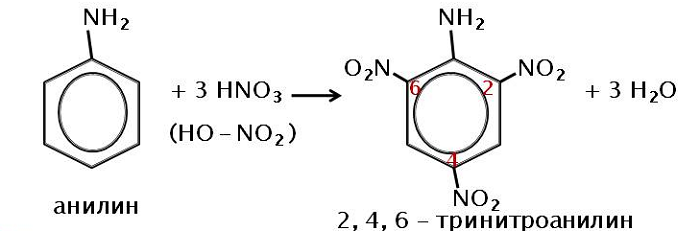
Нитрование, при котором происходит замещение в кольце ароматических аминов:
Вступает во взаимодействие с азотной кислотой, образуя тринитроанилин.
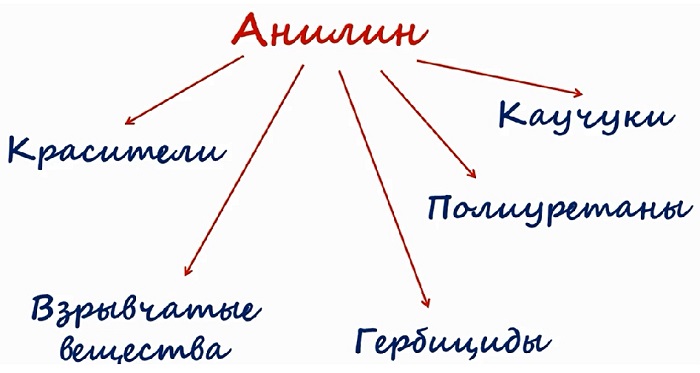
Применение анилина
Большая часть фениламина идёт для синтеза красителей. Его используют в получении типографской краски и синтетических красителей для текстильной промышленности.
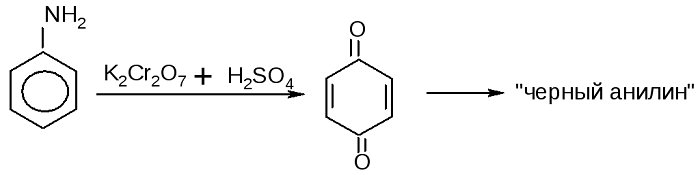
Так в кислой среде анилин окисляется дихроматом калия, в результате получается чёрный краситель. Эта реакция также рассматривается как качественная на фениламин:
Вещество является исходным для получения лекарственных препаратов. Сульфаниламидные соединения, получаемые на основе анилина, используют в медицине в качестве лекарств. Это производные анилина. К ним относятся: парацетамол, фенацетин и другие.
Также на основе соединения производят химические средства защиты растений, различные смолы, крем для обуви, взрывчатые вещества.