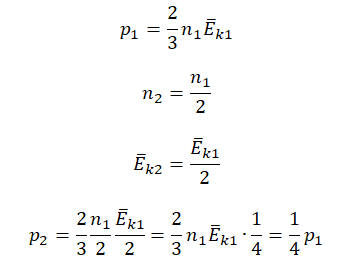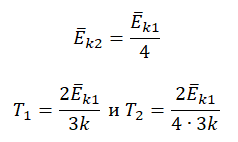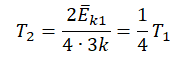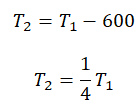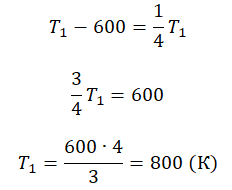- Ваш ответ
- решение вопроса
- Похожие вопросы
- Основное уравнение МКТ идеального газа
- теория по физике 🧲 молекулярная физика, МКТ, газовые законы
- Измерение температуры
- Основное уравнение МКТ идеального газа
- Следствия из основного уравнения МКТ идеального газа
- Тесты по физике 10 класс
- Выберите документ из архива для просмотра:
- Презентация ТЕСТ ТРЕНИРОВОЧНЫЙ ПО ТЕМЕ ОСНОВЫ МКТ ИДЕАЛЬНОГО ГАЗА презентация урока для интерактивной доски по физике (10 класс) на тему
- Скачать:
- Предварительный просмотр:
- Подписи к слайдам:
- По теме: методические разработки, презентации и конспекты
Ваш ответ
решение вопроса
Похожие вопросы
- Все категории
- экономические 43,423
- гуманитарные 33,634
- юридические 17,906
- школьный раздел 608,194
- разное 16,858
Популярное на сайте:
Как быстро выучить стихотворение наизусть? Запоминание стихов является стандартным заданием во многих школах.
Как научится читать по диагонали? Скорость чтения зависит от скорости восприятия каждого отдельного слова в тексте.
Как быстро и эффективно исправить почерк? Люди часто предполагают, что каллиграфия и почерк являются синонимами, но это не так.
Как научится говорить грамотно и правильно? Общение на хорошем, уверенном и естественном русском языке является достижимой целью.
Основное уравнение МКТ идеального газа
теория по физике 🧲 молекулярная физика, МКТ, газовые законы
Идеальный газ — газ, удовлетворяющий трем условиям:
- Молекулы — материальные точки.
- Потенциальная энергия взаимодействия молекул пренебрежительно мала.
- Столкновения между молекулами являются абсолютно упругими.
Реальный газ с малой плотностью можно считать идеальным газом.
Измерение температуры
Температуру можно измерять по шкале Цельсия и шкале Кельвина. По шкале Цельсия за нуль принимается температура, при которой происходит плавление льда. По шкале Кельвина за нуль принимается абсолютный нуль — температура, при котором давление идеального газа равно нулю, и его объем тоже равен нулю.
Обозначение температуры
- По шкале Цельсия — t. Единица измерения — 1 градус Цельсия (1 o C).
- По шкале Кельвина — T. Единица измерения — 1 Кельвин (1 К).
Цена деления обеих шкал составляет 1 градус. Поэтому изменение температуры в градусах Цельсия равно изменению температуры в Кельвинах:
При решении задач в МКТ используют значения температуры по шкале Кельвина. Если в условиях задачи температура задается в градусах Цельсия, нужно их перевести в Кельвины. Это можно сделать по формуле:
Если особо важна точность, следует использовать более точную формулу:
Пример №1. Температура воды равна o C. Определить температуру воды в Кельвинах.
T = t + 273 = 2 + 273 = 275 (К)
Основное уравнение МКТ идеального газа
Давление идеального газа обусловлено беспорядочным движением молекул, которые сталкиваются друг с другом и со стенками сосуда. Основное уравнение МКТ идеального газа связывает давление и другие макропараметры (объем, температуру и массу) с микропараметрами (массой молекул, скоростью молекул и кинетической энергией).
Основное уравнение МКТ
Давление идеального газа пропорционально произведению концентрации молекул на среднюю кинетическую энергию поступательного движения молекулы.
p = 2 3 . . n − E k
p — давление идеального газа, n — концентрация молекул газа, − E k — средняя кинетическая энергия поступательного движения молекул.
Выражая физические величины друг через друга, можно получить следующие способы записи основного уравнения МКТ идеального газа:
p = 1 3 . . m 0 n − v 2
m 0 — масса одной молекулы газа;
n — концентрация молекул газа;
− v 2 — среднее значение квадрата скорости молекул газа.
Среднее значение квадрата скорости не следует путать со среднеквадратичной скоростью v, которая равна корню из среднего значения квадрата скорости:
p = 1 3 . . ρ − v 2
k — постоянная Больцмана (k = 1,38∙10 –3 Дж/кг)
T — температура газа по шкале Кельвина
Пример №2. Во сколько раз уменьшится давление идеального одноатомного газа, если среднюю кинетическую энергию теплового движения молекул и концентрацию уменьшить в 2 раза?
Согласно основному уравнению МКТ идеального газа, давление прямо пропорционально произведению средней кинетической энергии теплового движения молекул и концентрации его молекул. Следовательно, если каждая из этих величин уменьшится в 2 раза, то давление уменьшится в 4 раза:
Следствия из основного уравнения МКТ идеального газа
Через основное уравнение МКТ идеального газа можно выразить скорость движения молекул (частиц газа):
v = √ 3 k T m 0 . . = √ 3 R T M . .
R — универсальная газовая постоянная, равная произведения постоянной Авогадро на постоянную Больцмана:
R = N A k = 8 , 31 Д ж / К · м о л ь
Температура — мера кинетической энергии молекул идеального газа:
Полная энергия поступательного движения молекул газа определяется формулой:
Пример №3. При уменьшении абсолютной температуры на 600 К средняя кинетическая энергия теплового движения молекул неона уменьшилась в 4 раза. Какова начальная температура газа?
Запишем формулу, связывающую температуру со средней кинетической энергией теплового движения молекул, для обоих случаев, с учетом что:
Составим систему уравнений:

Алгоритм решения
Решение
График построен в координатах (V;Ek). Процесс 1–2 представляет собой прямую линию, исходящую из начала координат. Это значит, что при увеличении объема растет средняя кинетическая энергия молекул. Но из основного уравнения МКТ идеального газа следует, что мерой кинетической энергии молекул является температура:
Следовательно, когда кинетическая энергия молекул растет, температура тоже растет.
Запишем уравнение Менделеева — Клапейрона:
Так как количество вещества одинаковое для обоих состояния 1 и 2, запишем:
ν R = p 1 V 1 T 1 . . = p 2 V 2 T 2 . .
Мы уже выяснили, что объем и температура увеличиваются пропорционально. Следовательно, давление в состояниях 1 и 2 равны. Поэтому процесс 1–2 является изобарным, давление во время него не меняется.
Процесс 2–3 имеет график в виде прямой линии, перпендикулярной кинетической энергии. Так как температуры прямо пропорциональна кинетической энергии, она остается постоянной вместе с этой энергией. Следовательно, процесс 2–3 является изотермическим, температура во время него не меняется. Мы видим, что объем при этом процессе уменьшается. Но так как объем и давление — обратно пропорциональные величины, то давление на участке 2–3 увеличивается.
pазбирался: Алиса Никитина | обсудить разбор | оценить
Первоначальное давление газа в сосуде равнялось р1. Увеличив объём сосуда, концентрацию молекул газа уменьшили в 3 раза, и одновременно в 2 раза увеличили среднюю энергию хаотичного движения молекул газа. В результате этого давление р2 газа в сосуде стало равным
Тесты по физике 10 класс
Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
Рабочие листы и материалы для учителей и воспитателей
Более 2 500 дидактических материалов для школьного и домашнего обучения
Столичный центр образовательных технологий г. Москва
Получите квалификацию учитель математики за 2 месяца
от 3 170 руб. 1900 руб.
Количество часов 300 ч. / 600 ч.
Успеть записаться со скидкой
Форма обучения дистанционная
311 лекций для учителей,
воспитателей и психологов
Получите свидетельство
о просмотре прямо сейчас!
Выберите документ из архива для просмотра:
Выбранный для просмотра документ Температура. Средняя кинетич.энергия.docx
МКТ. Температура и средняя кинетическая энергия молекул.
1. Какая из приведенных ниже формул является основным уравнением молекулярно-кинетической теории?
1. р = 

А. Только первая. Б. Только вторая. В. Обе формулы. Г. Ни одна из них.
2. Как изменится давление идеального газа на стенки сосуда, если в данном объеме скорость каждой молекулы удвоилась, а концентрация м о лекул не изменилась?
А. Не изменится. Б. Увеличится в 2 раза. В. Увеличится в 4 раза. Г. Ответ неоднозначный.
3. Молекула азота летит со скоростью v перпендикулярно к стенке сосуда. Чему равен модуль вектора изменения импульса молекулы?
А. 0. Б. mv . B . 2 m v . Г. 4 mv .
4. Какая из приведенных ниже формул устанавливает связь между микропараметрами газа и его измеряемым макропараметром? 1. Ē = 

А. Только 1. Б. Только 2. В. 1 и 2. Г. Ни 1, ни 2.
5. Как изменится средняя кинетическая энергия молекул идеального газа при увеличении абсолютной температуры в 2 раза?
А. Не изменится. Б. Увеличится в 2 раза. В. Увеличится в 4 раза. Г. Ответ неоднозначный.
6. Воздух в комнате состоит из смеси газов: водорода, кислорода, азота, водяных п аров, углекислого газа и др. Какие из физических параметров этих газов обязательно одинаковы при тепловом равновесии?
А. Температура. Б. Давление. В. Концентрация молекул. Г. Средний квадрат скорости теплового движения молекул.
7. В первом сосуде водород, а во втором — кислород. Сравните давления р 1 и р 2 в этих сосудах, если концентрация молекул и температура в обоих сосудах одинаковы.
А. р 1 = р 2. Б. р 1 = 16 р 2. В. р 2 = 16 р 1 . Г. Ответ неоднозначный.
8. Сравните средние квадратичные скорости молекул кислорода и азота воздуха ⊽ к и ⊽ а.
А. ⊽ к 

9. В первом сосуде находится азот, во втором – водород. Чему равно отношение давления р 1 давлению р 2. водорода при одинаковых значениях концентрации молекул и температуры?
А. 1. Б. 14. В. 28. Г. Отношение давлений может иметь различные значения.
10. Абсолютная температура идеального газа увеличилась в 3 раза при неизменной концентрации. Выберите правильное утверждение.
А. Средняя кинетическая энергия молекул увеличилась в 
Б. Давление газа увеличилось в 3 раза.
В. Средняя квадратичная скорость молекул газа увеличилась в 9 раз.
Г. Среди ответов А, Б, В нет правильного.
МКТ. Температура и средняя кинетическая энергия молекул.
1.Какая из приведенных ниже формул является уравнением молекулярно-кинетической теории?
1. р = 

А. Только первая. Б. Только вторая. В. Обе формулы. Г. Ни одна из них.
2. Как изменится средняя кинетичес к ая энергия идеального газа при уменьшении абсолютно й температуры в 2 раза?
А. Уменьшится в 4 раза. Б. Уменьшится в 2 раза. В. Не изменится. Г. Ответ неоднозначный.
3. Молекула кислорода летит со скоростью v перпендикулярно к стенке сосуда. Чему равен вектор изменения импульса молекулы?
А. 0. Б. m ⊽ . В. 2 m ⊽ . Г. -2 m ⊽ .
4. Какая из приведенных ниже формул устанавливает связь между микропараметрами газа и его измеряемым макропараметром?
1. р = 

А. Только 1. Б. Только 2. В. 1 и 2. Г. Ни 1, ни 2.
5. Как изменится средняя кинетичес к ая энергия идеального газа при уменьшении абсолютно й температуры в 2 раза?
А. Уменьшится в 4 раза. Б. Уменьшится в 2 раза. В. Не изменится. Г. Ответ неоднозначный.
6. Воздух в комнате состоит из смеси газов: водорода, кислорода, азота, водяных паров, углекислого газа и др. Какие из физических параметров этих газов обязательно одинаковы при тепловом равновесии?
А. Давление. Б. Средний квадрат скорости теплового движения молекул. В. Концентрация. Г. Средняя кинетическая э н ергия м о лекул.
7. Сравните давления p 1 водорода и p 2 кислорода, если концентрация газов и их среднеквадратичные скорости одинаковы:
8. Сравните средние квадратичные скорости молекул аргона и неона ⊽ а и ⊽ н при одинаковых температурах.
А. ⊽ н 

9. В первом сосуде находится водород, во втором – кислород. Чему равно отношение числа молекул водорода к числу молекул кислорода, если давление, объем и температура газов одинаковы?
А. 1. Б. 16. В. 
10. Давление идеального газа уменьшилось в 2 раза при неизменной концентрации. Выберите правильное утверждение.
А. Абсолютная температура увеличилась в 2 раза.
Б. Средняя квадратичная скорость молекул газа уменьшилась в 
В. Средняя кинетическая энергия молекул газа увеличилась в 2 раза.
Г. Среди ответов А, Б, В нет правильного.
Иродова И.А. Физика: Сборник заданий и тестов. 10-11 кл. – М., Гуманит. изд. центр Владос, 2001.
Кирик Л.А. Физика-10. Разноуровневые самостоятельные и контрольные работы. – М., Илекса, 2007.
Кабардин О.Ф. и др. Задания для контроля знаний учащихся по физике в средней школе: Дидакт. Материал. Пособие для учителей. – М., Просвещение, 1983.
Презентация ТЕСТ ТРЕНИРОВОЧНЫЙ ПО ТЕМЕ ОСНОВЫ МКТ ИДЕАЛЬНОГО ГАЗА
презентация урока для интерактивной доски по физике (10 класс) на тему
ТЕС ПРЕДНАЗНАЧЕН ДЛЯ ПРОВЕРКИ ЗНАНИЙ ПО ТЕМЕ «ОСНОВЫ МКТ ИДЕАЛЬНОГО ГАЗА». ЭТО ИНТЕРАКТИВНЫЙ ТЕСТ. В НЁМ ЕСТЬ ССЫЛКИ НА ПОВТОРИТЕЛЬНЫЙ МАТЕРИАЛ, ЕСЛИ ОТВЕТ НЕВЕРНЫЙ.
Скачать:
| Вложение | Размер |
|---|---|
| test_trenirovochnyy_osnovy_mkt_idealnogo_gaza.ppt | 476.5 КБ |
Предварительный просмотр:
Подписи к слайдам:
Проверь свои знания по теме «Основы МКТ идеального газа» Тренировочный тест
1.Наблюдаемые в микроскоп частицы гуммигута, взвешенные в воде, двигаются беспорядочно и бессистемно, хаотически. Это демонстрирует: Диффузию Броуновское движение
Броуновское движение – это тепловое, беспорядочное ( хаотичное) движение взвешенных в жидкости или газе частиц!
Молодец! Переходи к следующему вопросу
Неправильно! Вспомни теорию!
2.Укажи единицу измерения количества вещества 1 л 1 моль 1 стакан м 3
Количество вещества – это относительное число молекул в теле
Молодец! Переходи к следующему вопросу
Неправильно! Повтори теорию!
3.Какая из приведённых ниже формул является основным уравнением МКТ идеального газа?
Основное уравнение МКТ пишется в разных вариантах, но самый первый вариант Запомни !
Молодец! Переходи к следующему вопросу
Неправильно! Повтори теорию!
4.Какая физическая величина имеет размерность 1 м -3 ? объём плотность концентрация
Конечно же это концентрация молекул, т.е. распределение их по объёму
Молодец! Переходи к следующему вопросу
Неправильно! Повтори теорию!
5.Как изменится давление газа на стенки сосуда, если в данном объёме скорость каждой молекулы удвоилась, а концентрация молекул не изменилась? уменьшится в 4 раза Не изменится увеличится в 4 раза
Используй уравнение Напиши сначала начальные параметры Р 0 , а затем с изменениями Р и сравни результаты. Вот видишь всё просто
Молодец! Переходи к следующему вопросу
Неправильно! Повтори теорию!
Поздравляю! Ты выполнил тест, молодец!
Конец теста Всем спасибо за участие .
По теме: методические разработки, презентации и конспекты
ЭОР тест по теме «Уравнение состояния идеального газа. Газовые законы»
ЭОР тест по теме «Уравнение состояния идеального газа. Газовые законы»Цель данного ресурса: повторение, обобщение и систематизация знаний учащихся на различных этапах освоения материала. Подгото.
Обучающий тест для 10 класса к уроку по теме : «Изопроцессы и их графики. Законы идеальных газов» .
Обучающий тест для 10 класса к уроку по теме : «Изопроцессы и их графики. Законы идеальных газов» может быть использован в.
Интерактивный тест по теме «Основы молекулярно-кинетической теории идеального газа»
Тест создан в программе MS Excel 2007. Тест предназначен для проверки знаний по теме «Основы МКТ идеального газа» для студентов 1 курса (для учащихся 10 класса). Тест представлен в двух вариантах, каж.
Интерактивный тест «Уравнение состояния идеального газа»
Интерактивный тест по физике «Уравнение состояния идеального газа» предназначен для учащихся 10 класса.
Тест на закрепление темы Уравнение состояния идеального газа
Тест на закрепление темы Уравнение состояния идеального газа с код правильных ответов на 2 варианта.
Проверочный тест «Уравнение состояния идеального газа»
Интерактивный проверочный тест, созданный в программе Power Point.
Тест по МКТ идеального газа
Презентация для проведения итогового тестирования по теме «МКТ идеального газа» построена таким образом, что позволяет повторить пройденный материал.