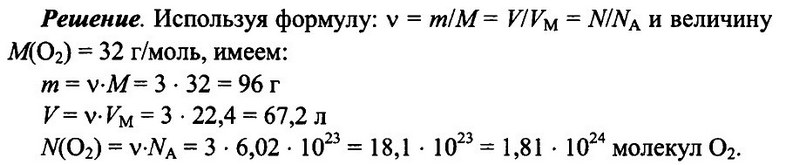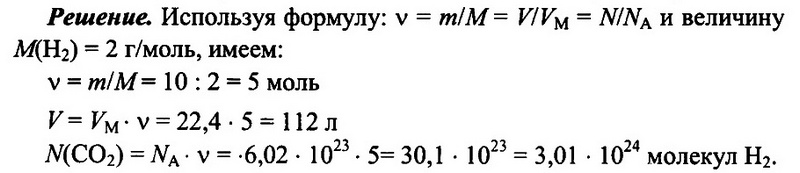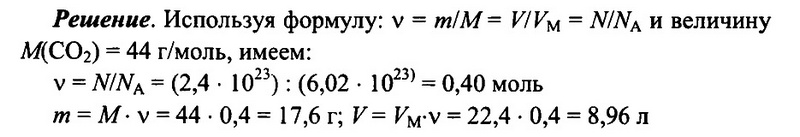Алгоритм решения задач по уравнению химической реакции
Запомни: Все задачи решаются на основе закона сохранения массы веществ: масса веществ, вступивших в реакцию, равна массе веществ, получившихся в результате реакции.
Схема решения задач:




|




Порядок решения задач:
1. Краткая запись условия задачи.
2. Запись уравнения химической реакции.
3. Запись известных и неизвестных величин над формулами веществ.
4. Запись под формулами веществ количества, молярные массы и массы(или молярные объемы и объемы) веществ.
5. Составление и решение пропорции.
6. Запись ответа задачи.
Образец решения задачи:
Задача: Сколько граммов оксида меди (II) образовалось при прокаливании 6,4 кг меди.


ν = 2 кмоль ν = 2 кмоль по уравнению реакции
М = 64кг/моль М = 80 кг/моль
m = 128кг m = 160 кг
Составляем пропорцию: 6,4 кг : 128 кг = Х кг : 160 кг
Х = 6,4 * 160 / 128 Х = 8 кг
Алгоритм решения задач по химическому уравнению.
Помните: 1. вещества взаимодействуют в массах, пропорциональных их количествам, т.е. массы веществ, участвующих
В реакции, относятся друг к другу так же, как и их количества;
Вещества вступают во взаимодействие в количествах, равных их стехиометрическим коэффициентам;
3. задача состоит из 3-ёх частей:
I — химическая – краткая запись данных, составление уравнения реакции;
II — аналитическая – анализ данных в условии и уравнения реакции;
III — математическая – расчеты по уравнению реакции.
Метод пропорции.
| Схема. | Порядок действий (пошаговый): | Пример: Какой объём газа выделится при взаимодействии 6,5 г цинка с избытком раствора серной кислоты? |
| I.Д а н о : m(n, V) реагента или продукта. Н а й т и : m(n, V) другого реагента или продукта | I.Запишите краткое условие задачи и уравнение химической реакции, подчеркните вещества, о которых идет речь в задаче. | Д а н о: Решение:   m (Zn) = 6,5г Zn + H2SO4 = ZnSO4 + H2 V (H2) ? m (Zn) = 6,5г Zn + H2SO4 = ZnSO4 + H2 V (H2) ? |
| II-1. Составление уравнения и соответствующие записи. a A + b B → c C + d D a моль b моль c моль d моль | II – 1.Данные из условия задачи запишите над формулами соответствующих веществ в уравнении. | 6,5г Хл  Zn + H2SO4 = ZnSO4 + H2 Помните:что спрашивают, то обозначается переменной (Х, У и т.д.) Zn + H2SO4 = ZnSO4 + H2 Помните:что спрашивают, то обозначается переменной (Х, У и т.д.) |
| II-2. Определение отношений данных в условии и в уравнении. m = n * M по услов. m1(B) m1(C) a A + b B → c C + d D a моль b моль c моль d моль M (B) M(C)по уравн.m (B) m(C) (m = M * n) | II – 2.Под этими же формуламизапишите данные из уравнения реакции в следующей последовательности: — количество вещества по уравнению (коэффициент = числу молей по уравне- нию) — молярную массу (или объем) вещества; — массу (объем) вещества по уравнению (воспользуйтесь формулой: m= M * n V = Vm * n) |    6,5г Хл Zn + H2SO4 = ZnSO4 + H2 6,5г Хл Zn + H2SO4 = ZnSO4 + H2   х 1 моль х 1 моль х 1 моль х 1 моль   М=65г/моль Vm=22,4л/моль m = 65г V = 22,4 л Помните: единицы измерения количеств веществ по условию и по уравнению должны совпадать! М=65г/моль Vm=22,4л/моль m = 65г V = 22,4 л Помните: единицы измерения количеств веществ по условию и по уравнению должны совпадать! |
| III. Составление и решение пропорции: m1(B) ‗ m1(C) m (B) m(C) | III.Составьте пропорцию и решите её. (крест-накрест) ( Для этого впишите в неё самую верх- нюю и самую нижнюю цифры, которые у Вас получились.) Запишите ответ. | 6,5г ‗ Хл 65г 22,4л Х ‗ 6,5г * 22,4 л 65г Х = 2,24л Ответ: V газа = 2,24 л. |
Метод сравнения количеств веществ.
Отличие данного метода от предыдущего в том, что все данные из условия переводятся в количества веществ:
- Как решать задачи по химии. Расчет по уравнениям химических реакций.
- Алгоритм решения задач по химии
- Расчет по уравнениям химических реакций с использованием понятия количества вещества
- Решение задач по химии через пропорцию
- Как сравнить количество веществ по уравнению
- Решение задач на количество вещества, массу и объем
- ФОРМУЛЫ ДЛЯ РЕШЕНИЯ ЗАДАЧ
- РЕШЕНИЯ ПРОСТЫХ ЗАДАЧ
- 📺 Видео
Видео:ТИПОВЫЕ ЗАДАЧИ ПО ХИМИИ: Химическое Количество Вещества, Моль, Молярная Масса и Молярный ОбъемСкачать

Как решать задачи по химии. Расчет по уравнениям химических реакций.
Как решать задачи по химии? Как проводить простейшие расчеты по уравнениям химических реакций? Сколько выделяется газа, образуется воды, выпадает осадка или сколько получается конечного продукта реакций? Сейчас мы постараемся разобрать все нюансы и ответить на эти вопросы, которые очень часто возникают при изучении химии.
Решение задач в химии является неотъемлемой частью в изучении этой сложной, но очень интересной науки.
Видео:Количество вещества. Моль. Число Авогадро. 8 класс.Скачать

Алгоритм решения задач по химии
- Прочитать условия задачи (если они есть). Да, об этом все знают — как же решить задачу без условий — но все же, для полноты инструкции, мы не могли не указать этот пункт.
- Записать данные задачи. На этом пункте мы не будем заострять внимание, так как требования различных учебных заведений, учителей и преподавателей могут значительно отличаться.
- Записать уравнение реакции. Теперь начинается самое интересное! Здесь нужно быть внимательным! Обязательно необходимо верно расставить коэффициенты перед формулами веществ. Если вы забудете это сделать, то все наши усилия буду напрасны.
- Провести соответствующие расчеты по химическому уравнению. Далее рассмотрим, как же сделать эти самые расчеты.
Для этого у нас есть два пути, как решить задачу по химии. Условно, назовем их правильным (используя понятия количества вещества) и неправильным (используя пропорции). Конечно же, мы бы рекомендовали решать задачи правильным путем. Так как у неправильного пути имеется очень много противников. Как правило, учителя считают, что ученики, решающие задачи через пропорции, не понимают самой сути протекания процессов химических реакций и решают задачи просто математически.
Видео:Как Решать Задачи по Химии // Задачи с Уравнением Химической Реакции // Подготовка к ЕГЭ по ХимииСкачать

Расчет по уравнениям химических реакций с использованием понятия количества вещества
Суть данного метода, состоит в том, что вещества реагируют друг с другом в строгом соотношении. И уравнение реакции, которое мы записали ранее, дает нам это соотношение. Коэффициенты перед формулами веществ дают нам нужные данные для расчетов.
Для примера, запишем простую реакцию нейтрализации серной кислоты и гидроксида натрия.
H_SO_ + NaOH → Na_SO_ + H_O
H_SO_ + 2NaOH → Na_SO_ + 2H_O
Исходя из этого уравнения, мы видим, что одна молекула серной кислоты взаимодействует с двумя молекулами гидроксида натрия. И в результате этой реакции получается одна молекула сульфата натрия и две молекулы воды.
Сейчас мы немного отступим от разбора задач, чтобы познакомиться с основными понятиями, которые пригодятся нам в решении задач по химии.
Рассчитывать количество молекул, например в 98 граммах серной кислоты — это не самое удобное занятие. Числа будут получаться огромными ( ≈ 6,022140857⋅10 23 молекул в 98 граммах серной кислоты) . Для этого в химии ввели понятие количества вещества (моль) и молярная масса.
1 Моль (единица измерения количества вещества) — это такое количество атомов, молекул или каких либо еще структурных единиц, которое содержится в 12 граммах изотопа углерода-12. Позднее выяснилось, что в 12 граммах вещества углерод-12 содержится 6,022140857⋅10 23 атомов. Соответственно, можно сказать, что 1 моль, это такая масса вещества, в которой содержится 6,022140857⋅10 23 атомов (или молекул) этого вещества.
Но ведь молекулы и атомы имеют различный состав и различное строение. Разные атомы содержат разное количество протонов и нейтронов. Соответственно 1 моль для разных веществ будет иметь разную массу, имея при это одинаковое количество молекул ( атомов). Эта масса называется молярной.
Молярная масса — это масса 1 моля вещества.
Используя данные понятия, можно сказать, что 1 моль серной кислоты реагирует с 2 молями гидроксида натрия, и в результате получается 1 моль сульфата натрия и 2 моль воды. Давайте запишем эти данные под уравнением реакции для наглядности.
beginH_SO_ & + & 2NaOH & → & Na_SO_ & + & 2H_O \ 1 : моль & & 2 : моль & & 1 : моль & & 2 : моль end
Следом запишем молярные массы для этих веществ
begin H_SO_ & + & 2NaOH & → & Na_SO_ & + & 2H_O \ 1 : моль & & 2 : моль & & 1 : моль & & 2 : моль \ 98 : г& & 40 : г & & 142 : г & & 18 : г end
Теперь, зная массу одного из веществ, мы можем рассчитать, сколько нам необходимо второго вещества для полного протекания реакции, и сколько образуется конечных продуктов.
Для примера, решим по этому же уравнению несколько задач.
Задача. Сколько грамм гидроксида натрия (NaOH) необходимо для того, чтобы 49 грамм серной кислоты (H2SO4) прореагировало полностью?
Итак, наши действия: записываем уравнение химической реакции, расставляем коэффициенты. Для наглядности, запишем данные задачи над уравнением реакции. Неизвестную величину примем за Х. Под уравнением записываем молярные массы, и количество молей веществ, согласно уравнению реакции:
begin49 : г & & X : г & & & & \ H_SO_ & + & 2NaOH & → & Na_SO_ & + & 2H_O \ 1 : моль & & 2 : моль & & 1 : моль & & 2 : моль \ 98 : г& & 40 : г & & 142 : г & & 18 : г end
Записывать данные под каждым веществом — не обязательно. Достаточно это будет сделать для интересующих нас веществ, из условия задачи. Запись выше дана для примера.
Примерно так должны выглядеть данные, записанные по условиям задачи. Не претендуем на единственно правильное оформление, требования у всех разные. Но так, как нам кажется, смотрится все довольно наглядно и информативно.
Первое наше действие — пересчитываем массу известного вещества в моли. Для этого разделим известную массу вещества (49 грамм) на молярную массу:
4998=0,5 моль серной кислоты
Как уже упоминалось ранее, по уравнению реакции 1 моль серной кислоты реагирует с 2 моль гидроксида натрия. Соответственно с 0,5 моль серной кислоты прореагирует 1 моль гидроксида натрия.
n(NaOH)=0.5*2=1 моль гидроксида натрия
Найдем массу гидроксида натрия, умножив количество вещества на молярную массу:
1 моль * 40 г/моль = 40 грамм гидроксида натрия.
Ответ: 40 грамм NaOH
Как видите, в решении задачи по уравнению реакции нет ничего сложного. Задача решается в 2-3 действия, с которыми справятся ученики начальных классов. Вам необходимо всего лишь запомнить несколько понятий.
Видео:Химические уравнения // Как Составлять Уравнения Реакций // Химия 9 классСкачать

Решение задач по химии через пропорцию
Ну и расскажем про второй способ вычислений по уравнениям химических реакций — вычисления через пропорцию. Этот способ может показаться немного легче, так как в некоторых случаях можно пропустить стадию перевода массы вещества в его количество. Чтобы было более понятно, объясню на том же примере.
Так же, как и в прошлом примере, запишем уравнение реакции, расставим коэффициенты и запишем над уравнением и под уравнением известные данные.
Для этого способа, нам так же понадобится записать под уравнением реакции, следом за молярной массой, массу вещества, соответствующую его количеству по уравнению. Если проще, то просто перемножить две строки под уравнением реакции, количество моль и молярную массу. Должно получиться так:
begin49 : г & & X : г & & & & \ H_SO_ & + & 2NaOH & → & Na_SO_ & + & 2H_O \ 1 : моль & & 2 : моль & & 1 : моль & & 2 : моль \ 98 : г& & 40 : г & & 142 : г & & 18 : г \ 98 : г & & 80 : г & & 142 : г & & 36 : г end
А теперь внимание, начинается магия! Нас интересует строка данных над уравнением, и самая нижняя строка под уравнением. Составим из этих данных пропорцию.
Далее находим неизвестное значение Х из пропорции и радуемся полученному значению:
Х=49*80/98=40 грамм
Как видим, получается тот же результат. Прежде всего, при решении задач в химии, главное все же — понимание химических процессов. Тогда решение задачи не станет для вас проблемой!
Видео:Расчеты по уравнениям химических реакций. 1 часть. 8 класс.Скачать

Как сравнить количество веществ по уравнению
Видео:Как расставлять коэффициенты в уравнении реакции? Химия с нуля 7-8 класс | TutorOnlineСкачать

Решение задач на количество вещества,
массу и объем
Ключевые слова: решение задач на количество вещества, решение задач по химии на массу и объем, какое количества вещества содержится, какое число молекул содержится, определите объем (н.у.), определите массу, какова масса порции, определите молярную массу, назовите вещество, найдите молярную массу, определите абсолютную массу молекулы, сколько атомов содержится, определите относительную плотность.
ФОРМУЛЫ ДЛЯ РЕШЕНИЯ ЗАДАЧ
Количество вещества характеризует число структурных единиц (атомов, молекул, ионов), которое содержится в определенном образце данного вещества. Единицей измерения количества вещества является моль. Количество вещества (ν) связано с числом структурных единиц (N) в образце вещества, его массой (m) и объемом (V) — для газообразных веществ при н. у. — следующими уравнениями:

Vm = 22,4 л/моль (мл/ммоль, м 3 /кмоль) при н.у.,
Na = 6,02 • 10 23 (постоянная Авогадро),
а молярная масса (М) численно равна относительной молекулярной массе вещества:
Наличие подобной взаимосвязи позволяет, зная одну из величин (количество вещества, массу, объем, число структурных величин) определить все другие величины.
РЕШЕНИЯ ПРОСТЫХ ЗАДАЧ
Задача № 1. Какое количество вещества содержится в 33 г оксида углерода (IV)?

Ответ: ν(СО2) = 0,75 моль.
Задача № 2. Какое число молекул содержится в 2,5 моль кислорода?

Ответ: N(O2) = 1,505 • 10 24 .
Задача № 3. Определите объем (н. у.), который займут 0,25 моль водорода.
Задача № 4. Какую массу будет иметь порция оксида серы (IV), объем которой 13,44 л (н. у.)?
Задача № 5. Имеется 3 моль кислорода О2 при н.у. Определите массу кислорода, его объем, а также число имеющихся молекул кислорода.
Ответ: m = 96 г; V = 67.2 л; N(O2) = 1,81 • 10 24 .
Задача № 6. Имеется 10 г водорода Н2. Определите количество водорода, его объем при н.у., а также число имеющихся молекул водорода.
Ответ: 5 моль; 112 л; 3,01 • 10 24 .
Задача № 7. Имеется 56 л хлора Сl2 при н.у. Определите количество вещества хлора, его массу и число имеющихся молекул хлора.
Ответ: 2,5 моль; 177,5 г; 1,5 • 10 24 .
Задача № 8. Имеется 2,4 • 10 23 молекул оксида углерода (IV) СO2. Определите количество вещества углекислого газа, его массу, а также объем (н.у.) углекислого газа.
Ответ: 0,4 моль; 17,6 г; 8,96 л.
Задача № 9. Какова масса порции оксида азота (IV), содержащей 4,816 • 10 23 молекул? Каков ее объем (н. у.)?
Задача № 10. Масса порции простого вещества, содержащей 1,806 • 10 24 молекул, равна 6 г. Определите молярную массу данного вещества и назовите его.
Внимание! В данном конспекте рассматриваются задачи обычной сложности. Чтобы перейти к конспекту решения сложных задач на количественные характеристики и задачи с кратким ответом нажмите на кнопку ниже…
Решение задач на количество вещества, массу и объем. Выберите дальнейшие действия:
📺 Видео
8 класс.Ч.1.Решение задач по уравнению реакций.Скачать

Составление уравнений химических реакций. 1 часть. 8 класс.Скачать

Как за 4 МИНУТЫ выучить Химию? Химическое Количество, Моль и Закон АвогадроСкачать

Расстановка Коэффициентов в Химических Реакциях // Подготовка к ЕГЭ по ХимииСкачать

Как решать задачи по химии? Расчет по уравнениям химических реакций | TutorOnlineСкачать

Решение задач на термохимические уравнения. 8 класс.Скачать

Как Решать Задачи по Химии // Задачи с Уравнением Химической Реакции // Химия ПростоСкачать

Расчеты по уравнениям химических реакций. 2 часть. 8 класс.Скачать

Химия 8 класс (Урок№10 - Расчёты по уравнениям химических реакций.)Скачать

Урок 141. Количество вещества. Молярная масса. Оценка размеров молекулСкачать

7. Решение задач по химическим уравнениям. Как найти массу, объем и количество вещества по реакции?Скачать

Молярная масса. 8 класс.Скачать

8 класс. ОВР. Окислительно-восстановительные реакции.Скачать

Как решать ЗАДАЧИ ПО ХИМИИ | Типовые задачи по химии | Задачи с уравнением химической реакцииСкачать