Пищевая, или питьевая сода, — широко известное в медицине, кулинарии и бытовом потреблении соединение. Это кислая соль, молекула которой образована положительно заряженными ионами натрия и водорода, анионом кислотного остатка угольной кислоты. Химическое название соды — бикарбонат или гидрокарбонат натрия. Формула соединения по системе Хилла: CHNaO3 (брутто-формула).
- Отличие кислой соли от средней
- Физические свойства пищевой соды
- Безопасность пищевой соды для человека
- Гидрокарбонат натрия: формула соединения
- Строение вещества
- Растворимость питьевой соды в воде
- Реакция обмена с другими солями
- Взаимодействие питьевой соды с кислотами
- Получение пищевой соды
- Где используется гидрокарбонат натрия? Применение пищевой соды в медицине
- Использование пищевой соды в быту
- Как получить пищевую соду уравнение реакции
- История создания
- Способы получения
- Виды соды
- Химические свойства
- Полезные свойства
- Возможный вред
- Медицинское применение
- В стоматологии
- В гастроэнтерологии
- В кардиологии
- В дерматологии
- При ЛОР-патологиях
- Использование в кулинарии
- Применение в хозяйстве
- Для удаления запахов
- Для ухода за одеждой
- Использование в косметологии
- Для похудения
- Другие способы использования
- Использование в промышленности
- Как выбрать и хранить
- Гидрокарбонат натрия
- Содержание
- Химические свойства
- Реакция с кислотами
- Термическое разложение
- Получение
- Применение
- В химической промышленности
- В кулинарии
- В медицине
- Противопоказания к применению в медицинских целях
- Пожаротушение
- В быту
- В транспорте
- Производство
- Хранение
- Безопасность
Отличие кислой соли от средней
Угольная кислота образуют две группы солей — карбонаты (средние) и гидрокарбонаты (кислые). Тривиальное название карбонатов — соды — появилось еще в древности. Следует различать среднюю и кислую соли по названиям, формулам и свойствам.
Na2CO3 — карбонат натрия, динатриевая соль угольной кислоты, кальцинированная стиральная сода. Служит сырьем для получения стекла, бумаги, мыла, используется как моющее средство.
NaHCO3 — натрия гидрокарбонат. Состав подсказывает, что вещество является мононатриевой солью угольной кислоты. Это соединение отличается наличием двух разных положительных ионов — Na + и Н + . Внешне кристаллические белые вещества похожи, их трудно отличить друг от друга.
Вещество NaHCO3 считается питьевой содой не потому, что употребляется внутрь для утоления жажды. Хотя с помощью этого вещества можно приготовить шипучий напиток. Раствор этого гидрокарбоната принимают внутрь при повышенной кислотности желудочного сока. При этом происходит нейтрализация избытка протонов Н + , которые раздражают стенки желудка, вызывают боль и жжение.
Физические свойства пищевой соды
Бикарбонат — это белые моноклинные кристаллы. В составе этого соединения присутствуют атомы натрия (Na), водорода (Н), углерода (С) и кислорода. Плотность вещества составляет 2,16 г/см3. Температура плавления — 50–60 °С. Натрия гидрокарбонат — порошок молочно-белого цвета — твердое мелкокристаллическое соединение, растворимое в воде. Питьевая сода не горит, а при нагревании свыше 70 °С разлагается на карбонат натрия, углекислый газ и воду. В производственных условиях чаще применяется гранулированный бикарбонат.
Безопасность пищевой соды для человека
Соединение не обладает запахом, его вкус — горько-соленый. Однако не рекомендуется нюхать и пробовать вещество на вкус. Вдыхание гидрокарбоната натрия может вызвать чихание и кашель. Одно из применений основано на способности пищевой соды нейтрализовать пахнущие вещества. Порошком можно обработать спортивную обувь, чтобы избавиться от неприятного запаха.
Питьевая сода (гидрокарбонат натрия) — безвредное вещество при контакте с кожей, но в твердом виде может вызвать раздражение слизистой оболочки глаз и пищевода. В низких концентрациях раствор не токсичен, его можно принимать внутрь.
Гидрокарбонат натрия: формула соединения
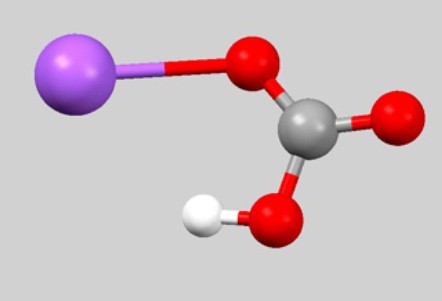
Брутто-формула CHNaO3 редко встречается в уравнениях химических реакций. Дело в том, что она не отображает связь между частицами, которые образуют гидрокарбонат натрия. Формула, обычно используемая для характеристики физических и химических свойств вещества, — NaHCO3. Взаимное расположение атомов отражает шаро-стержневая модель молекулы:
Если узнать из периодической системы значения атомных масс натрия, кислорода, углерода и водорода. то можно подсчитать молярную массу вещества гидрокарбонат натрия (формула NaHCO3):
Ar(Na) — 23;
Ar(O) — 16;
Ar(C) — 12;
Ar(H) — 1;
М (CHNaO3) = 84 г/моль.
Строение вещества
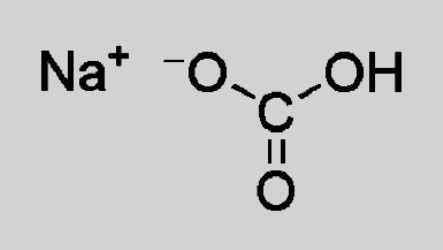
Гидрокарбонат натрия — ионное соединение. В состав кристаллической решетки входит катион натрия Na + , замещающий в угольной кислоте один атом водорода. Состав и заряд аниона — НСО3 – . При растворении происходит частичная диссоциация на ионы, которые образуют гидрокарбонат натрия. Формула, отражающая структурные особенности, выглядит так:
Растворимость питьевой соды в воде
В 100 г воды растворяется 7,8 г гидрокарбоната натрия. Вещество подвергается гидролизу:
NaHCO3 = Na + + НСО3 – ;
Н2О ↔ Н + + ОН – ;
НСО3 – + Н + = Н2О + СО2↑.
При суммировании уравнений выясняется, что в растворе накапливают гидроксид-ионы (слабощелочная реакция). Жидкость окрашивает фенолфталеин в розовый цвет. Окраска универсальных индикаторов в виде бумажных полосок в растворе соды меняется с желто-оранжевой на серую или синюю.
Реакция обмена с другими солями
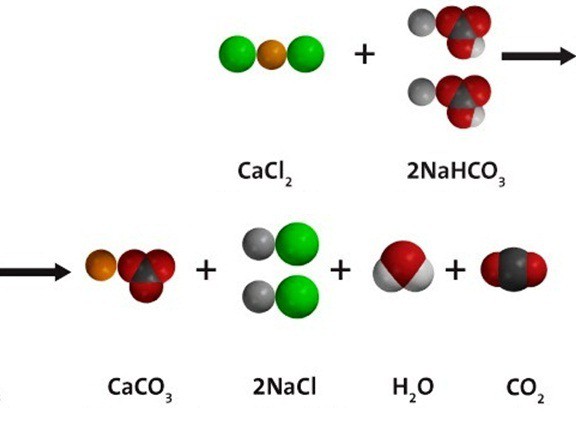
Водный раствор гидрокарбоната натрия вступает в реакции ионного обмена с другими солями при условии, что одно из вновь получившихся веществ — нерастворимое; либо образуется газ, который удаляется из сферы реакции. При взаимодействии с хлоридом кальция, как показано на схеме ниже по тексту, получается и белый осадок сарбоната кальция, и углекислый газ. В растворе остаются ионы натрия и хлора. Молекулярное уравнение реакции:
Взаимодействие питьевой соды с кислотами
Гидрокарбонат натрия взаимодействует с кислотами. Реакция ионного обмена сопровождается образованием соли и слабой угольной кислоты. В момент получения она разлагается на воду и углекислый газ (улетучивается).
Стенки желудка человека вырабатывают соляную кислоту, существующую в виде ионов
Н + и Cl – . Если принимать внутрь натрия гидрокарбонат, реакции происходят в растворе желудочного сока с участием ионов:
NaHCO3 = Na + + НСО3 – ;
HCl = Н + + Cl – ;
Н2О ↔ Н+ + ОН – ;
НСО3 – + Н + = Н2О + СО2↑.
Врачи не рекомендуют постоянно использовать при повышенной кислотности желудка гидрокарбонат натрия. Инструкция к препаратам перечисляет различные побочные действия ежедневного и длительного приема питьевой соды:
- повышение давления крови;
- отрыжка, тошнота и рвота;
- тревожность, плохой сон;
- снижение аппетита;
- боли в животе.
Получение пищевой соды
В лаборатории бикарбонат натрия можно получить из кальцинированной соды. Такой же метод применялся раньше в химическом производстве. Современный промышленный способ основан на взаимодействии аммиака с углекислым газом и слабой растворимости питьевой соды в холодной воде. Через раствор хлорида натрия пропускают аммиак и диоксид углерода (углекислый газ). Образуются хлорид аммония и раствор гидрокарбоната натрия. При охлаждении растворимость питьевой соды понижается, тогда вещество легко отделяется с помощью фильтрования.
Где используется гидрокарбонат натрия? Применение пищевой соды в медицине
Многим известно, что атомы металлического натрия энергично взаимодействуют с водой, даже ее парами в воздухе. Реакция начинается активно и сопровождается выделением большого количества теплоты (горением). В отличие от атомов, ионы натрия — стабильные частицы, не наносящие вреда живому организму. Наоборот, они принимают активное участие в регуляции его функций.
Как используется неядовитое для человека и полезное во многих отношениях вещество — гидрокарбонат натрия? Применение основано на физических и химических свойствах питьевой соды. Важнейшие направления — бытовое потребление, пищевая промышленность, здравоохранение, народная медицина, получение напитков.
Среди основных свойств бикарбоната натрия — нейтрализация повышенной кислотности желудочного сока, кратковременное устранение болевого синдрома при гиперацидности желудочного сока, язвенной болезни желудка и 12-перстной кишки. Антисептическое действие раствора питьевой соды применяется при лечении боли в горле, кашля, интоксикации, морской болезни. Промывают им полости рта и носа, слизистые оболочки глаз.
Широко используются разные лекарственные формы бикарбоната натрия, например порошки, которые растворяют и применяют для инфузий. Назначают растворы для приема пациентами внутрь, промывают ожоги кислотами. Для изготовления таблеток и ректальных суппозиториев также используется гидрокарбонат натрия. Инструкция к препаратам содержит подробное описание фармакологического действия, показаний. Список противопоказаний очень короткий — индивидуальная непереносимость вещества.
Использование пищевой соды в быту
Гидрокарбонат натрия — это «скорая помощь» при изжоге и отравлении. С помощью питьевой соды в домашних условиях отбеливают зубы, уменьшают воспаление при угревой болезни, протирают кожу для удаления избытка жирного секрета. Бикарбонат натрия смягчает воду, помогает очистить загрязнения с разных поверхностей.
При ручной стирке вещей из шерстяного трикотажа можно добавить в воду питьевую соду. Это вещество освежает цвет ткани и удаляет запах пота. Нередко при глажении изделий из шелка появляются желтые подпалины от утюга. В таком случае поможет кашица из питьевой соды и воды. Вещества надо как можно быстрее смешать и нанести на пятно. Когда кашица подсохнет, ее следует почистить щеткой, а изделие прополоскать в холодной воде.
В реакции с уксусной кислотой получается ацетат натрия и бурно выделяется углекислый газ, вспенивающий всю массу: NaHCO3 + СН3СООН = Na + + СН3СОО – + Н2О + СО2↑. Этот процесс идет всякий раз, когда при изготовлении шипучих напитков и кондитерских изделий питьевую соду «гасят» уксусом.
Вкус выпечки будет нежнее, если использовать не магазинный синтетический уксус, а сок лимона. На крайний случай можно заменить его смесью 1/2 ч. л. порошка лимонной кислоты и 1 ст. л. воды. Питьевая сода с кислотой добавляется в тесто в числе последних ингредиентов, чтобы можно было сразу ставить выпечку в духовку. Кроме бикарбоната натрия, иногда в качестве разрыхлителя используется гидрокарбонат аммония.
Как получить пищевую соду уравнение реакции

История создания
Пищевую соду в хлебопечении использовали с древности. Она была найдена археологами при раскопках пещер І-ІІ веков до н.э. Тогда ее добывали из золы морских водорослей или находили в виде минерала. Это химическое соединение активно использовали в древнем Египте.
Впервые химическая формула соединения — NaHCO3— была установлена ученым-французом Анри де Монсо. Благодаря этому открытию, пищевую соду стали получать синтетическим путем, что значительно удешевило ее стоимость и расширило спектр использования. С момента открытия формулы способы ее синтеза постоянно менялись, совершенствовались, становились экономически выгоднее.
Способы получения
Первый способ промышленного получения карбоната натрия заключался в растворении каменной соли в воде, смешивании раствора с известняком и древесным углем и последующим нагреванием в печи. Однако, как оказалось, на выходе получали не пищевую, а кальцинированную соду. Кроме того, в результате такой деятельности оставалось очень много токсичных отходов (сульфида кальция и хлороводорода), поэтому от него быстро отказались.
Сегодня пищевую соду производят двумя способами — «сухим» и «мокрым», в основе каждого из которых лежит реакция карбонизации (обогащения раствора углекислотой).
Виды соды
С химической точки зрения и области применения различают несколько разновидностей соды: пищевую (питьевую), кальцинированную (бельевую) и каустическую (гидроксид натрия).
Химические свойства
Гидрокарбонат натрия — это слабая кислая соль угольной кислоты. Представляет собой мелкие бесцветные кристаллы, которые при повышении температуры до 50-60°С начинают «отдавать» молекулу углекислого газа, постепенно разлагаясь до карбоната натрия (кальцинированной соды).
Реагирует с кислотами с образованием солей (хлорида, ацетата, сульфата натрия) и угольной кислоты, которая моментально расщепляется до воды и углекислоты. В воде порошок растворяется плохо и легко отделяется фильтрованием.
Полезные свойства

- кислотонейтрализующее;
- антисептическое;
- противовоспалительное;
- противозудное;
- подсушивающее;
- противогрибковое;
- разжижающее мокроту;
- смягчающее и отбеливающее кожу.
Такое множество полезных свойств позволяет использовать это соединение в народной и традиционной медицине для лечения многих заболеваний и нормализации самочувствия человека при различных патологических и физиологических состояниях.
Возможный вред
Пищевую соду следует употреблять внутрь в ограниченных количествах и по строгим показаниям. Кристаллы бикарбоната в большом количестве токсичны для слизистой органов пищеварения и могут вызвать сильное раздражение и ответные аллергические реакции.
Не рекомендуется употреблять растворы на основе гидрокарбоната натрия людям, страдающим эрозивно-язвенными процессами желудка и кишечника, пониженной кислотностью желудка и анацидным гастритом.
При регулярном вдыхании паров углекислого газа или кристаллов гидрокарбоната, например, на производстве соды, может возникать раздражение слизистой органов дыхания.
Частое употребление содового раствора грозит стойкими органическими нарушениями работы пищеварительной системы. Происходит ощелачивание желудочного сока, а также сдвиг в сильно щелочную сторону содержимого кишечника.
Медицинское применение
Гидрокарбонат натрия широко применяют в медицине. При этом соду используют в разных ее областях: дерматологии, гастроэнтерологии, кардиологии, пульмонологии, стоматологии, токсикологии, при ЛОР-патологиях. Помогает двууглекислый натрий от изжоги, тошноты, укачивания.
Это вещество применяют внутрь в виде содового напитка и наружно в сухом виде, в виде пасты или водного раствора для обтираний, примочек, ванночек.
В стоматологии

В гастроэнтерологии
При тошноте делают крепкий содовый раствор (1 ст.ложка на стакан воды) и медленно выпивают его. При сильной изжоге рекомендуется чайную ложку соды растворить в стакане воды и выпить. Таким образом, на некоторое время состояние больных улучшается. Однако, необходимо отметить, что при частых изжогах следует обратиться к врачу, а не лечиться содой дома. Привычное поступление щелочного раствора вызывает реакцию нейтрализации между соляной кислотой и содой, в результате чего выделяется много углекислого газа, который вызывает вздутие. Образовашаяся углекислота раздражает химиорецепторы желудка, стимулируя тем самым рефлекторное усиление образования желудочного сока.
В кардиологии
Гидрокарбонатные ванны способствуют нормализации артериального давления и сердцебиения, что полезно при перебоях в работе сердца и сосудов. Сода способствует усилению мочеотделения, чем уменьшает общий объем циркулирующей крови. Как результат уменьшается давление кровяного столба на стенки сосудов и немного падает артериальное давление.
Прием раствора гидрокарбоната натрия внутрь при резком повышении кровяного давления является средством первой помощи при гипертоническом кризе в домашних условиях. Если выпить содовый напиток вместе с гипотензивными лекарствами, эффект усилится .
В дерматологии
Мыльно-содовые ванночки и аппликации помогают избавиться от грибкового поражения ногтей, а также от мозолей и натоптышей. Пастой из пищевой соды и воды нужно обрабатывать места ожогов кожи при воздействии на нее кислот, а также участки кожи с солнечными ожогами. Смачивать водой с растворенной в ней содой нужно места укусов комаров и других насекомых на коже. При сильном зуде можно посыпать кожу сухим порошком.
При проблемах с запахом пота, содовым раствором следует обработать подмышки. Бактерии и грибки, которые размножаются в поте, продуцируют кислоты, вызывающие неприятный запах, погибнут. Гидрокарбонат натрия нейтрализует эти кислоты и проявляет умеренный антисептический эффект.
Ванночки для ног на основе гидрокарбоната делают при грибковых заболеваниях ступней и ногтей. Они также помогают смягчить загрубевшую кожу пяток перед педикюром. Горячие ванночки из крепкого раствора пищевой соды помогают при панариции (гнойном воспалении под ногтем).
При ЛОР-патологиях
Гидрокарбонат натрия при попадании в вязкую мокроту, реагирует с кислотами, содержащимися в ней. Образовавшиеся пузырьки углекислого газа и вода разжижают мокроту, увеличивают ее количество и облегчают откашливание.
Для приготовления отхаркивающего средства при трахеитах, ларингитах, бронхитах, а также при сильном кашле чайную ложку пищевой соды разводят в 200 мл теплого молока. Этот эликсир пьют перед сном. Вместо такого напитка можно делать паровые ингаляции с содой. Столовую ложку порошка разводят в литре горячей воды и дышат над ней. Для усиления эффекта в раствор можно добавить несколько капель эфирных масел эвкалипта, сосны или розмарина. Полосканиями горла раствором из соли и соды снимают воспаление гланд при ангине.
Внутривенное введение стерильного водного раствора натрия гидрокарбоната часто применяют в реанимации, инфекционных отделения и токсикологии при отравлениях, интоксикациях. метаболическом ацидозе.
Использование в кулинарии

Добавление ее в блюда из бобовых позволяет сократить время их приготовления. Если использовать соду в маринаде для мяса, можно смягчить жесткие мышечные волокна. Ягодные и фруктовые муссы при добавлении в них щепотки соды становятся слаще, а кофе и чай — более прозрачными и ароматными.
Для того чтобы избавиться от нитратов в овощах, их нужно замочить в содовом растворе. Потемневший картофель можно осветлить этим же способом.
Применение в хозяйстве
Незаменимо вещество и в быту. Оно является отличным чистящим средством. Хромированные изделия и столовое серебро для возвращения им блеска натирают сухой содой, промывают мыльной водой, а затем протирают насухо мягкой ветошью.
Порошок гидрокарбоната натрия, нанесенный на увлажненную губку, устраняет царапины и потертости на половых покрытиях из винила. Кафельную плитку, кухонную плиту, мойку и сантехнику можно очистить от загрязнений, обработав густой смесью соды и воды. Эта же смесь помогает избавиться от специфического кошачьего запаха в местах, где были «метки».
Для удаления запахов
Хорошая гигроскопичность двууглекислого натрия является причиной того, что он быстро впитывает ароматы, поэтому его можно использовать для устранения различных запахов. Чтобы избавиться от неприятных запахов в холодильнике, нужно насыпать сухой порошок в стакан и поставить его в дверцу холодильника. Меняя содержимое стакана по мере необходимости (раз в 1-2 месяца), можно навсегда избавиться от специфического «холодильного» запаха.
При устойчивом запахе кислого молока «пахнущие» емкости нужно почистить сухим порошком. Аналогично поступают с посудой, имеющей запах рыбы.
Если засыпать несколько столовых ложек порошка в сливное отверстие, а через несколько минут включить теплую воду, можно устранить неприятный запах из сифона под раковиной.
Питьевая сода поможет справиться также с неприятным запахом от ковра. Для этого ковер посыпают порошком, оставляют на 20-30 минут, а затем тщательно пылесосят. Однако такой способ подходит только для нелиняющих ковров.
С помощью пищевой соды можно также предупредить появление неприятных запахов, например, из стиральной или посудомоечной машины при их длительном простое. Уезжая на длительное время из дома, следует натереть сухим гидрокарбонатом внутреннюю поверхность машинок и оставить их дверцы приоткрытыми, а после возвращения — запустить их в режиме ополаскивания.
Для ухода за одеждой
Во время машинной стирки хорошо будет добавить в стиральный порошок соду. Это поможет избавиться от неприятного запаха в стиральной машинке, улучшит качество стирки и аромат выстиранного белья. Неприятно пахнущую одежду можно выстирать в машинке, обильно посыпав ее содой.
Мокрый купальник не заплесневеет и не будет неприятно пахнуть, если после купания в бассейне или в природном водоеме его сложить в пакет с содой, а дома хорошенько выполоскать и высушить.
Использование в косметологии

Для похудения
Гидрокарбонат натрия применяют также для похудения. Чтобы потерять до 2 кг за одну процедуру, можно наполнить ванну теплой водой и растворить в ней 0,5 кг морской соли и 0,3 кг обычной питьевой соды. Худеющему нужно погрузиться в такую ванну на 20 минут. При этом температура воды должна быть около 40°С. Содово-солевой раствор расслабляет мышцы, снимает усталость и нервное напряжение, очищает лимфатические сосуды, уменьшает отечность тканей. После ванной обтираться не следует: достаточно надеть теплый халат. Делать такие водные процедуры лучше перед сном.
Другие способы использования
Незаменима сода в походах. Ею можно:
- мыть посуду, не нанося вреда окружающей среде;
- заменить зубную пасту;
- затушить костер;
- смазать кожу в местах укуса насекомых.
Избавиться от неприятного запаха от обуви можно, если ее изнутри натереть сухой содой или смачивать содовым раствором. Смесь бикарбоната натрия и сахара устребляет тараканов.
Использование в промышленности
Питьевую соду в качестве пищевой добавки Е500 использует пищевая промышленность в изготовлении хлебобулочных, мучных, кондитерских, колбасных изделий, газированных напитков, а также для очистки промышленного оборудования.
Химическая промышленность использует гидрокарбонат натрия в производстве красителей, реактивов, средств бытовой химии, пенопластов. Бикарбонатом наполняют порошковые огнетушители.
В легкой промышленности соду применяют в кожевенном производстве, для изготовления искусственной кожи, шелковых и хлопковых тканей.
Как выбрать и хранить
Натрия гидрокарбонат должен храниться в закрытых пачках, чтобы не накапливать посторонних запахов. Перед покупкой необходимо встряхнуть пачку с содой. Если из нее посыплется мелкая пыль, это признак залежалости продукта и частичного распада соединения внутри пачки. Дома следует сразу же пересыпать порошок в герметичную емкость.
Храниться сода должна в сухих вентилируемых помещениях, вдали от сильно пахнущих продуктов. Температура хранения не ограничивается, однако нужно помнить, что чем она выше, тем быстрее продукт теряет свои свойства. Гарантийным сроком хранения является 12 месяцев, но если сода хранилась правильно и не утратила своей реактивности, срок ее годности не ограничен.
Проверить реактивность гидрокарбоната можно простым способом: при гашении щепотки соды уксусом будет образовываться пена из пузырьков газа.
Расширив спектр применения соды в домашнем хозяйстве, каждая хозяйка может сэкономить свой бюджет и открыть для себя много экологически чистых и гипоаллергенных средств для уборки, стирки и многого другого.
- Яковец Ю. С., Куприна А. В. – Сода в жизни человека // Юный ученый. — 2019 г.
- Даников Н. И. – Целебная сода. – Эксмо-Пресс, 2013 г. – 330 с.
Больше свежей и актуальной информации о здоровье на нашем канале в Telegram. Подписывайтесь: https://t.me/foodandhealthru
Специальность: инфекционист, гастроэнтеролог, пульмонолог .
Общий стаж: 35 лет .
Образование: 1975-1982, 1ММИ, сан-гиг, высшая квалификация, врач-инфекционист .
Гидрокарбонат натрия
| Гидрокарбонат натрия | |
|---|---|
 | |
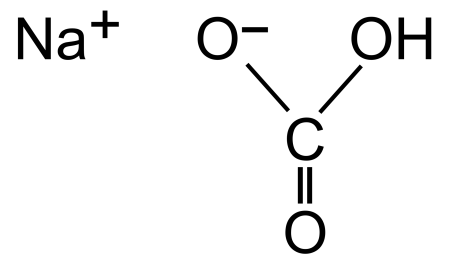 | |
| Систематическое наименование | гидрокарбонат натрия |
| Традиционные названия | пищевая (питьевая) сода, сода двууглекислая, двууглекислый натрий, бикарбонат натрия, кислый углекислый натрий |
| Хим. формула | CHNaO₃ |
| Рац. формула | NaHCO3 |
| Состояние | твёрдое |
| Молярная масса | 84,0066 г/моль |
| Плотность | 2,159 г/см³ |
| Т. разл. | 60—200 °C |
| Растворимость в воде | 9,59 г/100 мл |
| ГОСТ | ГОСТ 2156-76 ГОСТ 4201-79 ГОСТ 32802-2014 |
| Рег. номер CAS | 144-55-8 |
| PubChem | 516892 |
| Рег. номер EINECS | 205-633-8 |
| SMILES | |
| Рег. номер EC | 205-633-8 |
| Кодекс Алиментариус | E500(ii) |
| RTECS | VZ0950000 |
| ChEBI | 32139 |
| ChemSpider | 8609 |
| ЛД50 | 4220 мг/кг |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Гидрокарбонат натрия (лат. Natrii hydrocarbonas ), другие названия: бикарбонат натрия, чайная сада, питьевая или пищевая сода, двууглекислый натрий — неорганическое соединение, натриевая кислая соль угольной кислоты с химической формулой NaHCO3.
В обычном виде — мелкокристаллический порошок белого цвета.
Используется в промышленности, пищевой промышленности, в кулинарии, в медицине как нейтрализатор химических ожогов кожи и слизистых оболочек концентрированными кислотами и для снижения кислотности желудочного сока. Также применяется в буферных растворах.
Содержание
- 1 Химические свойства
- 1.1 Реакция с кислотами
- 2 Термическое разложение
- 3 Получение
- 4 Применение
- 4.1 В химической промышленности
- 4.2 В кулинарии
- 4.3 В медицине
- 4.3.1 Противопоказания к применению в медицинских целях
- 4.4 Пожаротушение
- 4.5 В быту
- 4.6 В транспорте
- 5 Производство
- 6 Хранение
- 7 Безопасность
Химические свойства
Гидрокарбонат натрия — кислая натриевая соль угольной кислоты. Проявляет все свойства соли сильного основания и слабой кислоты. В водных растворах имеет слабощелочную реакцию. В широком диапазоне концентраций в водном растворе pH раствора изменяется незначительно, на этом основано применение раствора вещества в качестве буферного раствора.
Реакция с кислотами
Гидрокарбонат натрия реагирует с кислотами с образованием соответствующей кислоте соли, например, хлорида натрия, сульфата натрия и угольной кислоты, которая в процессе реакции распадается на углекислый газ и воду, при этом углекислый газ выделяется из раствора в виде пузырьков:
В быту обычно применяется реакция «гашения соды» уксусной кислотой, с образованием ацетата натрия или гашение лимонной кислотой с образование цитрата натрия, реакция с уксусной кислотой:
Термическое разложение
При температуре выше 60 °C гидрокарбонат натрия начинает распадаться на карбонат натрия, углекислый газ и воду (процесс разложения наиболее эффективен при 200 °C, при более высоких температурах карбонат натрия начинает распадаться на оксид натрия и углекислый газ):
При этом процессе выделения воды в виде водяного пара и углекислого газa масса исходного продукта уменьшается примерно на 37 %.
Получение
В промышленности гидрокарбонат натрия получают аммиачно-хлоридным способом. В концентрированный раствор хлорида натрия, насыщенный аммиаком, под давлением пропускают углекислый газ. В процессе синтеза происходят две реакции:
В холодной воде гидрокарбонат натрия мало растворим, и его отделяют от охлаждённого раствора фильтрованием, а из полученного после фильтрования раствора хлорида аммония снова получают аммиак, возвращаемый в производство вновь:
Применение
Двууглекислый натрий (бикарбонат) применяется в химической, пищевой, лёгкой, медицинской, фармацевтической промышленности, цветной металлургии, в быту. Зарегистрирован в качестве пищевой добавки E500 (ii), входит в состав пищевой добавки E500.
В химической промышленности
Применяется для производства красителей, пенопластов и других органических продуктов, фторорганических соединений, продуктов бытовой химии, наполнителей в огнетушителях, Реагент для отделения диоксида углерода, сероводорода из газовых смесей, например, отходящих газов топливосжигающих установок. В этом процессе углекислый газ поглощается раствором гидрокарбоната натрия при повышенном давлении и пониженной температуре, далее поглощённый углекислый газ выделяется из раствора при подогреве и снижении давления;
В лёгкой промышленности — в производстве резины для подошв обуви и в производстве искусственных кож, кожевенном производстве при дублении и нейтрализации кожи после кислого дубления, текстильной промышленности при отделке шёлковых и хлопчатобумажных тканей;
В пищевой промышленности — в хлебопечении, производстве кондитерских изделий, приготовлении газированных напитков.
В кулинарии
Основное применение пищевой соды в пищевой промышленности и в быту — кулинария, где применяется, преимущественно, в качестве основного или дополнительного разрыхлителя в составе кислого и пресного теста. При добавлении питьевой соды в кислое тесто происходит реакция с молочной кислотой, продуцированной при заквашивании дрожжевыми микроорганизмами, при этой реакции выделяется углекислый газ, вспучивающий тесто.
При добавлении в пресное тесто углекислый газ выделяется при выпечке из-за термического разложения.
При применении соды в чистом виде важно соблюсти правильную дозировку, так как она оставляет в продукте карбонат натрия, дающий определённый привкус. Порядок замешивания для теста: соду — в муку, кислые компоненты (уксус, кефир и пр.) — в жидкость.
В медицине
Традиционно раствор питьевой соды используется для дезинфекции зубов и дёсен при зубных болях и полости рта и горла, при сильном кашле, ангине, фарингите, а также как общепринятое средство от изжоги и болей в желудке.
Применяется при заболеваниях, сопровождающиеся выраженным ацидозом (при диабете, инфекциях и др), для борьбы с ацидозом при хирургических вмешательствах (назначается 3-5 г. внутрь).
Применяется в качестве антиаритмического средства.
Как антацидное средство (как и все другие щелочи) применяется при язвенной болезни желудка, и двенадцатиперстной кишки, при повышенной кислотности желудочного сока.
Имеются так же данные о применении препарата (в виде капельных и внутривенных вливаний) при гипертонической болезни, симптоматической почечной гипертонии, и хронической почечной недостаточности. Эффект связан с увеличением выделения ионов натрия и хлора и возрастанием осмотического диуреза.
В виде свечей применяется против укачивания при морской и воздушной болезнях
Применяется в качестве отхаркивающего средства, т.к. повышая щелочные резервы крови, сдвигает в щелочную сторону реакцию бронхиальной слизи, делая мокроту менее вязкой.
При ринитах, конъюнктивитах, стоматитах, ларингитах и т.п. применяют для полосканий, промываний, ингаляций 0,5 — 2% р-ры гидрокарбоната натрия.
Применяется внутривенно с целью быстрого устранения метаболического ацидоза во время реанимационных мероприятий, заболеваниях почек.
Нужно иметь ввиду, что в результате применения может возникнуть т.н. кислотный рикошет (при реакции содой с соляной кислотой происходит выделение CO2, который оказывает раздражающее действие на стенку желудка, усиливая выделение гастрина).
В альтернативной медицине питьевая сода иногда заявляется как «лекарство» от рака, однако, никакой экспериментально подтверждённой эффективности применения такого «лечения» не существует.
Противопоказания к применению в медицинских целях
Индивидуальная гиперчувствительность; состояния, сопровождающиеся развитием алкалоза; гипокальциемия, при приеме внутрь усиливает алкалоз и повышает риск развития тетанических судорог, гипохлоремия — снижение концентрации в крови ионов Cl — , в том числе вызванная рвотой, или снижением всасывания в желудочно-кишечном тракте, может привести к тяжёлому алкалозу.
Является источником натрия, тем самым увеличивая объём циркулирующей крови, усугубляя отёки и повышая артериальное давление. Применение при сниженной скорости клубочковой фильтрации может привести к метаболическому алкалозу.
Пожаротушение
Гидрокарбонат натрия вместе с карбонатом аммония используется в качестве наполнителя в огнетушителях с сухим наполнением и в стационарных системах сухого пожаротушения. Это применение обусловлено тем, что от воздействия высокой температуры в очаге горения вещество выделяет углекислый газ, атмосфера которого затрудняет доступ кислорода воздуха в очаг горения.
В быту
Применяется как безопасное для здоровья средство для чистки поверхностей столовой и кухонной посуды, поверхностей кухонных столов, иных поверхностей, соприкасающихся с пищей, путем протирки их с помощью влажной тряпки с сухим порошком питьевой соды.
В транспорте
Применяется для нейтрализации следов электролита — серной кислоты на поверхности пластмассовых корпусов свинцовых аккумуляторов насыщенным водным раствором питьевой соды.
Производство
В Российской Федерации двууглекислый натрий выпускается в соответствии с требованиями и техническими условиями, выпускается на предприятиях АО «Башкирская содовая компания» в г. Стерлитамак, Республика Башкортостан, а также на Крымском содовом заводе в г. Красноперекопск, Крымский полуостров.
Хранение
Гидрокарбонат натрия хранят в закрытых упаковках, в сухом месте вдали от источников огня. Гарантийный срок хранения натрия двууглекислого — 12 месяцев со дня изготовления. Срок годности не ограничен.
Безопасность
Вещество нетоксично, пожаро- и взрывобезопасно.
Имеет солоноватый, мыльный вкус. При попадании пыли вещества на слизистые оболочки глаз и носа вызывает лёгкое раздражение. При частой работе в атмосфере, загрязнённой пылью двууглекислого натрия, может возникнуть раздражение верхних дыхательных путей. Предельно допустимая концентрация пыли бикарбоната натрия в воздухе производственных помещений 5 мг/м 3 .
- ГОСТ 2156-76. Натрий двууглекислый. Технические условия (с Изменениями № 1, 2, 3, 4).
- ГОСТ 32802-2014. Добавки пищевые. Натрия карбонаты E500. Общие технические условия.