Нитрат кальция Ca(NO3)2 — соль щелочного металла кальция и азотной кислоты. Белый, при нагревании разлагается. Хорошо растворяется в воде (гидролиза нет).
Относительная молекулярная масса Mr = 164,09; относительная плотность для тв. и ж. состояния d = 2,36; tпл = 561º C (разлагается).
- Способ получения
- Качественная реакция
- Химические свойства
- Нитрат кальция ГОСТ 4142-77
- Содержание
- Свойства
- Физические свойства
- Химические свойства
- Получение
- Реакции с получением нитрата кальция
- Применение
- В сельском хозяйстве
- В пиротехнике
- При получении сульфата кальция из 82г нитрата кальция получили 61?
- Получите тремя способамти : сульфат кальция?
- Масса сульфата кальция полученного при взаимодействии гидроксида кальция серной кислотой?
- Напиши уравнение реакцией, с помощью которых можно осуществить цепочку превращений веществ : А) Кальций — Оксид Кальция — Гидроксид кальция — Нитрат кальция — Карбонат кальция — Оксид кальция — Силика?
- При сгорании 12 г кальция получим оксид кальция?
- Определите массу гидроксида кальция полученного при взаимодействии 4г кальция с водой?
- Найти массу кальция необходимого для получения 5, 6г оксида кальция?
- Для получения нитрата кальция обработали карбонатом кальция массой 1 тонна получили 85% выхода теоретически возможного найти массу нитрата кальция?
- Рассчитаеть массу оксида кальция необходимого для получение 37Г Гидроксида кальция?
- Составить формулы — нитратов, сульфатов, фосфатов калия, кальция, хрома3?
- Сульфат калия и нитрат кальция реакция ионного обема?
Способ получения
1. Нитрат кальция можно путем взаимодействия кальция и разбавленной азотной кислоты, образуется нитрат кальция, оксид азота (I) и вода:
если кальций будет взаимодействовать с очень разбавленной азотной кислотой , то на выходе будет образовываться нитрат кальция, нитрат аммония и вода:
2. В результате взаимодействия сульфида кальция и концентрированной азотной кислоты образуется нитрат кальция, сера, оксид азота (IV) и вода:
Качественная реакция
Качественная реакция на нитрат кальция — взаимодействие с медью при нагревании в присутствии концентрированной кислоты:
1. При взаимодействии с серной кислотой и медью, нитрат кальция образует сульфат кальция, нитрат меди, бурый газ оксид азота и воду:
Химические свойства
1. Hитрат кальция разлагается при температуре 450 — 500º С с образованием нитрита кальция и кислорода:
а если температуре поднимется выше 561 о С, то на выходе реакции будут образовываться оксид кальция, оксид азота (IV) и кислород:
2. Нитрат кальция реагирует с простыми веществами :
2.1. Нитрат кальция вступает в реакцию с атомным водородом (цинком и в присутствии соляной кислоты). В результате реакции образуется нитрат кальция и вода :
3. Возможны реакции между нитратом кальция и сложными веществами :
Нитрат кальция вступает в реакцию с cолями :
В результате реакции между нитратом кальция и гидрофосфатом натрия при кипении образуется фосфат кальция, азотная кислота и нитрат натрия:
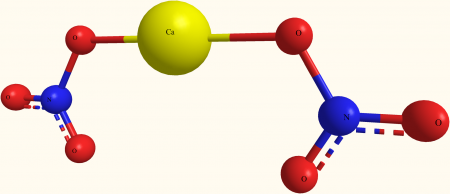
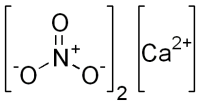
Нитрат кальция ГОСТ 4142-77
| Нитрат кальция | |
|---|---|
 | |
 | |
 | |
| Традиционные названия | кальциевая селитра, норвежская селитра, азотнокислый кальций |
| Хим. формула | Ca(NO3)2 |
| Состояние | гранулы сферической формы белого, светло-серого, светло-бежевого цвета |
| Молярная масса | |
| Т. всп. | негорючая °C |
| Мол. теплоёмк. | 149,33 Дж/(моль·К) |
| Энтальпия образования | -937,2 кДж/моль |
| Растворимость в воде | Безводной: 121,2 г/100 мл (20 °C); 271,0 г/100 мл (40 °C); 359 г/100 мл (51,6 °C). Тетрагидрата: 102 г/100 мл (0 °C); 129 г/100 мл (20 °C); (100 °C) 363 г/100 мл |
| Растворимость в | спирте и ацетоне |
| Кристаллическая структура | |
| Рег. номер CAS | |
| PubChem | 24963 |
| Рег. номер EINECS | 233-332-1 |
| SMILES | |
| RTECS | EW2985000 |
| ChEBI | 64205 |
| Номер ООН | 1454 |
| ChemSpider | 23336 и 21500286 |
| ГОСТ | ГОСТ 4142-77 |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
Кальция нитрат (кальциевая селитра, азотнокислый кальций) — неорганическая соль азотной кислоты. Соединение сильно гигроскопично, поэтому его хранят без доступа влаги. Химическая формула Ca(NO3)2.
Содержание
- 1 Свойства
- 1.1 Физические свойства
- 1.2 Химические свойства
- 2 Получение
- 2.1 Реакции с получением нитрата кальция
- 3 Применение
- 3.1 В сельском хозяйстве
- 3.2 В пиротехнике
Свойства
Физические свойства
Химические свойства
При 500 °C начинает разлагаться с выделением O2 и образованием сначала Ca(NO2)2, а затем CaO и NO2. Кальциевая селитра при нормальных условиях негорючая, пожаро- и взрывобезопасная, устойчивая в интервале температур от −60 °C до +155 °C.
Получение
Получают кальция нитрат действием HNO3 на известняк или поглощением нитрозных газов (в основном NO2) известковым молоком. Применяют кальция нитрат как азотное удобрение и для получения особо чистого CaO.
Для получения гранулированной кальциевой селитры используется способ низкотемпературной нейтрализации азотной кислоты природным известняком или продуктами переработки известняка.
Реакции с получением нитрата кальция
Нитрат кальция производится путём обработки известняка с азотной кислотой, после нейтрализации аммиака:
Он также является побочным продуктом процесса Оддо при добыче фосфата кальция:
Так же как нитраты других щелочноземельных металлов и LiNO3, кальциевая селитра при нагревании разлагается на выпуске диоксида азота:
Также нитрат кальция можно получить проделав следующие реакции:
Также образование нитрата кальция возможно и за счет атмосферных явлений:
Применение
Гранулированный, безводный нитрат кальция, применяется как добавка в бетон, в качестве удобрения, для приготовления рассола в холодильной технике, в производстве реактивов, стеклопластиков, а также как один из компонентов для производства взрывчатки.
В сельском хозяйстве
Нитрат кальция является физиологическим щелочным удобрением, пригодным для всех почв и прежде всего для закисленных почв. В сельском хозяйстве применяют как азотное удобрение. Выпускают в гранулированном виде; товарный продукт должен содержать не менее 15,5 % азота, кроме того, к нему добавляют в процессе производства 4—7 % нитрата аммония для уменьшения гигроскопичности удобрения; содержание влаги не должно превышать 15 %. Нитрат кальция вносят под все культуры. Наиболее эффективен на кислых почвах, особенно для весенней подкормки озимых.
В пиротехнике
Несмотря на то, что нитрат кальция в смеси с горючими веществами способен давать недорогой источник кирпично-красного пламени, применение его в этом качестве крайне ограничено из-за сильной гигроскопичности.
При получении сульфата кальция из 82г нитрата кальция получили 61?
Химия | 5 — 9 классы
При получении сульфата кальция из 82г нитрата кальция получили 61.
2г сульфата кальция.
Сколько % составит полученная масса от теоретически возможной.
M(Ca(NO3)2) = 164 г / моль
n(Ca(NO3)2) = m / M = 82 г / 164 г / моль = 0, 5 моль
M(CaSO4) = 136 г / моль
CaSO4) = m / M = 61, 2 г / 136 г / моль = 0, 45 моль
Сa(NO3)2 + CuSO4 = CaSO4↓ + Cu(NO3)2
Из УХР следует, что n(теор.
CaSO4) = n(Ca(NO3)2) = 0, 5 моль
CaSO4) * 100% = 0, 45 / 0, 5 * 100% = 90%
m(практ CaSO4) = 61.
Ca(NO3)2 + H2SO4 — — >CaSO4 + 2HNO3 164 136
M(Ca(NO3)2 = 164 g / mol M(CaSO4) = 136 g / mol
X = 82 * 136 / 164 = 68 g
η = m(теор) / m(практ) * 100%
Получите тремя способамти : сульфат кальция?
Получите тремя способамти : сульфат кальция.
Масса сульфата кальция полученного при взаимодействии гидроксида кальция серной кислотой?
Масса сульфата кальция полученного при взаимодействии гидроксида кальция серной кислотой.
Найдите массу сульфата кальция.
Напиши уравнение реакцией, с помощью которых можно осуществить цепочку превращений веществ : А) Кальций — Оксид Кальция — Гидроксид кальция — Нитрат кальция — Карбонат кальция — Оксид кальция — Силика?
Напиши уравнение реакцией, с помощью которых можно осуществить цепочку превращений веществ : А) Кальций — Оксид Кальция — Гидроксид кальция — Нитрат кальция — Карбонат кальция — Оксид кальция — Силикат кальция Б) Магний — Оксид магния — Хлорид магния — Нитрат магния — Оксид Магния — Ортофосфат магния В) Кальций — Гидроксид кальция — Карбонат кальция — Гидрокарбонат кальция — Карбонат кальция — Оксид кальция Г) Магний — Нитрат магния — Сульфат магния — Гидроксид магния — Оксид магния — Магний Д) Барий — Гидроксид Бария — Карбонат бария — Нитрат бария — Сульфат бария.
При сгорании 12 г кальция получим оксид кальция?
При сгорании 12 г кальция получим оксид кальция.
Определить массу полученного СаО.
Определите массу гидроксида кальция полученного при взаимодействии 4г кальция с водой?
Определите массу гидроксида кальция полученного при взаимодействии 4г кальция с водой.
Найти массу кальция необходимого для получения 5, 6г оксида кальция?
Найти массу кальция необходимого для получения 5, 6г оксида кальция.
Для получения нитрата кальция обработали карбонатом кальция массой 1 тонна получили 85% выхода теоретически возможного найти массу нитрата кальция?
Для получения нитрата кальция обработали карбонатом кальция массой 1 тонна получили 85% выхода теоретически возможного найти массу нитрата кальция.
Рассчитаеть массу оксида кальция необходимого для получение 37Г Гидроксида кальция?
Рассчитаеть массу оксида кальция необходимого для получение 37Г Гидроксида кальция.
Составить формулы — нитратов, сульфатов, фосфатов калия, кальция, хрома3?
Составить формулы — нитратов, сульфатов, фосфатов калия, кальция, хрома3.
Сульфат калия и нитрат кальция реакция ионного обема?
Сульфат калия и нитрат кальция реакция ионного обема.
На этой странице находится ответ на вопрос При получении сульфата кальция из 82г нитрата кальция получили 61?, из категории Химия, соответствующий программе для 5 — 9 классов. Чтобы посмотреть другие ответы воспользуйтесь «умным поиском»: с помощью ключевых слов подберите похожие вопросы и ответы в категории Химия. Ответ, полностью соответствующий критериям вашего поиска, можно найти с помощью простого интерфейса: нажмите кнопку вверху страницы и сформулируйте вопрос иначе. Обратите внимание на варианты ответов других пользователей, которые можно не только просмотреть, но и прокомментировать.
Ответ металлическая связь, т. К. представленны простые металлы и щелочноземельных металлов.
Это строение электронной оболочки Пример, возьмём Фосфор (P) Мы должны расписать что это за элемент такой, то есть Наверху пишем относительную атомную массу(31) Внизу пишем порядковый номер(15) Выглядит так : 31 P 15 И у элемента есть свои орбитали(о..
Формулы алканов : о, п Алкенов : з Алкины : а, м Алкадиены : н Спирты : р, е Простые эфиры : л В — ва оканчивающие на аль : д Кетоны : т Сложные эфиры : к Карбоновая кислота : c.
H2 + Cl2 = 2HCl V(HCl) = n * Vm n(Cl2) = V / Vm = 40 : 22, 4 = 1, 79 моль Составим пропорцию : 1. 79 : 1 = х : 2 ; х = 1. 79 * 2 : 1 = 3. 58 n (HCl) = 3, 58 моль V (HCl) = 3. 58×22. 4 = 80. 192 л Ответ. V (HCl) = 80. 192 л.
40 К МАЮТЬ НУКЛИДЫ КАЛИЯ.
Решение смотри на фото.
Неспелые фрукты изобилуют органическими кислотами и бедны сахарами. При созревании количество кислот уменьшается незначительно, но сильно возрастает доля сахаров, поэтому они становятся слаще. Для фруктов и ягод важно не только содержание сахаров, ..
M(H₂O) = 45 г m(NaCl) = 5 г масса раствора m(p) = m(H₂O) + m(NaCl) концентрация соли w(NaCl) = m(NaCl) / m(p) = m(NaCl) / w(NaCl) = 5 / (45 + 5) = 0, 10 (10%).














