| Хлорат натрия | |
|---|---|
 | |
| Систематическое наименование | Хлорат натрия |
| Традиционные названия | Хлорноватокислый натрий |
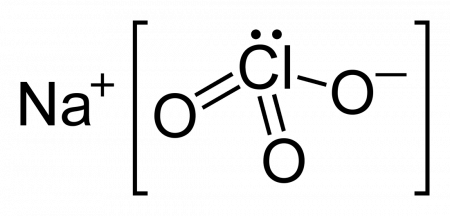
| Хим. формула | NaClO3 |
| Состояние | бесцветные кристаллы |
| Молярная масса | 106,44 г/моль |
| Плотность | 2,490; 2,493 г/см³ |
| Температура | |
| • плавления | 255; 261; 263 °C |
| • кипения | разл. 390 °C |
| Мол. теплоёмк. | 100,1 Дж/(моль·К) |
| Энтальпия | |
| • образования | -358 кДж/моль |
| Растворимость | |
| • в воде | 100,5 25 ; 204 100 г/100 мл |
| • в этилендиамине | 52,8 г/100 мл |
| • в диметилформамиде | 23,4 г/100 мл |
| • в моноэтаноламине | 19,7 г/100 мл |
| • в ацетоне | 0,094 г/100 мл |
| Рег. номер CAS | 7775-09-9 |
| PubChem | 516902 |
| Рег. номер EINECS | 231-887-4 |
| SMILES | |
| RTECS | FO0525000 |
| ChEBI | 65242 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Хлорат натрия — неорганическое соединение, соль металла натрия и хлорноватой кислоты с формулой NaClO3, бесцветные кристаллы, хорошо растворимые в воде.
Содержание
- 1 Получение
- 2 Физические свойства
- 3 Химические свойства
- 4 Применение
Получение
- Хлорат натрия получают действием хлорноватой кислоты на карбонат натрия:
Na2CO3 + 2HClO3 → 2NaClO3 + H2O + CO2↑
- или пропуская хлор через концентрированный раствор гидроксид натрия при нагревании:
6 NaOH + 3 Cl2 → NaClO3 + 5 NaCl + 3H2O
- Электролиз водных растворов хлорида натрия:
6 NaCl + 3H2O → e− NaClO3 + 5 NaCl + 3H2↑
Физические свойства
Хлорат натрия — бесцветные кристаллы кубической сингонии, пространственная группа P 213, параметры ячейки a = 0,6568 нм, Z = 4.
При 230-255°С переходит в другую фазу, при 255-260°С переходит в моноклинную фазу.
Хлорид натрия: способы получения и химические свойства
Хлорид натрия NaCl — соль щелочного металла натрия и хлороводородной кислоты. Белое кристаллические вещество. Плавится и кипит без разложения. Умеренно растворяется в воде (гидролиза нет);
Относительная молекулярная масса Mr = 58,44; относительная плотность для ж. и тв. состояния d = 2,165; tпл = 800,8º C; tкип = 1465º C;
Способ получения
1. Хлорид натрия можно получить путем взаимодействия натрия и разбавленной хлороводородной кислоты, образуются хлорид натрия и газ водород:
2Na + 2HCl = 2NaCl + H2↑.
2. При комнатной температуре, в результате взаимодействия натрия и хлора, образуется хлорид натрия:
2Na + Cl2 = 2NaCl
3. Концентрированный раствор гидроксида натрия реагирует с концентрированным раствором хлорида аммония при кипении. При этом образуются хлорид натрия, газ аммиак и вода:
NaOH + NH4Cl = NaCl + NH3↑ + H2O
4. При взаимодействии с разбавленной и холодной хлороводородной кислотой пер окси д натрия образует хлорид натрия и пероксид водорода:
5. Разбавленная хлороводородная кислота реагирует с гидроксидом натрия . Взаимодействие хлороводородной кислоты с гидроксидом натрия приводит к образованию хлорида натрия и воды:
NaOH + HCl = NaCl + H2O
6. В результате взаимодействия сульфата натрия и хлорида бария образуется сульфат бария и хлорид натрия:
Качественная реакция
Качественная реакция на хлорид натрия — взаимодействие его с нитратом серебра, в результате реакции происходит образование белого творожного осадка:
1. При взаимодействии с нитратом серебра , хлорид натрия образует нитрат натрия и осадок хлорид серебра:
NaCl + AgNO3 = NaNO3 + AgCl↓
Химические свойства
1. Хлорид натрия вступает в реакцию со многими сложными веществами :
2.1. Хлорид натрия взаимодействует с кислотами :
2.1.1. Хлорид натрия в твердом состоянии при кипении реагирует с концентрированной серной кислотой с образованием сульфата натрия и газа хлороводорода:
а если температуру опустить до 50º С, то твердый хлорид натрия и концентрированная серная кислота образуют гидросульфат натрия и газ хлороводород:
2.2. Хлорид натрия способен вступать в реакцию обмена со многими солями :
2.2.1. Твердый хлорид натрия реагирует с концентрированной и горячей серной кислотой и твердым перманганатом калия . Взаимодействие хлорида натрия с перманганатом калия и серной кислотой приводит к образованию сульфата марганца, натрия, калия, газа хлора и воды:
2.2.2. Хлорид натрия взаимодействует с гидросульфатом натрия при температуре 450–800º C . При этом образуются сульфат натрия и хлороводородная кислота:
2.2.3. При взаимодействии холодного хлорида натрия с насыщенным нитритом серебра выделяются нитрат натрия и осадок хлорид серебра:
NaCl + AgNO2 = NaNO2 + AgCl↓
Хлорат натрия
Хлорат натрия
натрий хлорноватокислый
α= 90°
белый
Содержание
Описание
Влияние температуры
Влияние примесей
Примечания
Способ получения
Существует несколько практических способов получения.
- Диспропорционирование раствора гипохлорита натрия при нагревании (75-80°С).
Уравнение реакции:
3NaClO = NaClO3 + 2NaCl
- Электролиз насыщенного раствора хлорида натрия при высокой температуре (более 70°С).
Уравнение реакции:
- Пропускание хлора через горячий раствор гидроксида натрия. Примесь хлорида натрия отделяется перекристаллизацией.
Уравнение реакции:
6NaOH + 3Cl2 = NaClO3 + 5NaCl + 3H2O

