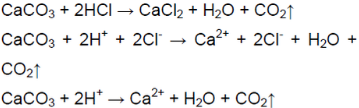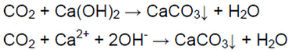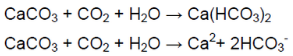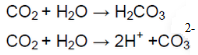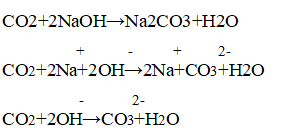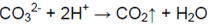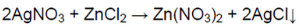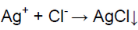- We are checking your browser. gomolog.ru
- Why do I have to complete a CAPTCHA?
- What can I do to prevent this in the future?
- Хлорид натрия: способы получения и химические свойства
- Способ получения
- Качественная реакция
- Химические свойства
- Как определить что в пробирке хлорид натрия напишите уравнение реакции в молекулярном и ионном виде
- Вопросы к параграфу 36 — ГДЗ по Химии 9 класс Учебник Рудзитис, Фельдман
- § 36. Практическая работа №6.
- Получение оксида углерода (IV). Распознавание карбонатов
- 1. Получение оксида углерода(IV) и изучение его свойств. 1) Поместите в пробирку несколько кусочков мела или мрамора и прилейте немного разбавленной соляной кислоты. Пробирку быстро закройте пробкой с газоотводной трубкой. Конец трубки поместите в другую пробирку, в которой находится 2—3 мл известковой воды. Несколько минут пропускайте выделяющийся газ через известковую воду. Что происходит, если на мел (мрамор) действуют соляной кислотой? Почему при пропускании образующегося газа через раствор известковой воды сначала происходит помутнение, а затем взвесь растворяется? 2) Конец газоотводной трубки выньте из раствора и сполосните в дистиллированной воде. Поместите трубку в пробирку с 2—3 мл дистиллированной воды и пропустите через нес выделяющийся газ. Через несколько минут выньте трубку из раствора и добавьте к нему несколько капель синего лакмуса. Что наблюдаете? 3) В пробирку налейте 2—3 мл разбавленного раствора гидроксида натрия, добавьте к нему несколько капель фенолфталеина и затем через раствор пропустите выделяющийся газ. Что наблюдаете? Напишите уравнения всех проведённых реакций в молекулярном, ионном и сокращённом ионном виде.
- 2. Распознавание карбонатов. В трех пробирках даны кристаллические вещества: сульфат натрия, хлорид цинка, карбонат калия. Определите, какое вещество находится в каждой пробирке. Сделайте вывод, что является качественной реакцией на карбонат-ионы. Напишите соответствующее уравнение реакции.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 7069b6cdae6897a6 • Your IP : 87.119.247.227 • Performance & security by Cloudflare
Хлорид натрия: способы получения и химические свойства
Хлорид натрия NaCl — соль щелочного металла натрия и хлороводородной кислоты. Белое кристаллические вещество. Плавится и кипит без разложения. Умеренно растворяется в воде (гидролиза нет);
Относительная молекулярная масса Mr = 58,44; относительная плотность для ж. и тв. состояния d = 2,165; tпл = 800,8º C; tкип = 1465º C;
Способ получения
1. Хлорид натрия можно получить путем взаимодействия натрия и разбавленной хлороводородной кислоты, образуются хлорид натрия и газ водород:
2Na + 2HCl = 2NaCl + H2↑.
2. При комнатной температуре, в результате взаимодействия натрия и хлора, образуется хлорид натрия:
2Na + Cl2 = 2NaCl
3. Концентрированный раствор гидроксида натрия реагирует с концентрированным раствором хлорида аммония при кипении. При этом образуются хлорид натрия, газ аммиак и вода:
NaOH + NH4Cl = NaCl + NH3↑ + H2O
4. При взаимодействии с разбавленной и холодной хлороводородной кислотой пер окси д натрия образует хлорид натрия и пероксид водорода:
5. Разбавленная хлороводородная кислота реагирует с гидроксидом натрия . Взаимодействие хлороводородной кислоты с гидроксидом натрия приводит к образованию хлорида натрия и воды:
NaOH + HCl = NaCl + H2O
6. В результате взаимодействия сульфата натрия и хлорида бария образуется сульфат бария и хлорид натрия:
Качественная реакция
Качественная реакция на хлорид натрия — взаимодействие его с нитратом серебра, в результате реакции происходит образование белого творожного осадка:
1. При взаимодействии с нитратом серебра , хлорид натрия образует нитрат натрия и осадок хлорид серебра:
NaCl + AgNO3 = NaNO3 + AgCl↓
Химические свойства
1. Хлорид натрия вступает в реакцию со многими сложными веществами :
2.1. Хлорид натрия взаимодействует с кислотами :
2.1.1. Хлорид натрия в твердом состоянии при кипении реагирует с концентрированной серной кислотой с образованием сульфата натрия и газа хлороводорода:
а если температуру опустить до 50º С, то твердый хлорид натрия и концентрированная серная кислота образуют гидросульфат натрия и газ хлороводород:
2.2. Хлорид натрия способен вступать в реакцию обмена со многими солями :
2.2.1. Твердый хлорид натрия реагирует с концентрированной и горячей серной кислотой и твердым перманганатом калия . Взаимодействие хлорида натрия с перманганатом калия и серной кислотой приводит к образованию сульфата марганца, натрия, калия, газа хлора и воды:
2.2.2. Хлорид натрия взаимодействует с гидросульфатом натрия при температуре 450–800º C . При этом образуются сульфат натрия и хлороводородная кислота:
2.2.3. При взаимодействии холодного хлорида натрия с насыщенным нитритом серебра выделяются нитрат натрия и осадок хлорид серебра:
NaCl + AgNO2 = NaNO2 + AgCl↓
Как определить что в пробирке хлорид натрия напишите уравнение реакции в молекулярном и ионном виде
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Вопросы к параграфу 36 — ГДЗ по Химии 9 класс Учебник Рудзитис, Фельдман
Авторы: Рудзитис Г.Е., Фельдман Ф.Г.
§ 36. Практическая работа №6.
Получение оксида углерода (IV). Распознавание карбонатов
1. Получение оксида углерода(IV) и изучение его свойств. 1) Поместите в пробирку несколько кусочков мела или мрамора и прилейте немного разбавленной соляной кислоты. Пробирку быстро закройте пробкой с газоотводной трубкой. Конец трубки поместите в другую пробирку, в которой находится 2—3 мл известковой воды. Несколько минут пропускайте выделяющийся газ через известковую воду. Что происходит, если на мел (мрамор) действуют соляной кислотой? Почему при пропускании образующегося газа через раствор известковой воды сначала происходит помутнение, а затем взвесь растворяется? 2) Конец газоотводной трубки выньте из раствора и сполосните в дистиллированной воде. Поместите трубку в пробирку с 2—3 мл дистиллированной воды и пропустите через нес выделяющийся газ. Через несколько минут выньте трубку из раствора и добавьте к нему несколько капель синего лакмуса. Что наблюдаете? 3) В пробирку налейте 2—3 мл разбавленного раствора гидроксида натрия, добавьте к нему несколько капель фенолфталеина и затем через раствор пропустите выделяющийся газ. Что наблюдаете? Напишите уравнения всех проведённых реакций в молекулярном, ионном и сокращённом ионном виде.
Поместили в пробирку несколько кусочков мела и прилили немного разбавленной соляной кислоты. Пробирку быстро закрыли пробкой с газоотводной трубкой. Конец трубки поместили в другую пробирку, в которой находится 2—3 мл известковой воды.
В результате реакции соляной кислоты с мелом выделяется углекислый газ:
Когда пропускали газ через известковую воду, она сначала мутнеет — выпадает осадок — карбонат кальция:
В ситуации избытка газа взвесь растворяется (карбонат превращается в гидрокарбонат, растворимый в воде):
Углекислый газ можно получить путём воздействия сильной кислоты на карбонат. Для его распознавания применяется известковая вода (при недостатке карбоната она мутнеет, при его избытке осадок растворяется).
Конец газоотводной трубки вынули из раствора и сполоснули в дистиллированной воде. Поместили трубку в пробирку с 2—3 мл дистиллированной воды и пропустили через нес выделяющийся газ. Через несколько минут вынули трубку из раствора и добавили к нему несколько капель синего лакмуса.
Раствор лакмуса окрасился в красный цвет, что говорит об образовании кислотной среды, которую обеспечивает угольная кислота:
Угольная кислота образуется при растворении углекислого газа в воде. Угольная кислота диссоциирует на ионы водорода, окрашивающие лакмус в красный цвет.
В пробирку налили 2—3 мл разбавленного раствора гидроксида натрия, добавили к нему несколько капель фенолфталеина и затем через раствор пропустили выделяющийся газ.
Раствор фенолфталеина, который окрасился в малиновый цвет при взаимодействии с гидроксидом натрия, поменял цвет на бледно розовый (образовалась соль, состоящая из катионов сильной щелочи и анионов слабой кислоты).
Углекислый газ реагирует с щелочами, образуя соль, которая при гидролизе образует слабощелочную среду.
2. Распознавание карбонатов. В трех пробирках даны кристаллические вещества: сульфат натрия, хлорид цинка, карбонат калия. Определите, какое вещество находится в каждой пробирке. Сделайте вывод, что является качественной реакцией на карбонат-ионы. Напишите соответствующее уравнение реакции.
К трём растворам добавили соляную кислоту
В двух пробирках реакция не идёт
С соляной кислотой не взаимодействуют сульфат натрия и хлорид цинка, в этих пробирках находятся эти вещества.
Выделяется газ без цвета и запаха
В пробирке карбонат калия:
Качественная реакция на карбонат-ионы — взаимодействие с сильной кислотой с выделением газа без цвета и запаха.
Добавили к раствору нитрат серебра (I)
В одной пробирке выпадает осадок белого цвета.
В пробирке находится хлорид цинка.
Белый осадок означает, что соль
является хлоридом (ионы Ag
связываются с ионами Сl).
В пробирке, в которой не произошло изменений, находится сульфат натрия.