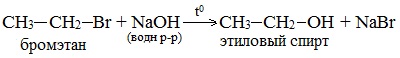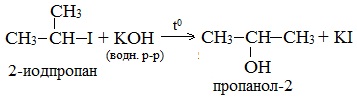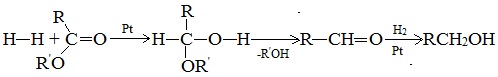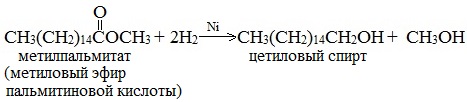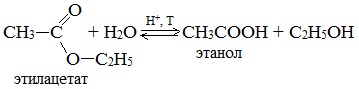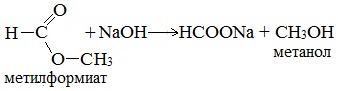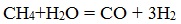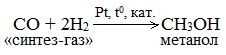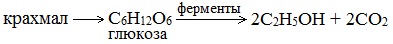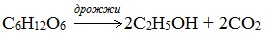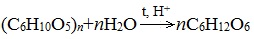К наиболее часто используемым химическим способам получения спиртов относятся:
1.Гидратация алкенов (промышленный способ получения этанола для технических целей)
(t, Р, кислая среда (катализатор))
2.Щелочной гидролиз галогеналканов (лабораторный способ получения)
(водный раствор щелочи, t)
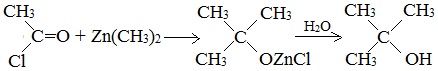
3.Восстановление альдегидов и кетонов (лабораторный способ получения)
(t, катализатор –Ni)
Особые способы получения метанола и этанола
1.Получение метанола из синтез-газа (водяной газ, генераторный газ)
(t, Р, оксидные катализаторы)
2.Получение этанола ферментативным брожением глюкозы (получение этилового спирта для пищевых и медицинских целей)
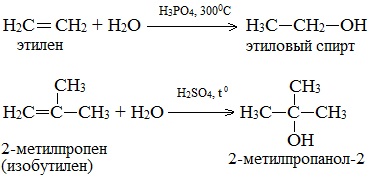
1. Гидратация алкенов
Гидратация алкенов используется в промышленности для получения спиртов из продуктов нефтепереработки.
Присоединение воды к алкенам происходит в присутствии разбавленной серной или фосфорной кислот. Эта реакция протекает в соответствии с правилом Марковникова, поэтому первичный спирт можно получить только из этилена, а остальные алкены дают вторичные или третичные спирты:
Этот метод в лабораторных условиях нашел ограниченную область применения для получения третичных спиртов.
2. Гидролиз галогеналканов в водном растворе щелочи
В лабораторных условиях спирты получают действием водного раствора щелочи на алкилгалогениды при нагревании, при этом атом галогена в галогеналкане замещается группой –ОН:
С помощью этой реакции можно получать первичные, вторичные и третичные спирты.
При действии спиртового раствора щелочи на галогеналканы происходит отщепление галогеноводорода и образование алкена.
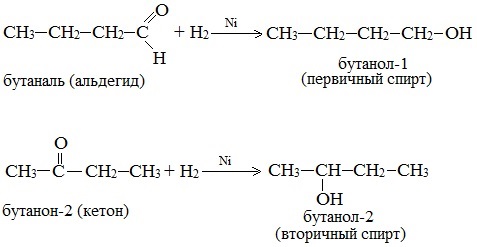
3. Восстановление карбонильных соединений (альдегидов и кетонов)
Дегидрирование спиртов по своей химической сущности является окислением. Обратная реакция – гидрирование альдегидов, кетонов и эфиров карбоновых кислот – является, таким образом, их восстановлением.
При действии водорода в присутствии катализаторов (Ni, Pt, Pd) альдегиды восстанавливаются до первичных спиртов, а кетоны – до вторичных спиртов:
4. Восстановление эфиров карбоновых кислот
Гидрирование сложных эфиров проходит через стадию образования альдегидов:
Этим методом в промышленности из метиловых эфиров высших кислот получают высшие первичные спирты, например:
5. Гидролиз сложных эфиров карбоновых кислот в щелочной среде
Гидролиз сложных эфиров карбоновых кислот протекает как в кислой, так и в щелочной среде (водные или спиртовые растворы NaOH, КОН, а также Ba (OH)2, Ca (OH)2, Ba (OH)2, Ca (OH)2). Однако к образованию спиртов приводит гидролиз, протекающий необратимо в щелочной среде:
6. Синтез спиртов из карбонильных соединений с помощью магнийорганических соединений
Спирты образуются при многочисленных реакциях металлоорганических соединений с различными соединениями, содержащими карбонильную группу >С=О. Этим способом можно получать как первичные спирты, так и вторичные и третичные:
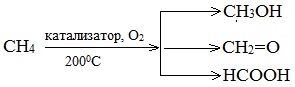
7. Окисление алканов
При мягком окислении метана кислородом воздуха в присутствии различных катализаторов образуются метанол, формальдегид или муравьиная кислота:
Специфические способы получения метанола и этанола
Производство метанола крупнотоннажное, т.к. метиловый спирт является исходным веществом для получения других продуктов органического синтеза.
В промышленности
1. Получение метанола из синтез-газа (водяной газ, генераторный газ)
а) Конверсия природного газа в синтез-газ
Его получают из метана с перегретым водяным паром:
б) Каталитический синтез метанола из оксида углерода (II) и водорода
В качестве катализаторов используют смесь оксидов цинка, меди и хрома, температуру поддерживают в интервале 200-300 о С, а давление – от 40 до 150 атм.
Газ на выходе из реактора содержит 3-5% CH3OH, затем газ охлаждают и конденсируют полученный метанол, а оставшийся газ смешивают с исходным газом и направляют снова в реактор.
Ранее метанол получали сухой перегонкой древесины без доступа воздуха (отсюда его название «древесный спирт»).
2. Получение этанола спиртовым брожением глюкозы
Ферментативный гидролиз крахмала – наиболее древний синтетический процесс, используемый человеком – до сих пор имеет огромное значение для получения этилового спирта.
Протекает только в присутствии ферментов, которые вырабатывают некоторые микроорганизмы, например, дрожжи:
Глюкоза содержится во фруктовых соках. Глюкозу можно получить гидролизом крахмала (зерно, картофель, целлюлозные опилки):
Acetyl
Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Гидроксипроизводные углеводородовОни подразделяются на два основных типа: спирты и фенолы. СпиртыСпиртами называют соединения, которые содержат одну или несколько гидроксильных групп вместо атомов водорода в алканах, алкенах и их циклических аналогах. По числу гидроксильных групп спирты подразделяются на одноатомные, двухатомные, трехатомные и т.д.: В природе спирты встречаются в виде сложных эфиров (жиры, воски, эфирные масла) и в свободном состоянии. Так, гексен-З-ол-1 содержится в зеленых листьях и фруктах, эфирных маслах, бензи- ловый спирт — в жасминном масле. Спирты находят широкое практическое применение. Они производятся в значительных количествах и используются в качестве полупродуктов для синтеза различных органических соединений. Диолы и глицерин применяются в производстве лекарственных препаратов, полимеров (полиэфиры, полиуретаны), взрывчатых веществ, пластификаторов. Спирты используются как растворители, являются главными компонентами антифризов, эмульгаторов, смазок, входят в состав парфюмерных изделий и медицинских препаратов. Глицерин является структурным компонентом животных и расти-тельных жиров, масел. Получение одноатомных спиртов 1. Гидратация алкенов Самым доступным и широко используемым в больших масштабах способом получения спиртов является гидратация алкенов. Алке- ны легко превращаются в спирты в результате либо прямого кислот- но-катализируемого присоединения воды, либо присоединения серной кислоты с последующим гидролизом алкилсульфатов: Этим способом могут быть синтезированы лишь те спирты, которые образуются в соответствии с правилом Марковникова. Кислотно-катализируемая гидратация алкенов лежит в основе современного промышленного способа получения этанола из этилена, пропанола-2 из пропилена, а также трет.-бутилового спирта из изобутилена: Для получения других спиртов этот метод имеет ограниченную область применения, поскольку гидратация алкенов часто сопровождается изомеризацией углеродного скелета за счет перегруппировок промежуточно образующихся карбокатионов. 2. Гидролиз галогенопроизводных Хлоропроизводные часто используют как промежуточные продукты с целью превращения путем гидролиза в соответствующие спирты и фенолы. В качестве гидролизующих агентов применяют 5- 10%-ный раствор Na2C03, NaOH или Са(ОН)2. Этот метод используют в промышленности для получения аллилового и бензилового спиртов: 3. Восстановление карбонилсодержащих соединений Восстановительное образование гидроксильной группы из других кислородсодержащих функциональных групп является одним из наиболее распространенных методов. Чаще всего в качестве исходных соединений используют альдегиды, кетоны и сложные эфиры. Насыщенные альдегиды и кетоны легко восстанавливаются водородом в присутствии Ni- и Pt-катализаторов в соответствующие первичные и вторичные спирты: Восстановление насыщенных альдегидов в промышленности применяют для получения пропанола-1, бутанола-1, изобутилового и некоторых высших спиртов. В промышленности применяется также восстановление ненасыщенных альдегидов как завершающий этап при получении некоторых спиртов. Так, известный в промышленности метод синтеза //-бутилового спирта из ацетальдегида предусматривает дегидратацию альдоля с последующим восстановлением кротонового альдегида: Аналогично получают также 2-этилгексанол, который используется для получения диалкилфталата — важнейшего пластификатора поливинилхлорида. Большие количества первичных спиртов, содержащих четное число атомов углерода, получают каталитическим восстановлением эфиров жирных кислот (жиров). Наиболее распространенным препаративным методом восстановления альдегидов и кетонов является использование в качестве восстановителей комплексных гидридов: боргидрида натрия (тетрагидробората натрия) и литийалюминогидрида (тетрагидроалюмината лития). Оба реагента восстанавливают альдегиды до первичных спиртов, а кетоны до вторичных. Боргидрид натрия является более предпочтительным вследствие его меньшей стоимости и безопасности в обращении. Он может быть использован даже в водном и спиртовом растворах, тогда как алюмогидрид лития реагирует с водой и со спиртами со взрывом. Боргидрид натрия обеспечивает избирательное восстановление карбонильной группы альдегидов и кетонов в присутствии в молекуле дополнительных функциональных групп, которых этот реагент не затрагивает. Алюмогидрид лития гораздо менее селективен, но, благодаря его значительной реакционной способности, им можно восстанавливать также карбоновые кислоты и их сложные эфиры и галогенангидриды до первичных спиртов: 4. Алфол-процесс (окисление парафинов) Высшие жирные спирты (Сб-С2о), используемые для синтеза моющих средств, получают в виде смеси при полимеризации этилена по видоизмененному способу Циглера-Натта, который называют ал- фол-процессом. На первой стадии получают триэтилалюминий по реакции: На следующей стадии проводят направленную теломеризацию (полимеризацию) триэтилалюминия с этиленом: Получившиеся высшие алюминийалкилы окисляют кислородом воздуха, что приводит к образованию алкоголятов алюминия: Алкоголяты гидролизуют водным раствором серной кислоты с образованием смеси высших жирных спиртов С6-С20. 5. Ферментативный гидролиз и брожение углеводов Превращение сахаров под действием фермента дрожжей — одна из наиболее древних химических реакций, используемых человеком для синтеза этилового спирта. Сахар (полисахарид) получают из различных источников — это патока из сахарного тростника или крах-мал, полученный из различных зерновых культур и картофеля. Полисахарид сначала гидролизуется до моносахаридов, а затем последние подвергаются брожению. В общем виде процесс выглядит так: Для получения технического (гидролизного) спирта используют древесину, отходы целлюлозно-бумажного производства. В присутствии концентрированных минеральных кислот, при 120 — 130°С, давлении до 15 атм. происходит гидролиз клетчатки. Далее брожением продуктов гидролиза получают технический спирт. Брожением крахмала с помощью других бактерий (Clostridium acetobutylicum) получают смесь бутанола-1 (60 %), ацетона (30 %) и этилового спирта (10 %). Этот процесс был разработан Вейцманом в 1911 г. для получения ацетона, используемого в производстве бездымного пороха. 6. Производство метанола на основе синтез-газа В настоящее время метанол получают, в основном, из синтез- газа и в самых больших объемах среди спиртов: 7. Гидроборирование — окисление алкенов Приведенный выше метод гидратации алкенов по правилу Мар- ковникова дополняется близким и эффективным методом гидробори- рования — окисления с обратной региоселективностью. Этот метод используют для синтеза первичных спиртов. Реакция представ-ляет собой электрофильное ^////-присоединение по двойной углерод- углеродной связи. Дибораны — димерные гидриды бора (ВН3)2 — легко присоединяются к алкенам, при этом образуются триалкилбораны: Триалкилборан окисляют пероксидом водорода в присутствии щелочи до первичного спирта: 8. Синтез спиртов из карбонилсодержащих соединений с помощью магнийорганических соединений Металлоорганические соединения, в основном магний- (реактив Гриньяра) и литийорганические, при взаимодействии с альдегидами, кетонами, эфирами и галогеноангидридами карбоновых кислот позволяют легко получать первичные, вторичные, третичные спирты с удлинением углеродной цепи. Этот метод является одним из надежных лабораторных способов получения спиртов. При взаимодействии реактивов Гриньяра и литийорганических соединений с карбонильными производными образуются алкоголяты металлов, которые действием воды или разбавленной кислоты можно превратить в соответствующие спирты: Этим способом можно получить спирты самого разнообразного строения, причем из формальдегида — первичные, из других альдегидов — вторичные и из кетонов — третичные спирты: Взаимодействие алкилмагнийгалогенидов с эфирами и гало- геноангидридами карбоновых кислот приводит к третичным спиртам. Сложные эфиры муравьиной кислоты в этих условиях образуют вторичные спирты. Реакция идет в две стадии: сначала в результате присоединения-отщепления по карбонильной группе образуется кетон, который далее реагирует со второй молекулой реактива Гриньяра, образуя алкоголят третичного спирта. Последующий гидролиз приводит к спирту: Так как галогеноангидриды являются более активными, а сложные эфиры менее активными по сравнению с промежуточными кетонами, последние можно выделить в индивидуальном виде. Для получения первичных спиртов используют также взаимодействие оксирана с реактивом Гриньяра. При этом образуются первичные спирты, у которых углеродная цепь длиннее, чем у исходного галогенопроизводного на два атома углерода: 2.2.1.2. Синтез многоатомных спиртов Гликоли (двухатомные спирты) и глицерин (трехатомный спирт) можно получать теми же способами, что и одноатомные спирты. Однако имеется ряд особенностей их методов получения. 1. Гидролиз галогенопроизводных Гликоли получают гидролизом дигалогенопроизводных, а также галогеногидринов в щелочной среде: Аналогичным способом из пропилена получают глицерин: 2. Гидроксилирование алкенов Наиболее известными среди обычных способов получения 1,2-диолов являются реакции, включающие гидроксилирование алкенов. Известен ряд окислительных реагентов, с помощью которых в мягких условиях возможно присоединение двух гидроксильных групп к алкенам. а) Окисление сткенов перманганатом калия или тетраоксидом осмия. Окисление алкенов перманганатом калия (реакция Вагнера) или тетраоксидом осмия (VIII) (реакция Крите) в нейтральной или щелочной среде приводит к вицинальным диолам. Так, из этилена образуется этиленгликоль: Важно указать, что в продуктах гидроксилирования два гид-роксила оказываются присоединенными с одной стороны двойной связи (син- присоединение или устаревшее название цис-присоединение). Так, в случае ?/мобутена-2 исключительно образуется мезо-форма бу- тандиола-2,3. Причиной этого является промежуточное образование циклического эфира, гидролиз которого приводит к продукту син- гидроксилирования: Сг///-гидроксилирование транс-бутена-2 завершается образованием рацемата бутандиола-2,3: Следует отметить, что в настоящее время реакция Вагнера находит незначительное синтетическое применение. Чаще гидроксилиро- вание алкенов проводят с использованием оксида осьмия (VIII). Аналогично перманганату калия, тетраоксид осьмия образует промежуточные эфиры: Обработка их водным раствором NaHS03 приводит к мезо- и 0,Ь-бутандиолам-2,3, соответственно (?/гл>присоединение). б) Гидратация оксидов алкенов (оксиранов, эпоксидов). Одним из способов получения вицинальных диолов является взаимодействие оксиранов с водой: Наиболее важным методом промышленного синтеза этиленгликоля является гидратация оксида этилена в нейтральной среде или при кислотном катализе. В отсутствии катализатора гидролиз оксида этилена требует достаточно жестких условий: 180°С и давления до 20 атм. В водном 0.5 % растворе серной кислоты раскрытие цикла происходит уже при 70°С и обычном давлении. В промышленности реализуются оба варианта. При эпоксидировании алкена и последующем гидролизе образующегося оксирана два гидроксила оказываются присоединенными с разной стороны плоскости двойной связи (шшш-присоединение). Поэтому из г/г/обутена-2 образуется 0,Ь-бутандиол-2,3, а из транс- бутена-2 — л/езо-бутандиол-2,3: Эпоксидирование алкенов можно провести пероксидом водо-рода, перкарбоновыми кислотами (реакция Прилежаева), а этилена — кислородом воздуха в присутствии серебра, нанесенного на оксид алюминия или карбид кремния. Гидроксилирование алкена можно провести также действием 30% пероксида водорода в уксусной кислоте в присутствии каталитических количеств конц. H2S04 при комнатной температуре. При этом образуются т/?ш/с-вицинальные двухатомные спирты (анты- присоединение): Аналогичный подход используют также для получения синтетического глицерина. В промышленности глицерин получают из пропилена, используя на последней стадии окисление аллилового спирта: в) Гидролиз (омыление) жиров. Жиры представляют собой сложные эфиры глицерина и высших карбоновых кислот. При гидролизе жиров перегретым паром или щелочью (омыление) получаются глицерин, высшие карбоновые кислоты или их соли: Получаемая в ходе гидролиза калиевая соль идет на изготовление жидкого мыла, а из натриевой соли получают твердые мыла. Задача 1. Какие спирты можно получить при гидратации следующих алкенов: а) 2-метилпропена; б) 2-метилбутена-1; в) 2,4-диметил пентена-2; г) 1-метилциклогексена? Задача 2. Из каких галогенопроизводных можно получить следующие спирты: а) изобутиловый спирт; б) 3,3-диметилбутанол-2, в) пропен-2-ол-1; г) пентандиол-2,3. Задача 3. Какие спирты можно синтезировать, исходя из метил- магнийбромида и следующих реагентов: Задача 4. Напишите структурные формулы реактивов Гриньяра и альдегидов или кетонов, которые необходимо использовать для получения каждого из изомерных пентиловых спиртов. Задача 5. Как из 3-метилбутена-1 можно получить следующие вещества: а) З-метилбутандиол-1,2; б) 3-метилбутандиол-2,3; в) 3-ме- тилбутанол-2? Задача 6. Какие спирты образуются в реакциях гидробори- рования-окисления следующих соединений: а) 3,3-диметилбутена-1; б) изобутилена; в) 1-метилциклопентена; г) 2-метилбутена-2; д) 2-фе- нилбутена-2; е) 1,2-диметилциклопентена? Задача 7. Напишите уравнения реакций с указанием реагентов, необходимых для получения бутанола-1 по каждому из следующих методов: а) восстановление альдегида с применением LiAlH4; б) гид- роборирование алкена и последующее окисление продукта; в) применение реактива Гриньяра; г) гидролиз галогеналкана; д) восстановление метилового эфира бутановой кислоты. Задача 8. Напишите уравнения реакций с указанием реагентов, необходимых для получения 1-фенилэтанола-1 из следующих исходных соединений: а) бензальдегида; б) бензилового спирта; в) стирола; г) фенилметилкетона; д) бензола. Задача 9. Предложите схему получения пентанола-1, применив следующие соединения в качестве исходного: а) пентена-1; б) 1-бро- мопентана; в) 1-бромобутана. Задача 10. Какой изомер или изомеры (шесть) гликолей общей формулы С4Н10О2 можно получить с помощью ниже приведенных методов:
Задача 11. Используя дополнительно только неорганические реагенты, осуществите следующие превращения:
Задача 12. Приведите схему получения глицерина из пропанола-1 и неорганических реагентов. Задача 13. Напишите схему превращения трет-бутшового спирта в изобутиловый спирт. Задача 14. Сделайте заключение о пригодности следующей схемы: для получения следующих спиртов:
Задача 15. Покажите, каким образом 2-метилпропанол-1 может быть превращен в следующие соединения: а) 2-метилпропандиол-1,2; б) 2-метил пропанол-2; в) 2-метилпропантриол-1,2,3. Задача 16. Предложите схему получения бутанола-2 из ацетилена и необходимых неорганических реагентов. Задача 17. Приведите схему синтеза 2-метилпентин-3-ола-2 из метилацетилена. Задача 18. Напишите схему получения 2-метилпентен-4-ола-2 из пропилена и неорганических соединений. Задача 19. Напишите схему синтеза гексин-1-ола-З из бутанола- 1 и ацетилена. Задача 20. Предложите метод синтеза 2,3-диметилбутанола-2, исходя из пропилена и неорганических реагентов. |