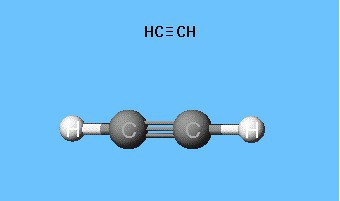
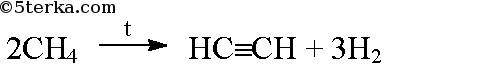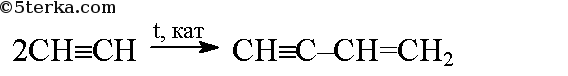Ацетилен представляет собой вещество, относящееся к классу алкинов. Иными словами, это углеводород, который имеет в каждой молекуле тройную связь. При этом химическая формула ацетилена выглядит следующим образом: С2Н2. Само по себе это вещество является бесцветным газом, который значительно легче воздуха. Получают ацетилен из метана. Вещество является химически активным и взрывоопасным.
- Как получить ацетилен
- Получение в промышленности
- Как осуществляется крекинг
- Применение ацетилена
- №4. Напишите уравнения реакций получения: а) ацетилена из метана; б) хлоропренового каучука из ацетилена; в) тетрахлорметана из метана.
- Метан: способы получения и свойства
- Гомологический ряд метана
- Строение метана
- Изомерия метана
- Химические свойства метана
- 1. Реакции замещения
- 1.1. Галогенирование
- 1.2. Нитрование метана
- 2. Реакции разложения метана (д егидрирование, пиролиз)
- 3. Окисление метана
- 3.1. Полное окисление – горение
- 3.2. Каталитическое окисление
- Получение метана
- 1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
- 2. Водный или кислотный гидролиз карбида алюминия
- 3. Декарбоксилирование солей карбоновых кислот (реакция Дюма)
- 4. Синтез Фишера-Тропша
- 5. Получение метана в промышленности
- 💥 Видео
Видео:3.2. Алкины: Способы полученияСкачать

Как получить ацетилен
Из метана в домашних условиях получить ацетилен очень сложно. Самый простой метод выделения данного газа – это реакция воды с карбидом кальция. Многие из вас, наверное, помнят, как бросали в лужи кусочки этого вещества и какая происходила реакция. При этом отмечалось бурное шипение. Что касается карбида кальция, то он постепенно таял, образовывая большое количество пены. Подобную реакцию можно записать так:
Многие используют технический карбид кальция, который содержит большое количество примесей. В результате этого при реакции с водой вещество выделяет неприятный запах. Возникает он из-за образования вместе с ацетиленом незначительного количества паров ядовитых газов. Чаще всего это фосфин, сероводород и так далее. Этот способ считается самым распространенным, так как получить ацетилен из метана можно только при помощи специального оборудования.
Видео:Ацетилен получениеСкачать

Получение в промышленности
Как получают ацетилен из метана в промышленных условиях? В настоящее время применяется только один метод – крекинг. В процессе получения ацетилена осуществляется разрыв связей -С-С. Происходит это в присутствии катализаторов и при воздействии достаточно высоких температур. Для получения используется метан – природный газ. Это недорогое и легкодоступное сырье. Именно по этой причине крекинг является наиболее обоснованным методом как в экономическом плане, так и в техническом.
Видео:ВСЕ ПРО АЛКАНЫ за 8 минут: Химические Свойства и ПолучениеСкачать

Как осуществляется крекинг
Осуществить превращения «метан — ацетилен» можно несколькими способами. В первом случае природный газ пропускают через предварительно раскаленные электроды. При этом температура может доходить до 1600 °С. После нагрева происходит быстрое охлаждение. Второй способ основан на использовании тепла, которое образуется в результате частичного сгорания ацетилена.
Уравнения реакций «метан — ацетилен» записываются следующим образом:
Специалисты не рекомендуют использовать для хранения ацетилена баллоны, оснащенные вентилями из бронзы. Ведь в состав этого сплава входит медь. Так как ацетилен химически активен, он может вступить в реакцию с металлом. В результате этого образуются взрывоопасные соли.
Видео:Реакция Дюма. Получение метанаСкачать

Применение ацетилена
Ацетилен – это вещество, которое широко применяется в различных промышленных отраслях. Чаще всего этот газ используют при изготовлении этилового спирта в качестве основного сырья. Помимо этого, ацетилен применяют для получения определенных видов каучука, уксусной кислоты и пластмассы.
Активно используется данный газ и при проведении сварочных работ, а также при резке различных металлов. Стоит отметить, что при окислении кислородом ацетилена образуется сильное пламя. Газ является источником достаточно яркого света в светильниках автономного типа. На основе ацетилена производят взрывчатые вещества, которые в дальнейшем применяются как детонаторы.
Видео:Решение задач на термохимические уравнения. 8 класс.Скачать

№4. Напишите уравнения реакций получения: а) ацетилена из метана; б) хлоропренового каучука из ацетилена; в) тетрахлорметана из метана.
а) При сильном нагревании из метана образуется ацетилен:
б) В присутствии катализатора из двух молекул ацетилена образуется одна молекула винилацетилена (реакция димеризации):
При присоединении к винилацетилену хлороводорода образуется 2-хлорбутадиен-1,3 (хлоропрен), при полимеризации которого образуется хлоропреновый каучук.
в) При полном хлорировании метана, то есть при замещении всех атомов водорода на хлор, образуется тетрахлорметан (четыреххлористый углерод):

задача №4
к главе «Глава VI. Природные источники углеводородов и их переработка. §§1-5 (стр. 74) Вопросы».
Видео:Как решать ОРГАНИЧЕСКИЕ ЦЕПОЧКИ? Основные типы химических реакцийСкачать

Метан: способы получения и свойства
Метан CH4 – это предельный углеводород, содержащий один атом углерода в углеродной цепи. Бесцветный газ без вкуса и запаха, легче воды, нерастворим в воде и не смешивается с ней.
Видео:Опыты по химии. Получение ацетилена и опыты с нимСкачать

Гомологический ряд метана
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4, или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Видео:Получение АЦЕТИЛЕНА. Получение КАРБИДА КАЛЬЦИЯ. Реакция КАРБИДА КАЛЬЦИЯ и ВОДЫ. Опыты по химии дома.Скачать

Строение метана
В молекуле метана встречаются связи C–H. Связь C–H ковалентная слабополярная. Это одинарная σ-связь. Атом углерода в метане образует четыре σ-связи. Следовательно, гибридизация атома углерода в молекуле метана– sp 3 :
При образовании связи С–H происходит перекрывание sp 3 -гибридной орбитали атома углерода и s-орбитали атома водорода:
Четыре sp 3 -гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109 о 28′ друг к другу:
Это соответствует тетраэдрическому строению молекулы.
| Например, в молекуле метана CH4 атомы водорода располагаются в пространстве в вершинах тетраэдра, центром которого является атом углерода |
Видео:Какой объем (л, н.у.) метана можно получить из 32,8 г ацетата натрия, если выход реакции 75?Скачать

Изомерия метана
Для метана не характерно наличие изомеров – ни структурных (изомерия углеродного скелета, положения заместителей), ни пространственных.
Видео:Получение метанаСкачать

Химические свойства метана
Метан – предельный углеводород, поэтому он не может вступать в реакции присоединения.
Для метана характерны реакции:
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для метана характерны только радикальные реакции.
Метан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой.
Видео:6.2. Ароматические углеводороды (бензол и его гомологи): Способы получения. ЕГЭ по химииСкачать

1. Реакции замещения
Для метана характерны реакции радикального замещение.
1.1. Галогенирование
Метан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании метана сначала образуется хлорметан:
Хлорметан может взаимодействовать с хлором и дальше с образованием дихлорметана, трихлорметана и тетрахлорметана:
| Химическая активность хлора выше, чем активность брома, поэтому хлорирование протекает быстро и неизбирательно. |
Бромирование протекает более медленно.
Реакции замещения в алканах протекают по свободнорадикальному механизму.
Свободные радикалы R∙ – это атомы или группы связанных между собой атомов, которые содержат неспаренный электрон.
Первая стадия. Инициирование цепи.
Под действием кванта света или при нагревании молекула галогена разрывается на два радикала:
Свободные радикалы – очень активные частицы, которые стремятся образовать связь с каким-либо другим атомом.
Вторая стадия. Развитие цепи.
Радикал галогена взаимодействует с молекулой алкана и отрывает от него водород.
При этом образуется промежуточная частица – алкильный радикал, который в свою очередь взаимодействует с новой нераспавшейся молекулой хлора:
Третья стадия. Обрыв цепи.
При протекании цепного процесса рано или поздно радикалы сталкиваются с радикалами, образуя молекулы, радикальный процесс обрывается.
Могут столкнуться как одинаковые, так и разные радикалы, в том числе два метильных радикала:
1.2. Нитрование метана
Метан взаимодействует с разбавленной азотной кислотой по радикальному механизму, при нагревании до 140 о С и под давлением. Атом водорода в метане замещается на нитрогруппу NO2.
| Например. При нитровании метана образуется преимущественно нитрометан: Видео:Получение ацетиленаСкачать  2. Реакции разложения метана (д егидрирование, пиролиз)При медленном и длительном нагревании до 1500 о С метан разлагается до простых веществ: Если процесс нагревания метана проводить очень быстро (примерно 0,01 с), то происходит межмолекулярное дегидрирование и образуется ацетилен: Пиролиз метана – промышленный способ получения ацетилена. Видео:Метан. Состав. Строение. Свойства. Получение и применение метанаСкачать  3. Окисление метанаАлканы – малополярные соединения, поэтому при обычных условиях они не окисляются даже сильными окислителями (перманганат калия, хромат или дихромат калия и др.). 3.1. Полное окисление – горениеАлканы горят с образованием углекислого газа и воды. Реакция горения алканов сопровождается выделением большого количества теплоты. Уравнение сгорания алканов в общем виде: При горении алканов в недостатке кислорода может образоваться угарный газ СО или сажа С. Промышленное значение имеет реакция окисления метана кислородом до простого вещества – углерода: Эта реакция используется для получения сажи. 3.2. Каталитическое окисление
Продукт реакции – так называемый «синтез-газ». Видео:29. Общая реакция горения для всех углеводородов. Как расставить коэффициенты реакции легкоСкачать  Получение метанаВидео:Окисление метанаСкачать  1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)Это один из лабораторных способов получения алканов. При этом происходит удвоение углеродного скелета. Реакция больше подходит для получения симметричных алканов. Получить таким образом метан нельзя. Видео:ЭТО ПОМОЖЕТ разобраться в Органической Химии — Алкены, Урок ХимииСкачать  2. Водный или кислотный гидролиз карбида алюминияЭтот способ получения используется в лаборатории для получения метана. Видео:Сколько г метан необходимо для получения ацетилена, если при получении, из ацетилена бензола (выходСкачать  3. Декарбоксилирование солей карбоновых кислот (реакция Дюма)Реакция Дюма — это взаимодействие солей карбоновых кислот с щелочами при сплавлении. R–COONa + NaOH → R–H + Na2CO3 Декарбоксилирование — это отщепление (элиминирование) молекулы углекислого газа из карбоксильной группы (-COOH) или органической кислоты или карбоксилатной группы (-COOMe) соли органической кислоты. При взаимодействии ацетата натрия с гидроксидом натрия при сплавлении образуется метан и карбонат натрия: Видео:Химические свойства алканов. 1 часть. 10 класс.Скачать  4. Синтез Фишера-ТропшаИз синтез-газа (смесь угарного газа и водорода) при определенных условиях (катализатор, температура и давление) можно получить различные углеводороды: Это промышленный процесс получения алканов. Синтезом Фишера-Тропша можно получить метан: Видео:10 класс - Химия - Алкины. Ацетилен. Состав и строение. ПолучениеСкачать  5. Получение метана в промышленностиВ промышленности метан получают из нефти, каменного угля, природного и попутного газа . При переработке нефти используют ректификацию, крекинг и другие способы. 💥 ВидеоКак Решать Задачи по Химии // Задачи с Уравнением Химической Реакции // Подготовка к ЕГЭ по ХимииСкачать  |