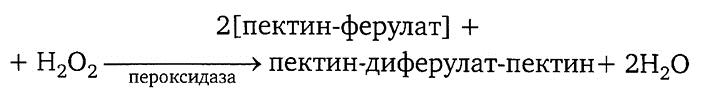Обращаем Ваше внимание, что в соответствии с Федеральным законом N 273-ФЗ «Об образовании в Российской Федерации» в организациях, осуществляющих образовательную деятельность, организовывается обучение и воспитание обучающихся с ОВЗ как совместно с другими обучающимися, так и в отдельных классах или группах.
МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ
Гилязова Диана Владимировна
ПЕКТИНОВЫЕ ВЕЩЕСТВА В РАСТИТЕЛЬНЫХ ОБЪЕКТАХ
Глава I . Литературный обзор
1.1. Биологически активные вещества растений
1.2. Пектиновые вещества
1.2.1. Строение и классификация
1.2.2. Свойства и функции пектиновых веществ
1.2.3. Применение пектиновых веществ
1.2.4. Основные виды сырья для производства пектиновых веществ
1.3. Оптические методы анализа пектиновых веществ
Глава II . Практическая часть
2.1. Выделение и определение пектиновых веществ
2.1.1. Методика выделения растворимого пектина
2.1.2. Определение количества растворимого пектина по
2.1.3. Качественное обнаружение пектиновых веществ (реакция Эрлиха)
2.2 Результаты эксперимента
2.2.1. Количественное определение пектиновых веществ
2.2.2. Качественное определение пектиновых веществ
Глава IV . Методическая часть
Все растения являются носителями биологически активных веществ, которые содержатся в них в малых количествах, но составляют наибольшую ценность растения, так как именно они обладают целебными свойствами. Эти чудодейственные соединения в медицине называют «физиологически активными», «фармакологически активными» или «действующими» веществами.
Поскольку в используемых частях растений всегда содержится целый комплекс физиологически активных веществ (ФАВ), то из их числа выделяют так называемые действующие и сопутствующие вещества. Под действующим веществом подразумевают преобладающее ФАВ, а все остальные, содержащиеся в растении наряду с ним, являются сопутствующими, так называемые синергисты.
Биологически активные вещества имеют разнообразный состав и относятся к различным классам химических соединений. Наиболее важными из них являются: витамины, минеральные вещества, эфирные и жирные масла, полифенольные соединения, сапонины, алкалоиды, полисахариды, органические кислоты и др.
Целью нашей работы является исследование биологически-активных веществ, в частности пектинов.
Пектиновые вещества относятся к группе не усваиваемых углеводов, обнаруженные практически во всех растениях в межклеточных тканях, клеточных стенках, листьях, овощах, фруктах и.т.д. Благодаря своей структуре, они обладают уникальными свойствами – являются эффективными природными соединениями, способными желировать растворы, связывать и выводить из организма различные токсичные вещества, ионы тяжелых металлов и радионуклидов, применяются в качестве пролонгаторов многих биологически активных и медицинских препаратов, заменителей плазмы крови, поверхностно активных соединений, ионообменников. Поэтому исследования в данной области являются актуальными.
Исходя из цели, поставлены следующие задачи:
1. Изучить литературу о значении физиологически активных веществ.
2. Исследовать структуру, свойства и физиологическую роль пектиновых веществ.
3. Определить количество растворимого пектина по пектату кальция в жоме сахарной свеклы, мякоти яблок и цедре апельсинов.
4. Качественно обнаружить пектиновые вещества (реакция Эрлиха)
5. Разработать уроки по химии для учащихся 10 классов на тему: «Углеводы».
1. Жом сахарной свеклы;
2. выжимки яблок;
3. цедра апельсина.
Глава I . Литературный обзор
Биологически активные вещества растений
Химический состав растений принято делить на две группы веществ: минеральные и органические; последние, в свою очередь, подразделяют на вещества первичного и вторичного синтеза.
Биологически активные вещества являются преимущественно веществами вторичного синтеза, а также липиды, углеводы и все витамины. Поскольку в используемых частях растений всегда содержится целый комплекс физиологически активных веществ (ФАВ), то из их числа выделяют так называемые действующие и сопутствующие вещества.
Под действующим веществом подразумевают преобладающее ФАВ, а все остальные, содержащиеся в растении наряду с ним, являются сопутствующими, так называемые синергисты [1].
Биологически активные вещества имеют разнообразный состав и относятся к различным классам химических соединений. Наиболее важными из них являются: витамины, минеральные вещества, эфирные и жирные масла, полифенольные соединения, сапонины, алкалоиды, сахара, органические кислоты и др.
С точки зрения пищевой ценности углеводы подразделяются на усваиваемые и неусваиваемые [2]. Усваиваемые углеводы – моносахариды и олигосахариды, крахмал, гликоген. Неусваиваемые – целлюлоза, гемицеллюлоза, инулин, пектин, гумми, слизи.
Основными сахарами растительного сырья являются глюкоза, фруктоза и сахароза. В зависимости от вида растения, суммарное содержание этих углеводов в сырье может составлять от 1 % до 20 %, при содержании сахарозы на уровне 0,1…1,0 %. Качественный состав и соотношение простых сахаров влияют на формирование своеобразного сладкого вкуса растительного сырья. Кроме того, в формирование вкуса растительного сырья также вносят полиолы, условно относимые к группе углеводов, например, сорбит (в плодах рябины обыкновенной его содержание составляет 9,0…10,4 %).
Сахара и полиолы достаточно легко переходят в водно-спиртовые экстракты, но наиболее значительно их содержание в соках из сочных плодов и ягод.
Полисахариды составляют основную часть сухого веса растений. Крахмал является энергетическим запасом; другие полисахариды выполняют скелетные функции, обеспечивая жесткость растительных клеток, прежде всего – целлюлоза: 1
Полисахариды – природные полимеры моносахаридов, соединенные гликозидными связями в линейные или разветвленные цепи. С точки зрения общих принципов строения, можно разделить на две группы: гомополисахариды, состоящие из моносахаридных единиц только одного типа, и гетерополисахариды, для которых характерно наличие двух и более типов мономерных звеньев. В качестве примера гомополисахаридов можно назвать маннаны, инулин, амилозу, амилопектин. Маннаны часто встречаются в кожуре орехов; инулин, являющийся резервным полисахаридом растений, в качестве мономера содержит фуранозу, что встречается достаточно редко. К гетерополисахаридам относятся пектиновые вещества, камеди и слизи – эти вещества представляют наибольший интерес для применения в пищевой и медицинской промышленности.
Пектиновые кислоты, пектаты и пектинаты растворимы в воде в присутствии сахаров, органических кислот с образованием плотных гелей.
Характерное свойство пектиновых веществ, используемое в пищевой и медицинской промышленности, – способность давать студни в присутствии сахаров и кислот. В чистом виде – это аморфные порошки с оттенками от белого до желтого, коричневого или серого цвета, почти без запаха, но растворимые в холодной воде, при нагревании образующие коллоидные растворы.
Слизи гумми (камеди) – группа коллоидных полисахаридов, к которым принадлежат растворимые в воде углеводы, образующие вязкие и клейкие растворы. Типичными представителями этой группы являются гумми, выделяемые в виде наплывов вишневыми, сливовыми и миндальными деревьями в местах повреждения ветвей и стволов. Слизи содержатся в большом количестве в льняных семенах и в зерне ржи. Именно их наличием объясняется высокая вязкость употребляемого в медицине отвара из льняных семян или же водной болтушки ржаной муки.
При исследовании состава полисахаридов вишневого клея было найдено, что они состоят из остатков галактозы, маннозы, арабинозы, п-глюкуроновой кислоты и незначительного количества ксилозы. Изучение слизей ржаного зерна показало, что они почти на 90% состоят из пентозанов. Эти слизи сильно набухают в воде и дают достаточно вязкие растворы.
Камеди находят широкое применение в производстве, поскольку они обладают такими ценными свойствами, как повышенная вязкость, клейкость, набухаемость и т.д. Камеди применяются в качестве связующих веществ и загустителей, служат эмульгаторами, основой для косметических и фармацевтических кремов и паст, стабилизаторами в пищевой промышленности [3].
Витамины (от лат. vita – жизнь) представляют собой низкомолекулярные биорегуляторы, необходимые для нормальной жизнедеятельности. Большинство из них поступают в организм человека с пищей в виде витаминов как таковых или их предшественников – провитаминов.
В настоящее время известно около 30 витаминов, из них около 20 поступают в организм с растительной и животной пищей. Растительное сырье является ценным источником витаминов для человека, его использование исключает опасность передозировки и возникновения побочного действия, неизбежное при длительном и неконтролируемом потреблении синтетических витаминных препаратов.
В растениях синтезируются все витамины, исключая витамин B 12. В дикорастущих видах наиболее распространены такие витамины, как аскорбиновая кислота (витамин C ) и P -активные флавоноиды (витамин P ), но в определённых количествах присутствуют и многие витамины группы B , а также витамины E и K . Витамины A и D встречаются в растительном сырье только в качестве провитаминов: в форме каротиноидов и стеринов.
Аскорбиновая кислота, или γ-лактон 2,3-дегидро- L -гулоновой кислоты (витамин С), синтезируется из глюкозы в ходе глюкуронового пути. Фермент L-гулонолактоноксидаза, ответственный за получение аскорбиновой кислоты, у приматов отсутствует, поэтому аскорбиновая кислота обязательно должна поступать с пищей. Аскорбиновая кислота участвует в самых разных реакциях: требуется для нормального состояния костей, соединительной ткани и кровеносных сосудов, для заживления рубцов. Есть и другие реакции, требующие присутствия витамина С как кофактора, например улучшение усвоения железа, катаболизм тирозина и синтез адреналина из тирозина.
Недостаточность витамина С развивается на фоне либо недостаточного потребления его организмом, либо при повышенной потребности в этом витамине [3].
Тиамин (витамин В1) образуется из замещенного пиримидина и тиазола, которые связываются между собой метиленовым мостиком.
В форме тиаминпирофосфата витамин B 1 является коферментом, катализирующим в организме человека процессы углеводного обмена, обеспечения энергией и ряд других ферментативных реакций. В мозге и печени тиамин очень быстро превращается в активную форму с помощью фермента тиаминдифосфотрансферазы.
Рибофлавин (витамин В2) является предшественником коферментов флавинмононуклеотида и флавинадениндинуклеотида, отвечающих за окислительно-восстановительные процессы, в том числе за обмен жиров и обеспечение организма энергией. Важен для восприятия цветов в процессе зрения.
Нормальная суточная потребность в рибофлавине составляет 2,5…3,0 мг. Недостаточность рибофлавина редко наблюдается у жителей большинства европейских стран, т.к. он содержится в необходимых количествах в хлебе, яйцах, молоке, мясе и т.д. Симптомы, связанные с недостаточностью рибофлавина, включают глоссит, себорею, ангулярный стоматит и фотофобию. На свету рибофлавин разрушается.
Ниацинамид (никотиновая кислота, никотинамид, ниацин), известный как витамин РР, или В3, участвует в обмене углеводов и обеспечении организма энергией. Важен для нервной и мышечной систем, кожных покровов и желудочно-кишечного тракта.
никотиновая кислота амид никотиновой кислоты
Никотиновая кислота при назначении фармакологических доз (2…4 г/день) понижает уровень холестерола в крови, это используется для лечения гиперхолестеролемии. Также никотиновая кислота ускоряет расход гликогена, что ведет к возрастанию уровня глюкозы в крови, поэтому терапия никотиновой кислотой не рекомендуется диабетикам и больным подагрой.
Пантотеновая кислота (витамин В5)синтезируется из аланина и пантоевой кислоты и необходима для синтеза коэнзима А (КоА) и компонента ацилпереносящего белка, который используется для синтеза жирных кислот и образования гормонов. Потребность в данном витамине составляет 10…15 мг в сутки. Недостаточность пантотеновой кислоты наблюдается очень редко, т.к. она широко распространена в пищевых продуктах.
Фолиевая кислота (витамин В9, или ВС) состоит из 3-х частей: перидинового кольца, пара-аминобензойной и глутаминовой кислот. Этот витамин играет важную роль в метаболизме нуклеиновых кислот и белков, необходим для процессов кроветворения, деления клеток, роста и развития всех органов и тканей.
Витамин А представлен тремя биологически активными формами: ретинолом, ретиналем (ретинальдегид) и ретиноевой кислотой. В растениях витамин A не встречается, но многие виды растительного сырья содержат предшественников этого витамина – каротины. При попадании β-каротинов в просвет кишечника происходит его расщепление каротиндиоксигеназой и образование ретиналя. Ретиналь потом восстанавливается до ретинола с помощью ретинальдегидредуктазы. Ретинолэтерифицируется пальмитиновой кислотой и вступает в кровь в составе хиломикронов. Потом остатки хиломикронов потребляются печенью, где и происходит накопление витамина А. Транспорт витамина А из печени к другим органам и тканям осуществляется в связанной формой ретинола с апоретинол-связывающим белком.
Витамин А запасается в печени, и поэтому его недостаточность (при потребности 0,8…1,5 мг в сутки) возникает достаточно редко. Ранним симптомом недостаточности витамина А является куриная слепота. Потом возникают фолликулярный гиперкератиноз, повышенная чувствительность к инфекциям, рак и железодефицитная анемия. Длительная недостаточность витамина А ведет к ксерофтальмии (кератинизация роговицы). Повышенная восприимчивость к раку связана с тем, что β-каротин является мощным антиоксидантом.
Витамин Е по химической природе представляет собой группу восьми близкородственных соединений – токоферолов и токотриенолов. Наибольшая E -витаминная активность присуща -токоферолу. Витамин Е абсорбируется из кишечника и накапливается в клеточных мембранах, жировых депо и циркулирующих липопротеинах. Основное место хранения витамина Е в организме человека – жировая ткань.
Суточная потребность в витамине E составляет 10…20 мг. Витамин Е является мощным антиоксидантом, связывает свободные радикалы и молекулярный кислород, предотвращая от окисления жирные кислоты мембран, снижая физическое и эмоциональное напряжение.
-Токоферол может связывать два пероксидных свободных радикала и потом, взаимодействуя с глюкуроновой кислотой, выводиться из организма в составе желчи. Главными симптомами недостаточности витамина Е является увеличение хрупкости эритроцитов, мышечная слабость и бесплодие [4].
1.1.3. Органические кислоты
Органические кислоты относятся к обязательным компонентам химического состава растительного сырья. В большинстве растительных объектов обнаружены нелетучие моно- и трикарбоновые кислоты, предельные и непредельные, в том числе гидрокси- и оксоксилоты. В продуктах переработки плодов, например, в мезге, могут быть выявлены летучие кислоты — муравьиная и уксусная [5].
В обмене веществ растительной клетки кислотам принадлежит исключительно важная роль: будучи в основном продуктами превращения сахаров, они участвуют в синтезе аминокислот, алкалоидов и многих других соединений. Ряд растений обладает способностью к синтезу и накоплению органических кислот и может служить сырьем для их промышленного получения [6].
Содержание органических кислот в дикорастущих плодах и ягодах варьирует в достаточно широких пределах – от 0,6 % до 6,0 %; наиболее высокая кислотность характерна для лимонника, барбариса, клюквы, облепихи, калины.
Перечень органических кислот, входящих в состав растительного сырья, достаточно широк, при этом наиболее распространёнными являются уксусная кислота, участвующая в обмене веществ всех без исключения растений в виде ацетил-КоА, а также яблочная, лимонная, щавелевая и янтарная кислоты, относящиеся к первичным продуктам фотосинтеза и принимающие участие в метаболизме растительной клетки.
Яблочная кислота ( COOH – CH 2– CH ( OH )– COOH )) является наиболее лабильной, она участвует в процессах фотосинтеза, подвергаясь быстрым изменениям и являясь промежуточным продуктом при биосинтезе многих соединений. Эта кислота известна в трёх стереоизомерных формах, но в растениях встречается только L -изомер [5].
Яблочная кислота является преобладающей в яблоках (0,4…0,7 г/100 гпродукта), большинстве видов косточковых; ею богаты красноплодная рябина, садовая земляника (1,2 г/100 г), клюква и крыжовник (1,0 г/100 г), малина (1,4 г/100 г) и облепиха (2,0 г/100 г), зеленые ягоды винограда (0,7…1,5 г/100 г), достаточно высокое содержание отмечается в сливе (3,5 % от а.с.в.) и ягодах барбариса (до 6 % от а.с.в.), выявлено присутствие яблочной кислоты в составе кислот айвы (0,5 г/100 г) и персиков (0,2 г/100 г), плодов цитрусовых, шиповника, ягод лимонника и черники, цветков календулы.
В виде малатов яблочная кислота накапливается в листьях мать-и-мачехи, чёрной смородины и подорожника (в последнем 0,2…0,5 %), траве хвоща и других видах сырья; особенно значительно в листьях сем. Толстянковых. Свободная кислота и её соли входят и в состав сопутствующих веществ ФАВ большинства видов сырья, заготавливаемого корневищами и корнями.
На примере винограда показано, что растения, произрастающие в северных районах, накапливают бóльшие количества яблочной кислоты, чем те же культуры, выращиваемые южнее. Данный факт находит объяснение в том, что при более высоких среднесуточных температурах яблочная кислота в плодах и зелёной массе растений расходуется на окисление быстрее винной, вследствие чего её доля в составе кислот снижается [7].
Лимонная кислота и ее соли цитраты:
Встречаются в растительном сырье не менее часто. Ими наиболее богаты плоды цитрусовых (лимон – 5,5…5,7 г/100 г), из которых преимущественно лимонную кислоту выделяли в промышленных масштабах до 1922 г.; гранаты, ягоды смородины (2,0…10,0 г/100 г), лимонника, малины, клюквы (1,1…3,0 г/100 г), в меньшем количестве лимонная кислота содержится в ягодах крыжовника (0,3 г/100 г) и земляники (0,1 г/100 г), айве (0,3 г/100 г), персиках (0,1…0,2 г/100 г) и яблоках (0,1 г/100 г), плодах шиповника, красноплодной рябины и боярышника; из травянистого сырья лимонная кислота идентифицирована в листьях черники, чёрной смородины, чистотела, подорожника (1,2…1,5 %) и некоторых других.
Щавелевая кислота ( HOOC – COOH ) является одним из побочных продуктов жизнедеятельности растительной клетки, поэтому химически наименее активна и накапливается в растительном сырье в основном в виде кальциевой соли (оксалаты – кристаллы различной, специфичной для вида растения, формы; этот признак используется при идентификации лекарственно-технического сырья), накапливаясь преимущественно в сочном травянистом сырье: листьях щавеля (оксалата кальция 0,56…0,93 г/100 г) и ревеня (2,37 г/100 г), траве хвоща, сочных чешуях луковичных растений, коре деревьев и т.п. Плодово-ягодная продукция щавелевой кислотой не богата (до 0,01…0,02 г/100 г),незначительные количества обнаружены в ягодах лимонника (0,06 г/100 г) и ягодах Брусничных.
Физиологически значимое содержание янтарной кислоты ( HOOC – CH 2– CH 2– COOH ) является характерным для ягод крыжовника, лимонника, красной смородины, черники и куманики, черешков ревеня. В достаточно высоких количествах (0,01…0,02 г/100 г) эта кислота и её соли сукцинаты содержатся в незрелых плодах и ягодах, например, вишне, черешне, сливе, яблоках, винограде. В числе других видов сырья, в кислотном комплексе которых выделены свободная янтарная кислота и её соли, можно отметить ягоды боярышника, корневища и корни родиолы, листья подорожника (0,2…0,5 %), горькой полыни, беладонны, мака, кукурузы.
Реже в растительном сырье встречается винная кислота ( COOH – CH ( OH )– CH ( OH )– COOH , D -изомер): в ягодах (зелёные – 0,8…1,3 г/100 г, вызревшие – от 0,2 до 1,0 г/100 г), стеблях и листьях винограда (до 3,7 % на сухую массу), красноплодной рябине, плодах боярышника, сливы и граната; ягодах малины, крыжовника, смородины, лимонника и брусники. В винограде наряду с D -кислотой содержатся пировиноградная кислота (следы) и неактивный DL -изомер винной кислоты – виноградная кислота. Кроме названных видов сырья, винная кислота входит в состав кислот листьев брусники, мать-и-мачехи, подорожника и т.д.
От содержания и состава органических кислот зависит не только вкус растительного сырья, но в какой-то степени и его ароматические свойства, что определяется наличием в летучей фракции свободных муравьиной, уксусной, пропионовой, масляной, каприловой и валериановой кислот и их эфиров. Названные кислоты обуславливают специфические оттенки аромата лекарственно-технического сырья, преимущественно растений-эфироносов, все они обладают резким, острым запахом. Так, муравьиная кислота ( HCOOH ) входит в состав органических кислот яблок, толокнянки, калины, шишкоягод можжевельника, ягод малины (1,76 мг/100 г), стеблей и листьев крапивы, травы тысячелистника и многих других видов сырья; в свободном состоянии она чаще встречается в зелёных листьях, считается, что она относится к промежуточным продуктам фотосинтеза. Уксусная кислота ( CH 3– COOH ) как в свободном состоянии, так и в составе сложных эфиров со спиртами, участвует в формировании вкусоароматических характеристик тех же калины и можжевельника, ягод брусники (следы), листьев мяты перечной, травы полыни и лесной земляники, тысячелистника, корневищ и корней валерианы, девясила и дягиля и т.д. Наличие валериановой и/или изовалериановой кислот (( CH 3)2 CH – CH 2– COOH ) установлено для листьев мяты и лавра благородного, травы иссопа, полыни и тысячелистника, лесной земляники, плодов калины, персиков и плодов какао, корневищ и корней валерианы и дягиля. В химический состав валерианы, кроме уже упомянутых органических кислот, входит масляная ( CH 3– CH 2– CH 2– COOH ); масляная кислота входит также в состав цветков ромашки аптечной.
Каприловая кислота обуславливает аромат персиков:
Пропионовая кислота ( CH 3– CH 2– COOH ) из всего многообразия растительного сырья найдена только в цветочных корзинках тысячелистника. Как видно из вышесказанного, для многих видов растительного сырья – источников эфирных масел – является характерным присутствие сразу всех летучих кислот[7].
Сложные эфиры органических кислот обуславливают характерный аромат растительного сырья: октилацетат – апельсина, метилбутират – абрикоса, изоамиловый эфир изовалериановой кислоты – яблок, себацинацетат – шишкоягод можжевельника обыкновенного, эфир борнеола с валериановой кислотой – корневищ и корней валерианы лекарственной и т.д.
Физиологически органические кислоты благоприятно влияют на процессы пищеварения, снижая рН среды и способствуя созданию определенного состава микрофлоры, тормозя процессы гниения в желудочно-кишечном тракте. Кислоты фенольной природы обладают бактерицидным действием. Усвояемые органические кислоты принимают участие и в формировании энергетической ценности продуктов питания и напитков с их участием: яблочная кислота – 2,4 ккал/г, лимонная – 2,5 ккал/г, молочная – 3,6 ккал/г и т.д. Винная кислота организмом человека не усваивается.
Некоторые органические кислоты участвуют в механизмах обменных процессов, отвечающих за контроль массы тела (например, гидроксилимонная кислота, ингибирующая цитрат лиазу в ферментной системе синтеза жирных кислот) – на этом свойстве базируется разработка БАД из лекарственно-технического растительного сырья, действие которых основано на угнетении синтеза жирных кислот из углеводов denovo . Янтарная кислота способствует улучшению энергетического обеспечения клеток головного мозга, миокарда, печени, почек; оказывает антиоксидантное и антигипоксическое действие (механизм действия связан с увеличением синтеза АТФ, торможением гликолиза и активацией аэробных процессов в клетках, усилением глюконеогенеза). Кроме того, янтарная кислота способствует стабилизации клеточных мембран, что предотвращает потерю ферментов и обеспечивает функционирование механизмов дезинтоксикации в клетках. На фоне флавоноидов и сапонинов (солодки, например) янтарная кислота проявляет противовоспалительное, дезинтоксикационное и спазмолитическое действие.
С гигиенических и токсикологических позиций отмечается способность органических кислот влиять на минеральный обмен. Так, щавелевая кислота интенсивно связывает кальций, а лимонная – напротив, способствует его усвоению организмом человека. Названные свойства органических кислот необходимо учитывать при составлении рецептур продуктов питания и напитков с ориентацией последних на определенные категории потребителей [8].
Строение и классификация
В 1790 году французский химик Луи Никола Воклен, активно исследовавший объекты растительного происхождения, выделил из фруктового сока вещество, хорошо растворимое в воде и обладающее свойством желировать водные растворы. Спустя 40 лет родилось современное название выделенного вещества – пектин (греч. «pektos» – свернувшийся, застывший). Структура пектина была выяснена лишь в 1924 году [9].
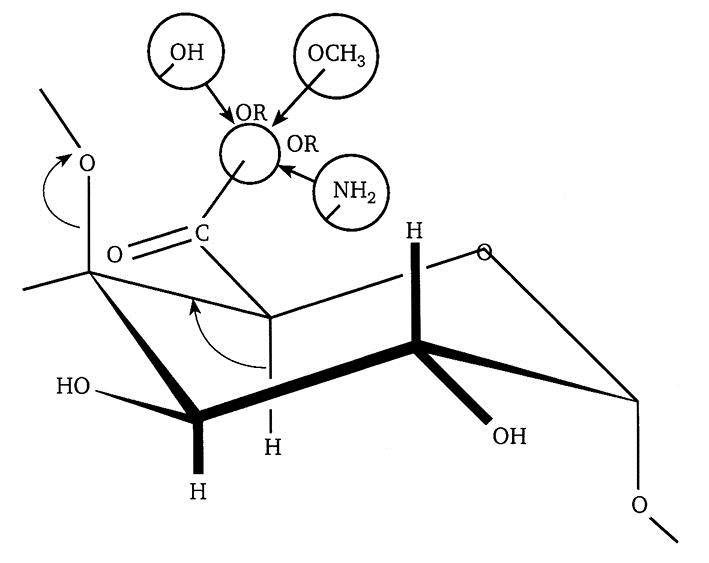
Пектиновые вещества, содержащиеся в растительных соках и плодах, представляют собой гетерополисахариды, построенные из остатков галактуроновой кислоты, соединенных α-(1,4)-гликозидными связями.
Полигалактуроновая кислота чаще в той или иной степени метоксилирована (этерифицирована метиловым спиртом).
В состав пектиновых веществ наряду с мономером D-галактуроновой кислоты входят сахара D-галактоза, L-рамноза, L-арабиноза, D-ксилоза. В некоторых пектиновых веществах обнаружены D-глюкоза, D-фруктоза, 2-0-метил-L-фруктоза, 2-0-метил-D-ксилоза и др. Таким образом, пектиновые вещества являются гетерополисахаридами [10].
Сахара присоединены к основной цепи полигалактуронана в виде олиго – и полисахаридных цепочек, причем остатки галактозы в них находятся в форме пиранозы и соединены между собой β-1,4-связью. Цепи галактана неразветвленные, сравнительно короткие. Цепи арабана, наоборот, длинные, разветвленные остатки арабинозы в них находятся в форме фуранозы и присоединяются к галактану по 1,3-связям. Присутствующая в растительной ткани фосфорная кислота может одновременно этерифицировать два гидроксила, принадлежащих различным цепям полигалактуронанов, и образовывать многочисленные разветвления. Последние могут возникать и при нейтрализации карбоксильных групп поливалентными катионами.
Пектиновые вещества относительно легко разделяются на две фракции – нейтральную и кислую. Первая представлена сахаридным комплексом, вторая — полигалактуронаном.
Согласно современной номенклатуре в пектиновых веществах различают протопектин, пектин, пектиновую кислоту и пектинаты, пектовую кислоту и пектаты.
— Протопектин – нерастворимый в воде природный пектин, сложного, точно не установленного строения. Предполагают, что в состав его входят все рассмотренные выше комплексы.
— Пектин, или растворимый пектин, — водорастворимые полигалактуроновые кислоты, метоксилированные в различной степени, образуется из протопектина под действием кислот, щелочей или фермента протопектиназы.
— Пектиновая кислота — высокомолекулярная полигалактуроновая кислота, часть карбоксильных групп которой этерифицирована метиловым спиртом. Соли ее называются пектинатами.
— Пектовая кислота получается из пектиновой кислоты в результате ее полного деметоксилирования. Растворимость пектовой кислоты меньше, чем пектиновой. Соли пектовой кислоты называются пектатами [ 11 ].
Отдельные представители пектиновых веществ в растительных тканях располагаются неравномерно. Протопектин вместе с другими полисахаридами входит в состав клеточных стенок и срединных пластинок молодых тканей. Растворимый пектин содержится во всех частях клетки, но главным образом в клеточном соке. Жесткость незрелых плодов определяется наличием в них значительного количества протопектина. Во время созревания плодов под влиянием органических кислот и фермента протопектиназы протопектин расщепляется, при этом плод становится менее жестким.
Пектины, полученные из различных растительных источников, представляют собой порошки без запаха от светлокремового до коричневого цвета. Цитрусовые пектины обычно светлее яблочных. Выделенный и очищенный пектин представляет собой белый порошок. Молекулярная масса пектина изменяется в широких пределах и колеблется от 15 000 до 360 000. Например, яблочный пектин имеет молекулярную массу от 17 000 до 200 000, цитрусовый от 23 000 до 360 000.
Пектин плохо растворяется в холодной воде, лучше в горячей с образованием коллоидного раствора – золя. Растворимость пектина возрастает с уменьшением молекулярной массы и увеличением степени этерификации. Пектиновые кислоты нерастворимы в воде. Пектины из водных растворов осаждаются спиртом и другими органическими растворителями.
Во влажной атмосфере пектины могут сорбировать до 20 % воды. В избытке воды они растворяются. Пектины не растворяются в растворах с cодержанием сухих веществ более 30 %. В отличие от сахарного песка, который сразу же после попадания в воду начинает растворяться, частица пектинового порошка, попав в воду, всасывает ее, словно губка, увеличиваясь в размерах в несколько раз, и только после достижения определенного размера начинает растворяться. Если частицы пектинового порошка при соприкосновении с водой находятся близко друг к другу, то, всасывая воду и разбухая, они слипаются, образуя один большой липкий ком, чрезвычайно медленно растворяющийся в воде[12].
В водных растворах макромолекула пектина имеет спиралевидно скрученную цепь, карбоксильные группы которой расположены одна под другой. При электролитической диссоциации этих групп возникают отталкивающие силы, вследствие чего спиральная молекула выпрямляется, увеличиваются ее линейный размер и вязкость. Пектин при катафорезе осаждается на аноде, что указывает на отрицательный электрический заряд его частиц.
В присутствии cахаров и кислот пектин образует студни. Желирующая способность пектинов увеличивается с увеличением молекулярной массы и степени этерификации. Богаты метоксильными группами пектины яблок, смородины, крыжовника, цитрусовых (7-12%). Кислоты уменьшают диссоциацию карбоксильных групп пектинов, уменьшаются и силы отталкивания. Кроме того, сахар отнимает у пектинов часть гидратной воды. В результате устойчивость пектинового золя снижается. Определенную роль при образовании желе играют и водородные связи, возникающие между карбоксильными и гидроксильными группами. Желе может образоваться в присутствии и поливалентных катионов, например кальция, связывающего карбоксильные группы двух макромолекул пектиновой кислоты. Пектиновые вещества содержатся во всех плодах и ягодах. Особенно их много в сливах, черной смородине, черешне и яблоках [6].
Пектины довольно стойки к действию кислот, под действием щелочей они разрушаются; легко подвергаются окислительному расщеплению. Ферменты, действующие на пектины, делятся на пектинэстеразы, гидролизующие сложноэфирные группировки, отщепляя метильные группы, и полигалактуроназы, расщепляющие полигалактуронидную цепь до олигоуронидов и далее до D-галактуроновой кислоты. Эти пектиновые ферменты встречаются в микроорганизмах и растениях, используют для расщепления пектиновых веществ при осветлении фруктовых соков [3].
1.2.2. Свойства и функции пектиновых веществ
В растительной клетке пектин выполняет функцию структурирующего агента в центральном слое клеточной стенке. Благодаря своей высокой способности к набуханию и своему коллоидному характеру пектин регулирует водный обмен растений.
Пектин, являясь не усваиваемым полисахаридом, образует группу пищевых волокон, которые выполняют весьма важные функции в организме, такие как:
— стимулируют моторную функцию кишечника;
— препятствуют всасыванию холестерина;
— играют положительную роль в нормализации состава микрофлоры кишечника, в ингибировании гнилостных процессов;
— оказывают влияние на липидный обмен, нарушение которого приводит к ожирению;
— адсорбирует желчные кислоты [13].
Кроме того, пектин обладает детоксицирующими свойствами, т.к. способен связывать токсичные элементы и радионуклиды и выводить их из человеческого организма (табл. 1 и 2). Это делает пектин и пектинсодержащие продукты ценной добавкой при производстве пищевых продуктов лечебно-профилактического назначения. Комплексообразующая способность пектина основана на его способности образовывать нерастворимые комплексные соединения с тяжелыми металлами и радионуклидами. Именно это свойство определяет пектин по рекомендации Всемирной организации здравоохранения (ВОЗ) как профилактическое средство в экологически загрязненных территориях. Профилактическая суточная доза пектина составляет 4 – 5 г, в условиях радиоактивного загрязнения – 15 – 16 г.
Видео:№10 кач реакции на крахмал, пектин и целлюлозуСкачать

Видео:Качественные реакции на белкиСкачать

ГК «Униконс»
Продвижение и реализация комплексных пищевых добавок, антисептиков и др. продукции.
Видео:Качественные реакции на катионы. 9 класс.Скачать

«Антисептики Септоцил»
Септоцил. Бытовая химия, антисептики.
Видео:РЕАКЦИИ ИОННОГО ОБМЕНА, ИОННОЕ УРАВНЕНИЕ - Урок Химия 9 класс / Подготовка к ЕГЭ по ХимииСкачать

«Петритест»
Микробиологические экспресс-тесты. Первые результаты уже через 4 часа.
Видео:Биохимия. Качественные реакции для определения белков, аминокислот и углеводов (С. Смирнов)Скачать

«АльтерСтарт»
Закваски, стартовые культуры. Изготовление любых заквасок для любых целей.
- Вы здесь:
- Библиотека технолога
- Пищевые добавки и ингредиенты
- Донченко — Пищевая химия. Гидроколлоиды
Видео:Качественные реакции в неорганике | ЕГЭ по ХИМИИ 2023Скачать

2.5. ПЕКТИНЫ
Промышленные пектины, используемые в качестве пищевых добавок, являются гетерополисахаридами, содержащими не менее 65% (по массе) остатков галактуроновой кислоты, которые могут быть представлены в виде свободной кислоты, ее метилового эфира или (в амидированных пектинах) амида кислоты (рис. 2.9). Стрелки указывают направление возможного превращения сложноэфирной формы путем (З-элиминирования.
Рис. 2.9. Структурные единицы галактуроновой кислоты, ее эфиры и амиды в молекуле пектина
Промышленные пектины обычно содержат сахар, который добавляют для стандартизации их свойств.
Пектиновые вещества (Е 440) – улучшители консистенции: загустители, уплотнители, гелеобразователи, стабилизаторы и эмульгаторы.
Пектиновые вещества представляют собой высокомолекулярные полисахариды, входящие в состав клеточных стенок и межклеточных образований совместно с целлюлозой, гемицеллюлозой и лигнином. В понятие пектиновые вещества входят гидратопектин (растворимый пектин), протопектин (нерастворимый в воде пектин), пектиновые кислоты и пектинаты, пектовые кислоты и пектаты.
Основным структурным признаком пектиновых веществ являются линейные молекулы полигалактуроновой кислоты, в которой мономерные звенья связаны гликозидной α-(1→4) -связью. В пищевой промышленности пектин получают из яблочных и цитрусовых выжимок, свекловичного жома, соцветий-корзинок подсолнечника, створок плодов-коробочек хлопчатника. В зависимости от вида сырья пектин имеет различные органолептические и физико-химические показатели. Пектин, как и другие гелеобразователи, не растворяется в среде, где существуют условия для студнеобразования. Основными свойствами пектиновых веществ, которые определяют области их применения в пищевой промышленности, являются студнеобразующая и комплексообразующая способности.
Высокоэтерифицированные пектины применяют в качестве студнеобразователя при производстве кондитерских (мармелад, пастила, зефир, желейные конфеты) и консервных (желе, джем, конфитюр, фрукты в желе) изделий; в качестве стабилизаторов при производстве молочных напитков, майонеза, маргарина, аналогов сливочного масла, соусов, мороженого, рыбных консервов; в качестве средства, замедляющего черствение в производстве хлебобулочных изделий; в качестве загустителей при производстве фруктовых соков и киселей. Низкоэтерифицированные пектины применяют при изготовлении овощных желе, паштетов, студней, сыров и пищевых продуктов детского, лечебного и профилактического питания.
Отрицательного действия пектина не установлено, и его применение в качестве пищевой добавки разрешено без ограничений во всех странах мира.
Для амидированного пектина, у которого часть свободных карбоксильных групп превращена в амиды, установлена величина ДСП – 25 мг/кг массы тела.
Амидированный пектин проверен Комитетом экспертов ФАО/ВОЗ по пищевым добавкам. Результаты долгосрочных исследований на крысах не содержат никаких доказательств канцерогенной активности этого вещества; исследования тератогенного действия также показали отсутствие неблагоприятных последствий.
2.5.1. КРАТКАЯ СХЕМА ПРОИЗВОДСТВА ПЕКТИНА
Пектины различного качества и в разном количестве присутствуют во многих плодах. Основным критерием выбора сырьевого источника является содержание в нем пектина в достаточном количестве и соответствующего качества.
Пектиносодержащее сырье можно подразделить на три основные группы.
К первой группе отнесены овощи: клубнеплоды (картофель), корнеплоды (свекла, морковь), листовые (капуста, лук), стеблевые (сельдерей), плодовые (баклажаны, томаты), тыквенные (арбузы, дыни, тыквы) и бобовые (горох, фасоль).
Вторая группа пектиносодержащего сырья включает плоды и делится на подгруппы: семечковые плоды (яблоки, айва), косточковые (вишня, черешня), ягоды настоящие (виноград, смородина), ягоды (земляника, клубника, малина), субтропические и тропические (лимоны, апельсины, мандарины, инжир, гранаты).
В третью группу включены другие виды промышленного сырья также с высоким содержанием пектина: листья чая и табака, стебли и соцветия-корзинки подсолнечника, створки плодов-коробочек хлопчатника, кора хвойных пород деревьев (сосна, ель, лиственница).
В первой группе наибольшее количество пектина содержится в корнеплодах (6,4-30,0%) и тыквенных овощах (1,7-23,6%); во второй – в семечковых (3,3-19,9%), тропических (5,5-15,8%) и субтропических (9,0-14,0%) плодах, ягодах настоящих (4,2-12,6%), в третьей группе – в стеблях (20,0-35,7%) и корзинках подсолнечника (до 24%).
В подгруппе корнеплодов наибольшее содержание пектиновых веществ у свеклы сахарной и кормовой (18-30%), моркови (6,4-20,0%), свеклы красной (8,1-14,9%). В подгруппе тыквенных овощей наибольший интерес в качестве промышленного пектиносодержащего сырья представляют арбуз кормовой (6,4-23,6%) и тыква (2,6-17%). Арбуз столовый и дыня могут быть рекомендованы для включения в профилактическое питание как продукты с относительно высоким содержанием пектиновых веществ.
В подгруппе семечковых плодов наибольшее количество пектиновых веществ содержится в яблоках (6,1-19,9%) и рябине (9,3–10,6%), несколько меньше – в айве (5,3-9,6%), грушах (3,3-8,0%). Однако из-за небольших объемов промышленной переработки рябины в качестве сырьевого источника для получения пектиносодержащих студнеобразователей (пасты, пюре) следует рассматривать айву и груши.
В подгруппе субтропических и тропических плодов высокое содержание пектиновых веществ наблюдается в инжире (5,5-15,8%), гранатах (10-14%), фейхоа и хурме (9-12%). Это позволяет сделать вывод о целесообразности использования этого вида сырья для производства пектиносодержащих пищевых изделий, так как рассматриваемые плоды помимо пектиновых содержат ряд других биологически активных веществ, определяющих их лечебные и диетические свойства.
Наиболее распространенные из субтропических плодов – цитрусовые: лимоны, апельсины, грейпфруты, мандарины – также практически не отличаются между собой по содержанию пектиновых веществ. В среднем количество пектина в их тканях колеблется в пределах 9-14 %.
В подгруппе ягод настоящих наибольшее количество пектиновых веществ содержится в красной смородине (4,2-12,6%), клюкве (6,6-11,0%), черной смородине (5,9-10,6%), крыжовнике (5,5-7,9%) и винограде (4,2-6,6%). Благодаря высокому содержанию пектина, витаминов С и Р, органических кислот и Сахаров, хорошо сбалансированных по вкусу, эту подгруппу плодов целесообразно использовать при производстве пектиносодержащих пищевых изделий.
Перспективными источниками сырья для промышленного производства пектина являются также свекловичный жом, стебли и соцветия-корзинки подсолнечника, створки плодов-коробочек хлопчатника, кора хвойных пород деревьев и кормовой арбуз.
Важной характеристикой пектиносодержащего сырья, помимо массовой доли пектина, является соотношение протопектина (ПП) и растворимого пектина (РП), обусловливающее различие в технологических параметрах извлечения пектина и его физико-химических свойствах.
В настоящее время основными промышленными сырьевыми источниками пектина являются цитрусовые отжимы и яблочные выжимки.
Из всего многообразия перерабатываемых в промышленности видов цитрусовых предпочтительными для получения высококачественного пектина являются выжимки лимонов и лаймов, хотя апельсиновая выжимка доступна в значительно больших объемах, а также может быть использована при производстве пектина различного назначения. Цитрусовые отжимы для получения пектина, как правило, промывают водой без использования кислоты, а затем тщательно высушивают до влажности 8-10%. Они также могут быть направлены на переработку и во влажном состоянии. Переработка влажных отжимов является наиболее целесообразной именно в случае апельсинового сырья, но при этом необходимо, чтобы источник большого количества выжимки был расположен в непосредственной близости от пектинового завода.
Пектин весьма чувствителен и к воздействию ферментов, содержащихся во влажной выжимке, и к нагреванию в ходе сушки и последующей обработки, и такая потеря качества должна максимально тщательно контролироваться. Производители пектина тратят значительные средства на обеспечение как наличия, так и качества сырья, так как именно качество является решающим фактором, определяющим тип промышленного пектина.
Хотя в последнее время было запатентовано большое количество разнообразных процессов производства пектина, большую часть пектинов получают путем их экстрагирования из сырья горячим водным раствором минеральной кислоты. Каждым производителем подбираются свои условия процесса применительно к основному виду сырья, перерабатываемого на его заводе.
Однако во всех случаях целью является образование жидкой массы, состоящей из легко фильтруемого посредством выбранной технологии твердого остатка и жидкой фазы, содержащей максимально возможную (при этом не вызывающую чрезмерного повышения вязкости) концентрацию высокомолекулярного пектина. Перед началом выделения пектина из раствора жидкий экстракт можно подвергнуть обработке с целью удаления всех примесей, а затем дополнительно очистить для удаления мельчайших частиц.
В принципе существует несколько способов выделения чистого пектина. Наиболее распространенным из них является смешивание пектинового экстракта с органическим растворителем, в котором пектин не растворим и выпадает в осадок, а примеси остаются в растворе. Международные стандарты позволяют использовать в качестве органического растворителя только метанол, этанол или изопропанол. В ходе процесса очищенный пектиновый экстракт концентрируется до содержания пектина приблизительно 2%, а затем смешивается с необходимым количеством спирта, что приводит к выпадению достаточно твердого осадка, чтобы его можно было отделить от пектина одним из способов, выбранным производителем: фильтрацией или центрифугированием. Пектин максимально отделяют от исходной жидкости и промывают один или несколько раз водно-спиртовым раствором для удаления солей и других примесей. Жидкость для промывания может содержать определенное количество пищевой щелочи, необходимое для корректировки рН раствора конечного пектина до заданного значения.
Другой метод, который в настоящее время не столь популярен, основан на способности основных солей алюминия образовывать ионообменные комплексы с анионными полимерами, такими как пектин. Происходит образование полимеризованных гидроксид-ионов алюминия, которые взаимодействуют с отрицательно заряженной молекулой пектина и образуют осадок. Преимуществом этого способа осаждения является то, что экстракт пектина необязательно должен быть концентрированным, и при соблюдении определенных условий происходит флокуляция осадка, что позволяет легко выделить его из большого объема жидкости. На этой стадии осажденный пектин из-за взаимодействия с ионами алюминия и наличия примесей приобретает зеленовато-желтый цвет. Перед обработкой водным раствором гидроксикислоты, которая приводит к выделению алюминия и получению очищенного пектина, «желтую массу» отпрессовывают, чтобы понизить содержание жидкости.
Как только выпавший в осадок (в результате любого из описанных приемов) пектин максимально отделен от спирта, его высушивают и измельчают до получения тонкого порошка. Пектин, произведенный таким способом, в зависимости от природы и качества исходного сырья будет иметь различную студнеобразующую способность, но в традиционных условиях приготовления джема будет быстро образовывать гель. Смешивая одну или несколько партий пектина с расчетным количеством сахара, который обеспечивает стандартный процесс, можно корректировать прочность геля. Другие, более тонкие изменения сводятся к минимуму в результате отбора исходных партий для смешивания на данной стадии, что позволяет обеспечивать необходимую консистенцию. В таком виде пектин можно продавать либо далее модифицировать, чтобы обеспечить возможность расширения областей его использования.
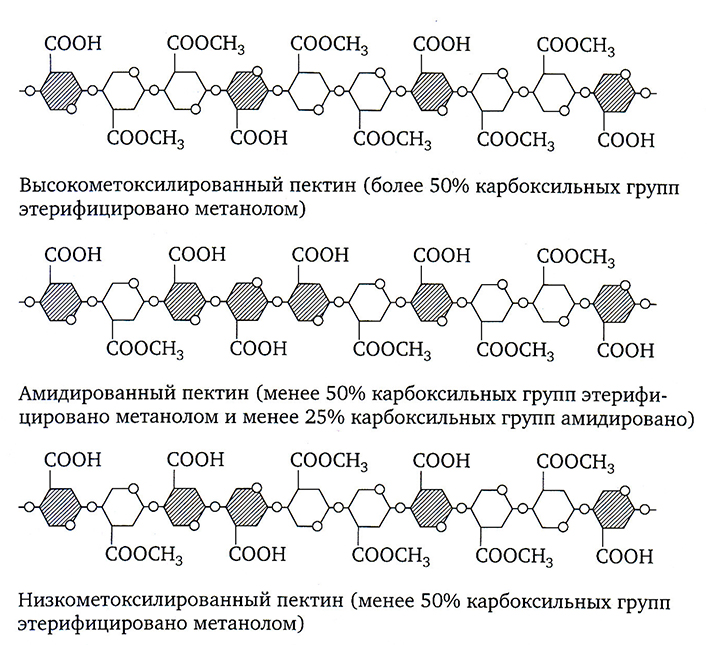
Из перечисленных видов сырья вырабатывают пектин трех основных видов (рис. 2.10):
- высокоэтерифицированный;
- низкоэтерифицированный;
- амидированный.
Степень этерификации промышленных высокоэтерифицированных пектинов обычно колеблется в пределах 58-75%. При использовании этих пектинов для формирования гелей содержание растворимых сухих веществ должно быть не менее 55%, а рН равным 2,8-3,5.
Высокоэтерифицированные пектины вырабатывают с разной скоростью студнеобразования – быстрой, среднебыстрой и медленной.
Низкоэтерифицированные пектины делятся на две основные группы:
- обычный низкоэтерифицированный пектин;
- амидированный низкоэтерифицированный пектин
Рис. 2.10. Основные виды промышленных пектинов
Обе подгруппы характеризуются способностью образовывать гелевые системы с низким содержанием сухих веществ и широким диапазоном значений рН. Оба типа образуют гели в присутствии кальция.
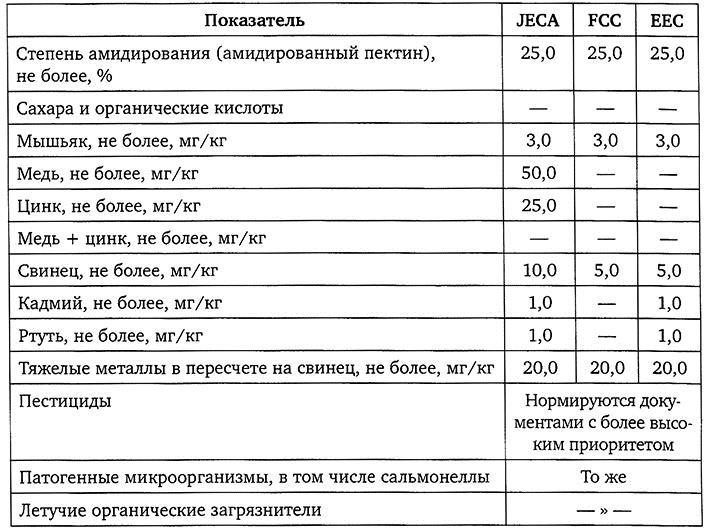
Требования к пищевому пектину в соответствии с международной нормативной документацией приведены в табл. 2.8.
Международные требования к пищевому пектину
Примечание: JECFA – Объединенный экспертный комитет по пищевым добавкам ВОЗ; FCC – Международный кодекс пищевых веществ; EEC – законодательство Европейского сообщества.
Помимо пищевого пектина промышленностью вырабатывается пектин для медицинских целей. Требования к нему определены USP – фармакопеей США.
С учетом расширения ассортимента пектиносодержащих пищевых изделий на мировом продовольственном рынке помимо амидированных, высоко- и низкоэтерифицированных пектинов промышленностью вырабатываются комбинированные пектины.
В настоящее время вырабатываются комбинированные пектины трех стандартных типов: быстро-, средне- и медленножелирующий.
2.5.2. СТРУКТУРА ПЕКТИНА
Как уже отмечалось, основным структурным признаком пектиновых веществ являются линейные молекулы полигалактуроновой кислоты, в которой мономерные звенья связаны гликозидной α-(1→4)-связью. Мономер имеет конфигурацию С1, поэтому гликозидные связи являются диаксиальными. У пектинов сахарной свеклы, подсолнечника, картофеля, груши в некоторых мономерных звеньях галактуронана спиртовые группы в положениях С2 и СЗ ацетилированы.
Гетерополисахаридный характер пектина обусловлен присутствием трех структурных единиц: пектовой кислоты, галактана и арабинана.
Пектовая кислота, кроме D-галактуроновой кислоты, включает нейтральные сахара: L-арабинозу, D-галактозу, L-рамнозу.
Существуют различные теории относительно распределения I-рамнозы в основной цепи молекулы пектина.
А. Риз (A. Rees) и его сотрудники считают, что в цитрусовом, яблочном и подсолнечном пектинах единицы L-рамнозы более или менее равномерно включены в галактуроновую цепь и соединены между собой (1→2)-связями:
где GalA – галактуронан; Rha – рамноза.
Длина полигалактуроновых последовательностей между звеньями L-рамнозы постоянна и составляет 25 ед. С основной галактуроновой цепью ковалентно связаны нейтральные сахара в виде боковых групп или даже боковых цепей. Длинные боковые цепи состоят в основном из остатков L-арабинозы, D-галактозы, короткие – из остатков D-метилксилозы, D-маннозы и L-фукозы. Эти результаты базировались на результатах частичного кислотного гидролиза, предшествовавшего фракционированию продуктов гельфильтрацией.
Однако другие исследователи, использовавшие подобные условия частичного кислотного гидролиза цитрусового пектина, но проводившие затем фракционирование полученных продуктов методом ионообменной хроматографии, не подтвердили эту гипотезу.
Исследования В. Пильника (V. Pilnic) и др., проведенные с яблочным пектином, показали, что L-рамнопиранозильные единицы неравномерно распределены в пределах основной цепи галактуронана. Молекула яблочного пектина, как наиболее изученного, по их мнению, состоит из «гладких» (линейных) участков и разветвленных фрагментов. Линейные фрагменты пектина являются гомогалактуронаном со степенью этерификации от 70 до 80%. В разветвленных фрагментах (1→2)-связанные рамнозильные звенья чередуются с (1→4)-связанными D-галактуроно-пиранозильными звеньями, образуя так называемый рамногалактуронан-1.
Длина данной чередующейся структуры неизвестна. По этому вопросу литературные сведения также противоречивы. Так, по данным американского исследователя К. Альберсхейма (С. Albersham), для некоторых пектинов она может содержать 300 L-рамнозильных и 300 D-галактуроновых кислотных звеньев. Приблизительно половина L-рамнозильных остатков связана через С4 с ответвлениями в виде линейных цепей из β-(1→4)-0-галактопиранозы и α-(1→5)-L-арабинофуранозы. К рамногалактуроновой цепи могут присоединяться и другие нейтральные сахара: манноза, фруктоза, глюкоза. Общее количество нейтральных Сахаров варьирует в зависимости от вида сырья, условий экстрагирования и последующих обработок.
Результаты исследований, проведенных нидерландским ученым А. Г. Ворагеном (A. G. Voragen), показали, что рамногалактуронан-1 (RG-I) состоит из 100 чередующихся звеньев:
дисахарид[→2)-α-L-рамнозил-(1→4)-α-D-галактозилуроновая кислота-(1→].
В зависимости от источника полисахарида от 20 до 80% L-рамнозильных остатков связаны через С 4 с арабинозой и галактозой (рис. 2.11). Результаты исследований показали, что длина боковых цепей может колебаться от одного до 50 и более гликозильных остатков. Иногда к концу боковых цепей присоединяются фукозил-, глюкоронозил- или 4-0-метил-глюкоронозил-остатки.
Рис. 2.11. Схематическая структура пектина:
Остатки ксилозы составляют около 1% RG-I, но их местоположение в молекуле не определено. Структура и механизм расщепления боковых цепей до настоящего времени изучены недостаточно. Фракционирование смеси боковых цепей RG-I при помощи высокоэффективной жидкостной хроматографии и последующий масс-спектроскопический анализ показали наличие по крайней мере 30 различных боковых цепей.
По мнению некоторых исследователей, наличие рамнозы в составе цепи пектиновых веществ свидетельствует о существовании двух различных видов гликозидных связей:
- кислотоустойчивых – между остатками галактуроновой кислоты, а также ее звеньями и рамнозой;
- менее кислотоустойчивых – между остатками рамнозы и галактуроновой кислоты.
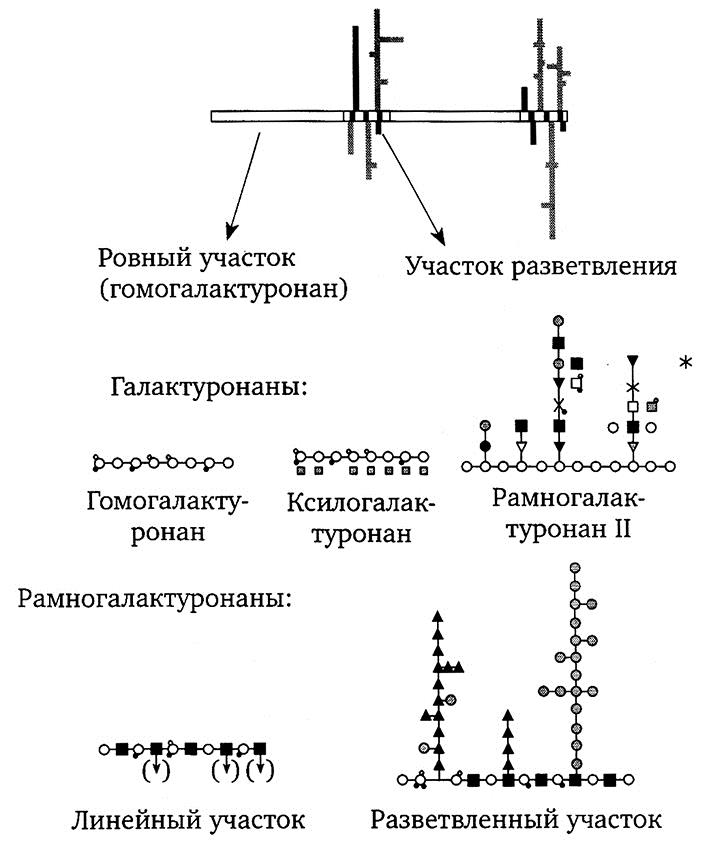
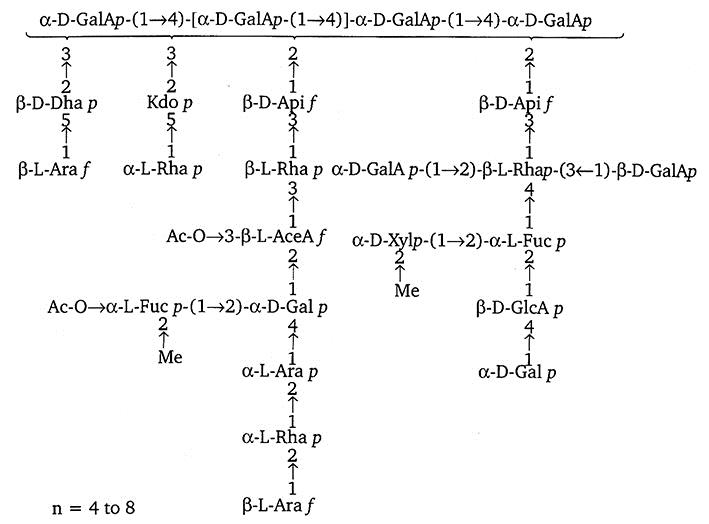
Исследования последних лет показали, что пектиновые вещества помимо гомогалактуронана, ксилогалактуронана, рамногалактуронана-I содержат также рамногалактуронан-II (рис. 2.12). Рамногалактуронан-II имеет очень сложное строение и состоит из 11 различных гликозидных остатков, включающих редко встречающиеся остатки апиозы, 2-O- метилфукозы, 2-O-метилксилозы, 1-рамнозил-(1→5)-3-дезокси-O- манно-2-октулозоновой кислоты и т.д.
Рис. 2.12. Модель структуры рамногалактуронана-Н (RG—II) с четырьмя олигогликозильными остатками
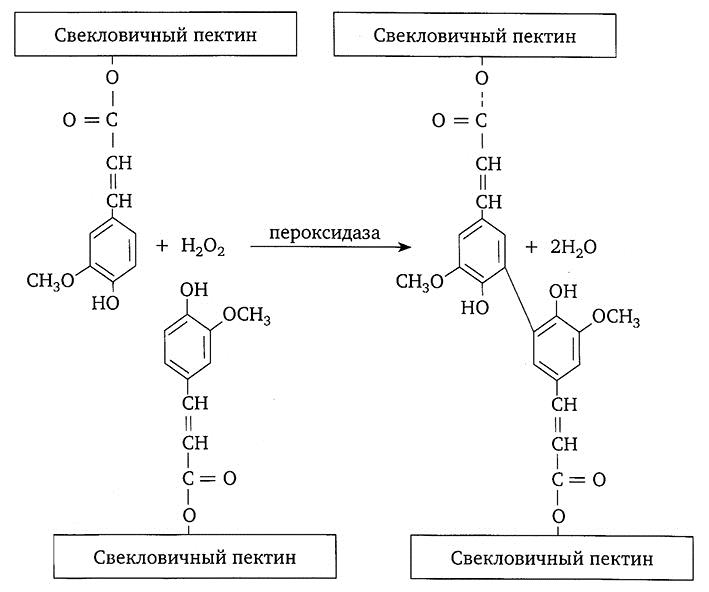
Структура пектина сахарной свеклы отличается от приведенных выше моделей тем, что она содержит значительное количество ацетильных и феруловых групп. Феруловая кислота связана эфирной связью с арабанами и галактанами боковых цепочек пектина. Свекловичный пектин содержит до 0,6% феруловых групп. В результате под действием фермента пероксидазы, способной катализировать окислительную конденсацию арабино- и галактопиранозных остатков пектиновых полисахаридов, происходит поперечная сшивка пектиновых молекул при помощи диферулатных мостиков по схеме
По последним данным, структурные элементы, присутствующие в молекуле пектиновых веществ, варьируются в зависимости от вида сырья.
Структура и химический состав пектиновых веществ определяют пространственную форму их молекул и характер взаимодействия с другими соединениями. Установлено, что пектиновые вещества обладают структурой с ограниченной гибкостью, стабилизируемой водородными и гидрофобными связями. Приведенный анализ отечественной и зарубежной литературы свидетельствует, что структуру боковых ветвей молекул пектиновых веществ до настоящего времени нельзя считать окончательно установленной.
2.5.3. СВОЙСТВА ПЕКТИНА
Одним из важнейших свойств пектиновых веществ является их комплексообразующая способность, основанная на взаимодействии молекулы пектина с ионами тяжелых и радиоактивных металлов. Это свойство дает основание рекомендовать пектин для включения в рацион питания лиц, находящихся в среде, загрязненной радионуклидами и имеющих контакт с тяжелыми металлами.
Известно, что комплексообразующие свойства пектиновых веществ зависят от содержания свободных карбоксильных групп, т.е. степени этерификации карбоксильных групп метанолом. Степень этерификации определяет линейную плотность заряда макромолекулы, а, следовательно, силу и способ связи катионов.
При высокой степени этерификации пектина (свыше 90%) свободные карбоксильные группы, в которые включены атомы С6, в значительной степени удалены друг от друга. При этом кальциевые или стронциевые соли пектовой кислоты практически полностью диссоциируют. С уменьшением степени этерификации, т.е. при увеличении заряда макромолекулы, связь пектиновых веществ с катионами возрастает, а константа стабильности пектатов увеличивается в функции, близкой к логарифмической зависимости. При степени этерификации 40% происходит изменение конформации, приводящей к агрегатированию пектиновых макромолекул и образованию прочной внутримолекулярной хелатной связи.
Комплексообразующая способность не зависит от молекулярной массы пектина и определяется коэффициентом селективности катионного обмена, являющегося характеристикой насыщения пектиновых веществ двухвалентным катионом. Для Cu 2+ , Pb 2+ , Со 2+ , Sr 2+ , Са 2+ он соответственно равен 3300, 2580, 241,120,121.
Исследование сорбционной способности пектовой кислоты показало, что рассматриваемые катионы по комплексообразующей способности, или активности, располагаются в определенный ряд:
Mn 2+ > Cu 2+ > Zn 2+ > Со 2+ > > Pb 2+ > Ni 2+ > Са 2+ > Mg 2+ > Cd 2+ .
Такая последовательность объясняется тем, что катионы двухвалентного марганца, меди, кобальта, никеля помимо соединений типа R(COO)2Me образуют соединения другого вида за счет взаимодействия (кроме карбоксильных) с оксигруппами макромолекул или за счет образования соли типа R(COO)Me(OOCCH3).
Комплексообразующая способность пектина зависит от рН среды. При разных значениях рН пектиновые вещества имеют различные значения комплексообразующей способности. Для пектина из свекловичного жома высокая комплексообразующая способность достигается при рН 5 (505,0 мг РЬ 2+ /г) и рН 10 (503,7 мг РЬ 2+ /г). При таких значениях свекловичный пектин связывал до 64-–68% от общего количества введенного стронция. Для пектина из соцветий подсолнечника наибольшая комплексообразующая способность наблюдается при рН 9 (455,0 мг РЬ 2+ /г), пектина из кормового арбуза – при рН 5 (380,0 мг РЬ 2+ /г), яблочного пектина – при рН 5 (312,3 мг РЬ 2+ /г), пектина из виноградных выжимок – при рН 10 (283,0 мг РЬ 2+ /г).
Таким образом, оптимальное значение рН среды, при котором происходит максимальное комплексообразование, для каждого типа пектина индивидуальное и зависит от вида пектиносодержащего сырья. Высокая комплексообразующая способность у всех пектиновых веществ наблюдается в интервале рН от 4 до 12, причем максимальные значения достигаются для многих пектинов при рН 5 и 9.
Следует, однако, отметить, что в более разбавленных растворах пектин проявляет ббльшую способность к комплексообразованию. При этом с увеличением концентрации пектина в растворе первоначально наблюдается даже снижение комплексообразующей способности. Это, вероятно, связано с взаимной блокировкой карбоксильных групп.
Существенное влияние на комплексообразующую способность оказывает парный эффект пектина и соли тяжелого металла. Одновременное снижение концентрации пектина в растворе при увеличении концентрации тяжелого металла в нем приводит к значительному увеличению константы связывания. Так, при взаимодействии в растворе одной части кобальта с 10 частями пектина, полученного из соцветий подсолнечника, связывается 7,8% металла, а при соотношении 1:100 – 80,2%, аналогично этому при снижении концентрации до 0,5% свекловичного пектина им связывается 75% стронция.
Благодаря комплексообразующему свойству по отношению к металлам пектин является незаменимым веществом в производстве пищевой продукции профилактического и лечебного питания. Оптимальная профилактическая доза пектина составляет не более 2-4 г в сутки для контактирующих с тяжелыми металлами, а в условиях радиоактивного загрязнения – не менее 15-16 г.
Не менее важным свойством пектиновых веществ, определяющим широкую область их применения в пищевой промышленности, является студнеобразующая способность. Студнеобразование зависит:
- от молекулярной массы пектина;
- степени этерификации его молекулы и содержания функциональных групп;
- концентрации сахара в растворе;
- количества балластных веществ, сопутствующих данному пектину;
- температуры и рН среды.
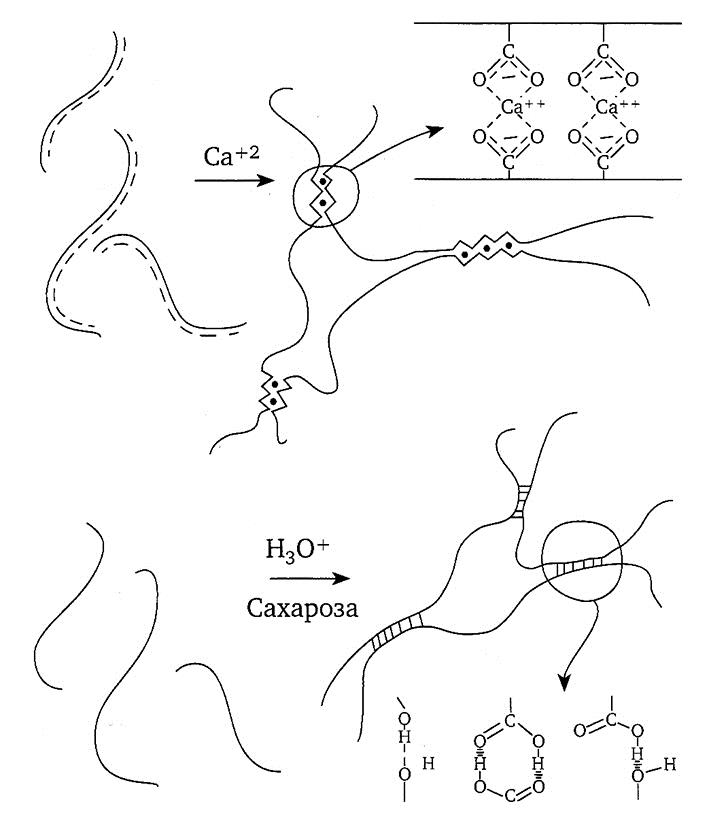
С учетом степени этерификации молекулы пектина различают два вида студней: с побочной валентностью и с основной (рис. 2.13).
Рис. 2.13. Механизм студнеобразования низкометоксилированного (а) и высокометоксилированного (б) пектинов
В зависимости от условий, при которых образуется студень, его структура создается при неодинаковом количественном участии различных связей. Прибавленная для студнеобразования кислота вытесняет катионы из пектиновой молекулы, создает свободные карбоксильные группы, уменьшает их диссоциацию, нейтрализуя электростатические силы отталкивания между молекулами пектовой кислоты.
Наиболее прочные студни образуются в присутствии лимонной, винной и триоксиглутаровой кислот.
Сахар в процессе студнеобразования выполняет роль дегидратирующего вещества. Наибольшая прочность студня достигается при добавлении сахарозы, наименьшая – мальтозы.
Для образования прочного студня в трехкомпонентной системе «пектин – сахар – кислота» необходимо их оптимальное соотношение, которое не носит абсолютного характера, а зависит от вида пектина, определяющего пределы соотношения компонентов рецептурной смеси. В практике оптимальным условием является приблизительное соотношение пектина, сахара и кислоты соответственно 1 : 60 : 1.
Студнеобразование пектина зависит от рН студня и температуры процесса. Для высокоэтерифицированных пектинов максимальная прочность студня достигается при рН 3,0-3,3, для низкоэтерифицированных – при рН 2,5-2,8. Снижение рН на 1/10 в определенных условиях студнеобразования может вызвать повышение оптимальной температуры на 5°С.
Следует отметить, что, несмотря на то что в литературе часто указывают оптимальное значение рН для получения студней максимальной прочности, научного объяснения взаимосвязи рН и студнеобразующей способности пектина не имеется.
Последние результаты подтверждают, однако, что пектины высокой степени этерификации стабилизируются в геле комбинацией гидрофобных взаимодействий и водородных связей.
Метоксильные эфирные группы являются гидрофобными частями пектиновой молекулы. Гидрофобные силы заставляют их сгруппироваться в агрегаты, причем они стремятся иметь как можно меньшую поверхность контакта с водой. В дополнении к этому водородные связи, например, между неэтерифицированными карбоксильными группами образуются тогда, когда значение рН в геле достаточно низкое и диссоциация карбоксильных групп в значительной степени подавлена.
Следует отметить, что водородные связи стабилизируют пектиновую сетку, но без гидрофильных взаимодействий метоксильных групп желирование по энергетическим причинам не произошло бы.
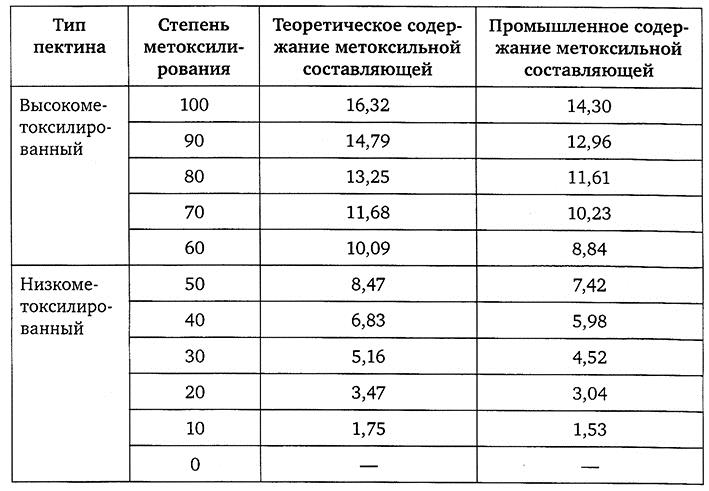
Содержание метоксильных групп определяет механизм студнеобразования (табл. 2.9).
Чем выше степень этерификации, тем выше доля гидрофобных сил в желировании. При этом доля водородных связей, образующихся по свободным, неэтерифицированным карбоксильным группам, уменьшается.
Влияние содержания метоксильных групп на механизм студнеобразования
Высокое значение рН обусловливает усиление отрицательных факторов, способствующих замедлению или прекращению желирования. В частности, диссоциированные карбоксильные группы мешают образованию пространственной структуры. Это, в свою очередь, оказывает влияние на интервал значений рН желирования. Подавление диссоциации при очень высоких значениях степени этерификации будет не таким существенным.
Чем выше степень этерификации, тем выше значение рН, при котором начинается желирование. Теоретически полностью этерифицированным пектинам (степень этерификации 100%) кислота для желирования не требуется.
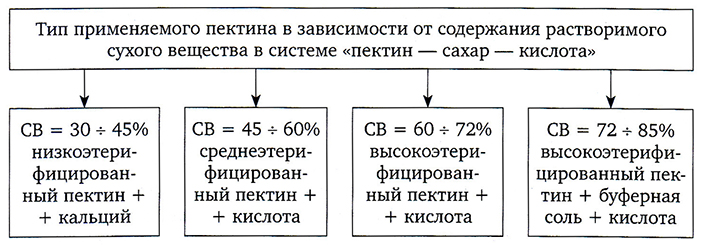
Гелевые структуры образуются при определенном содержании сухих веществ в системе «пектин – сахар – кислота». Данный показатель определяет тип применяемого пектина, в частности его степень этерификации (рис. 2.14).
Степень этерификации также оказывает влияние на температуру и время желирования.
Температура желирования – это температура, при которой гель во время его охлаждения переходит в пектиновый студень. Выше этой температуры желирование не происходит, хотя все условия для образования геля выполнены.
При снижении степени этерификации происходит уменьшение температуры желирования.
Рис. 2.14. Тип применяемого пектина с различной степенью этерификации в зависимости
от содержания растворимых сухих веществ в гелевой системе
Данный процесс наблюдается до момента, когда степень этерификации снижается до такого уровня, при котором реакции с добавленными или находящимися в воде ионами начинают оказывать достаточно сильное влияние на процесс желирования. Самую низкую температуру желирования (55-60°С) имеют пектины со степенью этерификации около 60%.
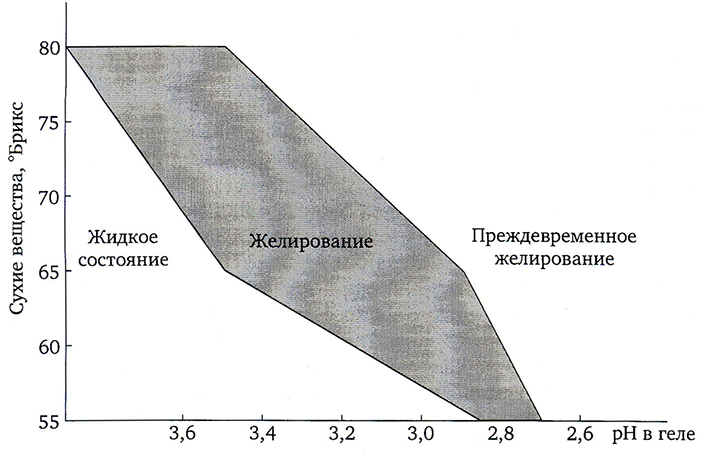
Необходимость высокой концентрации сахара для желирования пектинов высокой степени этерификации объясняется тем, что определенные сахара дополнительно стабилизируют гидрофобные взаимодействия (рис. 2.15).
Рис. 2.15. Область желирования пектинов высокой степени этерификации
Из рис. 2.15 ясно, что сахар и кислота в определенных пределах могут заменить друг друга в усилении прочности студня. Меньшее содержание сахара требует для желирования более низких значений рН, более высокие значения рН возможны при более высоких значениях сахара. При одинаковых содержаниях сахара гели с более низким значением рН тверже и более хрупкие.
Нижняя граница желирования для пектинов с высокой степенью этерификации находится в области содержания сухих веществ примерно 55%. В диапазоне от 55 до 58% лучше всего желируют пектины со степенью этерификации 75% и выше. В области более низкого содержания сухого вещества высокоэтерифицированные пектины не желируют.
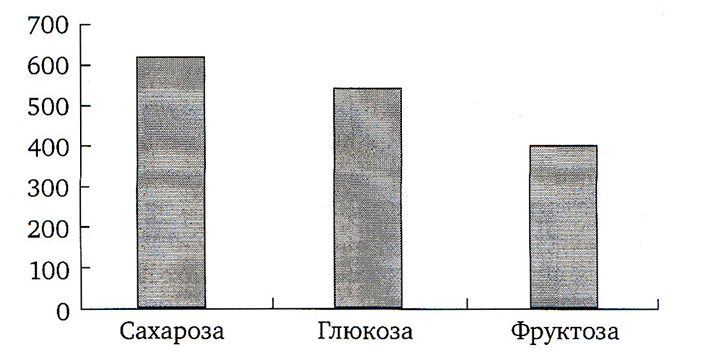
На скорость студнеобразования высокоэтерифицированных пектинов влияет не только содержание сухого вещества гелевой системы, но и вид сахара (рис. 2.16).
Рис. 2.16. Прочность геля в зависимости от вида Сахаров
Гели на фруктозе имеют более низкую температуру и более длительное время желирования, чем сравнимые с ними гели на основе сахарозы. При этом прочность геля в этом случае ниже, а доля вязкостных единиц выше. Усилить гелевую структуру можно путем увеличения дозировки пектина.
При замене сахарозы другими сахарами или сахарозаменителями, например высшими спиртами, следует учитывать их растворимость и способность к рекристаллизации. Например, для предотвращения процесса кристаллизации сахарозы возникает необходимость регулирования содержания редуцирующих Сахаров в пределах 26-30% путем введения в рецептурную композицию глюкозного сиропа (патоки). Часть редуцирующих Сахаров образуется при инверсии сахарозы, поэтому следует учитывать все технологические факторы влияющие на данный процесс. Такими факторами являются прежде всего температура и рН среды. С повышением температуры и рН системы содержание редуцирующих Сахаров увеличивается.
Зная данную закономерность процесса инверсии сахарозы, можно регулировать скорость студнеобразования и текстуру геля. Так, повышенное содержание редуцирующих Сахаров приводит к образованию слишком мягких гелей, склонных к выделению влаги. Такой процесс называется синерезисом.
Синерезис – нежелательное явление при образовании гелевой структуры. Причина его заключается в том, что пектин в продукте связывает свободную влагу.
Если при студнеобразовании и его последующей обработке требуемый эффект связывания достигается не полностью, проявляется тенденция к «сжатию» геля с выделением воды. Происходит синерезис.
Для геля, образованного высокоэтерифицированным пектином, данный эффект наблюдается в основном при его механическом разрушении или преждевременном студнеобразовании. Как только повреждается текстура гелей, возникает синерезис, усиливающийся при длительном хранении желейного изделия.
Закономерность изменения температуры желирования от степени этерификации обусловила выпуск промышленных пектинов, различающихся по температуре и времени студнеобразования:
- очень быстро желирующие, со степенью этерификации выше 72% и очень высокой температурой желирования (например, Classic AF201 немецкой фирмы Herbstreith und Fox);
- быстро желирующие, со степенью этерификации 70-72% и высокой температурой желирования (например, Classic AF202);
- желирующие со средней скоростью, со степенью этерификации выше 59–64% и средней температурой желирования (например, Classic AF4010);
- медленно желирующие, со степенью этерификации 56-63% и средней температурой желирования (например, Classic AF501).
Скорость желирования регулируют с помощью соединений, замедляющих студнеобразование и называемых ретардаторами.
Ретардаторами являются, как правило, соли одновалентных катионов, которые мешают сближению молекул пектина при высокой температуре. Катионы присоединяются к диссоциированным карбоксильным группам, в результате чего пектиновые цепочки не могут сблизиться для образования точек связывания. Возникновение гелевой структуры смещается во времени после установки нового диссоциационного равновесия.
В качестве ретардаторов используют соли молочной, винной, лимонной и фосфорной кислот. Эти соли повышают рН перед дозировкой кислоты, что позволяет предотвратить преждевременное желирование. Регулирование рН осуществляют последующим введением кислоты. Чем выше концентрация буферных солей, тем ниже температура и тем больше время желирования. Однако высокая дозировка буферных солей и кислот может отрицательно повлиять на вкус и прочность геля.
Ретардаторы могут влиять не только на температуру и время желирования, но и на структуру. Подбирая вид буферных солей, их соотношение и дозировку, можно получать различные гелевые структуры со свойствами от мягких до хрупких.
Для желирования высокоэтерифицированных пектинов оптимальным значением рН является 3,0-3,3. При этом образуются гели с прочной и эластичной текстурой. При рН около 3,6 получают продукты с «длинной» тягучей и вязкой текстурой.
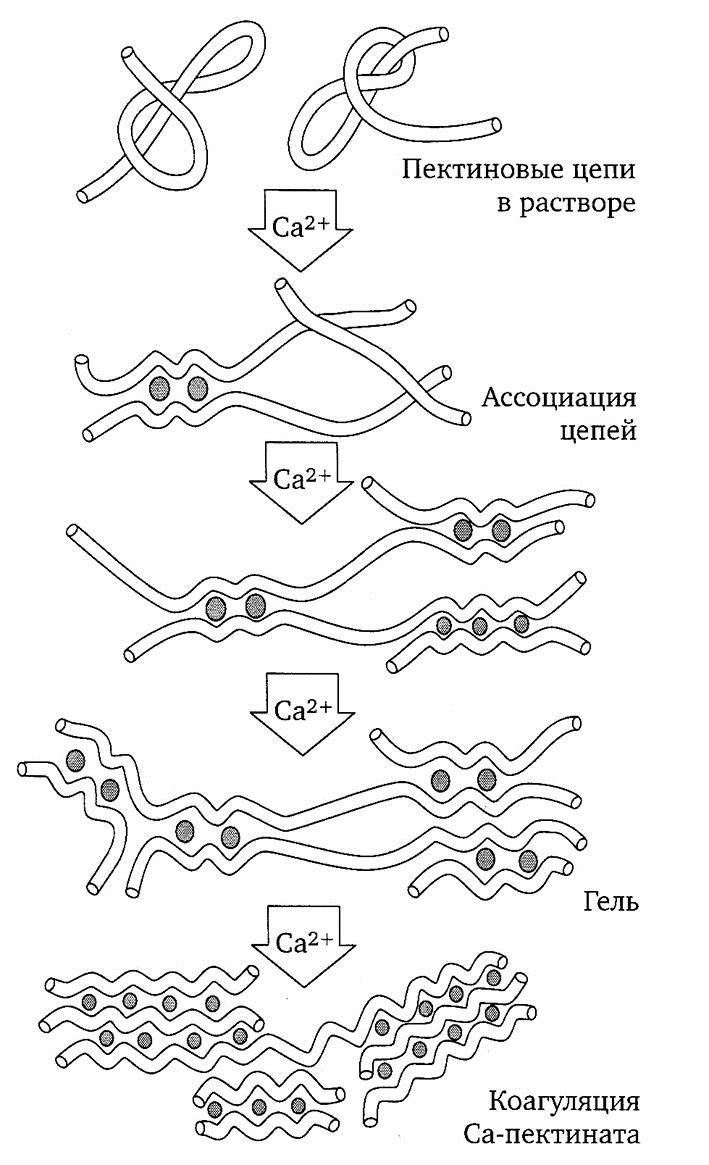
Желирование низкоэтерифицированного пектина можно представить следующим образом (рис. 2.17). При введении ионов кальция пектиновые цепи начинают группироваться, образуя кальциевые мостики. Из-за зигзагообразной формы пектиновых молекул между ними при сближении возникают полости, в которых находятся карбоксильные и гидроксильные группы. Они способствуют ассоциации пектиновых цепочек путем взаимодействия и образования комплексов с кальцием.
Рис. 2.17. Механизм желирования низкоэтерифицированного пектина
При передозировке ионов кальция в данных условиях студнеобразования пектинат кальция выпадает в осадок, т.е. наблюдается явление «преждевременного желирования».
На процесс студнеобразования низкоэтерифицировэнного пектина, так же как и в случае высокоэтерифицированного, влияет вид Сахаров или сахарозаменителей. Так, потребность в кальции для оптимального желирования при образовании геля на основе сорбита больше, чем в случае использования сахарозы. Такой же эффект наблюдается и в случае применения фруктозы.
Не менее существенное влияние на дозировку солей кальция оказывают вид и концентрация буферных солей. Увеличение концентрации буферных солей, особенно тех, которые способны связывать кальций, приводит к повышению содержания вводимых ионов кальция. К таким буферным солям относятся, в частности, соли лимонной кислоты.
Дозировку кальция следует увеличивать при повышении значения рН, изменении температуры розлива желейной массы. Так, при ее повышении большее количество ионов кальция может встроиться в гелевую структуру без преждевременного студнеобразования.
Таким образом, изменяя дозировку кальция, можно управлять не только прочностью геля, но и его реологическими и органолептическими показателями. При очень низкой концентрации кальция желейные изделия характеризуются высоковязкостной или слабожелированной текстурой, при средней – образуются гели, которые «растекаются на языке». При высокой концентрации солей кальция образуется эластичный гель, однако повышается его способность к синерезису.
Существенное влияние на студнеобразование оказывает химическое строение макромолекулы пектина.
Пектовая кислота, у которой все остатки галактуроновой кислоты имеют карбоксильные группы, нерастворима в воде и не обладает студнеобразующей способностью.
Наличие балластных веществ, связанных с пектином валентными связями (например, с другими полисахаридами), вызывает изменение конформации его макромолекулы и отрицательно сказывается на формировании и прочности студня.
Особенностью свекловичного пектина является наличие в его молекуле ацетильных групп. Ацетильные группы, связанные с гидроксильными группами пектиновых веществ, значительно ухудшают их студнеобразующие свойства. Наибольшее количество ацетильных групп содержится в пектине из сахарной свеклы (0,38-0,80%), из корзинок подсолнечника (0,45-0,90%), обусловливая их низкую студнеобразующую способность.
Нами изучена возможность повышения студнеобразующей способности пектинов сахарной свеклы путем их обработки химическими реагентами. Так, использование персульфата аммония или пероксида водорода приводит к повышению молекулярной массы растворимых пектинов за счет окислительной сшивки и сопровождается образованием прочного студня (рис. 2.18).
Рис. 2.18. Реакция окислительной перекрестной сшивки пероксидазой молекул пектина сахарной свеклы
Следует, однако, отметить, что свекловичный пектин образует гелевые структуры, характерные по механизму студнеобразования для низкоэтерифицированных пектинов.
Гели, полученные на основе свекловичного пектина, обладают также высокой водоудерживающей способностью, стабильны при соблюдении технологических режимов к синерезису и могут найти широкое применение в пищевой промышленности.
Пектин, являясь поверхностно активным веществом, обладает ярко выраженными эмульгирующими и пенообразующими свойствами.
Вязкость эмульсий пектина с жиром резко возрастает с увеличением концентрации эмульгатора и жира. Так, для 50%-ной эмульсии с 0,5% свекловичного пектина она равна 4,8 сП (сантипуаза), а с 1% – 5880 сП. При увеличении концентрации жира вязкость также повышается. Например, вязкость эмульсии при увеличении концентрации жира от 50 до 55% возрастает от 4,8 до 13,5 сП.
Лучшими эмульгирующими и пенообразующими свойствами обладают водные растворы солей подсолнечной пектовой кислоты с анилином, деметиланилином и о-толуидином. Пенообразующие свойства пектатов приближаются к свойствам яичного белка.
2.5.4. ПРИМЕНЕНИЕ ПЕКТИНА
Во всех случаях использования пектина очень важными факторами, определяющими его свойства, являются точные параметры продукта, рН, ионная сила и состав, концентрация и природа подсластителей, а в тех случаях, когда используются фрукты, – количество и природа содержащегося в них пектина. Таким образом, во всех случаях возможных изменений в составе пектина, включая смену времени года или вид плодов, перед запуском промышленного производства необходимо провести контрольную проверку на небольшой порции.
Во всех случаях применения пектина необходимо убедиться в том, что он полностью растворен до того, как будут достигнуты параметры гелеобразования. Пектин не растворяется при условиях, близких к условиям гелеобразования, в особенности высокометоксилированные пектины не растворяются в растворах сахара (при концентрации выше 20-25%). Как и в случае большинства камедей, важно обеспечить диспергирование частиц сухого порошка пектина до того, как произойдет их частичное растворение и слипание. Этого можно достигнуть или в системах с интенсивным перемешиванием (партиями или на линии), или путем предварительного смешивания пектина с сахаром, взятым в количестве, в несколько раз превышающем массу пектина, с последующим интенсивным перемешиванием. Иногда пектин можно диспергировать в сахарном сиропе, смесь затем разжижают перемешиванием, чтобы получить похожий результат.
Составы, в которые входит пектин, нуждаются обычно в корректировке с учетом конкретных производственных условий. Во всех случаях необходимо учитывать описанные выше факторы, которые оказывают влияние на процесс гелеобразования.
Самой первой областью применения пектина было его использование в производстве фруктовых джемов с концентрацией сухих веществ 60-70% и рН в диапазоне 3,0-3,3. В зависимости от природы и содержания фруктов в продукте, а также заданного содержания сухих веществ могут потребоваться различные количества и разные типы пектина. Выбор конкретного типа пектина будет определяться видом конечного продукта и способом его изготовления.
Джем можно изготовить с использованием традиционного метода варки в открытом котле, который потребует применения пектина с высокой скоростью желирования, или методом вакуумной варки при низкой температуре, для которого, во избежание преждевременного желирования, необходим медленножелирующий пектин. С использованием медленно- или крайне медленно желирующего пектина обычно изготавливаются прозрачные желе, поскольку такие пектины позволяют мелким пузырькам воздуха подняться на поверхность расфасованного продукта до того, как уже в самой емкости произойдет гелеобразование. Если возникает проблема всплытия фруктов, то целесообразно добавить некоторое количество низкометоксилированного пектина, который повышает вязкость в горячем состоянии.
Джемы и желе с низким содержанием сахара нельзя изготовить, используя высокометоксилированные пектины. Обычно самым эффективным является изготовление этой продукции с применением амидированных низкометоксилированных пектинов. Однако в Европе при изготовлении продукта, который позиционируется как «органический», могут быть использованы только неамидированные пектины. В случае продуктов с низким содержанием сахара для обеспечения их высокого качества особенно важно иметь в изобилии высококачественные фрукты. Вид используемого пектина должен подбираться применительно к конкретному продукту. В общем случае для продукта с меньшим содержанием сухих веществ требуется использование высокореактивных или быстрожелирующих низкометоксилированных пектинов.
Пектины используют и для производства фруктовых начинок. Начинки для хлебобулочных изделий должны обладать целым рядом различных свойств, но наиболее общим требованием является сохранение стабильности в процессе выпечки. Например, в открытых пирогах с начинками из ягод или плодов, нанесенными на их поверхность перед выпечкой, начинка должна обладать текучестью, чтобы придать поверхности гладкий, блестящий вид, но при этом не должна растекаться в процессе выпечки за пределы формы изделия. Для этой цели выбирают высокоэтерифицированные пектины со средней скоростью желирования.
В отличие от термонеобратимого поведения пектина, который использован в рецептурах термостабильных фруктовых начинок, в равной степени можно использовать пектиновую систему, образующую полностью термически обратимые гели при различных концентрациях сухих веществ. Примером является амидированный пектин в комбинации с фосфатными солями, которые регулируют как присутствие кальция, так и рН геля, что используется в производстве желейной глазури.
Условия, при которых становится возможным перекачивание фруктовых основ без отделения фруктов, связанные со способностью восстанавливать структуру в отсутствие механического воздействия, обычно наилучшим образом обеспечиваются амидированным низкометоксилированным пектином. В некоторых случаях возможно использовать традиционную смесь пектина с добавками. Такая смесь может содержать помимо пектина фосфатные соли и источник кальция, например ортофосфат кальция.
В молочных продуктах и в их аналогах, таких как продукты, приготовленные из сои, пектин может выполнять две различные функции Высокометоксилированные пектины могут выступать в роли стабилизаторов дисперсий белков при пониженных рН, как, например, в йогурте или напитках на молочно-соковой основе. Низкометоксилированные пектины ведут себя по-другому и могут, взаимодействуя с кальцием, образовывать гель или в молоке, или в более кислых продуктах.
Пектин обеспечивает эффективную коллоидную защиту молекул казеина в диапазоне рН 3,9-4,1, типичном для йогурта. Перед началом проведения термической обработки крайне важно гомогенизировать йогурт для распада белковых агрегатов в присутствии пектина. Необходимое для этого количество пектина будет зависеть от условий гомогенизации и отразится на вязкости продукта. Избыток пектина, превышающий количество, необходимое для стабилизации дисперсии, вызовет повышение вязкости конечного продукта, что иногда может оказаться желательным, а иногда – нет. Обычно перед началом гомогенизации в продукт нужно добавить около 0,4% специально отобранного и стандартизованного пектина, который вводят либо в виде раствора, либо в виде дисперсии в сахаре или в сиропе. В некоторых случаях для достижения максимальной стабильности за термической обработкой может последовать дальнейшая гомогенизация, как правило, при более низком давлении. Готовый напиток, таким образом, не имеет мутноватого оттенка и не осаждается.
Аналогичные преимущества использования пектина возможны для смесей молока и фруктовых соков. Пектин придает фруктовому напитку на молочной основе настоящий фруктовый вкус, аромат и кислотность.
Тот же принцип может быть применен к газированным молочным напиткам и другим продуктам, включая напитки на основе молочной сыворотки, которые могут быть стабилизированы во избежание осаждения растворимых сывороточных белков.
Низкометоксилированные амидированные пектины можно использовать для получения молочного геля, непосредственно диспергируя пектиновый порошок (по возможности смешанный с сахаром, масса которого в несколько раз превышает массу пектина) в холодном молоке и затем нагревая при постоянном перемешивании до температуры кипения, при которой происходит растворение пектина. Требуемое для этой процедуры количество пектина составляет 0,6-0,9%, а текстура геля, в зависимости от выбранного типа пектина, может изменяться от жесткой и хрупкой до очень мягкой, кремообразной. Можно также изготовить фруктовый сироп, который при добавлении в холодное молоко образует слегка желированный фруктовый десерт.
Пектиновые гели можно использовать в качестве альтернативы желатину во фруктовых десертах и бисквитах. Желирование в пектиновых гелях может проходить очень быстро, поэтому сразу после кратковременной стадии охлаждения к ним можно добавить другие компоненты, такие как бисквит или сливки, создавая сложный десерт, который можно изготавливать на поточной линии. Гели обеспечивают продукту привлекательную, легкую текстуру с замечательным вкусом и ароматом. Для получения продуктов типа муссов нужно добавить взбитые сливки или белковые взбивающие агенты.
Для повышения качества хлебобулочных изделий в стране и за рубежом применяют различного рода улучшители, воздействующие на компоненты пшеничного теста и обеспечивающие получение высококачественной продукции. Все более широкое применение в качестве улучшителей находят поверхностно-активные вещества (ПАВ), позволяющие интенсифицировать процесс производства хлеба, улучшить качество хлебобулочных изделий и сохранить их свежесть.
В настоящее время все большее применение в хлебопечении в качестве анионоактивного ПАВ имеют пектин и его производные.
В технологии хлебопечения важными являются такие свойства пектиновых веществ, как набухаемость, вязкость, способность образовывать гели, регулировать кристаллообразование, повышать водопоглотительную способность, эмульгирующие свойства.
Учеными ряда научных учреждений проведены исследования по использованию в приготовлении хлеба различных видов пектинов – яблочного, цитрусового, свекловичного. Установлено, что внесение в тесто пектинов влияет на биологические, коллоидные и микробиологические процессы приготовления теста. При внесении пектинов в тесто наблюдается укрепление клейковины. Наиболее заметное действие на упрочение структурно-механических свойств теста оказывал свекловичный пектин, затем яблочный и цитрусовый. Возможным механизмом положительного влияния пектина является электростатическое взаимодействие между белками клейковины и пектиновыми веществами с образованием белково-полисахаридных комплексов сложного состава. Эта способность пектинов предопределяет их использование при переработке слабой муки или с пониженным содержанием клейковины.
При выпечке хлеба с внесением 0,1-0,5% пектина к массе муки традиционными способами качество готового изделия улучшается по таким показателям, как объемный выход, пористость и сжимаемость мякиша, формоустойчивость.
В ассортименте безалкогольных напитков функционального назначения все большее значение уделяют напиткам, обогащенным пектиновыми веществами, так как именно в гидратированной форме пектин оказывает на организм человека более эффективное физиологическое воздействие.
Пектин обычно считается одной из самых безопасных и наиболее широко применяемых пищевых добавок, допустимое суточное потребление (ДСП) которой «не регламентируется», что определено решениями комитета JECFA для целей Codex Alimentarius и Научного комитета по продуктам питания ЕС (Scientific Committee for Food – SCF). На это указывает также тот факт, что согласно законодательству США пектин отнесен к общепринятым безопасным добавкам (GRAS). В ЕС пектины – амидированные и неамидированные – имеют различные спецификации (Е 440(ii) и Е 440(i) соответственно), однако разрешенные области применения для них остаются одинаковыми, за исключе-нием органических пищевых продуктов, в которых допускается использование только Е 440(i) – неамидированных пектинов.
Видео:Вся правда о пектине. Какие виды пектина есть, чем они отличаются (часть 1)Скачать

Е.В. Аверьянова, М.Н. Школьникова ПЕКТИН: МЕТОДЫ ВЫДЕЛЕНИЯ И СВОЙСТВА
- Евгения Оленина 4 лет назад Просмотров:
1 МИНИСТЕРСТВО ОБРАЗОВАНИЯ И НАУКИ РФ Бийский технологический институт (филиал) федерального государственного бюджетного образовательного учреждения высшего профессионального образования «Алтайский государственный технический университет им. И.И. Ползунова» Е.В. Аверьянова, М.Н. Школьникова ПЕКТИН: МЕТОДЫ ВЫДЕЛЕНИЯ И СВОЙСТВА Методические рекомендации к выполнению лабораторных работ для студентов направлений подготовки «Биотехнология», «Продукты питания из растительного сырья», магистрантов направления подготовки «Продукты питания из растительного сырья» Бийск Издательство Алтайского государственного технического университета им. И.И. Ползунова 2015
2 УДК (076) ББК А19 Рецензент: А.Л. Верещагин, д. х. н., профессор кафедры ОХЭТ А19 Аверьянова, Е.В. Пектин: методы выделения и свойства: методические рекомендации к выполнению лабораторных работ для студентов направлений подготовки «Биотехнология», «Продукты питания из растительного сырья», магистрантов направления подготовки «Продукты питания из растительного сырья» / Е.В. Аверьянова, М.Н. Школьникова; Алт. гос. техн. ун-т, БТИ. Бийск: Изд-во Алт. гос. техн. ун-та, с. В методических рекомендациях приведены примеры получения пектина из различного растительного сырья, ряд методик по качественному и количественному анализу пектиновых веществ, их свойства и применение в пищевой и фармацевтической промышленности. УДК (076) ББК Рассмотрены и одобрены на заседании кафедры «Биотехнология». Протокол 5 от г. Аверьянова Е.В., Школьникова М.Н., 2015 БТИ АлтГТУ, 2015
3 СОДЕРЖАНИЕ Введение Номенклатура и структура пектиновых веществ Свойства Извлечение пектина из растительного сырья Методы определения пектиновых веществ Методы качественного определения Методы количественного определения пектиновых веществ Количественное определение протопектина Количественное определение пектиновых и пектовых кислот и их солей Лабораторная работа 1 «Выделение пектина из сырья растительного происхождения» Лабораторная работа 2 «Методы определения физико-химических характеристик пектиновых веществ» Техника безопасности при выполнении лабораторных работ Приложение А Литература
4 ВВЕДЕНИЕ Пектиновые вещества это группа высокомолекулярных полисахаридов, входящих в состав клеточных стенок и межклеточных образований растений совместно с целлюлозой, гемицеллюлозой, лигнином. Наибольшее количество пектиновых веществ находится в плодах и корнеплодах. В промышленности пектин получают из яблочных выжимок, свеклы, корзинок подсолнечника. Различают нерастворимые пектины (протопектины), которые входят в состав первичной клеточной стенки и межклеточного вещества, и растворимые, содержащиеся в клеточном соке, из которого пектиновые вещества можно получить осаждением спиртом. При созревании и хранении плодов нерастворимые формы пектина переходят в растворимые, с этим связано размягчение плодов при созревании и хранении. Переход нерастворимых форм в растворимые происходит также при тепловой обработке растительного сырья, осветлении плодово-ягодных соков. Пектин находит широкое применение в различных отраслях народного хозяйства: в консервной и кондитерской промышленности для получения желе, мармелада, джема, повидла, конфитюра; при производстве мороженого в качестве эмульгаторов и стабилизаторов пены; в химической и фармацевтической промышленности при изготовлении клея, моющих средств, ионообменных смол, кинопленок и искусственных волокон на основе нитропектина и ацетилпектина; в сельском хозяйстве для получения стойких инсектицидных эмульсий. На основе пектина готовятся различные медицинские препараты: кровоостанавливающие, для лечения заболевания желудочно-кишечного тракта. Установлено, что пектиновые вещества тормозят процессы гниения в кишечнике больше, чем искусственно введенные дезинфицирующие вещества. Наличие в составе пектиновых веществ уроновых кислот повышает сопротивляемость организма. Пектин способствует снижению кровяного давления, выведению из организма холестерина, рекомендуется для диетического питания. Благодаря способности пектиновых веществ не расщепляться под действием ферментов желудка, а также взаимодействовать с ионами различных металлов, они используются как профилактическое средство при интоксикации организма тяжелыми металлами. 4
5 1 НОМЕНКЛАТУРА И СТРУКТУРА ПЕКТИНОВЫХ ВЕЩЕСТВ Пектины представляют собой полисахариды клеточных стенок. Основным компонентом пектиновых полисахаридов являются полиуроновые кислоты. У высших растений они состоят из остатков D-галактуроновой кислоты, связанных С-1 С-4-связями, на долю которой, в зависимости от источника происхождения пектиновых веществ, приходится от 83 до 90 %. Карбоксильная группа каждого остатка D-галактуроновой кислоты может существовать в разных состояниях: образовывать соли с ионами определенных металлов, чаще всего кальция (пектат), причем атомы двух- и трехвалентных металлов могут связывать несколько цепей полигалактуроновой кислоты; соль может быть одновременно и метоксилирована (пектинат), или оставаться немодифицированной (пектовая кислота основа всех видов пектиновых веществ), или быть частично метоксилированной (эту форму обычно называют пектином). COOR O O O O O COOR O O O n O COOR O O O O Пектовая кислота Пектат.. Пектин. Пектинат.. R Н Ме + Н и СН 3 Ме + и СН 3 Незначительную часть в составе пектиновых веществ составляют нейтральные полисахариды арабинаны и галактаны, что и обусловливает гетерополисахаридный характер пектина. Арабинаны представляют собой разветвленные полимеры, состоящие из остатков L-арабофуранозы, соединенные между собой α-с-1 С-5-связями. Галактаны неразветвленные цепи, образованные из остатков D-галактопиранозы, соединенных b-с-1 С-4-связями. При этом возможно, что часть карбоксильных групп галактуроновой кислоты этерифицирована указанными нейтральными полисахаридами. Молекулярная масса пектиновых веществ достигает
6 Согласно современным представлениям пектин имеет линейную структуру, в которой остатки D-галактуроновой кислоты имеют пиранозную конфигурацию (рисунок 1, а). Используют и другой способ изображения молекулы пектина, в котором отдельные кольца повернуты относительно друг друга и лежат в различных плоскостях (рисунок 1, б). Рисунок 1 Структурная формула пектина Рисунок 2 Пространственная структура молекулы пектина 6
7 В течение длительного времени не существовало четко сформулированной номенклатуры пектиновых веществ. В литературе применялось около 50 различных терминов. В настоящее время утвердилась следующая номенклатура пектиновых веществ, разработанная Комитетом Американского химического общества и официально принятая в 1944 г.: — пектин (pectin) водорастворимое вещество, свободное от целлюлозы и состоящее из частично или полностью метоксилированных остатков полигалактуроновой кислоты. В зависимости от количества метоксильных групп и степени полимеризации существуют различные пектины. Н-пектин (-pectin) высокоэтерифицированный пектин. Имеет степень этерификации, т. е. отношение числа этерифицированных карбоксильных групп на каждые 100 карбоксильных групп пектиновой кислоты, более 50 %; L-пектин (L-pectin) низкоэтерифицированный пектин. Имеет степень этерификации менее 50 %; — пектиновые вещества (pectic substances) физические смеси пектинов с сопутствующими веществами (например, пентозанами и гексозанами); — пектиновые кислоты (pectin acid) высокомолекулярные полигалактуроновые кислоты, небольшая часть карбоксильных групп которых этерифицирована метиловым спиртом. Соли пектиновых кислот называются нормальными или кислыми пектинатами (pectinates); — пектовые кислоты (pectic acid) полностью деметоксилированные пектины с нетронутой цепью. Соли пектовых кислот называются нормальными или кислыми пектатами (pectates); — протопектин (protopectin) нерастворимый в воде природный пектин растений, состоящий в основном из сети пектиновых цепей, образованных в результате соединения многовалентных ионов металла с неэтерифицированными группами COO (образование ионных мостиковых связей), и в незначительном количестве при помощи эфирных мостиков с 3 PO 4 ; — производные пектина пектины с различными группами, связанными по главным валентностям, например ацетилпектин. Структура и химический состав пектиновых веществ определяют пространственную форму их молекул и характер взаимодействия с другими соединениями. Установлено, что пектиновые вещества обладают структурой с ограниченной гибкостью, стабилизируемой водородными и гидрофобными связями. 7
8 2 СВОЙСТВА Пектин полисахарид с длинной спиралевидно-скрученной цепью повторяющихся единиц и высоким молекулярным весом обладает свойствами лиофильного коллоида. В отличие от других природных коллоидов (желатин, агар-агар) золи пектина переходят в гель только в присутствии сахара и кислоты или поливалентных металлов. Пектин, выделенный из растений, в высушенном виде представляет собой порошок от белого до серо-коричневого цвета в зависимости от источника получения и степени очистки. Он не обладает запахом, слизистый при пробе на язык. Пектин растворяется в воде, особенно при нагревании, осаждается спиртом и другими органическими растворителями. При повышении температуры выше 100 С пектин разлагается. Быстрое разложение наступает в присутствии ионов хлора. Пектиновые растворы оптически активные, правовращающие, удельное вращение постоянно при значении рн около от 3,0 до 6,5. Характерными показателями пектина являются: молекулярный вес, метоксильное число, ацетильное число, растворимость в воде, вязкость золя, желеобразующая способность. Ввиду того что каждый пектин представляет собой смесь молекул с разной длиной цепи, может быть установлен только средний молекулярный вес (таблица 1). Таблица 1 Молекулярный вес пектиновых веществ Пектин Молекулярный вес 1 Яблочный Цитрусовый Свекловичный Корзинок подсолнечника Кормового арбуза Надземная часть ревеня огородного 2300 Различия в молекулярном весе пектинов зависят не только от его источника, но и от способа получения, вызывающего различную степень деградации молекулы. Содержание метоксильных групп является важным показателем пектиновых веществ. Степень этерификации полигалактуроновой кислоты меняется в широких пределах в зависимости от источника получения и способа извлечения от полностью лишенной метоксильных групп (пектовой кислоты) до полностью замещенных всех карбоксильных остатков полигалактуроновой кислоты. 8
9 Пектины, полученные из разных растений, значительно различаются по степени этерификации (таблица 2). Таблица 2 Содержание метоксильных и ацетильных групп в пектиновых веществах Пектин Содержание метоксильных групп, % Содержание ацетильных групп, % 1 Яблочный 7,15 11,4 0,30 0,69 2 Цитрусовый 6,90 9,60 0,24 0,50 3 Свекольный 3,70 5,50 0,40 2,50 4 Корзинок подсолнечника 5,30 6,50 нет данных Метоксильное число имеет большое значение для желирующих свойств пектина. Для желеобразующего пектина установлена норма содержания метоксильных групп не ниже 7 %. Значительно в меньшем количестве содержатся в пектине ацетильные группы. Ацетильное число колеблется в широких пределах: от сотых долей процента до 2,5 %. Ацетильные группы оказывают отрицательное влияние на желирование. Установлены допустимые пределы содержания ацетильных групп для студнеобразующего пектина не более 1 %. Наилучшим растворителем пектиновых веществ является вода. Растворяются они также в 84%-ной фосфорной кислоте и жидком аммиаке; в глицерине и формамиде набухают. В остальных органических и неорганических растворителях они практически нерастворимы. Растворимость пектина в воде возрастает с увеличением степени этерификации и с уменьшением степени полимеризации. Из двух пектинов с одинаковой длиной цепи легче растворим тот, у которого выше метоксильное число; из двух пектинов одинаковой степени этерификации легче растворим обладающий меньшим молекулярным весом. Характерной особенностью пектинового золя как лиофильного коллоида является непропорционально высокое возрастание вязкости при увеличении его концентрации. Вязкость золя пектина зависит от молекулярного веса и форм молекулы пектина, вокруг которой образуется жидкостный слой (сольватация). Раствор приобретает новые механические свойства, возникает внутренняя структура золя. Возникновение 9
10 коллоидной «сетки» золя обусловливает структурную вязкость, изменяющуюся при изменении давления. При повышении давления у структурированного золя вязкость быстро снижается вследствие нарушения эластичной структуры. Характерным и важным свойством пектина является его способность давать студни в присутствии сахара и кислот, отсюда и их название (от греческого слова «пектос» соединяющий). Желирующая способность пектина растительного, широко используемая пищевой промышленностью, у разных растений далеко не одинакова и зависит от относительной молекулярной массы пектина, от степени метоксилирования остатков галактуроновой кислоты и количества сопутствующих балластных веществ, концентрации сахара в растворе, температуры и рн среды. Особенно необходимо знать о наличии пектиновых веществ в тех случаях, когда пектиновые вещества накапливаются в лекарственносырьевых объектах в значительных количествах (ягоды клюквы, алтейский корень, солодковый корень и др.) и участвуют в суммарном лечебном эффекте, проявляемом основными действующими веществами. В водных растворах молекула пектина имеет форму спирали, карбоксильные группы которой расположены друг под другом. Изменения в форме молекулы пектина связаны с диссоциацией свободных и нейтрализованных карбоксильных групп. При электролитической диссоциации карбоксильные группы получают отрицательный заряд, вследствие чего между ними возникают силы отталкивания. Эти силы отталкивания выпрямляют спиральную молекулу и увеличивают ее линейные размеры и вязкость. Высокая вязкость плодово-ягодных соков обусловливается в основном присутствием в них пектиновых веществ. Пектин обладает способностью образовывать различные виды гелей. Основные два типа гелей образуются в присутствии сахара и кислоты или при взаимодействии с поливалентными металлами. В гелях первого типа при добавлении кислоты диссоциация карбоксильных групп подавляется, чем уменьшаются силы отталкивания. Добавление сахара как дегидратирующего вещества нарушает сольватацию, наступает взаимное сближение частичек пектина золь переходит в гель, при этом образуется сетка пектиновых молекул, в которой блокируется сахарный раствор. Между карбоксильными и гидроксильными группами цепей пектиновой кислоты возникают водородные связи. Возможно, что водородные связи образуются также между карбоксильными и гидроксильными группами пектиновых молекул и полярными группами сахара. 10
11 O O O COO O O O O O O O COO O O O O O COOC 3 O O O O O O O O O COOC 3 O O O O O O Гели второго типа возникают при взаимодействии раствора низкометоксилированного пектина с ионами поливалентных металлов. Известно, что пектовая кислота и частично метоксилированная пектиновая образуют соли с металлами пектаты и пектинаты. Соли щелочных металлов растворимы в воде, соли поливалентных металлов практически нерастворимы. Двухвалентный кальций образует мостики между молекулами пектина через карбоксильные группы (ковалентные связи). При этом создается трехмерная структура геля, в которой удерживается блокированная жидкость. O O O CO O O O O O O O CO Ca Ca O O CO O O O O O CO O O O При повышении температуры пектины разрушаются. Этот процесс сопровождается уменьшением вязкости и желирующей способности. Понижение вязкости и желирующей способности вызывается 11
12 разрушением суперструктуры пектиновых веществ. Оптимальной для сушки пектиновых веществ является температура, приблизительно равная 80 С. При сушке выше этой температуры желеобразование пектина ухудшается в связи с происходящей деградацией. Под действием кислот молекулы растворимых пектиновых веществ могут претерпевать одновременно два существенных изменения: а) омыление этерифицированных карбоксильных групп; б) разрушение молекулы вследствие разрыва гликозидной связи между остатками D-галактуроновой кислоты. При действии сильной минеральной кислоты на высокоэтерифицированную пектиновую даже при комнатной температуре через несколько недель происходит ее омыление до нерастворимой полигалактуроновой кислоты, выпадающей в осадок. Одновременно с метоксильными омыляются и ацетильные группы пектиновой молекулы. При повышении температуры кислотное омыление происходит быстрее. При дальнейшем же повышении температуры скорость этого процесса еще более возрастает, но вместе с тем начавшийся распад макромолекул по главным валентностям увеличивается настолько, что деградация начинает преобладать над омылением. Деградация и омыление пектиновой кислоты два полностью независимых друг от друга процесса. Понижение значения рн способствует омылению эфирных групп, повышение температуры разрыву гликозидных связей. Так, при температуре около 50 С может происходить омыление, которое не сопровождается значительной деградацией макромолекулы. Продолжительный кислотный гидролиз ведет к полной деградации пектиновой молекулы вплоть до галактуроновой кислоты. При концентрации кислоты от 12 до 19 % и температуре реакции до С происходит докарбоксилирование входящей в состав пектиновых веществ D-галактуроновой кислоты. Под воздействием 12%-ной соляной кислоты и температуре С полиуроновые кислоты, из которых построен пектин, способны образовывать фурфурол. Процесс образования фурфурола складывается из трех последовательно протекающих реакций: а) гидролиза полиуроновой кислоты; б) декарбоксилирования уроновой кислоты с образованием соответствующей пентозы; в) дегидратации пентозы с образованием фурфурола. Под действием избытка щелочи протопектин разлагается. Пектиновые кислоты при этих условиях целиком деметилируются. Омыление щелочью идет даже при комнатной температуре. Щелочное омыление протекает гораздо быстрее, чем кислотное; при достаточном ко- 12
13 личестве основания оно совершается за несколько часов. Одновременно с метоксильными омыляются и ацетильные группы. Щелочь не только вызывает омыление, но может при известных условиях разрушать связи в цепи макромолекулы пектиновых веществ и изменять коллоидные свойства растворов в сторону возникновения более высокодисперсных коллоидных систем. При комнатной температуре гликозидные связи в цепи макромолекул разрушаются незначительно. При нагревании пектиновых растворов с разбавленными щелочами это разрушение происходит интенсивно. При осторожном добавлении гидроокиси калия или натрия к разбавленным растворам пектиновых кислот образуются сначала кислые, а затем нейтральные пектинаты. Гидроокиси щелочноземельных металлов дают с пектиновыми веществами труднорастворимые осадки. При действии окислителей пектиновые вещества разрушаются. Перекись водорода, аскорбиновая кислота, смесь перекиси водорода и аскорбиновой кислоты, хлор, иодная кислота, молекулярный кислород, метапериодат натрия вызывают разложение пектиновой молекулы. Перекись водорода оказывает значительное деградирующее действие даже в малой концентрации. Продуктами окисления в этом случае будут двуокись углерода, муравьиная кислота и формальдегид. Катализаторами процесса являются ферросоли, гидразин, фенилгидразин и др. Аскорбиновая кислота разрушает пектиновые вещества в присутствии кислорода. Окислительное действие аскорбиновой кислоты усиливается от прибавления метиленовой сини и перекиси водорода. В результате окисления аскорбиновой кислотой происходит разрушение суперструктуры пектиновых веществ, которое сопровождается уменьшением вязкости растворов. Метапериодат натрия окисляет второй и третий углеродные атомы галактуроновой кислоты, образуя новые функциональные группы. При этом нарушается устойчивость гликозидной связи в щелочной среде и облегчается распад пектиновых молекул. В присутствии сахарозы окислительный распад пектиновых веществ подавляется, т. е. сахароза является ингибитором окисления пектиновых веществ. Отношение пектинатов к различным окислителям является важной их характеристикой, определяющей способы переработки и выделения пектинов из растительного сырья. Карбоксильные и гидроксильные группы пектиновой или пектовой кислот могут вступать в химические реакции, полученные при этом соединения рассматриваются как соответствующие производные двух видов. 13
14 При взаимодействии пектиновых веществ с кислотами реагируют гидроксильные группы. Существуют азотнокислые, муравьинокислые эфиры пектинов, ацетилпектины, нитропектины и т. д. Гидроксильные группы пектиновых веществ могут также алкилироваться, при этом получаются соответствующие простые эфиры. При взаимодействии пектиновых веществ с метилиодидом, диметилсульфатом, диазометаном в реакцию вступают карбоксильные группы пектиновых веществ. При обработке метиловых эфиров полигалактуроновой кислоты различной степени этерификации жидким аммиаком в атмосфере азота эфиры переводятся в соответствующие амиды. При взаимодействии метилового эфира пектиновой кислоты с гидразином получается пектиновый гидразид. При нейтрализации этого гидразида хлорной кислотой получаются перхлораты. Известны также силильные производные пектина, в которых активные атомы водорода замещены кремниевой кислотой или силильными группами. Карбоксильные группы пектина могут восстанавливаться до первичных спиртовых групп с помощью алюмогидрида лития или боргидрида натрия. Довольно легко происходит сшивка пектиновых веществ формальдегидом в присутствии соляной кислоты как катализатора, в результате чего образуется метилольный полуацеталь пектина. При взаимодействии пектиновых веществ с полифункциональными соединениями образуются пространственные трехмерные структуры. В качестве связующих агентов используют диметилдихлорсилан, глиоксаль, дихлорэтилсульфамид и др. В Приложении А даны сведения о физико-механических и теплофизических свойствах пектина. Данные взяты из учебного пособия [1]. 14
15 3 ИЗВЛЕЧЕНИЕ ПЕКТИНА ИЗ РАСТИТЕЛЬНОГО СЫРЬЯ Содержание пектиновых веществ в растительных материалах колеблется в широких пределах: от 0,1 0,5 до 50 %. Наибольшее содержание пектина в лимонных выжимках (30 35 %), в апельсиновых и мандариновых отжимах (25 30 %), околоплодниках подсолнечника (около 25 %), свекловичном жоме (20 25 %), яблочных выжимках (5 15 %). Локализованы пектиновые вещества в различных частях растений неравномерно. Так, в цитрусовых плодах основное количество пектинов сосредоточено в альбедо, в яблоках в эпидермисе, колленхиме и прилегающих тканях, в сахарной свекле в мякоти. Для получения пектина используют свежее, сульфитированное и сушеное сырье. Сушка и сульфитирование пектиносодержащего сырья вызваны необходимостью удлинения сроков его хранения перед переработкой. В сушеном сырье замедляются микробиологические и физикохимические процессы, в результате чего количество и качество пектиновых веществ в процессе хранения изменяются незначительно. В сульфитированном сырье в процессе хранения качество пектина ухудшается, студнеообразующая способность снижается в среднем на %. Сушеное растительное сырье представляет собой капиллярнопористую систему, имеющую капилляры различных длин и диаметров. Процесс пропитки сырья происходит через поры пектоцеллюлозной оболочки клетки под влиянием капиллярных сил. При набухании изменяются геометрические параметры сырья, оно увеличивается в размерах. Скорость набухания сырья определяет скорость поглощения экстракта сырьем, что оказывает влияние на константы массопередачи в начальный период экстрагирования. Чтобы интенсифицировать процесс экстрагирования пектина и максимально извлечь его, растительная ткань перед гидролизом должна быть в набухшем состоянии, т. е. процессу гидролиза-экстрагирования пектиновых веществ из растительного сырья должен предшествовать процесс набухания сушеной растительной ткани. По качественным показателям наиболее ценным пектинсодержащим сырьем является свежее сырье. 15
16 4 МЕТОДЫ ОПРЕДЕЛЕНИЯ ПЕКТИНОВЫХ ВЕЩЕСТВ 4.1 Методы качественного определения Осаждение спиртом Хорошо известно, что пектины осаждаются из раствора при добавлении двух или более объемов этилового спирта. При этом получается прозрачный желатинозный осадок. В случае сильно разбавленных растворов, или частично деградированных, или имеющих низкую метоксильную составляющую осадок получается менее желатинозным. Наиболее полно осаждение происходит при подкислении раствора соляной кислотой (конечной концентрации 5 %). В некоторых случаях, особенно при осаждении большим количеством спирта (выше 70 %), осаждаются и непектиновые вещества: пентозаны, крахмал, растительная камедь. Если же осадок отсутствует, значит и пектиновые вещества в исходном растворе тоже отсутствуют Определение флокуляцией щелочноземельными основаниями Пектины осаждаются при кипячении с гидроокисью кальция. Реакция состоит в деметоксилировании пектиновых кислот и последующем осаждении их в виде пектата кальция. Гидроокись бария вызывает более быструю флокуляцию. Осаждение замедляется сахарозой. Присутствие натриевых, калиевых или аммониевых солей мешает флоккуляции Определение с применением фруктовых соков, богатых танином Разбавленные экстракты или отжатый сок некоторых растений (яблок, груш), богатых танином, применяются в качестве очень чувствительных реактивов на пектиновые вещества. Для этой цели сок зрелых плодов, приготовленный прессованием, кипятится и фильтруется в горячем виде. Полученный реактив стабилен в течение нескольких лет, если его хранить в холодильнике под слоем толуола. Осаждение пектинов этим реактивом производится следующим образом: к 1 мл реактива прибавляется по каплям 2 мл испытуемого раствора; раствор сначала мутнеет, а затем появляется осадок. Этот метод обнаружения пектиновых веществ не получил широкого распространения из-за того, что еще недостаточно выяснен механизм реакции и ее специфичность Образование окраски или флуоресценции с перманганатом калия Пектиновые вещества можно обнаружить по их реакции с 0,25%-ным раствором перманганата калия. При нагревании раствора, 16
17 содержащего смесь этих веществ и перманганата калия, до температуры кипения образуется интенсивное окрашивание в золотистый цвет со слабой зеленоватой флуоресценцией. Камедь и агар дают при этой реакции красное окрашивание без флуоресценции. Механизм реакции, ее чувствительность и специфичность пока не выяснены в достаточной степени Образование желтой окраски со щелочами К 0,5 см 3 раствора, который должен содержать, по крайней мере, 0,5 % пектиновых веществ, добавляют несколько капель 2%-ного раствора гидроокиси калия. При этом появляется сильное желтое окрашивание. Окраску лучше наблюдать после пятнадцатиминутного стояния при комнатной температуре. При подкислении образуется белый хлопьевидный осадок пектовой кислоты. В более концентрированном растворе образуется твердый желтый гель. Окраска не проявляется в разбавленном растворе. Альгиновая и аскорбиновая кислоты дают такую же реакцию Определение пектиновых кислот через метанол Задача нахождение метанола, полученного после щелочного омыления пектинов. Если при подготовке к анализу пектиновые вещества подвергают очистке, то делают это при помощи ацетона, так как этиловый спирт мешает обнаружению метоксильных групп. К 5 мл исследуемого раствора, нагретого до температуры 70 С, прибавляют 5 мл 10%-ного раствора гидроокиси натрия. После десятиминутного отстаивания раствор подкисляется до слабокислой реакции разбавленной серной кислотой, а затем подвергается перегонке. Собираются первые 5 мл дистиллята. В маленьком цилиндре со шлифом смешивают 0,25 мл полученного дистиллята, 4,75 мл воды и 2 мл 3%-ного раствора перманганата калия, содержащего 15 % фосфорной кислоты. После десятиминутного отстаивания при периодическом помешивании к смеси прибавляют 2 мл раствора, содержащего серную и щавелевую кислоты (5 г щавелевой кислоты растворяют в 100 мл 50%-ной серной кислоты), и после этого добавляют 5 мл модифицированного реактива Шиффа. Смесь перемешивается и отстаивается в течение часа в закрытом сосуде. Полученная окраска сравнивается с окраской в холостой пробе, проводимой параллельно. Если испытуемая смесь имеет более глубокую окраску, чем холостая проба, она содержит метанол, который образовался из пектиновых веществ и анализируемого образца. Количество метанола, которое можно затем пересчитать на пектины, определяется визуально, колориметрически, фотометрически (путем сравнения с окраской растворов, содержащих определенные количества метилового спирта). 17
18 Реактив Шиффа готовится следующим образом: 0,2 г солянокислого розанилина растворяется в 20 мл горячей воды. Раствор охлаждается и в него добавляется 2 г сульфата натрия, растворенного в 20 мл воды и 2 мл соляной кислоты. Смесь разбавляется до 200 мл и выдерживается в холодильнике перед употреблением, по крайней мере, 24 ч. Из всех методов качественного определения пектинов этот метод является наиболее сложным по исполнению; кроме того, для его проведения необходимо иметь десяток различных реактивов Определение через галактуроновую кислоту Определение галактуроновой кислоты в гидролизатах пектиновых веществ является удобным методом идентификации этих веществ. Пектины осаждаются из раствора двойным объемом 96%-ного этанола, затем растворяются в воде и гидролизуются пектиназой или соляной кислотой. Гидролизованный раствор фильтруется и исследуется на содержание D-галактуроновой кислоты. Для этой цели используется реакция Толленса с нафторезорцином или ее модификация. Равные объемы растворов галактуроновой и концентрированной соляной кислот нагревают 1 мин с 1 мл 1%-ного раствора нафторезорцина в этиловом спирте. После охлаждения к смеси прибавляют равный объем эфира, размешивают и оставляют стоять до образования двух слоев. В присутствии D-галактуроновой кислоты эфирный слой окрашивается в сине-фиолетовый цвет. Определению мешает присутствие арабинозы и фруктозы. Приведенные методы качественного определения пектиновых веществ страдают одним общим недостатком: все они основаны на реакциях, которые не являются специфическими для пектинов, так как для этих соединений до сих пор не найдены специфические растворители, осадители, красители. Однако, соблюдая предосторожности, которые указаны при описании этих методов, всегда можно получить данные о наличии или отсутствии пектиновых веществ в объекте исследования. 4.2 Методы количественного определения пектиновых веществ Количественное определение пектинов всегда производится в растворах, поэтому объект исследования должен находиться в растворенном состоянии. Переведение в раствор пектиновых веществ, находящихся в твердых смесях, уже описывалось при изложении методов качественного определения, однако чаще приходится иметь дело с их определением в растительных объектах. 18
19 Нужно иметь в виду, что при экстрагировании пектиновых веществ из растительных материалов сравнимые результаты могут быть получены только в том случае, если пользоваться одними и теми же приемами экстракции при их строгом соблюдении. Существуют два метода количественного извлечения пектинов из растительных материалов: 1) фракционное извлечение пектиновых веществ; 2) быстрое получение всего экстракта. По первому методу подлежащий анализу хорошо измельченный растительный материал экстрагируется на водяной бане десятикратным количеством 95%-ного этилового спирта для удаления сахаров, смолы, воска и т. д. Нерастворившийся осадок отфильтровывается, промывается 95%-ным спиртом, затем смесью спирта и эфира, снова эфиром и сушится при 85 С. Обработанный таким образом материал экстрагируется в приборе, который удобен для многократных последовательных обработок (рисунок 3). Материал помещается в сосуд А, снабженный фильтром из пористого стекла, и заливается предварительно нагретой до необходимой температуры экстракционной жидкостью. Требуемая для этого температура поддерживается при помощи водяной бани Б. После завершения процесса жидкость при помощи водяного насоса отсасывается через трубку В в приемник. Если необходимо, проводят несколько экстракций одной и той же пробы одной или несколькими жидкостями. При этом можно собирать либо весь экстракт сразу, либо по фракциям. При достаточном количестве раствора (около 50 мл на 1 г экстрагируемого материала) и хорошем размешивания можно извлечь 99 % пектиновых веществ за 4 5 последовательных обработок. Экстрагирующая жидкость выбирается в зависимости от того, в какой форме пектиновые вещества находятся в объекте исследования. Чаще всего в качестве ее применяют воду или 0,1 Н соляную кислоту. Рисунок 3 Экстрактор Вейх-Филипса 19
20 Но если объект исследования содержит нерастворимые в воде пектинаты и пектаты, экстрагирующей жидкостью должен быть очень слабый раствор щелочи, так как при действии соляной кислоты получились бы нерастворимые низкометоксилированные пектиновые и пектовые кислоты. По второму методу в трехлитровую колбу помещают 100 г хорошо измельченного испытуемого материала и заливают таким количеством горячей воды, чтобы при добавлении необходимого количества реактивов общий объем не превышал двух литров. Содержимое колбы нагревается на водяной бане до С, после чего прибавляется сернистая кислота из расчета, чтобы конечная концентрация ее была 0,4 0,6 %. Экстракция длится 60 мин при С. После этого колба вынимается из водяной бани и быстро охлаждается струей холодной воды. Затем в нее доливается дистиллированная вода до метки 2 л, содержимое размешивается и отстаивается в полном покое. Из отстоявшегося экстракта отбирается необходимое для проведения анализа количество жидкости. 4.3 Количественное определение протопектина Как известно, протопектин нерастворим в воде. Из растительной ткани или любого другого испытуемого материала сначала экстрагируются водорастворимые пектиновые вещества, затем образец подвергается обработке, которая переводит в растворимое состояние протопектин. Из хорошо измельченной пробы сначала удаляются растворимые пектины путем экстракции в течение 2 ч тремя последовательными порциями холодной (от 20 до 25 С) дистиллированной воды из расчета 100 мл на 1 г пробы. Такая экстракция удаляет из образца 98 % растворимых пектиновых веществ. Оставшийся протопектин можно перевести в растворимое состояние обработкой 0,5%-ным раствором оксалата аммония при 85 С в течение 2 ч или раствором соляной кислоты обычными приемами и определить методами, принятыми для пектиновой и пектовой кислот, а также для их солей. Предлагаемый метод количественного определения протопектина является простым и доступным, но ввиду того, что граница между нерастворимыми и растворимыми пектиновыми веществами очень неопределенная, этот метод можно считать до некоторой степени условным. 4.4 Количественное определение пектиновых и пектовых кислот и их солей Первой операцией при определении массовой доли пектиновых веществ в растительном сырье является извлечение и перевод в растворенное состояние. 20
21 Для этого берут навеску массой 25 г влажного или 10 г сухого исследуемого материала, тщательно растирают его в ступке до однородной массы. Количественно переносят в коническую колбу на 150 мл, смывая ступку водой, затем добавляют в колбу 100 мл дистиллированной воды с температурой 40 С. Колбу с материалом и водой выдерживают на водяной бане при температуре 40 С в течение 30 мин. По истечении этого времени содержимое колбы отфильтровывают через бумажный складчатый фильтр. Операцию повторяют, заливая твердый остаток в колбе 75 мл, а затем ещё раз мл воды, отфильтровывая каждый раз жидкость через тот же фильтр. Полученные экстракты собирают в мерную колбу на 250 мл и доводят до метки дистиллированной водой. Полученный раствор гидратированных пектинов используют для дальнейших анализов. Для определения массовой доли в растительном сырье протопектина и пектовой кислоты остаток измельченного растительного материала на фильтре заливают 50 мл 0,3 Н раствора соляной кислоты и переносят в коническую колбу на 250 мл, закрывают колбу пробкой с обратным холодильником и выдерживают 30 мин на кипящей водяной бане. По истечении этого времени экстракт отфильтровывают через складчатый фильтр в мерную колбу на 500 мл. Остаток на фильтре 3 4 раза промывают 75 мл дистиллированной воды, промывные воды фильтруют через бумажный фильтр в ту же колбу. Фильтр вместе с остатком растительного материала переносят в коническую колбу, заливают от 50 до 70 мл 1%-ного раствора лимоннокислого аммония и помещают на кипящую водяную баню на 30 мин. Полученный экстракт отфильтровывают через бумажный фильтр в ту же мерную колбу. Фильтр промывают горячей дистиллированной водой, после чего содержимое колбы охлаждают и доводят до метки. Полученные экстракты гидратированного пектина и протопектина исследуют одним из следующих методов Кальций-пектатный метод Метод основан на осаждении пектовых кислот в виде кальциевых солей. Это один из наиболее точных методов. Он прост, доступен и имеет хорошую сходимость параллельных анализов. В зависимости от цели исследования можно определить отдельно растворимый пектин, протопектин или сумму пектиновых веществ. Ход анализа при определении пектинов в обоих растворах одинаков. Отличие в том, что раствор протопектина предварительно нейтрализуют NaO до прибавления щелочи, необходимой для его гидролиза. Для гидролиза пектиновых веществ к 50 мл исследуемого раствора прибавляют равный объем 0,4%-ного (1 Н) раствора NaO и оставляют на 8 10 ч при комнатной температуре. По истечении этого времени раствор подкисляют тем же объемом 1 Н уксусной кислоты. 21
22 Образовавшиеся пектовые кислоты осаждают 50 мл 10%-ного раствора СаСО 3. Полученный осадок пектата кальция отфильтровывают через заранее высушенный до постоянной массы и взвешенный с бюксом бумажный фильтр. Осадок на фильтре промывают 0,5%-ным раствором СаСl 2, затем 5 6 раз холодной дистиллированной водой для удаления ионов хлора (проверка по реакции на Сl с азотнокислым серебром). Для снижения зольности осадок дополнительно промывают 3 4 раза горячей дистиллированной водой. Фильтр с осадком переносят в бюкс и сушат до постоянной массы при температуре С. Массу осадка, полученную по разности между массой бюкса с осадком на фильтре и массой бюкса с фильтром, умножают на 0,9235 для пересчета на пектовую кислоту. Если масса пектата кальция превышает 0,03 г, опыт необходимо повторить с меньшим количеством экстракта. Погрешность метода составляет 0,3 %. Источник ошибок: возможность перехода в осадок пектата кальция непектиновых примесей. Если в исследуемом объекте эти вещества не находятся в растворенном состоянии, их следует перевести в раствор каким-либо из существующих методов Карбазольный метод Метод основан на определении пектинов по образованию гидролизованного до D-галактуроновой кислоты исследуемого пектинового раствора с карбазоловым реактивом. Пектиновый раствор подкисляют серной кислотой до рн 1,0 1,5. Затем пектины осаждают подкисленным этиловым спиртомректификатом с рн 4,7 4,8. Образовавшийся осадок отделяют центрифугированием при скорости 3000 об/мин в течение 10 мин и промывают подкисленным спиртом. Промытый осадок гидролизуют концентрированной серной кислотой, добавляют 0,2%-ный спиртовый раствор карбазолового реактива и производят замер оптической плотности на фотоэлектроколориметре ФЭК-М или аналогичном при длине волны 535 нм с зеленым фильтром. Предпочтительно использовать кювету с рабочей длиной 20 мм. Отсчет на ФЭКе проводят по шкале оптической плотности. Количество пектиновых веществ определяют с помощью калибровочной кривой, построенной по чистой D-галактуроновой кислоте. Недостаток карбазольного метода в том, что результаты часто искажены из-за недостаточно тщательной промывки пектинового осадка от сахарозы, продукты гидролиза которой (в основном глюкоза) дают с карбазолом тот же цвет, хотя и менее интенсивный, чем D- галактуроновая кислота. 22
23 4.4.3 Количественное определение в растворе без деметоксилирования Существует несколько модификаций этого метода, из которых наиболее распространены следующие Первый вариант метода К 50 мл исследуемого раствора прибавляют концентрированную соляную кислоту до достижения ее конечной концентрации 0,15 Н. Затем при непрерывном, энергичном перемешивании вводят по каплям 100 мл 95%-ного этилового спирта. Через 1 ч полученный осадок отфильтровывают через бумажный складчатый фильтр, тщательно промывают смесью воды и этанола (1:2), содержащей 0,2 % соляной кислоты. Промытый осадок растворяют на фильтре горячей водой. При плохой растворимости осадка к горячей воде прибавляют несколько капель щелочи. Количество фильтрата должно быть равным 50 мл. Полученный фильтрат нейтрализуют и снова осаждают этиловым спиртом. Образовавшийся осадок снова отфильтровывают, промывают сначала смесью воды с этанолом (1:2), затем 95%-ным этиловым спиртом, переносят количественно горячей водой в предварительно высушенный до постоянной массы и взвешенный тигель и сушат в сушильном шкафу при температуре С до постоянной массы. Разность между массой тигля с осадком после сушки и пустого тигля представляет собой количество пектина в 50 мл раствора Второй вариант метода К 100 мл исследуемого раствора прибавляют 20 мл концентрированной соляной кислоты. Из подкисленного раствора пектин осаждают 100 мл 95%-ного этилового спирта. Спустя 15 мин выпавший осадок отфильтровывают через плотное шелковое полотно, которое осторожно разворачивают и помещают в открытую широкую чашку осадком вверх. Осадок заливают 300 мл 95%-ного спирта, растирают и отжимают. Такую промывку повторяют 3 4 раза до отрицательной реакции на ион хлора. После тщательного отжатия осадок переносят количественно в предварительно взвешенный пористый тигель, сушат и сжигают его. Количество пектиновых веществ определяется по разности между массами остатков после сушки и после сжигания. Достоинством метода осаждения этиловым спиртом является его простота. Однако он недостаточно точен, так как вместе с пектином соосаждаются балластные по отношению к пектину вещества Осаждение ацетоном К исследуемому раствору, содержащему приблизительно 0,2 % пектиновых веществ, прибавляют ацетон до его конечной 23
24 концентрации в растворе 50 %. После 5 мин отстаивания смеси осадок отфильтровывают через бумажный фильтр, количественно переносят его, смывая холодной водой, в мерную колбу на 100 мл, доводят до метки. Для лучшего растворения осадка раствор подогревают. После охлаждения раствора прибавляют ацетон для осаждения пектиновых веществ. Осадок снова отфильтровывают через взвешенный беззольный фильтр, промывают 60%-ным ацетоном, сушат при температуре 100 С и сжигают. Разность между массами остатков после сушки и после сжигания представляет собой количество пектина в исследуемом растворе. Достоинство данного метода состоит в том, что получается более плотный осадок, чем при осаждении спиртом. Кроме того, ацетон легче регенерируется. Недостатком является большая погрешность метода, так как при осаждении ацетоном в осадок могут выпадать непектиновые вещества Определение пектиновых веществ по оптическому вращению Этот метод применим для цитрусовых пектинов. Анализ проводится следующим образом. Вначале измеряют удельное вращение исходного раствора, после чего пектиновые вещества количественно осаждают в виде медной соли и отфильтровывают. Затем измеряют удельное вращение фильтрата. Разность вращений до и после осаждения пектиновых веществ прямо пропорциональна их концентрации (удельное вращение цитрусового пектина +230 град). Приведенный метод определения концентрации пектиновых веществ широкого распространения не получил, так как пектины, выделенные из различных источников различными методами, имеют разные величины удельного вращения. Кроме того, медь осаждает из растворов и другие вещества, например белки. Следовательно, нужно вводить дополнительные операции по предварительной очистке испытуемого раствора от непектиновых составляющих Количественное определение пектиновых веществ в растворе, сопровождающееся деметоксилированием Осаждение соляной кислотой Пектовые кислоты осаждаются из растворов сильными минеральными кислотами. Вследствие того, что при определенных условиях растворимость пектовых кислот даже в горячей воде очень низкая, это свойство может быть использовано для количественного определения пектинов. Сущность метода определения пектиновых веществ через пектовую кислоту путем осаждения соляной кислотой заключается в следующем. К 25 мл приблизительно 1%-ного раствора пектиновых веществ 24
25 прибавляют от 8 до 12 г сахарозы и осаждают 200 мл 95%-ного этилового спирта. Осадок отфильтровывают, а затем растворяют на фильтре дистиллированной водой. Полученный раствор омыляют 0,2 1%-ным раствором гидроокиси натрия в течение 15 мин и осаждают соляной кислотой (1:2,5) при кипячении в течение 5 мин. Выпавший осадок отфильтровывают и промывают горячей водой почти до отрицательной реакции на хлор-ион. Фильтрат должен быть прозрачным. Если это не так, определение повторяют: омыляют пектиновый раствор более концентрированной щелочью и при более низкой температуре. Полученный осадок смывают в тигель и высушивают сначала на паровой бане, а затем в сушильном шкафу при 98 С. Вес пектиновой кислоты определяют как разность между массами до и после определения золы. Результаты, полученные по этому методу, обычно занижены, вероятно, вследствие деградации пектиновых веществ во время нагревания с кислотой Объемное измерение осадка пектовой кислоты Этот метод заключается в омылении пектиновых веществ гидроокисью натрия, осаждении пектовой кислоты соляной кислотой и центрифугировании полученного осадка при об/мин точно 15 мин. Количество пектиновых веществ определяется по объему осадка пектовой кислоты после центрифугирования. Метод основан на осаждении пектовых кислот сильными минеральными кислотами. К 200 мл исследуемого раствора прибавляют 2,5 мл 40%-ного раствора гидроокиси натрия и оставляют при комнатной температуре в течение 15 мин. Образовавшуюся пектовую кислоту осаждают 10 мл концентрированной соляной кислоты и центрифугируют при 3000 об/мин в течение 10 мин в градуированной центрифужной пробирке. Пользуясь калибровочной кривой и объемом полученного осадка, определяют концентрацию пектиновых веществ. Для построения калибровочной кривой используют данные таблицы 3. Таблица 3 Зависимость концентрации пектиновых веществ от объема осадка Концентрация пектина, % Объем осадка Метиловый эфир пектовой кислоты Полигалактуронаны пектовой кислоты, мл 0,05 0,35 11,0 0,10 0,70 21,5 0,15 0,105 30,0 0,20 0,140 34,5 0,25 0,175 39,7 0,30 0,210 44,0 Метод достаточно точен, результаты анализов хорошо воспроизводимы. Погрешность определения 0,01 %. 25
26 Метод можно применять только для определения концентрации данного препарата, а также для приблизительного определения пектиновой кислоты в соках, так как объем осадка зависит не только от его количества, но и от размера молекулы исходной пектиновой кислоты и, следовательно, характера осадка Определение при помощи титрования пектовой кислоты Полигалактуроновая кислота, являющаяся основой всех пектиновых веществ, может быть выделена из них и оттитрована раствором основания. Данные титрования достаточно точно определяют количество пектиновых или пектовых кислот в растворе или экстракте. Первой операцией при проведении определения по этому методу является осаждение пектинов ацетоном. К исследуемому раствору прибавляют при помешивании такое количество ацетона, чтобы конечная концентрация его была равной 60 %. Смесь отстаивают несколько минут и фильтруют через бумажный складчатый фильтр. Осадок промывают на фильтре 60%-ным ацетоном и смывают в тот же стакан холодной водой. Полученный водный раствор кипятится для удаления ацетона и доведения объема жидкости до 40 мл, затем его переносят в градуированный сосуд на 200 мл и охлаждают. После этого его тщательно титруют 0,1 Н гидроокисью натрия. По окончании титрования производят щелочное омыление пектиновых веществ: к оттитрованному раствору прибавляют еще 10 мл щелочи, сосуд закрывают и отстаивают в течение 30 мин при комнатной температуре. Избыток щелочи оттитровывают 0,1 Н соляной кислотой и прибавляют еще 50 мл 0,1 Н соляной кислоты. Содержимое перемешивают и сосуд помещают на кипящую водяную баню на 10 мин. Затем смесь охлаждают, содержимое сосуда доводят до 200 мл, перемешивают и отфильтровывают. Отмеренное количество фильтрата титруют 0,1 Н гидроокисью натрия. В таких же условиях проводят холостой опыт. Теоретически 1 мл 0,1 Н гидроокиси натрия эквивалентен 0,177 г чистой полигалактуроновой или пектовой кислоты. Приведенные методы прямые и достаточно точные. Недостатком их является длительность определения. Источником ошибок в этом случае может быть недостаточная очистка препарата пектина, выделяемого из исследуемого раствора и используемого для титрования. 26
27 5 ЛАБОРАТОРНАЯ РАБОТА 1 «ВЫДЕЛЕНИЕ ПЕКТИНА ИЗ СЫРЬЯ РАСТИТЕЛЬНОГО ПРОИСХОЖДЕНИЯ» Цель работы: овладение практическими приемами по извлечению пектина из различного растительного сырья и сравнение органолептических характеристик разных видов пектина. Продолжительность работы 6 часов. Оборудование и материалы: соляная кислота (0,03 Н раствор).. спирт этиловый 96%-ный. щавелевая кислота, 0,5%-ный раствор. сульфат алюминия.. аммиак.. оксалат аммония 1%-ный раствор. ацетон. стакан на 1 л колба Бунзена.. воронка Бюхнера. колба на 1 л.. колба на 0,5 л. холодильник шариковый. баня водяная 2000 мл 1600 мл 1500 мл 1250 мл 500 мл 200 мл 50 мл 6 шт. 1 шт. 1 шт. 3 шт. 3 шт. 6 шт. 6 шт. Опыт 1. Из корочек плодов цитрусовых Корочки апельсина, лимона или мандарина в количестве 50 г измельчают в мясорубке, помещают в мешочек из ткани и заливают в стакане спиртом для удаления эфирного масла, пигментов и других примесей. Стакан накрывают часовым стеклом и ставят не менее чем на 1 ч на водяную баню, нагретую до 70 С. После этого материал отжимают на воронке Бюхнера и снова заливают спиртом (отработанный спирт отгоняют из раствора на водяной бане, высушивают прокаленным сульфатом меди и используют в дальнейшей работе). Операцию повторяют до тех пор, пока спиртовой экстракт будет лишь слабо окрашен в желтый цвет, на это уходит около 500 мл этанола. Отмытую массу помещают в колбу на 500 мл, заливают 200 мл 0,03 Н НСl и нагревают 1 ч на кипящей водяной бане. Горячую вытяжку фильтруют через вату, остаток дважды промывают на фильтре небольшими порциями горячей воды. После охлаждения фильтрат частично нейтрализуют аммиаком до слабокислой реакции (индикатор лакмус) и упаривают на водяной бане (желательно в вакууме) до 70 мл. К оставшемуся сиропу добавляют два объема спирта. Выпавший сырой 27
🎦 Видео
10 класс Качественные реакции на белкиСкачать

Качественные реакции в органической химииСкачать

Все качественные реакции в органике | Химия ЕГЭ 2022 | УмскулСкачать

ЭКЗО- и ЭНДО- термические реакции. Химия – ПростоСкачать

Видеоурок: Практическая работа № 4. Цветные реакции на белкиСкачать

Качественные реакции в органикеСкачать

Как решать ОРГАНИЧЕСКИЕ ЦЕПОЧКИ? Основные типы химических реакцийСкачать

25. Схема реакции и химическое уравнениеСкачать

Как определить опасный ли алкоголь? (Jack Daniel's) Реакция марганцовки на метиловый спирт.Скачать

Опыты по химии. Цветные реакции белка: биуретовая; ксантопротеиноваяСкачать

Все качественные реакции органических соединений за 45 минут | Химия 10 класс | УмскулСкачать

ПЕКТИН что это такое и как его использовать | Е440Скачать

Можно ли отличить опасный для здоровья метанол от этилового спиртаСкачать