Пропанол-2, изопропиловый спирт CH3CH2CH2OH – органическое вещество, молекула которого содержит, помимо углеводородной цепи, одну группу ОН.
Общая формула предельных нециклических одноатомных спиртов: CnH2n+2O.
- Строение пропанола-2
- Водородные связи и физические свойства спиртов
- Изомерия пропанола-2
- Структурная изомерия
- Химические свойства пропанола-2
- 1.1. Взаимодействие с раствором щелочей
- 1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
- СН3–CHOK –CH 3 + H2O → СН3–CHOH–CH3 + KOH
- 2. Реакции замещения группы ОН
- 2.1. Взаимодействие с галогеноводородами
- 2.2. Взаимодействие с аммиаком
- 2.3. Этерификация (образование сложных эфиров)
- 2.4. Взаимодействие с кислотами-гидроксидами
- 3. Реакции замещения группы ОН
- 3.1. Внутримолекулярная дегидратация
- 3.2. Межмолекулярная дегидратация
- 4. Окисление спиртов
- 4.1. Окисление оксидом меди (II)
- 4.2. Окисление кислородом в присутствии катализатора
- 4.3. Жесткое окисление
- 4.4. Горение спиртов
- 5. Дегидрирование пропанола-2
- Получение пропанола-1
- 1. Щелочной гидролиз галогеналканов
- 2. Гидрирование карбонильных соединений
- 3. Гидратация алкенов
- Изопропиловый спирт: температура кипения, описание вещества, применение
- Изопропиловый спирт – что это такое?
- Физические свойства
- Основные характеристики изопропилового спирта
- Химические свойства
- Получение
- Применение
- Применение изопропанола в химической и автомобильной промышленности
- Применение изопропанола в других видах хозяйственной деятельности
- Токсичность
- Изопропиловый спирт
- Изопропиловый спирт
- Введение
- Изопропиловый спирт
- 1. Открытие
- 2. Физические свойства
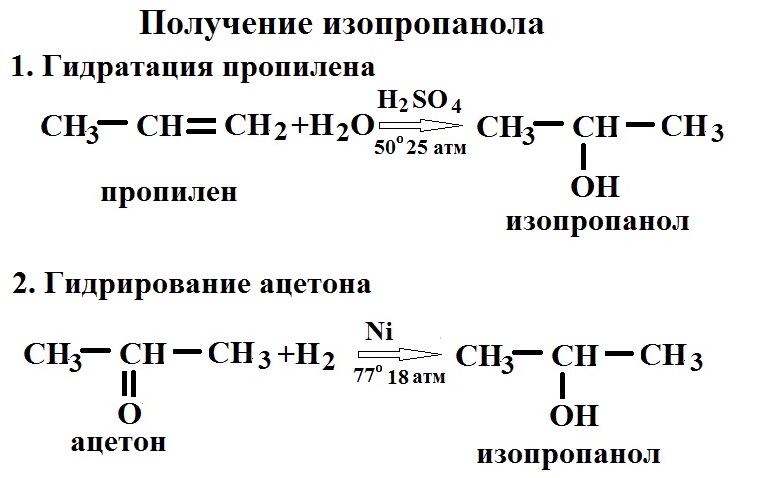
- 3. Получение
- 3.1. Получение из углеводов
- 3.2. Гидратация пропилена серной кислотой в жидкой фазе
- 3.3. Гидратация пропилена в газовой фазе на катализаторах
- 3.4. Лабораторные методы
- 3.5. Очистка полученного спирта
- 4. Химические свойства
- 5. Применение
- 6. Токсикология
- См.. также
- Примечания
Строение пропанола-2
В молекулах спиртов, помимо связей С–С и С–Н, присутствуют ковалентные полярные химические связи О–Н и С–О.
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
| Атом кислорода в спиртах находится в состоянии sp 3 -гибридизации. |
В образовании химических связей с атомами C и H участвуют две 2sp 3 -гибридные орбитали, а еще две 2sp 3 -гибридные орбитали заняты неподеленными электронными парами атома кислорода.
Поэтому валентный угол C–О–H близок к тетраэдрическому и составляет почти 108 о .
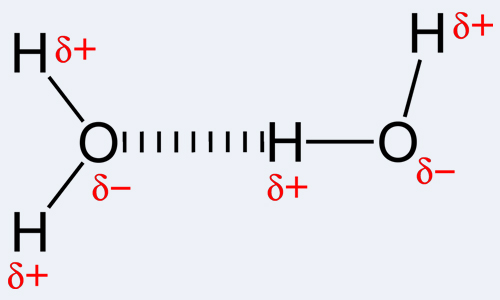
Водородные связи и физические свойства спиртов
Спирты образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому спирты – жидкости с относительно высокой температурой кипения (температура кипения пропанола +92 о С).
Водородные связи образуются не только между молекулами спиртов, но и между молекулами спиртов и воды. Поэтому пропанол-2 очень хорошо растворим в воде. Молекулы пропанола-2 в воде гидратируются:
| Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. |
Пропанол-2 смешивается с водой в любых соотношениях.
Изомерия пропанола-2
Структурная изомерия
Для пропанола-2 характерна структурная изомерия – изомерия положения гидроксильной группы и межклассовая изомерия.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Спирты являются межклассовыми изомерами с простыми эфирами. Общая формула и спиртов, и простых эфиров — CnH2n+2О.
| Например. Межклассовые изомеры с общей формулой С3Н8О пропиловый спирт СН3–CH2–CH2–OH и метилэтиловый эфир CH3–O–CH2–CH3 |
| Пропиловый спирт | Метилэтиловый эфир |
| СН3–CH2–CH2–OH | CH3–O–CH2–CH3 |
Изомеры с различным положением группы ОН отличаются положением гидроксильной группы в молекуле. Такая изомерия характерна для спиртов, которые содержат три или больше атомов углерода.
| Например. Пропанол-1 и пропанол-2 |
| Пропанол-1 | Пропанол-2 |
 |  |
Химические свойства пропанола-2
Спирты – органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Химические реакции гидроксисоединений идут с разрывом одной из связей: либо С–ОН с отщеплением группы ОН, либо связи О–Н с отщеплением водорода. Это реакции замещения, либо реакции отщепления (элиминирования).
Свойства спиртов определяются строением связей С–О–Н. Связи С–О и О–Н — ковалентные полярные. При этом на атоме водорода образуется частичный положительный заряд δ+, на атоме углерода также частичный положительный заряд δ+, а на атоме кислорода — частичный отрицательный заряд δ–.
Такие связи разрываются по ионному механизму. Разрыв связи О–Н с отрывом иона Н + соответствует кислотным свойствам гидроксисоединения. Разрыв связи С–О соответствует основным свойствам и реакциям нуклеофильного замещения.
С разрывом связи О–Н идут реакции окисления, а с разрывом связи С–О — реакции восстановления.
Таким образом, для спиртов характерны следующие свойства:
|
1. Кислотные свойства пропанола-2
| Спирты – неэлектролиты, в водном растворе не диссоциируют на ионы; кислотные свойства у них выражены слабее, чем у воды. |
1.1. Взаимодействие с раствором щелочей
При взаимодействии спиртов с растворами щелочей реакция практически не идет, т. к. образующиеся алкоголяты почти полностью гидролизуются водой.
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому пропанол-2 не взаимодействует с растворами щелочей.
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Пропанол-2 взаимодействует с активными металлами (щелочными и щелочноземельными). При этом образуются алкоголяты. При взаимодействии с металлами спирты ведут себя, как кислоты.
| Например, пропанол-2 взаимодействует с калием с образованием изопропилата калия и водорода . |
2СН3–CH OH –CH3 + 2K → 2СН3–CHOK –CH 3 + H 2
Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
| Например, изопропилат калия разлагается водой: |
СН3–CHOK –CH 3 + H2O → СН3–CHOH–CH3 + KOH
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии спиртов с галогеноводородами группа ОН замещается на галоген и образуется галогеналкан.
| Например, пропанол-2 реагирует с бромоводородом. |
2.2. Взаимодействие с аммиаком
Гидроксогруппу спиртов можно заместить на аминогруппу при нагревании спирта с аммиаком на катализаторе.
| Например, при взаимодействии пропанола-2 с аммиаком образуется изопропиламин. |
2.3. Этерификация (образование сложных эфиров)
Cпирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры.
| Например, изопропанол реагирует с уксусной кислотой с образованием изопропилацетата (изопропилового эфира уксусной кислоты): |
2.4. Взаимодействие с кислотами-гидроксидами
Спирты взаимодействуют и с неорганическими кислотами, например, азотной или серной.
| Например, при взаимодействии пропанола-2 с азотной кислотой образуется изопропилнитрат. |
3. Реакции замещения группы ОН
В присутствии концентрированной серной кислоты от спиртов отщепляется вода. Процесс дегидратации протекает по двум возможным направлениям: внутримолекулярная дегидратация и межмолекулярная дегидратация.
3.1. Внутримолекулярная дегидратация
При высокой температуре происходит внутримолекулярная дегидратация и образуется соответствующий алкен.
| Например, из пропанола-2 под действием концентрированной серной кислоты при высокой температуре образуется пропилен: |
3.2. Межмолекулярная дегидратация
При низкой температуре происходит межмолекулярная дегидратация: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. Продуктом реакции является простой эфир.
| Например, при дегидратации пропанола-2 при низкой температуре образуется диизопропиловый эфир: |
4. Окисление спиртов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на каталитическое, мягкое и жесткое.
| Вторичные спирты окисляются в кетоны: в торичные спирты → кетоны |
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора.
4.1. Окисление оксидом меди (II)
Cпирты можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества. Вторичные спирты окисляются до кетонов.
| Например, пропанол-2 окисляется оксидом меди (II) при нагревании до ацетона |
4.2. Окисление кислородом в присутствии катализатора
Cпирты можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.).
| Например, при окислении пропанола-2 образуется ацетон |
4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) вторичные спирты также окисляются до кетонов.
| При нагревании первичного спирта с перманганатом или дихроматом калия в кислой среде может образоваться также альдегид, если его сразу удаляют из реакционной смеси. |
| Например, при взаимодействии изопропанола с перманганатом калия в серной кислоте образуется ацетон |
4.4. Горение спиртов
Образуются углекислый газ и вода и выделяется большое количество теплоты.
| Например, уравнение сгорания пропанола-2: |
5. Дегидрирование пропанола-2
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования. При дегидрировании первичных спиртов образуются альдегиды.
| Например, при дегидрировании пропанола-2 образуется ацетон. |
Получение пропанола-1
1. Щелочной гидролиз галогеналканов
При взаимодействии галогеналканов с водным раствором щелочей образуются спирты. Атом галогена в галогеналкане замещается на гидроксогруппу.
| Например, при нагревании 2-хлорпропана с водным раствором гидроксида натрия образуется пропанол-2 |
СН3–CHCl –CH 3 + NaOH → СН3–CHOH–CH3 + NaCl
2. Гидрирование карбонильных соединений
Присоединение водорода к альдегидам протекает при нагревании в присутствии катализатора. При гидрировании кетонов образуются вторичные спирты.
| Например: при гидрировании ацетона образуется изопропанол |
3. Гидратация алкенов
Гидратация (присоединение воды) алкенов протекает в присутствии минеральных кислот. При присоединении воды к алкенам образуются спирты.
Для несимметричных алкенов реакция идёт преимущественно по правилу Марковникова.
Изопропиловый спирт: температура кипения, описание вещества, применение
Изопропиловый спирт (пропанол-2, изопропанол, i-propanol, isopropyl alcohol) – химическое соединение, получившее широкое распространение благодаря растворяющей способности, дезинфицирующим и консервирующим свойствам. Этот спирт используют во многих видах промышленности, а также автомобилисты и медики.
Изопропиловый спирт – что это такое?
Изопропиловый спирт – вторичный одноатомный спирт. Химическая формула изопропанола СН3 – СН (ОН) – СН3. Изопропанол можно рассматривать как производное насыщенного углеводорода пропана СН3 – СН2 – СН3, в молекуле которого один атом водорода замещен на спиртовую — гидроксильную группу (-ОН). Поскольку гидроксильная группа в молекуле одна, то спирт называют одноатомным. Как видно из химической формулы изопропилового спирта, углерод, связанный с гидроксильной группой, соединен с двумя группами СН3. Поэтому спирт называют вторичным.
Структурная формула изопропилового спирта, а также формулы некоторых других одноатомных спиртов приведены на рисунке.
Физические свойства
Многие свойства изопропанола, температура кипения например, обусловлены наличием спиртовой группы (-ОН). Эта группа обладает высокой полярностью. В результате чего группа –ОН одной молекулы изопропанола образует связь с группой –ОН другой молекулы изопропанола. Таким образом, молекулы ассоциируются, то есть соединяются между собой. Такую связь называют водородной. Она слабая, но имеет большое значение в природе.
Благодаря водородным связям вода H2O при обычных условиях — жидкость, а не газ, как, например, похожее по строению вещество H2S сероводород. Именно наличие водородных связей приводит к тому, что твердая фаза воды – лед — имеет меньшую плотность в природе, чем жидкая фаза, в результате чего лед не тонет.
Образование водородных связей объясняет высокую температуру кипения изопропилового спирта и других низкомолекулярных спиртов в сравнении с соединениями схожего строения. Например, температура кипения пропана -42 °С, то есть пропан при любых температурах выше -42°С находится в газообразном состоянии. Температура кипения изопропилового спирта намного выше и составляет 82,4 °С. Это означает, что изопропанол при обычной температуре находится в жидком состоянии.
Если сравнить температуру кипения изопропилового спирта и метилового, то у первого она несколько выше: 82 градуса против 65. Это означает, что при обычных условиях изопропиловый спирт меньше испаряется, чем метиловый.
Температура плавления и температура кипения изопропилового спирта и некоторых других соединений представлены в таблице.
| Вещество | Температура кипения, о С | Температура плавления, о С |
| Метанол | 65 | -98 |
| Этанол | 78 | -117 |
| Пропанол | 97 | -127 |
| Изопропанол | 82 | -88 |
| Пропан | -42 | -190 |
Образование водородных связей между спиртовыми группами изопропанола и молекулами воды обуславливает растворимость этого спирта в воде. Растворимость зависит от количества углеродных атомов в цепи, чем их меньше, тем лучше растворяется спирт. Поэтому среди спиртов наибольшей растворимостью в воде обладает метанол, который можно смешать с водой в любом соотношении. Этанол растворяется в воде чуть хуже метанола, а изопропанол — хуже этанола.
Основные характеристики изопропилового спирта
Растворяется в ацетоне, в бензоле хорошо растворяется, смешивается с водой, эфиром, этанолом.
Плотность 0,7851 г/см 3 (20 °С).
Нижний предел взрываемости — 2,5% (по объему).
Температура плавления -89,5 °С.
Температура кипения +82,4°С.
Зависимость температуры кипения изопропилового спирта от давления представлена в таблице.
| Давление паров, мм рт.ст. | Температура кипения, о С |
| 1 | -26,1 |
| 10 | 2,4 |
| 40 | 23,8 |
| 100 | 39,5 |
| 400 | 67,8 |
| 1020,7 | 90 |
Химические свойства
Изопропиловый спирт представляет собой бесцветную жидкость. Обладает характерным запахом, не похожим на запах этилового спирта. Не проводит электрический ток.
Вступает в многочисленные химические реакции, что используется для промышленных синтезов. Большая часть произведенного изопропилового спирта идет на производство ацетона. Для получения ацетона изопропанол необходимо окислить сильным окислителем – смесью K2Cr2O7 + H2SO4 или KMnO4 + H2SO4.
Получение
В России в 2017 году произведено около 40 тыс. тонн изопропилового спирта, почти на 20% меньше, чем в 2016 году. Объем производства достаточно мал — за этот же период метанола произведено почти 4 млн тонн.
Производят изопропиловый спирт в России два предприятия: ЗАО «Завод синтетического спирта» в городе Орске Оренбургской области и ООО «Синтез Ацетон» в городе Дзержинске Нижегородской области.
В Орске производят изопропанол методом сернокислотной гидратации пропилена или пропан-пропиленовой фракции, полученной из газов термического или каталитического крекинга. Получают два вида изопропанола, отличающихся степенью очистки: технический (87%) и абсолютизированный (99,95%). В Дзержинске изопропанол получают гидрированием ацетона.
Побочным продуктом при получении изопропилового спирта гидратацией пропилена является диизопропиловый спирт, который представляет особую ценность как вещество, имеющее высокое октановое число, равное 98.
Применение
Изопропиловый спирт – отличный растворитель, поэтому имеет широкую сферу применения. Его используют в основном в химической промышленности, а также в нефтеперерабатывающей, лесохимической, мебельной, медицинской, пищевой, парфюмерной отраслях промышленности, в полиграфии, домашнем хозяйстве. Направления применения:
- растворитель,
- консервант,
- обезвоживающее средство,
- экстрагент примесей,
- стабилизатор,
- антиобледенитель.
Применение изопропанола в химической и автомобильной промышленности
Применение в химической промышленности следующее:
- сырье для производства ацетона,
- производство пластмасс – полиэтилена низкого давления и полипропилена,
- синтез изопропилацетата,
- производство инсектицидов,
- растворитель при производстве этилцеллюлозы, ацетилцеллюлозы, нитроцеллюлозы в лакокрасочной промышленности,
- безопасная транспортировка нитроцеллюлозы (в нее добавляют 30% изопропанола),
- экстрагент в тонкой химической технологии.
- применение в нефтеперерабатывающей промышленности:
- растворитель карбамида, применяемого для депарафинизации дизельного топлива,
- добавка к маслам, усиливающая их антикоррозионные свойства и понижающая температуру застывания,
- «удаление» воды из бензиновых баков.
Вода попадает в топливные магистрали и баки нефтебаз путем конденсации из влажного воздуха. При низких температурах она замерзает и может образовать ледяную пробку. При добавлении абсолютированного изопропанола вода в нем растворяется и не замерзает.
В автомобильной промышленности:
- «удаление» воды из бензобаков путем ее растворения,
- как компонент топлива для повышения октанового числа и уменьшения токсичных выбросов,
- антиобледенитель ветрового стекла,
- антифриз для радиаторов,
- удаление тормозной жидкости с гидравлических тормозных систем.
Применение изопропанола в других видах хозяйственной деятельности
Применение в мебельной и лесохимической промышленности:
- экстракция смол из древесины в смеси с другими растворителями,
- снятие старого лакового покрытия, растворитель французской полировки, клеев, масел,
- связующее вещество в полиролях и очистителях.
В полиграфии изопропанол применяют для увлажнения в печатных процессах. В электронике — в качестве растворителя для очистки контактных разъемов, магнитных лент, головок дисков, лазерных линз, для удаления термопасты, очистки клавиатуры, ЖК-мониторов, стеклянных экранов. Нельзя применять его только для очистки винила, так как изопропанол вступает с ним в реакцию.
Применение в медицинской промышленности и медицине:
- входит в состав антисептических растворов, пропитывающих жидкостей для салфеток,
- обеззараживающее средство для протирания места инъекции,
- 75% водный раствор используют как дезинфицирующее средство для рук,
- дезинфицирующие тампоны,
- осушитель для профилактики отита,
- консервирующее средство для сохранения генетического материала и анализов (менее токсичен, чем формальдегид).
Изопропанол имеет преимущества перед этанолом: более выраженное антисептическое действие и низкую цену. Поэтому в тех случаях, когда раньше применяли этанол, сейчас используют изопропанол.
В косметической и парфюмерной промышленностях изопропанол применяют в производстве:
- косметических средств,
- средств личной гигиены,
- духов, одеколонов, лаков.
В пищевой промышленности изопропанол используют при производстве замороженных продуктов в качестве хладоносителя.
В домашнем хозяйстве:
- для очищения различных поверхностей, кроме резиновых и виниловых,
- для удаления пятен с тканей, древесины,
- для удаления клея от наклеек (на бумажные изопропанол не действует).
Токсичность
Изопропанол применяется в медицине в качестве местного антисептика. При местном использовании быстро испаряется и не оказывает негативного влияния.
При вдыхании паров раздражает дыхательные пути, может вызвать головную боль. Высокая концентрация изопропанола в воздухе тормозит работу ЦНС, приводит к потере сознания. Поэтому работать с изопропанолом можно только в хорошо проветриваемом помещении.
Внутрь изопропанол не применяется, поскольку он токсичен. Попадая в печень, превращается в ядовитое вещество — ацетон, поражающий печень, почки и головной мозг. 200 мл изопропанола являются смертельной дозой.
Изопропиловый спирт
Изопропиловый спирт
- 1 Открытие 2 Физические свойства 3 Получение
- 3.1 Получение из углеводов 3.2 Гидратация пропилена серной кислотой в жидкой фазе
- 3.2.1 Метод концентрированной кислоты 3.2.2 Метод разбавленной кислоты
3.3 Гидратация пропилена в газовой фазе на катализаторах 3.4 Лабораторные методы 3.5 Очистка полученного спирта
4 Химические свойства 5 Применение 6 Токсикология
Введение
Изопропиловый спирт
Изопропиловый спирт (2-пропанол, пропан-2-ол, изопропанол, диметилкарбинол) CH 3 CH (OH) CH 3 — самый вторичный одноатомный спирт алифатического ряда. Относится к веществам 3-го класса опасности (умеренно опасные вещества) по степени воздействия на организм, имеет наркотическое действие. ПДК для паров изопропанола в воздухе составляет 10 мг / м?. Отравление изопропиловым спиртом наступает вследствие вдыхания паров, содержащих концентрацию, превышающую ПДК, кумулятивных свойств не имеет [2]. Потребление даже в небольших дозах вызывает отравление. Широко используется как растворитель в промышленности и технический спирт в средствах для чистки стекла, оргтехники и др..
Товарный изопропанол содержит от 91 до 99,5% спирта. Технические условия для этого продукта не установлено, из-за чего препарат, который поступает на продажу, по составу может соответствовать даже азеотропной смеси с водой. Степень чистоты спирта может колебаться в широких пределах в зависимости от способа его получения и использованной сырья.
1. Открытие
Изопропиловый спирт открыл 1955 года М. Бертло при обработке пропилена концентрированной серной кислотой и разложении продукта реакции водой [3].
2. Физические свойства
Давление паров изопропанола
Изопропиловый спирт растворим в воде, этаноле, эфиром и хлороформе. Растворяет этилцеллюлозу, поливинилбутирал, много масел, алкалоиды, резины и природные смолы [4]. Нерастворимый в растворах солей. В отличие от этанола или метанола, изопропиловый спирт можно выделить из водного раствора добавлением неорганической соли, в частности хлорида или сульфата натрия [5].
Изопропиловый спирт с водой образует азеотроп с точкой кипения 80,37 ? C и долей спирта 87,7% масс. (91% об.). Водно-спиртовая смесь способна снижать температуры плавления [5].
Со снижением температуры растет вязкость изопропанола. При температуре ниже -70 ? C изопропиловый спирт по вязкости напоминает кленовый сироп.
3. Получение
3.1. Получение из углеводов
В небольших количествах изопропиловый спирт, рядом с бутанолом, получают при брожении углеводов [6] [7] [8]
3.2. Гидратация пропилена серной кислотой в жидкой фазе
Основной способ получения изопропанола в промышленности — через косвенную гидратацию пропилена серной кислотой (CH 3 CHCH 2 + H 2 O).
Сырьем обычно служит пропан — пропиленовая смесь газов крекинга или пропиленовая смесь газов пиролиза нефти. При этом процессе возможны следующие химические реакции взаимодействия пропилена с серной кислотой и водой :
Изопропилсульфат реагируя с пропиленом, дает диизопропилсульфат:
Диизопропилсульфат при реакции с водой снова образует изопропилсульфат и изопропиловый спирт
Кроме того, изопропиловый спирт реагирует с диизопропилсульфатом с образованием диизопропиловый эфир и изопропилсульфату:
Пространственное изображение молекулы изопропанола
Многочисленные исследования гидратации пропилена серной кислотой привели к возникновению двух различных методов:
метода концентрированной кислоты; метода разбавленной кислоты.
3.2.1. Метод концентрированной кислоты
Газы стабилизации с крекинг — установок с содержанием пропилена 20-24% сначала отмывают в скрубберах от сероводорода [9] [10]. Затем удаляют выше углеводороды фракционной перегонкой и концентрируют пропилен до минимум 50%. Абсорбцию пропилена можно существенно улучшить с помощью абсорбционного масла, большей частью газойля. Абсорбционное масло облегчает переработку низькоконцентрованого пропилена. Кроме того, оно значительно снижает склонность к полимеризации при использовании высококонцентрированного пропилена.
Абсорбция проводится противотоком в экстракционной колонне с 8 тарелками под давлением 8-10 кгс / см? в 92%-ной серной кислоте при 20 ? С. На каждой тарелке имеется слой абсорбционного масла. После экстракции давление серной кислоты снижают, в отстойнике отделяется экстракционное масло и снова подается в колонну. Экстракт содержит около 1,1-1,3 моль С 3 Н 6 / моль H 2 SO 4. Расход кислоты составляет
12 кг на 10 л 100%-ного изопропилового спирта, расход пропилена — около 39 м? (теоретически — 32 м?).
Температура на отдельных тарелках экстракционной колонны не должна превышать 20 ? С, иначе возможны значительные потери пропилена через полимеризацию.
С отстойника экстракт поступает в освинцованной реакционный аппарат с турбомишалкою, где разбавляется водой до получения 40%-ного раствора, в течение примерно 1 ч при 50 ? С. После 4-часового пребывания в аппарате без перемешивания спирт и образован диизопропиловый эфир экстрагируются водяным паром. Пары спирта и эфира промываются 1% раствором едкого натра. После разведения водой до концентрации 15% конденсат выдерживают несколько дней для отделения полимера. При ректификации сначала выделяют
2% легко кипящих компонентов, во второй колонне изопропиловый спирт концентрируют до 91,3%-ной азеотропной смеси, которая кипит при 80,4 ? С. Выход изопропилового спирта составляет 85-90% по отношению к исходному пропилена.
Для получения безводного изопропилового спирта азеотропную смесь обезвоживают бензолом или диизопропиловый эфиром, реже — диэтиловым эфиром. Главный продукт, который находится в сборнике разделен на 2 слоя, частично возвращается в верхнюю часть колонны (верхний слой из изопропилового спирта и бензола), частично подается в колонну для концентрации (нижний слой из водного изопропилового спирта) для регенерации остатков изопропилового спирта и бензола. Безводный изопропиловый спирт (> 99%) отгоняется снизу колонны.
Все детали аппаратов, которые контактируют с разбавленной серной кислотой изготавливаются или с свинца, или меди. После промывания 1% раствором едкого натра сталь — наиболее подходящий материал для изготовления емкостей, труб и колонн.
3.2.2. Метод разбавленной кислоты
Схематическое изображение молекулы изопропанола
По методу разбавленной кислоты пропилен абсорбируется под давлением 25 кгс / см? при 65 ? С в 70%-ной серной кислоте. При этом диизопропилсульфат не образуется, а изопропиловый спирт получают сразу без дальнейшего разведения водой [11] [12].
В абсорбционной безтарильчату колонну, заполненную 70%-ной серной кислотой, нагнетается предварительно компримированного крекинг — газ, содержащий пропилен. Серная кислота поглощает 1 моль С 3 Н 6 на моль H 2 SO 4. Крекинг-газ с начальным содержанием пропилена около 20-25% абсорбируется до остаточного содержания 5-6%.
Остаточный газ экстрагируется в колонне с колпачковыми тарелками свежей 70%-ной серной кислотой, которая выходит из колонны для омыления, до остаточного содержания пропилена 1%. Затем серная кислота с 0,2% пропилена проходит через безтарильчату колонну. В отгонным колонне и колонне для омыления к смеси серной кислоты и изопропилсульфату прилагается вода до получения 60%-ного раствора, а изопропилсульфат омилюеться. 85%-ный изопропиловый спирт отгоняется. С низа колонны выводится 70%-ная серная кислота, которую можно сразу применять для следующего цикла.
3.3. Гидратация пропилена в газовой фазе на катализаторах
Классический метод получения изопропилового спирта в жидкой фазе имеет некоторые недостатки. Так, потери кислоты довольно значительные, а затраты на ее регенерацию существенны. Кроме того, большие трудности вызывает коррозия оборудования. Поэтому было осуществлено многочисленные опыты по прямого присоединения воды в олефинов на неподвижном слое катализатора. В результате был разработан метод гидратации этилена с применением фосфорной кислоты на цеолите (кизельгур).
Реакция непосредственного преобразования олефинов в спирт является равновесной, протекания реакции способствуют низкая температура, высокий давление и высокое соотношение пара: олефины.
Из многих возможных катализаторов реакции прямой гидратации олефинов для промышленного применения рекомендуется только два [ ]
фосфорная кислота на носителе; оксид вольфрама с промотором.
3.4. Лабораторные методы
Изопропиловый спирт можно получить каталитической гидратацией пропилена при наличии серной кислоты. Максимальный выход спирта (67%) было достигнуто использованием 99%-ной серной кислоты при 15 ? С. При 100 ? С и использовании 85%-ной кислоты плохо поглощаются даже небольшие количества пропилена [13].
Гидратация пропилена также возможна при наличии оксида вольфрама. В этом методе наблюдается высокий выход спирта и образуется меньшее количество полимеров, чем в предыдущем. В тех случаях, когда катализаторы таблетированные при давлении 10 4 кг / см?, конверсия при 250 ? С составляла 16%. Если же таблетирования проводили при давлении 5 ? 10 3 кг / см?, то конверсия при этой же температуре составляла лишь 10% [14].
3.5. Очистка полученного спирта
Очищают изопропиловый спирт, полученный из таких олефинов, как пропилен, обрабатывая его сначала водным раствором едкого натра, а затем подвергая многократной перегонке. Перед последней перегонкой спирт стабилизируют и избавляют от постороннего запаха, добавляя небольшое количество хлористой меди (0,5% или меньше) [15].
Безводный изопропиловый спирт получают, насыщая водную смесь аммиаком и диоксидом углерода. При этом образуются два слоя. Слой, содержащий большее количество воды, перегоняют, получая аммиак, диоксид углерода и азеотропную смесь. Слой с меньшим содержанием воды также подвергают фракционной перегонке с получением азеотроп и безводного спирта [16]
Товарный продукт очищают, осушая его над магниевой лентой и подвергая фракционной перегонке в колонке Дафтона высотой 180 см. Чистейшая фракция кипит при 82,33 — 82,39 ? С [17].
Еще один метод очистки изопропилового спирта заключается в его осушки сначала над хлористым кальцием, а затем — над оксидом бария. После этого его трижды подвергают тщательной фракционной перегонке [18].
«Абсолютный» изопропиловый спирт можно получить перегонкой в ??эффективной колонке над свежегашеной известью. Фракцию, кипящую при 82-82,4 ? С, собирают и встряхивают в течение 2 дней с безводным сульфатом меди, после чего перегоняют несколько раз до достижения постоянной температуры кипения. Полученный таким способом спирт содержит меньше 0,10% воды [19].
Еще один способ получения чистого изопропанола заключается в его сушке над магнием и перегонке над сульфаниловая кислота [20].
Существует и быстрый метод получения безводного изопропилового спирта. Товарный 91%-ный спирт встряхивают с водным раствором едкого натра (взятым в количестве 10% от массы спирта), после чего отделяют от водного раствора, снова встряхивают с большим количеством раствора едкого натра, декантують и перегоняют. Если смешать полученный таким образом продукт с 8 объемами сероуглерода, ксилола или петролейного эфира, то при этом не будет наблюдаться даже незначительного помутнения [21].
Водный раствор изопропилового спирта можно сконцентрировать встряхиванием с хлористым натрием. Верхний слой содержит около 87% пропанола-2 и 2-3% хлористого натрия. Перегонка дает 91%-на азеотропную смесь.
4. Химические свойства
Изопропиловый спирт окисляется до соответствующего кетонов — ацетона. Окислительным агентом в этом процессе может выступать хромовая кислота.
Также ацетон с изопропанола можно получить дегидрогенизации на нагретом медном катализаторе :
Изопропиловый спирт используется одновременно и как растворитель, и как реагент в реакции Меервейна-Пондорфа-Верлея и других процессах, связанных с перемещением водорода. С помощью трехбромистым с изопропанола можно получить 2-бромопропан, а в результате процесса дегидратации при нагревании при наличии серной кислоты, образуется пропилен.

Как и большинство спиртов, изопропиловый спирт взаимодействует с активными металлами (в частности, натрием), образуя алкоголяты.
Реакция с алюминием (инициирована незначительным количеством ртути) применяется для приготовления катализатора — алкоголята алюминия [22].
Из типичных для спиртов реакций, можно привести взаимодействия изопропилового спирта с:
- амидами металлов
- нитрил металлов
- реактивами Гриньяра
- галогеноводнямы (Х: F, Cl, Br, I)