- Серная кислота
- Строение молекулы и физические свойства
- Способы получения
- Химические свойства
- Please wait.
- We are checking your browser. gomolog.ru
- Why do I have to complete a CAPTCHA?
- What can I do to prevent this in the future?
- Серная кислота
- Серная кислота. Общая характеристика, получение, химические свойства
Серная кислота
Строение молекулы и физические свойства
Серная кислота H2SO4 – это сильная кислота, двухосновная, прочная и нелетучая. При обычных условиях серная кислота – тяжелая маслянистая жидкость, хорошо растворимая в воде.
Растворение серной кислоты в воде сопровождается выделением значительного количества кислоты. Поэтому по правилам безопасности в лаборатории при смешивании серной кислоты и воды мы добавляем серную кислоту в воду небольшими порциями при постоянном перемешивании.
Валентность серы в серной кислоте равна VI.
Способы получения
1. Серную кислоту в промышленности производят из серы, сульфидов металлов, сероводорода и др. Один из вариантов — производство серной кислоты из пирита FeS2.
Основные стадии получения серной кислоты :
- Сжигание или обжиг серосодержащего сырья в кислороде с получением сернистого газа.
- Очистка полученного газа от примесей.
- Окисление сернистого газа в серный ангидрид.
- Взаимодействие серного ангидрида с водой.
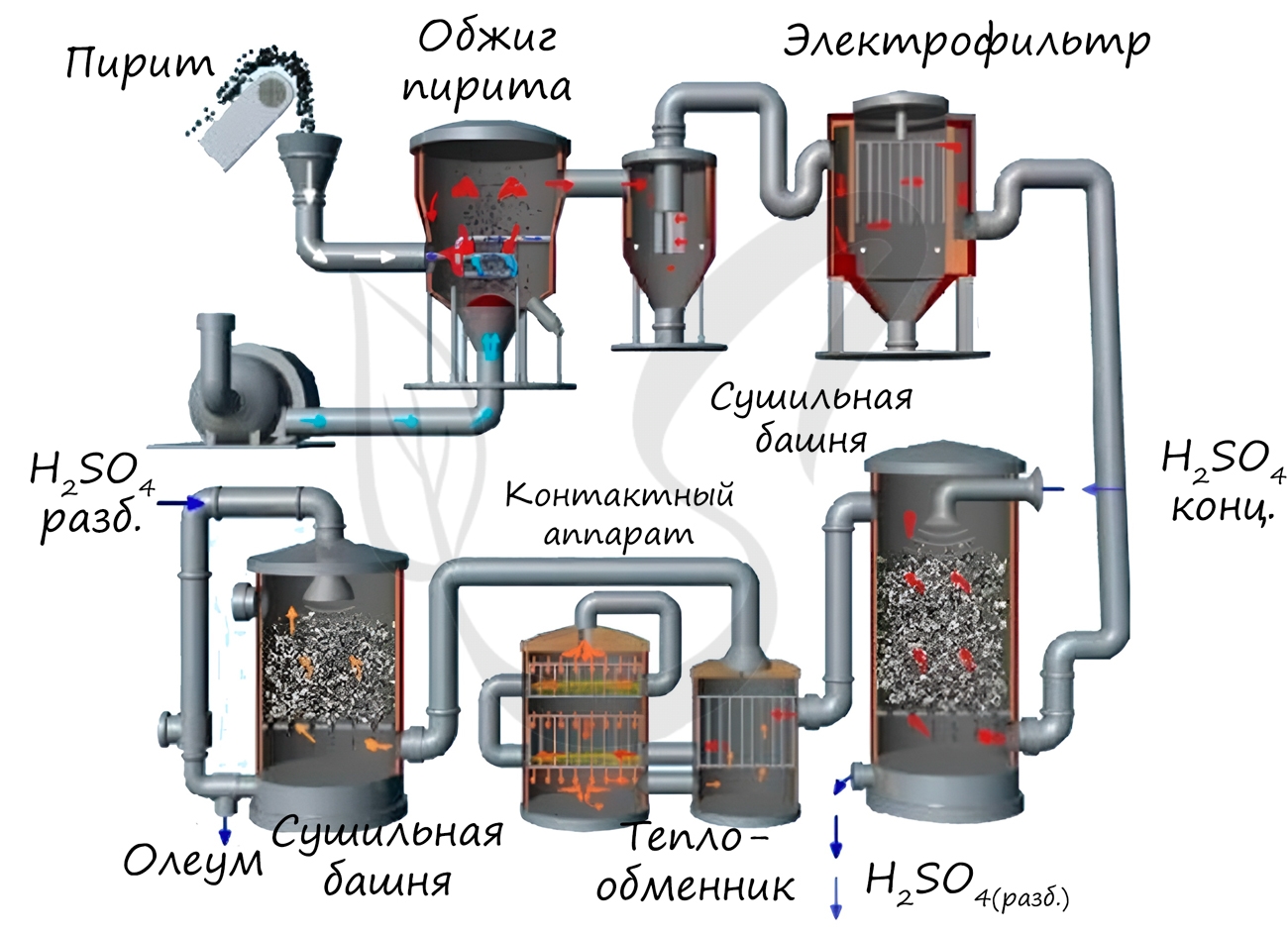
Рассмотрим основные аппараты, используемые при производстве серной кислоты из пирита (контактный метод):
| Аппарат | Назначение и уравнения реакций |
| Печь для обжига | 4FeS2 + 11O2 → 2Fe2O3 + 8SO2 + Q Измельченный очищенный пирит сверху засыпают в печь для обжига в «кипящем слое». Снизу (принцип противотока) пропускают воздух, обогащенный кислородом, для более полного обжига пирита. Температура в печи для обжига достигает 800 о С |
| Циклон | Из печи выходит печной газ, который состоит из SO2, кислорода, паров воды и мельчайших частиц оксида железа. Такой печной газ очищают от примесей. Очистку печного газа проводят в два этапа. Первый этап — очистка газа в циклоне. При этом за счет центробежной силы твердые частички ссыпаются вниз. |
| Электрофильтр | Второй этап очистки газа проводится в электрофильтрах. При этом используется электростатическое притяжение, частицы огарка прилипают к наэлектризованным пластинам электрофильтра). |
| Сушильная башня | Осушку печного газа проводят в сушильной башне – снизу вверх поднимается печной газ, а сверху вниз льется концентрированная серная кислота. |
| Теплообменник | Очищенный обжиговый газ перед поступлением в контактный аппарат нагревают за счет теплоты газов, выходящих из контактного аппарата. |
| Контактный аппарат | 2SO2 + O2 ↔ 2SO3 + Q В контактном аппарате производится окисление сернистого газа до серного ангидрида. Процесс является обратимым. Поэтому необходимо выбрать оптимальные условия протекания прямой реакции (получения SO3):
Как только смесь оксида серы и кислорода достигнет слоев катализатора, начинается процесс окисления SO2 в SO3. Образовавшийся оксид серы SO3 выходит из контактного аппарата и через теплообменник попадает в поглотительную башню. |
| Поглотительная башня | Получение H2SO4 протекает в поглотительной башне. Однако, если для поглощения оксида серы использовать воду, то образуется серная кислота в виде тумана, состоящего из мельчайших капелек серной кислоты. Для того, чтобы не образовывался сернокислотный туман, используют 98%-ную концентрированную серную кислоту. Оксид серы очень хорошо растворяется в такой кислоте, образуя олеум: H2SO4·nSO3. Образовавшийся олеум сливают в металлические резервуары и отправляют на склад. Затем олеумом заполняют цистерны, формируют железнодорожные составы и отправляют потребителю. |
Общие научные принципы химического производства:
- Непрерывность.
- Противоток
- Катализ
- Увеличение площади соприкосновения реагирующих веществ.
- Теплообмен
- Рациональное использование сырья
Химические свойства
Серная кислота – это сильная двухосновная кислота .
1. Серная кислота практически полностью диссоциирует в разбавленном в растворе по первой ступени:
По второй ступени серная кислота диссоциирует частично, ведет себя, как кислота средней силы:
HSO4 – ⇄ H + + SO4 2–
2. Серная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Например , серная кислота взаимодействует с оксидом магния:
Еще пример : при взаимодействии серной кислоты с гидроксидом калия образуются сульфаты или гидросульфаты:
Серная кислота взаимодействует с амфотерным гидроксидом алюминия:
3. Серная кислота вытесняет более слабые из солей в растворе (карбонаты, сульфиды и др.). Также серная кислота вытесняет летучие кислоты из их солей (кроме солей HBr и HI).
Например , серная кислота взаимодействует с гидрокарбонатом натрия:
Или с силикатом натрия:
Концентрированная серная кислота реагирует с твердым нитратом натрия. При этом менее летучая серная кислота вытесняет азотную кислоту:
Аналогично – концентрированная серная кислота вытесняет хлороводород из твердых хлоридов, например , хлорида натрия:
4. Т акже серная кислота вступает в обменные реакции с солями.
Например , серная кислота взаимодействует с хлоридом бария:
5. Разбавленная серная кислота взаимодействует с металлами, которые расположены в ряду активности металлов до водорода. При этом образуются соль и водород.
Например , серная кислота реагирует с железом. При этом образуется сульфат железа (II):
Серная кислота взаимодействует с аммиаком с образованием солей аммония:
Концентрированная серная кислота является сильным окислителем . При этом она обычно восстанавливается до сернистого газа SO2. С активными металлами может восстанавливаться до серы S, или сероводорода Н2S.
Железо Fe, алюминий Al, хром Cr пассивируются концентрированной серной кислотой на холоде. При нагревании реакция возможна.
При взаимодействии с неактивными металлами концентрированная серная кислота восстанавливается до сернистого газа:
При взаимодействии с щелочноземельными металлами и магнием концентрированная серная кислота восстанавливается до серы:
При взаимодействии с щелочными металлами и цинком концентрированная серная кислота восстанавливается до сероводорода:
6. Качественная реакция на сульфат-ионы – взаимодействие с растворимыми солями бария. При этом образуется белый кристаллический осадок сульфата бария:
Видеоопыт взаимодействия хлорида бария и сульфата натрия в растворе (качественная реакция на сульфат-ион) можно посмотреть здесь.
7. Окислительные свойства концентрированной серной кислоты проявляются и при взаимодействии с неметаллами.
Например , концентрированная серная кислота окисляет фосфор, углерод, серу. При этом серная кислота восстанавливается до оксида серы (IV):
Уже при комнатной температуре концентрированная серная кислота окисляет галогеноводороды и сероводород:
Please wait.
We are checking your browser. gomolog.ru
Why do I have to complete a CAPTCHA?
Completing the CAPTCHA proves you are a human and gives you temporary access to the web property.
What can I do to prevent this in the future?
If you are on a personal connection, like at home, you can run an anti-virus scan on your device to make sure it is not infected with malware.
If you are at an office or shared network, you can ask the network administrator to run a scan across the network looking for misconfigured or infected devices.
Another way to prevent getting this page in the future is to use Privacy Pass. You may need to download version 2.0 now from the Chrome Web Store.
Cloudflare Ray ID: 7071451e4fff596b • Your IP : 85.95.179.80 • Performance & security by Cloudflare
Серная кислота
Серная кислота — сильная двухосновная кислота, при н.у. маслянистая жидкость без цвета и запаха.
Обладает выраженным дегидратационным (водоотнимающим) действием. При попадании на кожу или слизистые оболочки приводит к тяжелым ожогам.
Замечу, что существует олеум — раствор SO3 в безводной серной кислоте, дымящее жидкое или твердое вещество. Олеум применяется при изготовлении красителей, органическом синтезе и в производстве серной кислот.
Получение
Известны несколько способов получения серной кислоты. Применяется промышленный (контактный) способ, основанный на сжигании пирита, окислении образовавшегося SO2 до SO3 и последующим взаимодействием с водой.
Нитрозный способ получения основан на взаимодействии сернистого газа с диоксидом азота IV в присутствии воды. Он состоит из нескольких этапов:
В окислительной башне смешивают оксиды азота (II) и (IV) с воздухом:
Смесь газов подается в башни, орошаемые 75-ной% серной кислотой, здесь смесь оксидов азота поглощается с образованием нитрозилсерной кислоты:
В ходе гидролиза нитрозилсерной кислоты получают азотистую кислоту и серную:
В упрощенном виде нитрозный способ можно записать так:
Химические свойства
- Кислотные свойства
В водном растворе диссоциирует ступенчато.
Сильная кислота. Реагирует с основными оксидами, основаниями, образуя соли — сульфаты.
KOH + H2SO4 = KHSO4 + H2O (гидросульфат калия, соотношение 1:1 — кислая соль)
2KOH + H2SO4 = K2SO4 + 2H2O (сульфат калия, соотношение 2:1 — средняя соль)
С солями реакция идет, если в результате выпадает осадок, образуется газ или слабый электролит (вода). Серная кислота, как и многие другие кислоты, способна растворять осадки.
Серная кислота окисляет неметаллы — серу и углерод — соответственно до угольной кислоты (нестойкой) и сернистого газа.
Реакции с металлами
Реакции разбавленной серной кислоты с металлами не составляют никаких трудностей: она реагирует как самая обычная кислота, например HCl. Все металлы, стоящие до водорода, вытесняют из серной кислоты водород, а стоящие после — не реагируют с ней.
Подчеркну, что реакции разбавленной серной кислоты с железом и хромом не сопровождаются переходом этих элементов в максимальную степень окисления. Они окисляются до +2.
Cu + H2SO4(разб.) ⇸ (реакция не идет, медь не может вытеснить водород из кислоты)
Концентрированная серная кислота ведет себя совершенно по-иному. Водород никогда не выделяется, вместо него с активными металлами выделяется H2S, с металлами средней активности — S, с малоактивными металлами — SO2.
Холодная концентрированная серная кислота пассивирует Al, Cr, Fe, Ni, Be, Co. При нагревании или амальгамировании данных металлов реакция идет.
Обратите особое внимание, что при реакции железа, хрома с концентрированной серной кислотой достигается степень окисления +3. В подобных реакциях с разбавленной серной кислотой (написаны выше) достигается степень окисления +2.
Иногда в тексте задания даны подсказки. Например, если написано, что выделился газ с неприятным запахом тухлых яиц — речь идет об H2S, если же написано, что выделилось простое вещество — речь о сере (S).
© Беллевич Юрий Сергеевич 2018-2022
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Серная кислота. Общая характеристика, получение, химические свойства
Серная кислота, также известная как масло витриола, или купоросное масло представляет собой минеральную кислоту, состоящую из элементов серы, кислорода и водорода, с молекулярной формулой H2SO4.
Она является бесцветной, не имеющей запаха вязкой жидкостью, которая растворима в воде и синтезируется в реакциях, которые являются сильно экзотермическими.
Чистая серная кислота является вязкой прозрачной жидкостью, как масло, и это объясняет старое название кислоты («масло витриола»).
Обладает следующими важными характеристиками:
- гигроскопичная — легко поглощает водяной пар из воздуха;
- коррозионная — сильный окислитель и дегидратирующий агент;
- вызывает ожоги — даже при малых концентрациях способна к образованию химических и вторичных термических ожогов.
Серная кислота в истории
Изучение витриола (купороса) — категории стекловидных минералов, из которых может быть получена кислота, началось в древности.
- Одни из самых ранних дискуссий о происхождении и свойствах витриола — в работах греческого врача Диоскорида (I век нашей эры) и римского натуралиста Плиния Старшего (23-79 годы нашей эры).
Средневековые алхимики исламской эпохи, Джабир ибн Хайян (721 — 815, также известный как Гебер), Рази (865 — 925) и Джамаль Дин аль — Ватват (1318), включили купорос в списки классификации минералов.
- Ибн Сина (Авиценна) сосредоточился на медицинских применениях и различных разновидностях витриола.
Мухаммад ибн Закарий аль-Рази (854-925) считается первым, кто произвел серную кислоту. Серная кислота была названа «маслом витриола» средневековыми европейскими алхимиками, потому что она была приготовлена обжаркой «зелёного купороса» (сульфата железа (II)) в железной реторте.
- В XVII веке германо — голландский химик Иоганн Глаубер приготовил серную кислоту, сжигая серу вместе с селитрой (нитрат калия, KNO3), в присутствии пара. По мере разложения солевого раствора он окислял серу до SO3, который объединялся с водой для получения серной кислоты.
В 1736 году лондонский фармацевт Джошуа Уорд использовал этот метод для начала первого крупномасштабного производства серной кислоты.
- В 1746 году в Бирмингеме Джон Робак применил этот способ для получения H2SO4 в камерах со свинцовой облицовкой, которые были более прочными, менее дорогими и более крупными, чем ранее использовавшиеся стеклянные контейнеры. Этот процесс позволил эффективно индустриализовать производство серной кислоты.
После нескольких уточнений этот способ, называемый процессом в свинцовой камере или «камерный процесс», оставался стандартом для производства серной кислоты в течение почти двух столетий.
В 1831 году британский торговец уксусом Перегрин Филлипс запатентовал «контактный процесс», который был гораздо более экономичным процессом производства серного ангидрида и концентрированной серной кислоты.
Получение серной кислоты
Существует несколько способов получения серной кислоты, в частности
- процесс влажной серной кислоты (метод WSA), мокрый катализ;
- метод «свинцовой камеры» — первый индустриальный способ получения серной кислоты;
- «контактный метод» — современный способ получения больших объемов H2SO4.
Серная кислота и Вода
Концентрированная серная кислота обладает очень мощным дегидратирующим свойством, удаляя воду (H2O) из других химических соединений, включая сахар и другие углеводы, и получая углерод, тепло и пар.
Приготовление разбавленной кислоты может быть опасным из-за тепла, выделяющегося в процессе разбавления.
Вода обладает более высокой теплоемкостью, чем кислота, и поэтому сосуд из холодной воды будет поглощать тепло по мере добавления кислоты.
Поскольку реакция гидратации серной кислоты является очень экзотермической, разбавление всегда должно осуществляться добавлением кислоты к воде, а не воды к кислоте.
Реакция находится в равновесии, которое способствует быстрому протонированию воды, добавление кислоты к воде гарантирует, что кислота является ограничительным реагентом.
Эту реакцию лучше всего рассматривать как образование ионов гидроксония:
Серная кислота и Ожоги
Серная кислота способна вызывать сильные ожоги, особенно когда она находится в высоких концентрациях.
- Она легко разлагает белки и липиды посредством гидролиза амида и сложного эфира при контакте с живыми тканями, такими как кожа и мышцы;
- проявляет сильное дегидратирующее свойство на углеводах, высвобождая дополнительное тепло и вызывая вторичные термические ожоги;
- быстро атакует роговицу и может вызвать постоянную слепоту, если плеснуть на глаза;
- в случае проглатывания она необратимо повреждает внутренние органы и может даже привести к летальному исходу;
- сильные окислительные свойства делают ее сильно коррозионной по отношению ко многим металлам и могут привести к его разрушению на других материалах.
По этим причинам ущерб, наносимый серной кислотой, потенциально является более серьезным, чем ущерб, наносимый другими сравнительно сильными кислотами, такими как соляная кислота и азотная кислота.
Серная кислота и ее Опасность
Основными профессиональными рисками, создаваемыми этой кислотой, являются контакт с кожей, приводящий к ожогам и вдыхание паров.
- Воздействие паров в высоких концентрациях приводит к немедленному и сильному раздражению глаз, дыхательных путей и слизистых оболочек: это быстро прекращается после воздействия, хотя существует риск последующего отека легких, если повреждение тканей было более сильным.
При более низких концентрациях наиболее часто сообщаемым симптомом хронического воздействия сернокислотных аэрозолей является эрозия зубов, обнаруженная практически во всех исследованиях.
- Повторное воздействие сернокислых туманов может повысить вероятность развития рака легких до 64 процентов.
В США допустимый предел воздействия на серную кислоту установлен на уровне 1 мг/м3: пределы в других странах аналогичны. Были сообщения о приеме серной кислоты в пищу, приводящем к дефициту витамина B12 с комбинированной дегенерацией.
- В таких случаях чаще всего поражается спинной мозг, но зрительные нервы могут демонстрировать демиелинизацию, потерю аксонов и глиозы.
Серная кислота и ее Применение
Производство H2SO4 в стране является хорошим показателем ее промышленной прочности.
Мировое производство в 2004 году составило около 180 миллионов тонн при следующем географическом распределении:
- Азия — 35%,
- Северная Америка (включая Мексику) — 24%,
- Африка 11%, Западная Европа — 10%,
- Восточная Европа и Россия — 10%,
- Австралия и Океания — 7%,
- Южная Америка — 7%.
Большая часть этого количества (≈60%) потребляется на удобрения, в частности на суперфосфаты, фосфат аммония и сульфаты аммония.
Около 20% используется в химической промышленности для производства моющих средств, синтетических смол, красителей, фармацевтических препаратов, нефтяных катализаторов, инсектицидов и антифризов, а также в различных процессах, таких как кислотизация нефтяных скважин, восстановление алюминия, проклеивание бумаги, обработка воды.
Около 6% применений относятся к пигментам и включают краски, эмали, печатные краски, мелованные ткани и бумагу.
Остальное количество ( ≈14% ) применяется в таких отраслях, как производство взрывчатых веществ, целлофана, ацетата и вискозного текстиля, смазочных материалов, цветных металлов и батарей.
Серная кислота и Водоросли
H2SO4 используется в качестве защиты некоторыми морскими видами, например, фаэофит Desmarestia munda (порядок Desmarestiales) концентрирует серную кислоту в клеточных вакуолях.
- Под воздействием воздуха они выделяют кислоту, тем самым разрушая себя и близлежащие морские водоросли в процессе.
Серная кислота и Венера
Серная кислота образуется в верхних слоях атмосферы Венеры при фотохимическом воздействии Солнца на диоксид углерода, диоксид серы и водяной пар.
- Ультрафиолетовые фотоны с длинами волн менее 169 нм могут фотодиссоциировать диоксид углерода на монооксид углерода и атомный кислород.
В верхних, более холодных частях атмосферы Венеры серная кислота существует в виде жидкости, а густые облака серной кислоты полностью затмевают поверхность планеты, если смотреть сверху.
- Постоянные венерины облака производят концентрированный кислотный дождь, так как облака в атмосфере Земли производят водный дождь.
Серная кислота и Европа
Инфракрасные спектры, полученные космическим аппаратом NASA Galileo, показывают различные поглощения на спутнике Юпитера Европе, которые приписываются одному или нескольким гидратам серной кислоты.
- H2SO4 в растворе с водой вызывает значительное снижение температуры плавления воды до 210 К (− 63 С), и это делает более вероятным существование жидких растворов под ледяной коркой Европы.
Трактовка спектров несколько спорна. Некоторые планетологи предпочитают присваивать спектральные особенности сульфатному иону, возможно, как части одного или нескольких минералов на поверхности Европы.
Серная кислота на Земле
Чистая серная кислота не встречается естественным образом на Земле в безводной форме из-за ее большого сродства к воде.
- Разбавленная серная кислота является составной частью кислотного дождя, который образуется атмосферным окислением диоксида серы в присутствии воды, то есть окислением сернистой кислоты.
Диоксид серы является основным побочным продуктом, получаемым при сжигании серосодержащих видов топлива, таких как уголь или нефть.
- Серная кислота образуется путем окисления сульфидных минералов, таких как сульфид железа.
- В стратосфере, втором слое атмосферы, который обычно находится между 10 и 50 км над поверхностью Земли, серная кислота образуется в результате окисления вулканического диоксида серы гидроксильным радикалом.
Поскольку серная кислота достигает перенасыщения в стратосфере, она может образовать частицы аэрозоля и обеспечить поверхность для роста аэрозоля путем конденсации и коагуляции с другими аэрозолями вода-серная кислота, что приводит к образованию стратосферного аэрозольного слоя.
Таблица 1: Химические свойства серной кислоты
Реагенты
Разбавленная H2SO4
Концентрированная H2SO4
Металлы активные
(Ca, Na, Ba, Zn, Mg)
Металлы средней активности
(Fe, Sn, Cr, Co, Ni, Pb)
Малоактивные металлы
(Hg, Ag, Cu, Bi)
H2SO4 (k.) + Au, Pt ≠ ни при каких условиях