—>Просмотров : 407 | —>Добавил : Biz-ledy (05.02.2021) (Изменено: 05.02.2021)
| Всего ответов: 1 | ||||||||||||||||||||||||||||||||||||||||||||||||||
Содержание Обсуждение вопроса:Если разбавлять водой хлорид сурьмы (III), то выпадает осадок хлорокиси сурьмы: SbCl₃ + H₂O → SbOCl + 2HCl Для того чтобы раствор сделать снова прозрачным — добавим соляной кислоты для того, что бы подавить гидролиз. SbOCl + 2HCl → SbCl₃ + H₂O Опыт 3. Влияние разбавления на гидролиз хлорида сурьмыСтепень гидролиза солей зависит от их природы. В случае гидролиза SbCl3 идут следующие процессы: 1) SbCl3 + HOH D Sb(OH)Cl2 + HCl Sb 3+ + HOH D Sb(OH) 2+ + H + 2) Sb(OH)Cl2 + (HOH) D SbOCl¯ + HCl Sb(OH) 2+ + НОН D Sb(OH)2 + + H + Sb(OH) 2+ + Cl — D SbOCl¯ + H + + H2O В результате гидролиза по второй ступени образуется Sb(OH)2Cl — неустойчивое вещество, которое разлагается с образованием осадка оксохлорида сурьмы SbOCl. Это приводит к смещению равновесия гидролиза вправо. Поэтому растворы SbCl3 можно готовить только в сильнокислой среде. Налейте в пробирку примерно 1 мл SbCl3. Добавьте к раствору SbCl3 примерно 5 капель дистиллированной воды. Что наблюдаете? Добавьте в реакционную смесь 1 мл соляной кислоты (2н). Что наблюдаете? Добавьте к раствору еще 1-2 мл дистиллированной воды. Что наблюдаете? Запишите наблюдения и уравнения реакции гидролиза SbCl3. Объясните причины образования и растворения осадка SbOCl. Опыт 4. Взаимное усиление гидролиза (необратимый гидролиз) Гидролиз соли усиливается, если связать один из ионов, образующийся в результате гидролиза, в слабый электролит. В результате гидролиза соли слабого основания и сильной кислоты в растворе образуются свободные ионы Н + (рН — (рН>7). Но ионы Н + и ОН — связываются в слабый электролит Н2О. Поэтому степень гидролиза солей увеличивается, то есть гидролиз одной соли усиливает гидролиз другой. В результате гидролиз таких солей доходит до конца. Так, если смешать растворы Al2(SO4)3 и Na2CO3, то в результате образуется осадок Al(ОН)3 и выделится СО2, но не образуется Al2(CO3)3. Al 3+ + НОН D AlОН 2+ + Н + При взаимодействии растворов: Н + + OН — D Н2О В соответствии с принципом Ле Шателье это усиливает гидролиз обеих солей: AlОН 2+ + НОН D Al(ОН)2 + + Н + В результате всех этих процессов образуются следующие соединения: К пяти каплям раствора сульфата алюминия прибавьте 5-6 капель раствора карбоната натрия. Что наблюдаете? Докажите, что образуется осадок Al(ОН)3, а не Al2(CO3)3. Для этого проверьте растворимость образовавшегося осадка в HCl (2н) и NaOH (2н). Запишите наблюдения и уравнения реакций. Напишите уравнения и признаки реакций при смешивании растворов сульфата алюминия и карбоната натрия. Рассчитайте, при каком значении рН начинается образование осадка Al(ОН)3, если концентрация [Al 3+ ] в растворе равна 0,1 моль/л. Хлорид сурьмы III
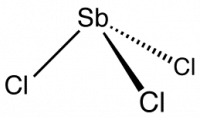
Хлорид сурьмы III — бинарное неорганическое соединение сурьмы и хлора с формулой SbCl3, бесцветные кристаллы, очень хорошо растворимые в холодной воде. Содержание
Получение
2 Sb + 3 Cl2 → 2 SbCl3
Sb2O3 + 6 HCl → 60−80oC 2 SbCl3 + 3 H2O
2 Sb2O3 + 6 Cl2 → 1000oC 4 SbCl3 + 3 O2
2 Sb2S3 + 9 Cl2 → 250oC 4 S SbCl3 + 3 S2Cl2 Физические свойстваХлорид сурьмы III образует бесцветные гигроскопичные диамагнитные кристаллы. Вызывает ожоги на коже. Очень хорошо растворимые в воде. Концентрированные водные растворы устойчивы и называются «сурьмяное масло» (едкая, жгучая, ядовитая жидкость). Разбавленные водные растворы подвергаются гидролизу. Растворяется в хлороформе, четырёххлористом углероде, бензоле, диоксане и других органических растворителях. | ||||||||||||||||||||||||||||||||||||||||||||||||||