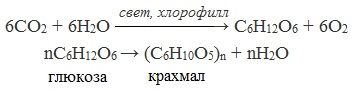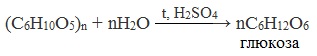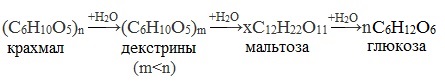Крахмал – ценный питательный продукт. Он входит в состав хлеба, картофеля, круп и наряду с сахарозой является важнейшим источником углеводов в человеческом организме.
Химическая формула крахмала (С6(Н2О)5) n .
- Строение крахмала
- Амилоза
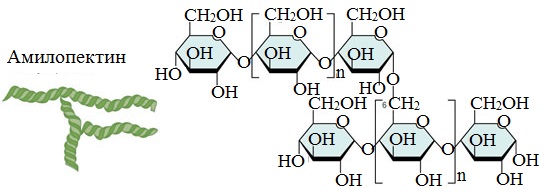
- Амилопектин
- Биологическая роль крахмала. Гликоген
- Превращение крахмала в организме человека и животных
- Нахождение в природе
- Физические свойства
- Химические свойства крахмала
- Получение крахмала
- Применение крахмала
- Химические свойства крахмала подтвердить уравнениями реакций
- Урок химии с ИКТ «Крахмал»
- Ход урока
- I. Организационная часть.
- II. Проверка домашнего задания.
- III. Изучение учебного материала по плану с использованием презентации.
- IV. Закрепление изученного материала (демонстрация слайда «Вопросы»).
- V. Итог урока.
Строение крахмала
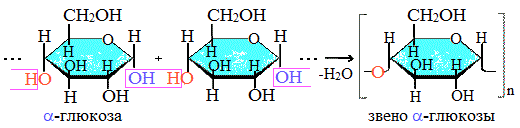
Крахмал состоит из 2 полисахаридов, построенных из остатков циклической a-глюкозы.
Как видно, соединение молекул глюкозы происходит с участием наиболее реакционноспособных гидроксильных групп, а исчезновение последних исключает возможность образования альдегидных групп, и они в молекуле крахмала отсутствуют. Поэтому крахмал не дает реакцию «серебряного зеркала».
Крахмал состоит не только из линейных молекул, но и из молекул разветвленной структуры. Этим объясняется зернистое строение крахмала.
В состав крахмала входят:
- амилоза (внутренняя часть крахмального зерна) — 10-20%;
- амилопектин (оболочка крахмального зерна) — 80-90%.
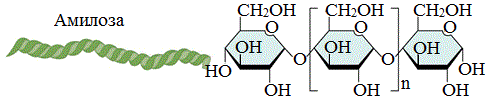
Амилоза
Амилоза растворима в воде и представляет собой линейный полимер, в котором остатки α–глюкозы связаны друг с другом через первый и четвертый атомы углерода (α-1,4-гликозидными связями).
Цепь амилозы включает 200 — 1000 остатков a-глюкозы (средняя мол. масса 160 000) .
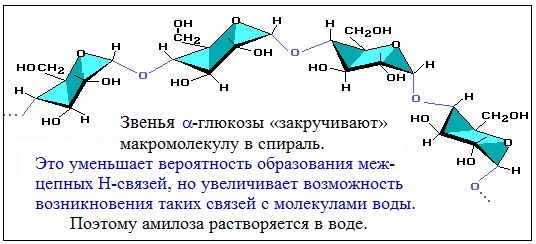
Макромолекула амилозы представляет собой спираль, каждый виток которой состоит из 6 звеньев a-глюкозы.
Амилопектин
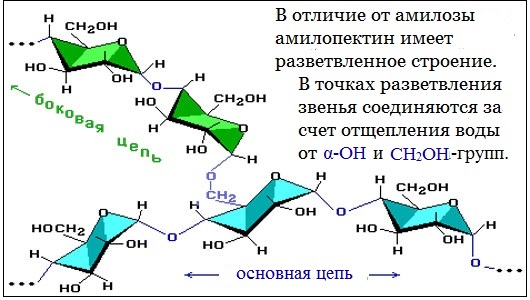
В отличие от амилозы, амилопектин не растворим в воде, и имеет разветвленное строение.
Подавляющее большинство глюкозных остатков в амилопектине связаны, как и в амилозе α-1,4-гликозидными связями. Однако в точках разветвлений цепи имеются α-1,6-гликозидные связи.
Молекулярная масса амилопектина достигает 1-6 млн.
Молекулы амилопектина также довольно компактны, так как имеют сферическую форму.
Биологическая роль крахмала. Гликоген
Крахмал – главное запасное питательное вещество растений, основной источник резервной энергии в растительных клетках.
Остатки глюкозы в молекулах крахмала соединены достаточно прочно и в то же время под действием ферментов легко могут отщепляться, как только возникает потребность в источнике энергии.
Амилоза и амилопектин гидролизуются под действием кислот или ферментов до глюкозы, которая служит непосредственным источником энергии для клеточных реакций, входит в состав крови и тканей, участвует в обменных процессах.
Гликоген (животный крахмал) – полисахарид, молекулы которого построены из большого числа остатков α–глюкозы. Он имеет сходное строение с амилопектином, но отличается от него большей разветвленностью цепей, а также большей молекулярной массой.
Содержится гликоген главным образом в печени и в мышцах.
Гликоген – белый аморфный порошок, хорошо растворяется даже в холодной воде, легко гидролизуется под действием кислот и ферментов, образуя в качестве промежуточных веществ декстрины, мальтозу и при полном гидролизе – глюкозу.
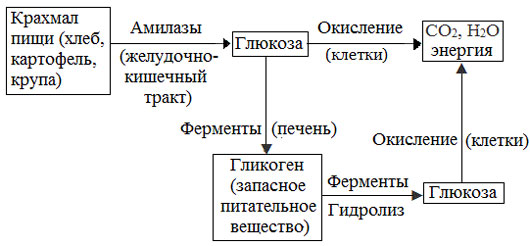
Превращение крахмала в организме человека и животных
Нахождение в природе
Крахмал широко распространен в природе. Он образуется в растениях в процессе фотосинтезе и накапливается в клубнях, корнях, семенах, а также в листьях и стеблях.
Крахмал содержится в растениях в виде крахмальных зерен. Наиболее богато крахмалом зерно злаков: риса (до 80%), пшеницы (до 70%), кукурузы (до 72%), а также клубни картофеля (до 25%). В клубнях картофеля крахмальные зерна плавают в клеточном соке, в злаках они плотно склеены белковым веществом клейковиной.
Физические свойства
Крахмал – белое аморфное вещество, без вкуса и запаха, нерастворимое в холодной воде, в горячей воде набухает и частично растворяется, образуя вязкий коллоидный раствор (крахмальный клейстер).
Крахмал существует в двух формах: амилоза – линейный полимер, растворимый в горячей воде, амилопектин – разветвлённый полимер, не растворимый в воде, лишь набухает.
Химические свойства крахмала
Химические свойства крахмала объясняются его строением.
Крахмал не дает реакцию «серебряного зеркала», однако ее дают продукты его гидролиза.
1. Гидролиз крахмала
При нагревании в кислой среде крахмал гидролизуется с разрывом связей между остатками α-глюкозы. При этом образуется ряд промежуточных продуктов, в частности мальтоза. Конечным продуктом гидролиза является глюкоза:
Процесс гидролиза протекает ступенчато, схематически его можно изобразить так:
Видеоопыт «Кислотный гидролиз крахмала»
Реакцию превращения крахмала в глюкозу при каталитическом действии серной кислоты открыл в 1811 г. русский ученый К.Кирхгоф (реакция Кирхгофа).
2. Качественная реакция на крахмал
Так как молекула амилозы представляет собой спираль, то при взаимодействии амилозы с йодом в водном растворе молекулы йода входят во внутренний канал спирали, образуя так называемое соединение включения.
Раствор иода окрашивает крахмал в синий цвет. При нагревании окрашивание исчезает (комплекс разрушается), при охлаждении появляется вновь.
Крахмал + J2 – синее окрашивание
Видеоопыт «Реакция крахмала с йодом»
Данная реакция используется в аналитических целях для обнаружения, как крахмала, так и йода (йодкрахмальная проба)
3. Большинство глюкозных остатков в молекулах крахмала имеют по 3 свободных гидроксила (у 2,3,6-го атомов углерода), в точках разветвления – у 2-го и 3-го атомов углерода.
Следовательно, для крахмала возможны реакции, характерные для многоатомных спиртов, в частности образование простых и сложных эфиров. Однако эфиры крахмала большого практического значения не имеют.
Качественную реакцию на многоатомные спирты крахмал не дает, так как плохо растворяется в воде.
Получение крахмала
Из растений извлекают крахмал, разрушая клетки и отмывая его водой. В промышленном масштабе его получают главным образом из клубней картофеля (в виде картофельной муки), а также кукурузы, в меньшей степени – из риса, пшеницы и других растений.
Получение крахмала из картофеля
Картофель моют, измельчают и промывают водой и перекачивают в большие сосуды, где происходит отстаивание. Вода извлекает из измельченного сырья крахмальные зерна, образуя так называемое «крахмальное молоко».
Полученный крахмал ещё раз промывают водой, отстаивают и сушат в струе теплого воздуха.
Получение крахмала из кукурузы
Зерна кукурузы замачивают в теплой воде разбавленной сернистой кислоты с целью размягчения зерна и удаления из него основной части растворимых веществ.
Набухшее зерно дробят для удаления ростков.
Ростки, после всплывания на поверхность воды, отделяют и используют в дальнейшем для получения кукурузного масла.
Кукурузную массу повторно измельчают, обрабатывают водой для вымывания крахмала, затем отделяют отстаиванием или с помощью центрифуги.
Применение крахмала
Крахмал широко применяется в различных отраслях промышленности (пищевой, фармацевтической, текстильной, бумажной и т.п.).
Он является основным углеводом пищи человека – хлеба, круп, картофеля.
В значительных количествах перерабатывается на декстрины, патоку и глюкозу, используемые в кондитерском производстве.
Из крахмала, содержащегося в картофеле и зерне злаков, получают этиловый, н-бутиловый спирты, ацетон, лимонную кислоту, глицерин.
Крахмал используется как клеящее средство, применяется для отделки тканей, крахмаления белья.
В медицине на основе крахмала готовятся мази, присыпки и т.д.
Химические свойства крахмала подтвердить уравнениями реакций
I. Фильм: “Полисахариды”
II. Физические свойства
Крахмал белый порошок, нерастворимый в холодной воде и образующий коллоидный раствор (крахмальный клейстер) в горячей воде. Существует в двух формах: амилоза – линейный полимер, растворимый в горячей воде, амилопектин – разветвлённый полимер, не растворимый в воде, лишь набухает.
III. Нахождение в природе
Крахмал – основной источник резервной энергии в растительных клетках – образуется в растениях в процессе фотосинтеза и накапливается в клубнях, корнях, семенах:
Содержится в клубнях картофеля, зёрнах пшеницы, риса, кукурузы.
Гликоген (животный крахмал), образуется в печени и мышцах животных.
IV. Строение
Состоит из остатков α — глюкозы.
В состав крахмала входят:
- амилоза (внутренняя часть крахмального зерна) – 10-20%
- амилопектин (оболочка крахмального зерна) – 80-90%
Цепь амилозы включает 200 – 1000 остатков α-глюкозы и имеет неразветвленное строение.
Амилопектин состоит из разветвленных макромолекул, молекулярная масса которых достигает 1 — 6 млн.
Амилоза и амилопектин гидролизуются под действием кислот или ферментов до глюкозы, которая служит непосредственным источником энергии для клеточных реакций, входит в состав крови и тканей, участвует в обменных процессах. Поэтому крахмал – необходимый резервный углевод питания.
Подобно амилопектину построен гликоген (животный крахмал), макромолекулы которого отличаются большей разветвлённостью:
V. Применение
Крахмал широко применяется в различных отраслях промышленности (пищевой, бродильной, фармацевтической, текстильной, бумажной и т.п.).
- Ценный питательный продукт.
- Для накрахмаливания белья.
- В качестве декстринового клея.
VI. Химические свойства полисахаридов
1. Гидролиз
Гидролиз протекает ступенчато:
Охлаждённый крахмальный клейстер + I2 (раствор) = синее окрашивание, которое исчезает при нагревании.
Макромолекула амилозы представляет собой спираль, каждый виток которой состоит из 6 звеньев α-глюкозы.
При взаимодействии амилозы с йодом в водном растворе молекулы йода входят во внутренний канал спирали, образуя так называемое соединение включения. Это соединение имеет характерный синий цвет. Данная реакция используется в аналитических целях для обнаружения, как крахмала, так и йода (йодкрахмальная проба)
Урок химии с ИКТ «Крахмал»
Разделы: Химия
Цели урока:
- изучение строения макромолекул крахмала, физических и химических свойств и применения крахмала;
- развитие практических навыков, умения сравнивать и выделять основные признаки в строении и свойствах;
- развитие познавательного интереса, коммуникативных качеств;
- воспитание положительного интереса, познавательности и культуры умственного труда.
Тип урока: Изучение нового материала.
Вид урока: Комбинированный урок.
Методы
- обучения: показательный, диалогический;
- преподавания: программируемый, объяснительный;
- учения: практический, частично-поисковый.
Оборудование урока: учебник «Органическая химия» под ред. И.И. Новошинского, видеопроектор, интерактивная доска, компьютер, мультимедийная программа, образец крахмала, вода, йод, пробирки, штативы для пробирок.
Ход урока
I. Организационная часть.
II. Проверка домашнего задания.
III. Изучение учебного материала по плану с использованием презентации.
План урока:
- Строение молекулы крахмала.
- Физические свойства.
- Нахождение в природе.
- Химические свойства.
- Крахмал как питательное вещество.
- Применение крахмала.
1. Строение макромолекул крахмала
(демонстрация слайда «Строение молекулы крахмала»)
Крахмал – это природный полимер, его молекулярная формула (C6 H10O5)п. Исследования показали, что крахмал представляет собой продукт, состоящий из двух полимерных веществ: растворимой в воде амилозы (20%) и нерастворимого в воде амилопектина (80%).
Крахмал образуется в результате фотосинтеза при поглощении энергии солнечного излучения.
Сначала синтезируется глюкоза:
Глюкоза далее превращается в крахмал:
Макромолекулы крахмала различны по размерам и по строению: число звеньев C6H10O5 в составе различно, поэтому неодинакова и их молекулярная масса. Ученым удалось доказать, что макромолекулы крахмала состоят из остатков молекул циклической α – глюкозы.
2. Физические свойства (демонстрация образца крахмала)
Крахмал – белый, нерастворимый в воде порошок, встречается в виде зерен, форма и размеры которых характерны для каждого рода растений. В холодной воде он набухает и образует гель. В горячей воде он образует коллоидный раствор – клейстер. Эти свойства крахмала определяют области его применения (демонстрация слайда «Физические свойства»).
3. Нахождение в природе.
Крахмал – одно из важнейших питательных веществ для человека. Крахмал чрезвычайно распространен в растительном мире. Для различных растений он является запасным питательным материалом и содержится главным образом в плодах, семенах и клубнях. Картофель содержит около 24% крахмала, зерна пшеницы и кукурузы – около 72-75%, риса – около 86% (демонстрация слайда «Нахождение в природе»).
4. Химические свойства.
а) Гидролиз крахмала
б) Качественная реакция крахмала с йодом
(лабораторный опыт или компьютерный эксперимент)
(демонстрация слайда « Химические свойства»).
5. Крахмал как питательное вещество (сообщения учащихся).
Для организма человека крахмал служит основным поставщиком углеводов – одного из важнейших компонентов пищи. Под действием ферментов крахмал гидролизуется до глюкозы, которая окисляется в клетках до углекислого газа и воды с выделением энергии, необходимой для функционирования живого организма. Из продуктов питания наибольшее количество крахмала содержится в хлебе, макаронных и других мучных изделиях, крупах, картофеле.
6. Применение крахмала (сообщения учащихся).
В значительных количествах крахмал перерабатывается на декстрины, патоку и глюкозу, используемые в пищевой промышленности. Из продуктов гидролиза получают пищевой спирт, молочную кислоту и другие ценные продукты. Крахмал используют как клеящее средство, применяют для отделки тканей, в медицине на основе крахмала готовят некоторые мази и присыпки.
IV. Закрепление изученного материала (демонстрация слайда «Вопросы»).
1. Составьте уравнения реакций получения молочной кислоты, исходя из крахмала:
Как называются реакции 1 и 2?
2. Сок зеленого яблока дает реакцию с йодом. Сок спелого яблока восстанавливает аммиачный раствор оксида серебра. Как объяснить эти явления?
3 Проверка знаний по тестам (Приложение 4)
V. Итог урока.
Домашнее задание: гл.6, §30 читать
Библиография использованных ресурсов:
- Угринович Н.Д. Информатика и информационные технологии. – М.: лаборатория базовых знаний, 2002.
- Киселев С.В., Куранов В.П. Оператор ЭВМ. – М.:ИПРО, Издательский цент «Академия», 2000.
- Учебное электронное издание» Химия» (8-11 класс) «Виртуальная лаборатория», лаборатория систем мультимедиа, МарГТУ, 2004.
- Мультимедийное учебное пособие нового образца, издательство «Просвещение», 2004.
- Новошинский И.И. Органическая химия. – Москва, Русское слово, 2009.