О чем эта статья:
11 класс, ЕГЭ/ОГЭ
- Определение гидролиза
- Условия гидролиза
- Индикаторы среды раствора
- Виды гидролиза
- Соль с сильным основанием и сильной кислотой
- Соль со слабым основанием и сильной кислотой
- Соль с сильным основанием и слабой кислотой
- Ступенчатый гидролиз
- Обратимый и необратимый гидролиз
- Степень гидролиза
- Вопросы для самопроверки:
- Растворы; электролитическая диссоциация; гидролиз солей
- Растворы; электролитическая диссоциация; гидролиз солей
- Учебные вопросы:
- 9.1. Растворы и их классификация
- 9.2. Физическая и химическая теория растворов; тепловые явления при растворении
- 9.3. Растворимость и ее зависимость от природы веществ
- Гидролиз солей
Определение гидролиза
| Гидролиз — это процесс взаимодействия сложного химического вещества с водой, итогом которого становится разложение молекул этого вещества. Сам термин происходит от двух греческих слов: hydor, что значит «вода», и lysis, то есть «распад». |
Гидролизации подвержены как органические, так и неорганические вещества: углеводы, белки, оксиды, карбиды, соли и т. д. Например, гидролиз органических соединений напрямую связан с пищеварением — с его помощью происходит распад и усвоение клетками организма жиров, белков, углеводов. Но сейчас мы займемся неорганической химией и рассмотрим гидролизацию на примере солей.
| Гидролиз солей — это реакция взаимодействия ионов соли с Н + и ОН − ионами воды, которая ведет к распаду исходного соединения. В результате такого ионного обмена образуется слабый электролит — кислотный, щелочной или нейтральный. |
Условия гидролиза
Далеко не все соединения распадаются, вступая в реакцию с молекулами воды. Сейчас мы на примере солей рассмотрим, какие вещества подвергаются гидролизу, а какие нет, и от чего это зависит.
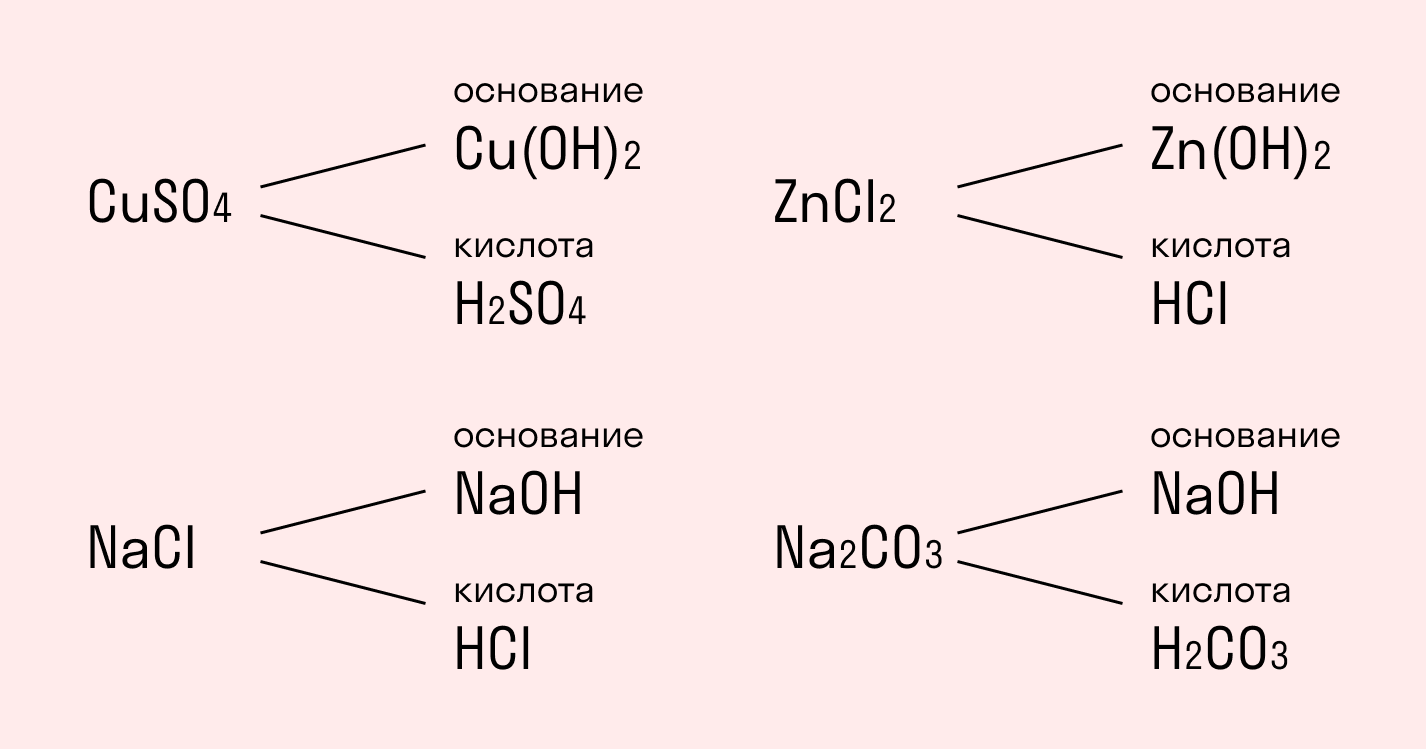
Начнем с того, что любая соль включает основание — амфотерный гидроксид, и кислотный остаток.
сульфат меди CuSO4состоит из основания Cu(ОН)2и кислоты H2SO4;
хлорид натрия NaCl состоит из основания NaOH и кислоты HCl;
хлорид цинка ZnCl2состоит из основания Zn(ОН)2 и кислоты HCI;
карбонат натрия Na2CO3состоит из основания NaOH и кислоты H2CO3.
В жизни первым разрушается самое слабое, и гидролиз в химии действует по тому же принципу. В ходе этой реакции распадаются более слабые соединения (основания или кислотные остатки). Слабый катион или слабый анион вступают во взаимодействие с ионами воды и связывают один из них или оба. В растворе образуется избыток ионов H + или гидроксильная группа OH − .
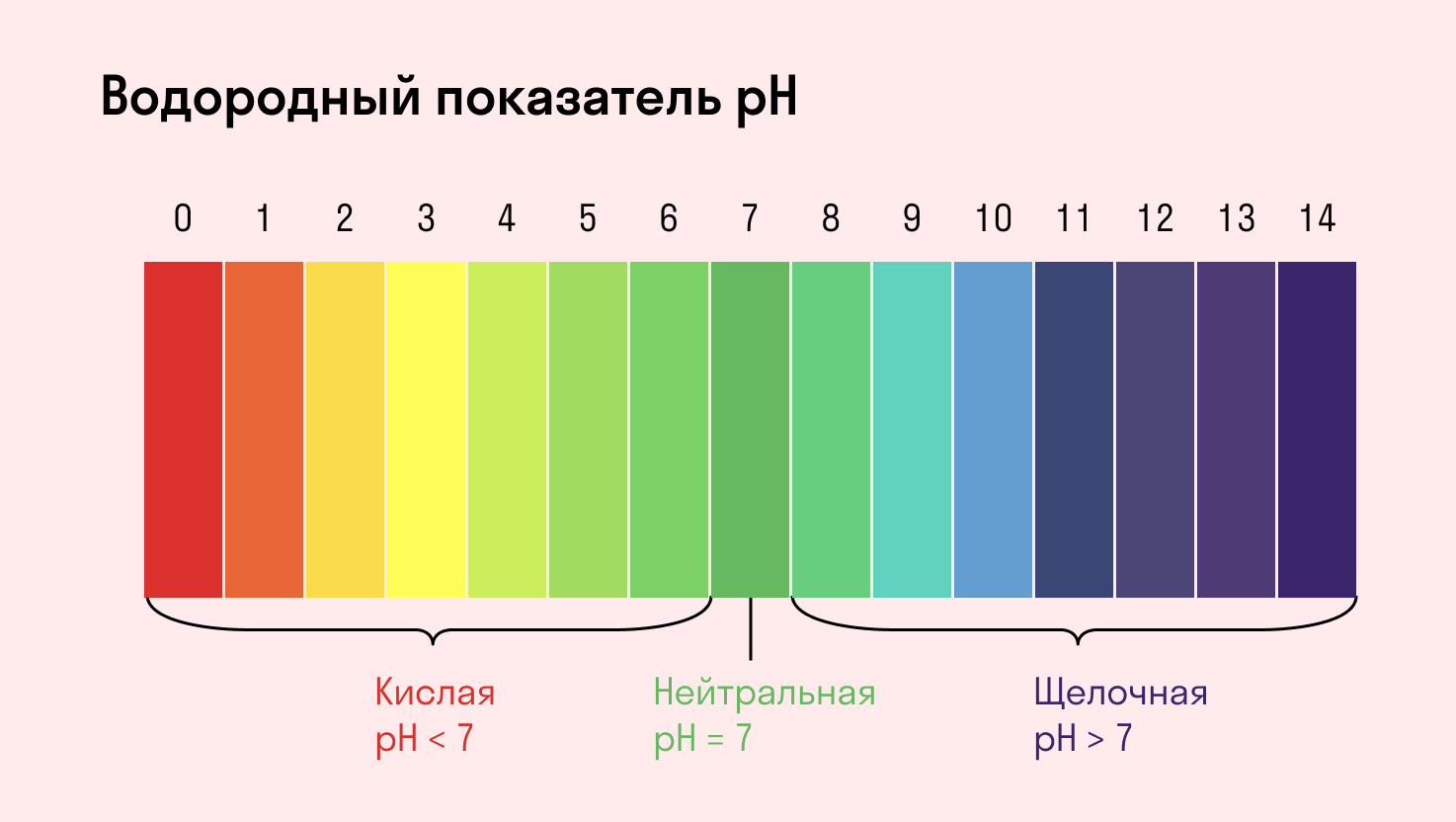
В зависимости от того, какие соли подвергаются гидролизу — со слабым основанием или слабой кислотой, в итоге может получиться кислая, щелочная или нейтральная среда водного раствора.
А что происходит, если соль состоит из сильного основания и сильного кислотного остатка? Ничего. 🙂 В этом случае ее сильные катионы и анионы не взаимодействуют с ионами воды. Такая соль не распадается, то есть не подвержена гидролизу.
Схема химической реакции гидролиза выглядит так:
XY + HOH ↔ XH + HOY
В данном случае:
XY — формула соли;
XH — кислотный остаток;
Индикаторы среды раствора
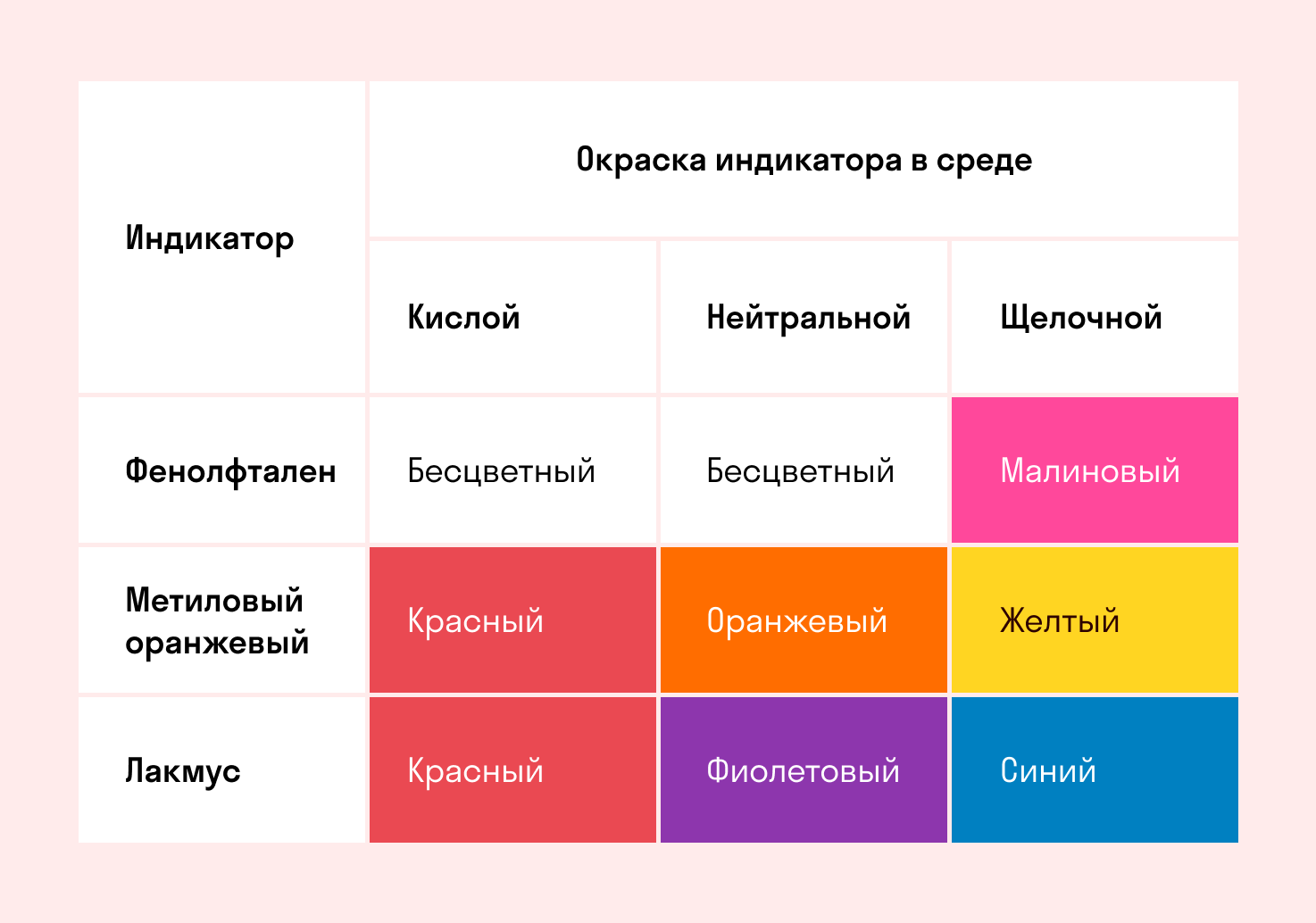
Для определения среды раствора за считанные секунды используются специальные индикаторы. Самый распространенный из них — лакмусовая бумага, но также популярны фенолфталеин и метиловый оранжевый. В нейтральной среде они не меняют свой цвет, а в кислотной или щелочной — приобретают другую окраску.
Изменение цвета индикатора однозначно говорит о том, что произошла гидролизация. Однако если цвет остался тем же — это не всегда означает отсутствие гидролиза. Среда будет почти нейтральной и в том случае, когда гидролизу подвергается соль со слабым основанием и слабой кислотой. Но об этом поговорим дальше, а пока посмотрите таблицу.
Виды гидролиза
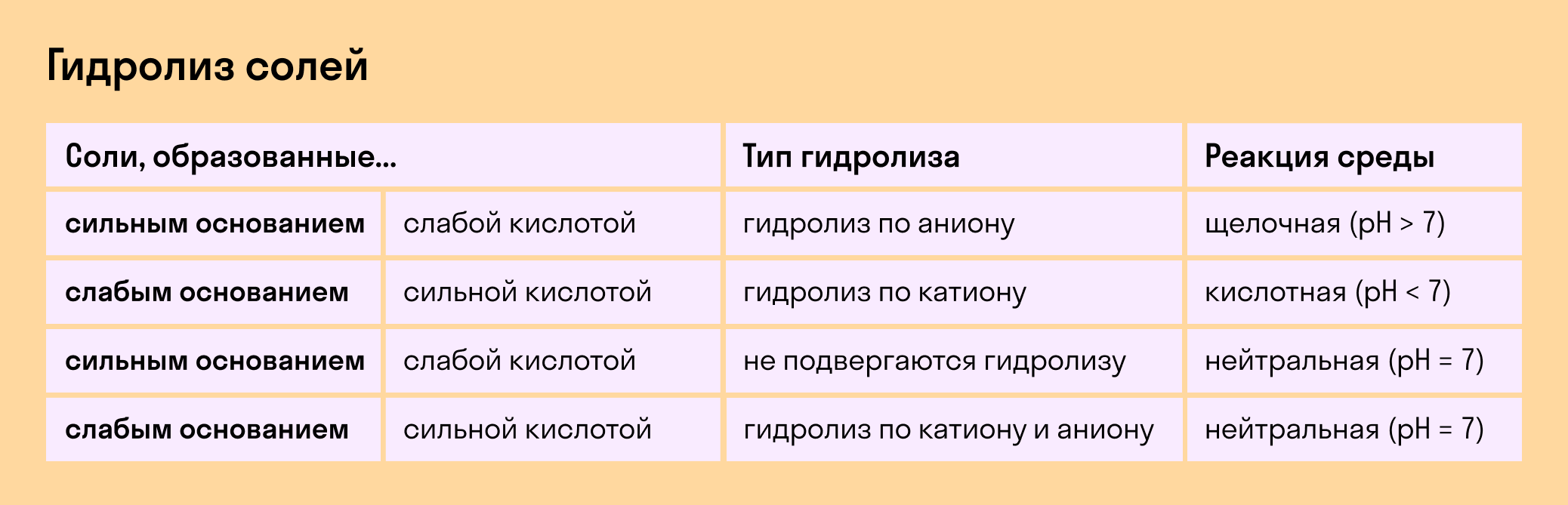
Мы выяснили, что в составе соли может быть слабый ион, который и отвечает за гидролизацию. Он находится в основании, в кислотном остатке или в обоих компонентах, и от этого зависит тип гидролиза.
Соль с сильным основанием и сильной кислотой
Гидролиз отсутствует. Как вы уже знаете, при наличии сильного основания и сильного кислотного остатка соль не распадается при взаимодействии с водой. Так, например, невозможен гидролиз хлорида натрия (NaCl), поскольку в составе этого вещества нет слабых ионов. К таким же не подверженным гидролизации солям относят KClO4, Ba(NO3)2 и т. д.
Среда водного раствора — нейтральная, т. е. pH = 7.
Реакция индикаторов: не меняют свой цвет (лакмус остается фиолетовым, а фенолфталеин — бесцветным).
Соль со слабым основанием и сильной кислотой
Гидролиз по катиону. Как мы помним, гидролизация происходит только при наличии слабого иона, в данном случае — иона основания. Его катион вступает в реакцию и связывает гидроксид-ионы воды OH − . В итоге образуется раствор с избытком ионов водорода H + .
Среда водного раствора — кислая, pH меньше 7.
Реакция индикаторов: фенолфталеин остается бесцветным, лакмус и метиловый оранжевый — краснеют.
Нитрат аммония NH4NO3 состоит из слабого основания NH4OH и сильного кислотного остатка HNO3, поэтому он гидролизуется по катиону, то есть его катион NH4 + связывает ионы воды OH − .
Соль с сильным основанием и слабой кислотой
Гидролиз по аниону. Если слабым оказывается ион кислотного остатка, его отрицательно заряженная частица (анион) взаимодействует с катионом водорода H + в молекуле воды. В итоге получается раствор с повышенным содержанием OH − .
Среда водного раствора — щелочная, pH больше 7.
Реакция индикаторов: фенолфталеин становится малиновым, лакмус — синим, а метиловый оранжевый желтеет.
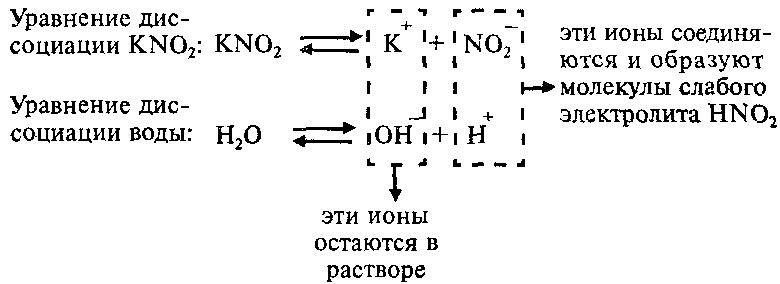
Нитрат калия KNO2 отличается сильным основанием KOH и слабым кислотным остатком HNO2, поэтому он гидролизуется по аниону. Другими словами, анион кислоты NO2 − связывает ионы воды H + .
Молекулярное уравнение: KNO2 + H2O ↔ HNO2 + KOH
Ионное уравнение: K + + NO2 − + HOH ↔ HNO2 + K + + OH −
Гидролиз по катиону и аниону. Если у соли оба компонента — слабые, при взаимодействии с водой в реакцию вступает и анион, и катион. При этом катион основания связывает ионы воды OH − а анион кислоты связывает ионы H +
Среда водного раствора: нейтральная, слабокислая или слабощелочная.
Реакция индикаторов: могут не изменить свой цвет.
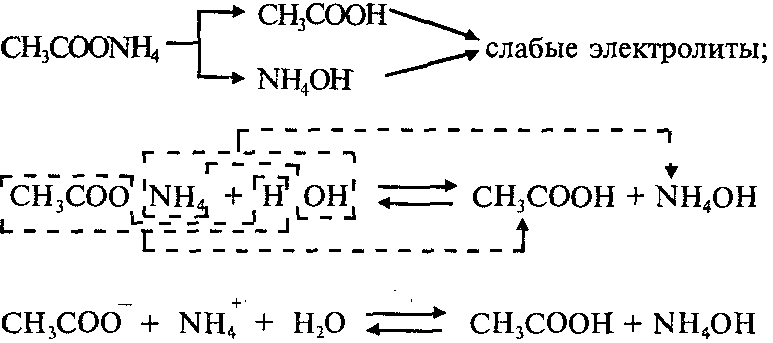
Цианид аммония NH4CN включает слабое основание NH4OH и слабую кислоту HCN.
Молекулярное уравнение: NH4CN + H2O ↔ NH4OH + HCN
Ионное уравнение: NH4 + + CN − + HOH ↔ NH4OH + HCN
Среда в данном случае будет слабощелочной.
Обобщим все эти сведения в таблице гидролиза солей.
Ступенчатый гидролиз
Любой из видов гидролиза может проходить ступенчато. Так бывает в тех случаях, когда с водой взаимодействует соль с многозарядными катионами и анионами. Сколько ступеней будет включать процесс — зависит от числового заряда иона, отвечающего за гидролиз.
Как определить количество ступеней:
если соль содержит слабую многоосновную кислоту — число ступеней равняется основности этой кислоты;
если соль содержит слабое многокислотное основание — число ступеней определяют по кислотности основания.
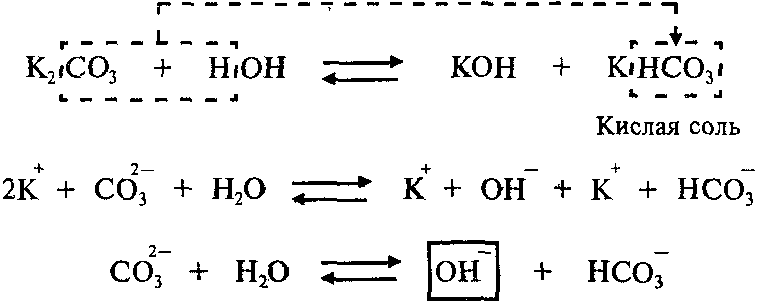
Для примера рассмотрим гидролиз карбоната калия K2CO3. У нас есть двухосновная слабая кислота H2CO3, а значит, гидролизация пройдет по аниону в две ступени.
I ступень: K2CO3+HOH ↔ KOH+KHCO3, итогом которой стало получение гидроксида калия (KOH) и кислой соли (KHCO3).
II ступень: K2HCO3+HOH ↔ KOH+H2CO3, в итоге получился тот же гидроксид калия (KOH) и слабая угольная кислота (H2CO3).
Для приблизительных расчетов обычно принимают в учет только результаты первой ступени.
Обратимый и необратимый гидролиз
Химические вещества могут гидролизоваться обратимо или необратимо. В первом случае распадается лишь некоторое количество частиц, а во втором — практически все. Если соль полностью разлагается водой, это необратимый процесс, и его называют полным гидролизом.
Необратимо гидролизуются соли, в составе которых есть слабые нерастворимые основания и слабые и/или летучие кислоты. Такие соединения могут существовать лишь в сухом виде, их не получить путем смешивания водных растворов других солей.
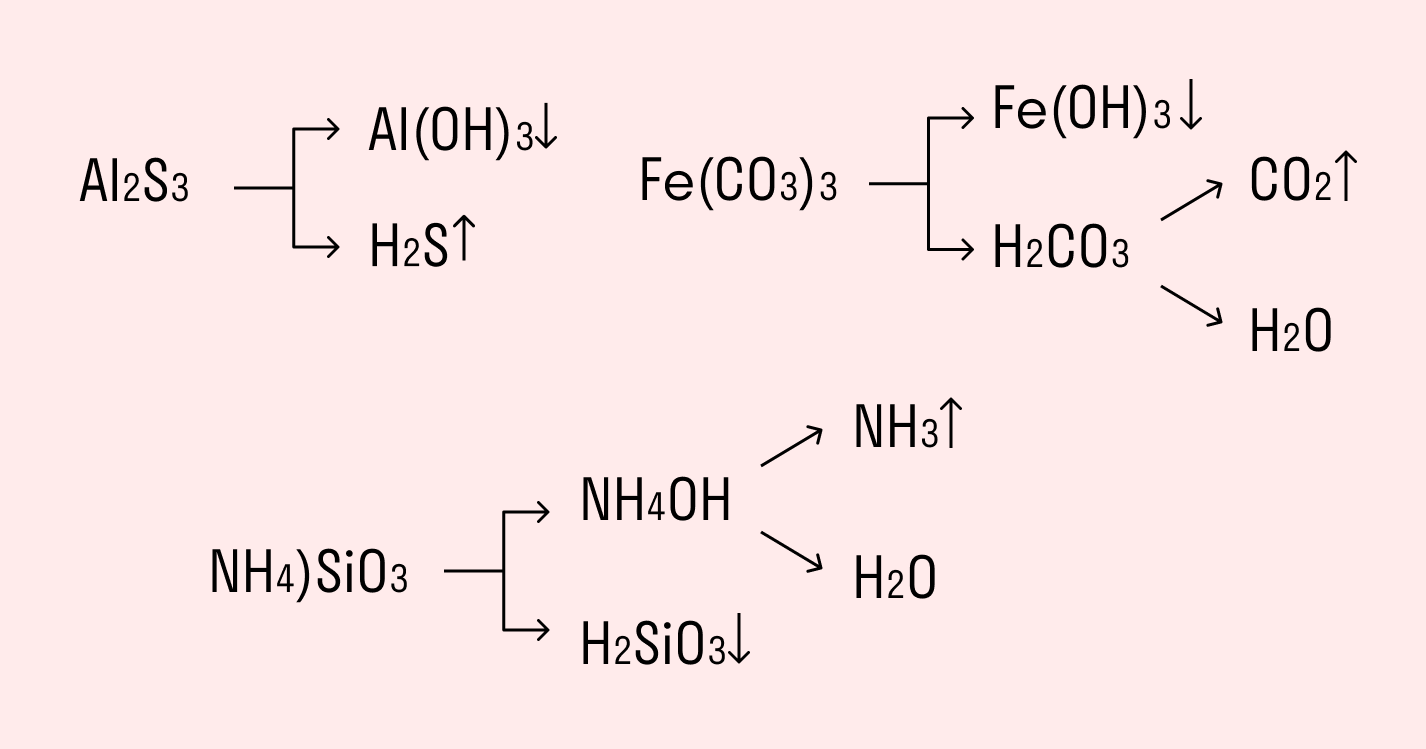
Например, полному гидролизу подвергается сульфид алюминия:
Как видите, в результате гидролизации образуется гидроксид алюминия и сероводород.
Необратимые реакции при взаимодействии с водой имеют место и в органической химии. В качестве примера рассмотрим полный гидролиз органического вещества — карбида кальция, в результате которого образуется ацетилен:
Степень гидролиза
Взаимодействие соли или другого химического соединения с водой может усиливаться или ослабляться в зависимости от нескольких факторов. Если нужно получить количественное выражение гидролиза, говорят о его степени, которая указывается в процентах.
h — степень гидролиза,
nгидр. — количество гидролизованного вещества,
nобщ. — общее количество растворенного в воде вещества.
На степень гидролизации может повлиять:
температура, при которой происходит процесс;
концентрация водного раствора;
состав участвующих в гидролизе веществ.
Можно усилить гидролиз с помощью воды (просто разбавить полученный раствор) или стимулировать процесс повышением температуры. Более сложным способом будет добавление в раствор такого вещества, которое могло бы связать один из продуктов гидролиза. К соли со слабой кислотой и сильным основанием нужно добавить соль со слабым основанием и сильной кислотой.
Для ослабления гидролиза раствор охлаждают и/или делают более концентрированным. Также можно изменить его состав: если гидролизация идет по катиону — добавляют кислоту, а если по аниону — щелочь.
Итак, мы разобрались, что такое гидролиз солей и каким он бывает. Пора проверить свои знания и ответить на вопросы по материалу.
Вопросы для самопроверки:
Назовите необходимое условие для гидролиза.
Какие типы гидролиза вы знаете?
В каком случае в результате гидролиза может образоваться слабощелочная или слабокислая среда?
По какому типу гидролизуется соль с сильным основанием и слабым кислотным остатком?
При гидролизе соли с сильным основанием и слабой кислотой для ослабления процесса нужно добавить в раствор кислоту или щелочь?
Как воздействует на гидролиз разбавление раствора водой?
Как определяется количество ступеней гидролиза?
Какая среда раствора образуется при гидролизации солей NaF, KCl, FeBr2, Na2PO4? Ответов может быть несколько.
Какие из солей гидролизуются по катиону: Csl, FeSO4, RbNO3, CuSO4, Mn(NO3)2? Ответов может быть несколько.
Какая из солей не подвергается гидролизу: K2HPO4, KNO3, KCN, Ni(NO3)2?
Растворы; электролитическая диссоциация; гидролиз солей
Электронное учебное пособие
Растворы; электролитическая диссоциация; гидролиз солей
В результате изучения данной темы вы узнаете:
В результате изучения данной темы вы научитесь:
Учебные вопросы:9.1. Растворы и их классификацияРастворами называют гомогенные системы, в которых одно вещество распределено в среде другого (других) веществ. Растворы состоят из растворителя и растворенного вещества (веществ). Эти понятия условны. Если одним из составляющих растворов веществ является жидкость, а другими — газы или твердые вещества, то растворителем обычно считают жидкость. В других случаях растворителем считают тот компонент, которого больше. Газообразные, жидкие и твердые растворы В зависимости от агрегатного состояния растворителя различают газообразные, жидкие и твердые растворы. Газообразным раствором является, например, воздух и другие смеси газов. Морская вода — наиболее распространенный жидкий раствор различных солей и газов в воде. К твердым растворам принадлежат многие металлические сплавы. Истинные и коллоидные растворы По степени дисперсности различают истинные и коллоидные растворы (коллоидные системы). При образовании истинных растворов растворенное вещество находится в растворителе в виде атомов, молекул или ионов. Размер частиц в таких растворах равен 10 –7 — 10 –8 см. Коллоидные растворы относятся к гетерогенным системам, в которых частицы одного вещества (дисперсная фаза) равномерно распределены в другом (дисперсионная среда). Размер частиц в дисперсных системах находится в пределах от 10 –7 см до 10 –3 и более см. Следует отметить, что здесь и далее везде мы будем рассматривать истинные растворы. Ненасыщенные, насыщенные и пересыщенные растворы Процесс растворения связан с диффузией, т. е. с самопроизвольным распределением частиц одного вещества между частицами другого. Так, процесс растворения твердых веществ, имеющих ионное строение, в жидкостях можно представить следующим образом: под влиянием растворителя разрушается кристаллическая решетка твердого вещества, а ионы распределяются равномерно по всему объему растворителя. Раствор останется ненасыщенным до тех пор, пока в него может переходить еще некоторое количество вещества. Раствор, в котором вещество при данной температуре больше не растворяется, т.е. раствор, находящийся в состоянии равновесия с твердой фазой растворяемого вещества, называется насыщенным. Растворимость данного вещества равна его концентрации в насыщенном растворе. При строго определенных условиях (температура, растворитель) растворимость есть величина постоянная. Если растворимость вещества увеличивается с ростом температуры, то охлаждая насыщенный при более высокой температуре раствор, можно получить пересыщенный раствор, т.е. такой раствор, концентрация вещества в котором выше концентрации насыщенного раствора (при данных температуре и давлении). Пересыщенные растворы очень неустойчивы. Легкое сотрясение сосуда или введение в раствор кристаллов вещества, находящегося в растворе, вызывает кристаллизацию избытка растворенного вещества, и раствор становится насыщенным. Разбавленные и концентрированные растворы Не следует путать ненасыщенный и насыщенный растворы с разбавленным и концентрированным. Понятия разбавленный и концентрированный растворы – относительные и между ними нельзя провести четкой границы. Они определяют соотношение между количествами растворенного вещества и растворителя. В общем случае, разбавленные растворы – это растворы, содержащие небольшие количества растворенного вещества по сравнению с количеством растворителя, концентрированные – с большим содержанием растворенного вещества. Например, если при 20 o С растворить в 100 г воды 25 г NaCl, то полученный раствор будет концентрированным, но ненасыщенным, поскольку растворимость хлорида натрия при 20 o С составляет 36 г в 100 г воды. Максимальная масса AgI, которая растворяется при 20 o С в 100 г Н2О равна 1,3·10 –7 г. Полученный при этих условиях раствор AgI будет насыщенным, но очень разбавленным. 9.2. Физическая и химическая теория растворов; тепловые явления при растворенииФизическая теория растворов была предложена В. Оствальдом (Германия) и С. Аррениусом (Швеция). Согласно этой теории частицы растворителя и растворенного вещества (молекулы, ионы) равномерно распределяются по всему объему раствора вследствие процессов диффузии. При этом между растворителем и растворенным веществом отсутствует химическое взаимодействие. Химическая теория была предложена Д.И. Менделеевым. Согласно представлениям Д.И. Менделеева между молекулами растворяемого вещества и растворителем происходит химическое взаимодействие с образованием неустойчивых, превращающихся друг в друга соединений растворенного вещества с растворителем – сольватов. Русские ученые И.А. Каблуков и В.А. Кистяковский объединили представления Оствальда, Аррениуса и Менделеева, заложив тем самым основу современной теории растворов. Согласно современной теории в растворе могут существовать не только частицы растворенного вещества и растворителя, но и продукты физико-химического взаимодействия растворенного вещества с растворителем – сольваты. Сольваты – это неустойчивые соединения переменного состава. Если растворителем является вода, их называют гидратами. Сольваты (гидраты) образуются за счет ион-дипольного, донорно-акцепторного взаимодействий, образования водородных связей и т.д. Например, при растворении NaCl в воде между ионами Na + , Cl – и молекулами растворителя возникает ион-дипольное взаимодействие. Образование гидратов аммиака при его растворении в воде происходит за счет образования водородных связей. Гидратная вода иногда настолько прочно связывается с растворенным веществом, что выделяется вместе с ним из раствора. Кристаллические вещества, содержащие молекулы воды, называются кристаллогидратами, а вода, входящая в состав таких кристаллов, называется кристаллизационной. Примерами кристаллогидратов является медный купорос CuSO4·5H2O, алюмокалиевые квасцы KAl(SO4)2·12H2O. Тепловые эффекты при растворении В результате изменения структуры веществ при переходе их из индивидуального состояния в раствор, а также в результате происходящих взаимодействий изменяются свойства системы. На это указывают, в частности, тепловые эффекты растворения. При растворении происходят два процесса: разрушение структуры растворяемого вещества и взаимодействие молекул растворенного вещества с молекулами растворителя. Взаимодействие растворенного вещества с растворителем называется сольватацией. На разрушение структуры растворяемого вещества затрачивается энергия, а взаимодействие частиц растворенного вещества с частицами растворителя (сольватация) – процесс экзотермический (идет с выделением теплоты). Таким образом, процесс растворения может быть экзотермическим или эндотермическим, в зависимости от соотношения этих тепловых эффектов. Например, при растворении серной кислоты наблюдается сильное разогревание раствора, т.е. выделение теплоты, а при растворении нитрата калия – сильное охлаждение раствора (эндотермический процесс) . 9.3. Растворимость и ее зависимость от природы веществРастворимость – наиболее изученное свойство растворов. Растворимость веществ в различных растворителях колеблется в широких пределах. В табл. 9.1 приведена растворимость некоторых веществ в воде, а в табл. 9.2 – растворимость йодида калия в различных растворителях. Таблица 9.1.Растворимость некоторых веществ в воде при 20 o С Гидролиз солейВодные растворы солей имеют разные значения рН и показывают различную реакцию среды — кислую, щелочную, нейтральную. Например, водный раствор хлорида алюминия AlCl3 имеет кислую среду (рН 7), растворы хлорида натрия NaCl и нитрита свинца Pb(NO2)2 — нейтральную среду (pН = 7). Эти соли не содержат в своем составе ионы водорода Н + или гидроксид-ионы ОН — , которые определяют среду раствора. Чем же можно объяснить различные среды водных растворов солей? Это объясняется тем, что в водных растворах соли подвергаются гидролизу. Слово «гидролиз» означает разложение водой («гидро» — вода, «лизис» — разложение). Гидролиз — одно из важнейших химических свойств солей. Гидролизом соли называется взаимодействие ионов соли с водой, в результате которого образуются слабые электролиты. Сущность гидролиза сводится к химическому взаимодействию катионов или анионов соли с гидроксид-ионами ОН — или ионами водорода Н + из молекул воды. В результате этого взаимодействия образуется малодиссоциирующее соединение (слабый электролит). Химическое равновесие процесса диссоциации воды смещается вправо. Поэтому в водном растворе соли появляется избыток свободных ионов Н + или ОН — , и раствор соли показывает кислую или щелочную среду. Гидролиз — процесс обратимый для большинства солей. В состоянии равновесия только небольшая часть ионов соли гидролизуется. Любую соль можно представить как продукт взаимодействия кислоты с основанием. Например, соль NaClO образована слабой кислотой HClO и сильным основанием NaOH. В зависимости от силы исходной кислоты и исходного основания соли можно разделить на 4 типа: Соли I, II, III типов подвергаются гидролизу, соли IV типа не подвергаются гидролизу Рассмотрим примеры гидролиза различных типов солей. I. Соли, образованные сильным основанием и слабой кислотой, подвергаются гидролизу по аниону. Эти соли образованы катионом сильного основания и анионом слабой кислоты, который связывает катион водорода Н + молекулы воды, образуя слабый электролит (кислоту). Пример: Составим молекулярное и ионные уравнения гидролиза нитрита калия KNO2. Соль KNO2 образована слабой одноосновной кислотой HNO2 и сильным основанием KОН, что можно изобразить схематически так: Напишем уравнение гидролиза соли KNO2: Каков механизм гидролиза этой соли? Так как ионы Н + соединяются в молекулы слабого электролита HNО2, их концентрация уменьшается и равновесие процесса диссоциации воды по принципу Ле-Шателье смещается вправо. В растворе увеличивается концентрация свободных гидроксид-ионов ОН — . Поэтому раствор соли KNO2 имеет щелочную реакцию (pН > 7). Вывод: Соли, образованные сильным основанием и слабой кислотой, при растворении в воде показывают щелочную реакцию среды, pН > 7. II. Соли, образованные слабым основанием и сильной кислотой, гидролизуются по катиону. Эти соли образованы катионом слабого основания и анионом сильной кислоты. Катион соли связывает гидроксид-ион ОН — воды, образуя слабый электролит (основание). Пример: Составим молекулярное и ионное уравнения гидролиза йодида аммония NH4I. Соль NH4I образована слабым однокислотным основанием NH4OH и сильной кислотой НI: При растворении в воде соли NH4I катионы аммония NH4 + связываются с гидроксид-ионами ОН — воды, образуя слабый электролит – гидроксид аммония NH4OH. В растворе появляется избыток ионов водорода Н + . Среда раствора соли NH4I – кислая, рН — из молекулы воды и образует слабое основание, и анионом слабой кислоты, который связывает ионы Н + из молекулы воды и образует слабую кислоту. Реакция растворов этих солей может быть нейтральной, слабокислой или слабощелочной. Это зависит от констант диссоциации слабой кислоты и слабого основания, которые образуются в результате гидролиза. Пример 1: Составим уравнения гидролиза ацетата аммония CH3COONH4. Эта соль образована слабой уксусной кислотой СН3СООН и слабым основанием NH4ОH: Реакция раствора соли CH3COONH4 – нейтральная (рН=7), потому что Kд(СН3СООН)=Kд(NH4ОH). Пример 2: Составим уравнения гидролиза цианида аммония NH4CN. Эта соль образована слабой кислотой HCN и слабым основанием NH4ОH: Реакция раствора соли NH4CN — слабощелочная (pН > 7), потому что Kд(NH4ОH)> Kд(HCN). Как уже было отмечено, для большинства солей гидролиз является обратимым процессом. В состоянии равновесия гидролизуется только небольшая часть соли. Однако некоторые соли полностью разлагаются водой, т. е. для них гидролиз является необратимым. Необратимому (полному) гидролизу подвергаются соли, которые образованы слабым нерастворимым или летучим основанием и слабой летучей или нерастворимой кислотой. Такие соли не могут существовать в водных растворах, К ним, например, относятся: Пример: Составим уравнение гидролиза сульфида алюминия Al2S3: Гидролиз сульфида алюминия протекает практически полностью до образования гидроксида алюминия Al(OH)3 и сероводорода H2S. Поэтому в результате обменных реакций между водными растворами некоторых солей не всегда образуются две новые соли. Одна из этих солей может подвергаться необратимому гидролизу с образованием соответствующего нерастворимого основания и слабой летучей (нераствориой) кислоты. Например: Суммируя эти уравнения, получаем: или в ионном виде: IV. Соли, образованные сильной кислотой и сильным основанием, не гидролизуются, потому что катионы и анионы этих солей не связываются с ионами Н + или ОН — воды, т. е. не образуют с ними молекул слабых электролитов. Равновесие диссоциации воды не смещается. Среда растворов этих солей — нейтральная (рН = 7,0), так как концентрации ионов Н + и ОН — в их растворах равны, как в чистой воде. Вывод: Соли, образованные сильной кислотой и сильным основанием, при растворении в воде гидролизу не подвергаются и показывают нейтральную реакцию среды (рН = 7,0). Ступенчатый гидролиз Гидролиз солей может протекать ступенчато. Рассмотрим случаи ступенчатого гидролиза. Если соль образована слабой многоосновной кислотой и сильным основанием, число ступеней гидролиза зависит от основности слабой кислоты. В водном растворе таких солей на первых ступенях гидролиза образуются кислая соль вместо кислоты и сильное основание. Ступенчато гидролизуюгся соли Na2SO3, Rb2CО3, K2SiO3, Li3PO4 и др. Пример: Составим молекулярное и ионное уравнения гидролиза карбоната калия K2СО3. Гидролиз соли K2СО3 протекает по аниону, потому что соль карбонат калия образована слабой кислотой Н2СО3 и сильным основанием KОН: Так как Н2СО3 – двухосновная кислота, гидролиз K2СО3 протекает по двум ступеням. Продуктами первой ступени гидролиза K2СО3 являются кислая соль KHCO3 и гидроксид калия KОН. Вторая ступень (гидролиз кислой соли, которая образовалась в результате первой ступени): Продуктами второй ступени гидролиза K2СО3 являются гидроксид калия и слабая угольная кислота Н2СО3. Гидролиз по второй ступени протекает в значительно меньшей степени, чем по первой ступени. Среда раствора соли K2СО3 — щелочная (рН > 7), потому что в растворе увеличивается концентрация ионов ОН — . Если соль образована слабым многокислотным основанием и сильной кислотой, то число ступеней гидролиза зависит от кислотности слабого основания. В водных растворах таких солей на первых ступенях образуется основная соль вместо основания и сильная кислота. Ступенчато гидролизуются соли MgSО4, CoI2, Al2(SO4)3, ZnBr2 и др. Пример: Составим молекулярное и ионное уравнения гидролиза хлорида никеля (II) NiCl2. Гидролиз соли NiCl2 протекает по катиону, так как соль образована слабым основанием Ni(OH)2 и сильной кислотой НСl. Катион Ni 2+ связывает гидроксид-ионы ОН — воды. Ni(OH)2 — двухкислотное основание, поэтому гидролиз протекает по двум ступеням. Продуктами первой ступени гидролиза NiCl2 являются основная соль NiOHCl и сильная кислота HCl. Вторая ступень (гидролиз основной соли, которая образовалась в результате первой ступени гидролиза): Продуктами второй ступени гидролиза являются слабое основание гидроксид никеля (II) и сильная хлороводородная кислота НCl. Однако степень гидролиза по второй ступени намного меньше, чем по первой ступени. Среда раствора NiCl2 — кислая, рН + . Гидролизу подвергаются не только соли, но и другие неорганические соединения. Гидролизуются также жиры, углеводы, белки и другие вещества, свойства которых изучаются в курсе органической химии. Поэтому можно дать более общее определение процесса гидролиза: Гидролиз — это реакция обменного разложения веществ водой. |