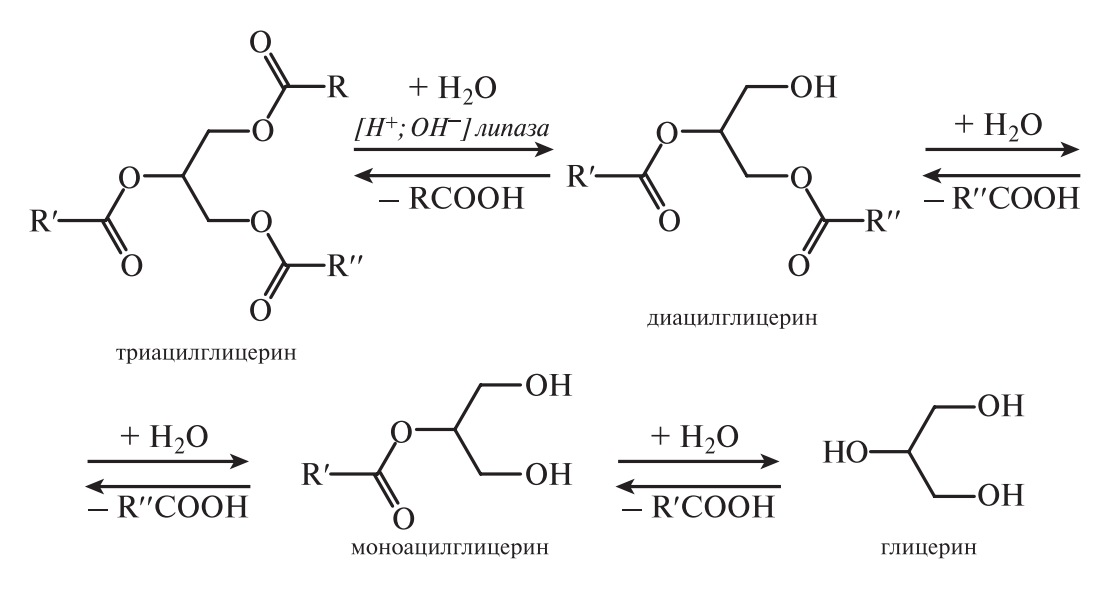
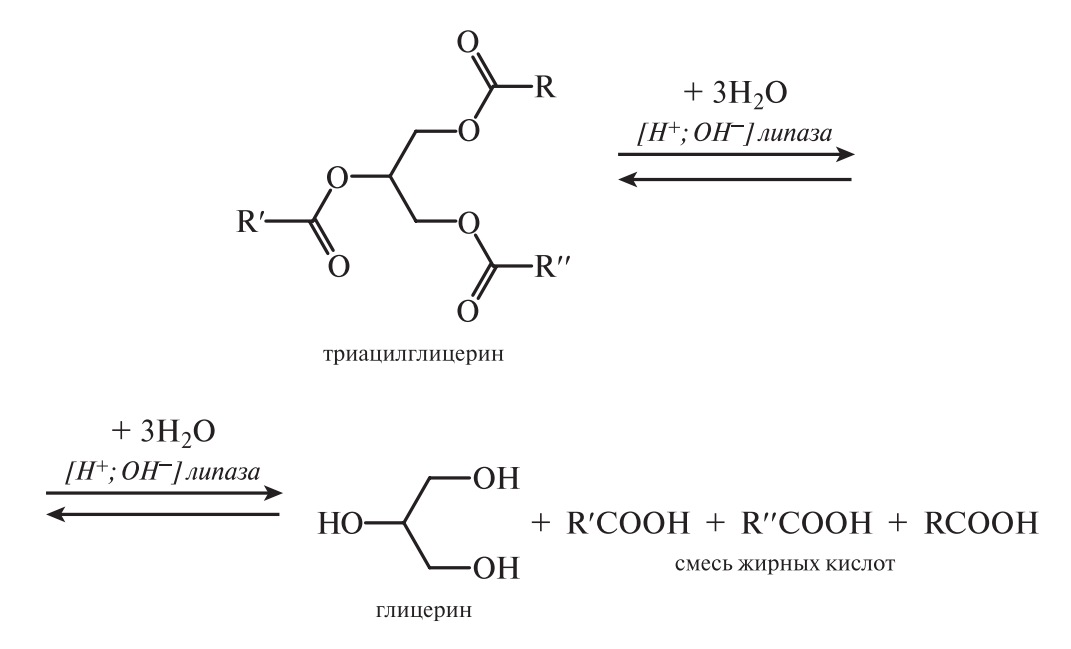
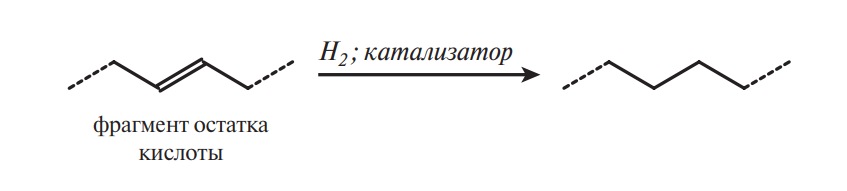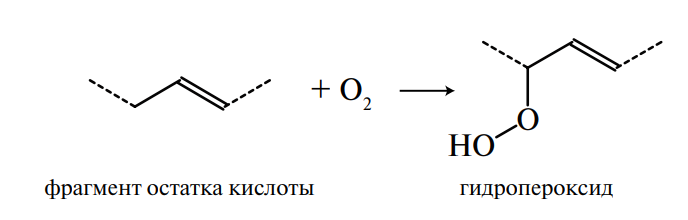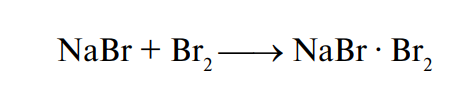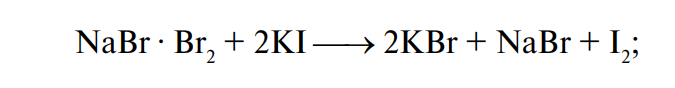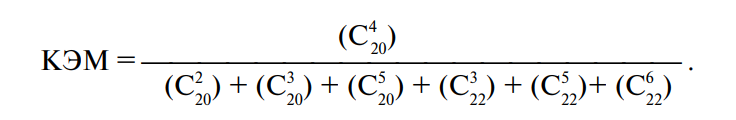Под влиянием щелочей, кислот, фермента липазы триацилглицерины гидролизуются с образованием ди-, затем моноацилглицеринов и, в конечном счете, жирных кислот и глицерина.
В присутствии кислотных катализаторов (сульфокислоты, H2SO4) процесс ведут при 100°С в избытке воды. В отсутствие катализаторов расщепление проводят при температуре 220—225°С под давлением 2—2,5 МПа («безреактивное» расщепление). Гидролиз концентрированными водными растворами гидроксида натрия (омыление) является основой процесса получения («варки») мыла. На скорость гидролиза ацилглицерина влияют строение и положение ацилов, температура, катализаторы. С ростом длины углеродной цепи, увеличением ненасыщенности (при той же длине углеродной цепи) ацилов скорость гидролиза снижается.
Гидролиз триацилглицеринов широко применяется в технике для получения жирных кислот, глицерина, моно- и диацилглицеринов.
Гидролитический распад жиров, липидов зерна, муки, крупы и других жиросодержащих пищевых продуктов является одной из причин ухудшения их качества, в конечном счете — порчи. Особенно ускоряется этот процесс при повышении влажности хранящихся продуктов, температуры, активности липазы. Скорость и глубину гидролиза масел и жиров (в том числе содержащихся в пищевом сырье и в готовых продуктах) можно охарактеризовать с помощью кислотного числа. Кислотное число — это количество миллиграммов едкого калия, необходимое для нейтрализации свободных жирных кислот, содержащихся в 1 г масла или жира. Кислотное число для ряда пищевых продуктов нормируется стандартами и является одним из показателей, характеризующих их качество.
- ГЛИЦЕРИДЫ (АЦИЛГЛИЦЕРОЛЫ)
- Гидролиз ацилглицеринов полное и суммарное уравнение реакции условия особенности
- Жиры и масла (Липиды). Состав, свойства, выделение и пищевая ценность жиров и масел
- 1. Состав и строение липидов. Жирно-кислотный состав масел и жиров
- 2. Реакции ацилглицеринов с участием сложноэфирных групп
- 2.1. Гидролиз триацилглицеринов
- 2.2. Переэтерификация
- 3. Реакции ацилглицеринов с участием углеводородных радикалов
- 3.1. Присоединение водорода (гидрирование ацилглицеринов)
- 3.2. Окисление ацилглицеринов
- 4. Свойства и превращения глицерофосфолипидов
- 5. Методы выделения липидов из сырья и пищевых продуктов и их анализ
- 6. Пищевая ценность масел и жиров
- 7. Превращения липидов при производстве продуктов питания
ГЛИЦЕРИДЫ (АЦИЛГЛИЦЕРОЛЫ)
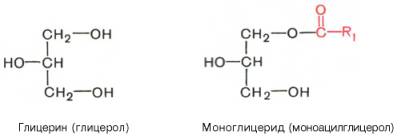
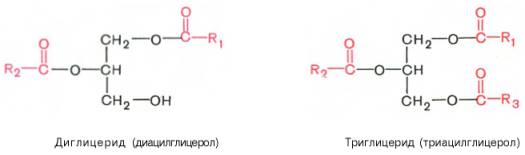
Глицериды (ацилглицерины, или ацилглицеролы ) представляют собой сложные эфиры трехатомного спирта глицерина и высших жирных кислот. Если жирными кислотами этерифицированы все три гидроксильные группы глицерина (ацильные радикалы R1, R2и R3могут быть одинаковы или различны), то такое соединение называют триглицеридом (триацилглице-рол), если две – диглицеридом (диацилглицерол) и, наконец, если этери-фицирована одна группа – моноглицеридом (моноацилглицерол):
Наиболее распространенными являются триглицериды, часто называемые нейтральными жирами или просто жирами. Нейтральные жиры находятся в организме либо в форме протоплазматического жира, являющегося структурным компонентом клеток, либо в форме запасного, резервного, жира. Роль этих двух форм жира в организме неодинакова. Протоплазматический жир имеет постоянный химический состав и содержится в тканях в определенном количестве, не изменяющемся даже при патологическом ожирении, в то время как количество резервного жира подвергается большим колебаниям.
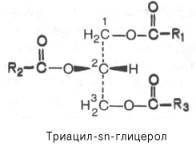
Как отмечалось, основную массу природных нейтральных жиров составляют триглицериды. Жирные кислоты в триглицеридах могут быть насыщенными и ненасыщенными. Из жирных кислот чаще встречаются пальмитиновая, стеариновая и олеиновые кислоты. Если все три кислотных радикала принадлежат одной и той же жирной кислоте, то такие три-глицериды называют простыми (например, трипальмитин, тристеарин, триолеин и т.д.), если разным жирным кислотам, то смешанными. Названия смешанных триглицеридов образуются в зависимости от входящих в их состав жирных кислот, при этом цифры 1, 2 и 3 указывают на связь остатка жирной кислоты с соответствующей спиртовой группой в молекуле глицерина (например, 1-олео-2-пальмитостеарин). Необходимо отметить, что положение крайних атомов в молекуле глицерина на первый взгляд равнозначно, тем не менее их обозначают сверху вниз – 1 и 3. Это объясняется прежде всего тем, что в структуре триглицерида при пространственном ее рассмотрении крайние «глицериновые» атомы углерода становятся уже не равнозначными, если гидроксилы 1 и 3 ацилированы разными жирными кислотами. При необходимости применяют также систему стереохими-ческой нумерации (обозначают sn – stereochemical n u m b e r i n g ) : например, 1,2-дистеарил-3-пальмитил-sn-глицерол:
По этой системе, если в проекции Фишера гидроксильная группа при 2-м углеродном атоме глицерина располагается слева, атому углерода, находящемуся над ним, присваивается номер 1, а расположенному под ним – номер 3.
Действительно, углероды 1 и 3 глицерола, учитывая их пространственное расположение, неидентичны. Особенно четко это видно на примере молекулы триглицерида. Ферменты это различают и всегда специфичны только к одному из трех углеродов глицерина. Так, глицеролкиназа фосфорилирует глицерин в положении sn-3, в результате чего образуется глицерол-3-фосфат, но не глицерол-1-фосфат.
Жирные кислоты, входящие в состав триглицеридов, практически определяют их физико-химические свойства. Так, температура плавления триглицеридов повышается с увеличением числа и длины остатков насыщенных жирных кислот. Напротив, чем выше содержание ненасыщенных жирных кислот, или кислот с короткой цепью, тем ниже точка плавления.
Животные жиры (сало) обычно содержат значительное количество насыщенных жирных кислот (пальмитиновой, стеариновой и др.). благодаря чему при комнатной температуре они твердые. Жиры, в состав которых входит много ненасыщенных кислот, при обычной температуре жидкие и называются маслами. Так, в конопляном масле 95% всех жирных кислот приходится на долю олеиновой, линолевой и линоленовой кислот и только 5% – на долю стеариновой и пальмитиновой кислот. В жире человека, плавящемся при температуре 15°С (при температуре тела он жидкий), содержится 70% олеиновой кислоты.
Глицериды способны вступать во все химические реакции, свойственные сложным эфирам. Наибольшее значение имеет реакция омыления, в результате которой из триглицеридов образуются глицерол и жирные кислоты. Омыление жира может происходить как при ферментативном гидролизе, так и при действии кислот или щелочей.
Гидролиз ацилглицеринов полное и суммарное уравнение реакции условия особенности
Жиры и масла (Липиды). Состав, свойства, выделение и пищевая ценность жиров и масел
- Опубликовано: 18 ноября, 2020
1. Состав и строение липидов. Жирно-кислотный состав масел и жиров
Липидами (от греч. lipos жир) называют сложную смесь жироподобных органических соединений с близкими физико-химическими свойствами, которая содержится в клетках растений, животных и микроорганизмах. Липиды широко распространены в природе и вместе с белками и углеводами составляют основную массу органических веществ всех живых организмов, являясь обязательным компонентом каждой клетки. Они широко используются при получении многих продуктов питания, являются важными компонентами пищевого сырья, полупродуктов и готовых пищевых продуктов, во многом определяя их пищевую и биологическую полноценность и вкусовые качества.
Липиды нерастворимы в воде (гидрофобны*), хорошо растворимы в органических растворителях (бензине, диэтиловом эфире, хлороформе и др.). В растениях липиды накапливаются главным образом в семенах и плодах.
* Гидрофобность — «боязнь воды», вещества не взаимодействуют с водой.
Ниже приведено содержание липидов (в %) в разных культурах:
- Подсолнечник (семянка) 30–58
- Хлопчатник (семена) 20–29
- Соя (семена) 15–25
- Лен (семена) 30–48
- Арахис (ядро) 50–61
- Маслины (мякоть) 28–50
- Kонопля (семена) 32–38
- Тунг (ядро плода) 48–66
- Рапс (семена) 45–48
- Горчица (семена) 25–49
- Kлещевина (семена) 35–59
- Пшеница (зерновка) 2,7
- Рожь (зерновка) 2,5
- Kукуруза (зерновка) 5,6
- Рис (зерновка) 2,9
- Овес (зерновка) 7,2
- Просо (зерновка) 4,5
- Гречиха 3,8
- Арбуз (семена) 14–45
- Kакао (бобы) 49–57
- Kокосовая пальма (копра) 65–72
- Kедр (ядро ореха) 26–28
У животных и рыб липиды концентрируются в подкожных, мозговой и нервной тканях и тканях, окружающих важные органы (сердце, почки). Содержание липидов в тушке осетров может достигать 20–25 %, сельди — 10 %; у туш наземных животных оно сильно колеблется: 33 % — свинина, 9,8 % — говядина, 3,0 % — поросята. В молоке оленя — 17–18 %, козы — 5,0 %, коровы — 3,5–4,0 % липидов. Содержание липидов в отдельных видах микроорганизмов может достигать 60 %. Содержание липидов в растениях зависит от сорта, места и условий их произрастания, а у животных — от вида, состава корма, условий содержания и т. д.
По химическому строению липиды являются производными жирных кислот, спиртов, альдегидов, построенных с помощью сложноэфирной, простой эфирной, фосфоэфирной, гликозидной связей. Липиды делят на две основные группы: простые и сложные липиды. К простым нейтральным липидам (не содержащим атомов азота, фосфора, серы) относят производные высших жирных кислот и спиртов: глицеролипиды, воски, эфиры холестерина, гликолипиды и другие соединения. Существуют и другие классификации липидов. По мнению отдельных авторов, в эту группу органических соединений следует включить изопреноиды (терпены и их производные) и стероиды. Молекулы сложных липидов содержат в своем составе не только остатки высокомолекулярных карбоновых кислот, но и фосфорную или серную кислоты.
По строению и способности к гидролизу липиды разделяют на омыляемые и неомыляемые. Омыляемые липиды при гидролизе образуют несколько структурных компонентов, а при взаимодействии со щелочами — соли жирных кислот (мыла).
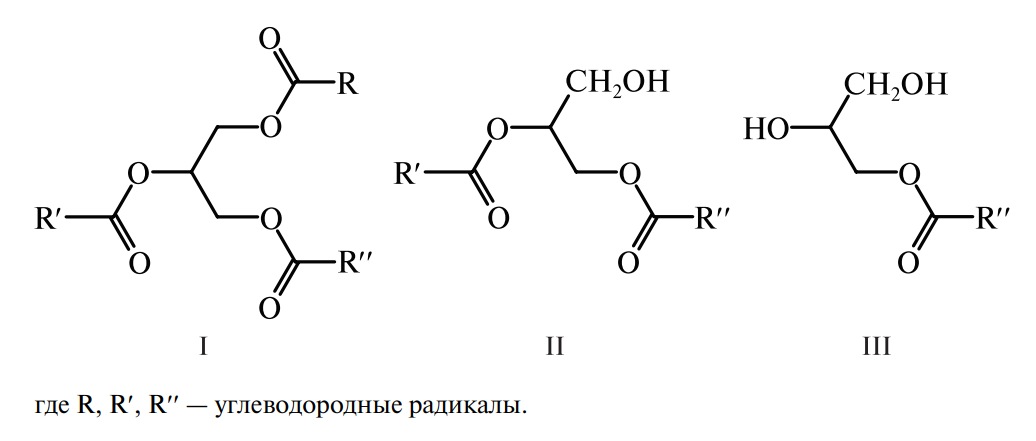
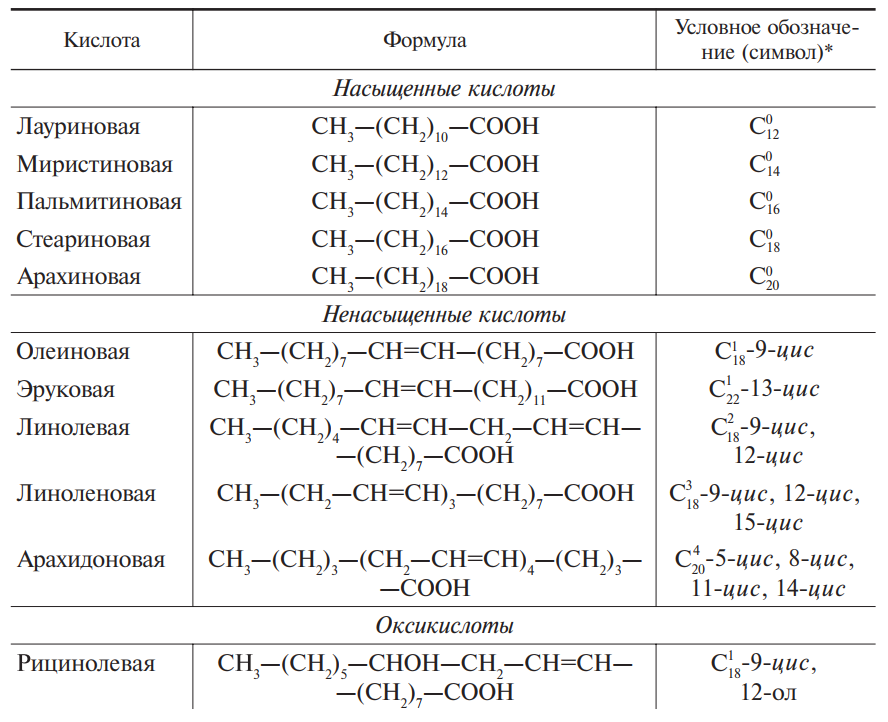
Наиболее важная и распространенная группа простых нейтральных липидов — ацилглицерины. Ацилглицерины (или глицериды) — это сложные эфиры глицерина и высших карбоновых кислот (табл. 1). Они составляют основную массу липидов (иногда до 95 %) и, по существу, именно их называют жирами, или маслами. В состав жиров входят главным образом триацилглицерины (I), а также диацилглицерины (II) и моноацилглицерины (III):
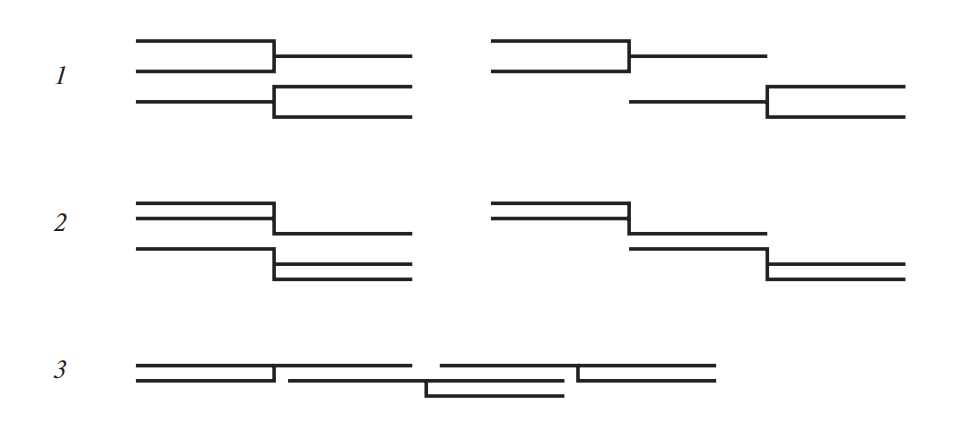
Триацилглицерины (ТАГ), молекулы которых содержат одинаковые остатки жирных кислот (ЖК), называются простыми, в противном случае — смешанными. Природные жиры и масла содержат главным образом смешанные триацилглицерины. Чистые ацилглицерины — бесцветные вещества без вкуса и запаха. Окраска, запах и вкус природных жиров определяются наличием в них специфических примесей, характерных для каждого вида жира. Температуры плавления и застывания ацилглицеринов не совпадают, что обусловлено наличием нескольких кристаллических модификаций. По современным представлениям, молекулы триацилглицеринов в кристаллах в зависимости от ориентации кислотных групп могут иметь форму вилки 1, кресла 2, стержня 3 (рис. 1).
Температура плавления триацилглицеринов, содержащих остатки транс-ненасыщенных кислот, выше, чем у ацилглицеринов, содержащих остатки цис-ненасыщенных кислот с тем же числом атомов углерода. Каждое масло характеризуется специфическим коэффициентом преломления (тем больше, чем выше ненасыщенность жирных кислот, входящих в его состав, и молекулярная масса).
Смеси индивидуальных ацилглицеринов либо образуют твердые растворы (то есть смешанные кристаллы), либо дают эвтектику (механические смеси кристаллов). Эвтектическая смесь имеет температуру плавления более низкую, чем исходные компоненты по отдельности.
Таблица 1. Основные карбоновые кислоты, входящие в состав природных масел и жиров
* В символ входят число атомов углерода и количество двойных связей между углеродными атомами в молекуле кислоты, номер первого ненасыщенного атома углерода, конфигурация.
Рис. 1. Возможные конфигурации и характер упаковки молекул триацилглицеринов в кристаллах
Разница в температурах плавления глицеридов разного состава лежит в основе демаргаринизации — выделения из смеси наиболее высокоплавкой фракции глицеридов (получение хлопкового пальмитина, пальмового стеарина). Плотность триацилглицеринов 900–960 кг/м3 (при 15 °С); она уменьшается с ростом длины цепи жирно-кислотных остатков и возрастает с увеличением числа изолированных двойных связей.
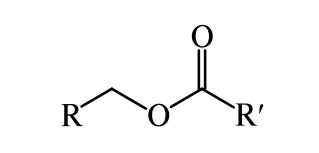
Другой важной группой простых липидов (ПЛ) являются воски. Восками называют сложные эфиры высших одноосновных карбоновых кислот (С 0 18 –С 0 30) и одноатомных (содержащих одну группу ОН) высокомолекулярных (с 18–30 атомами углерода) спиртов:
где R, R′ — углеводородные радикалы.
Воски широко распространены в природе. В растениях они покрывают тонким слоем листья, стебли, плоды, предохраняя их от смачивания водой, высыхания, действия микроорганизмов. Содержание восков в зерне и плодах невелико. В оболочках семян подсолнечника содержится до 0,2 % восков от массы оболочки, в семенах сои — 0,01 %, риса — 0,05 %. Воски — важный компонент воскового налета виноградной ягоды — прюина.
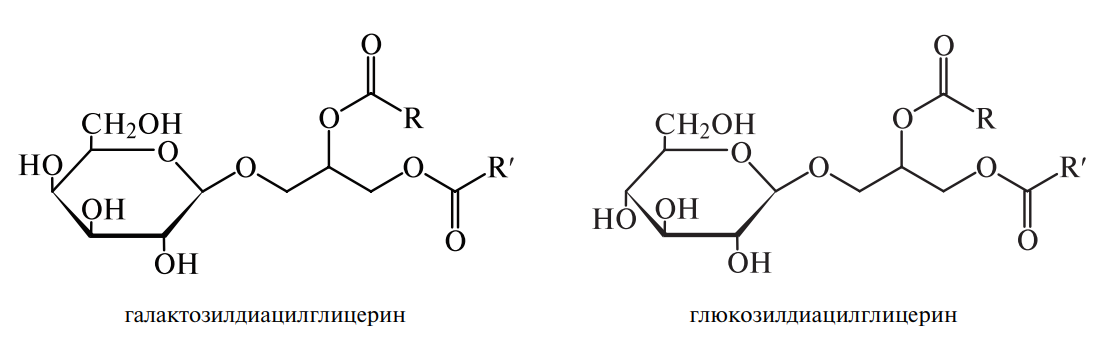
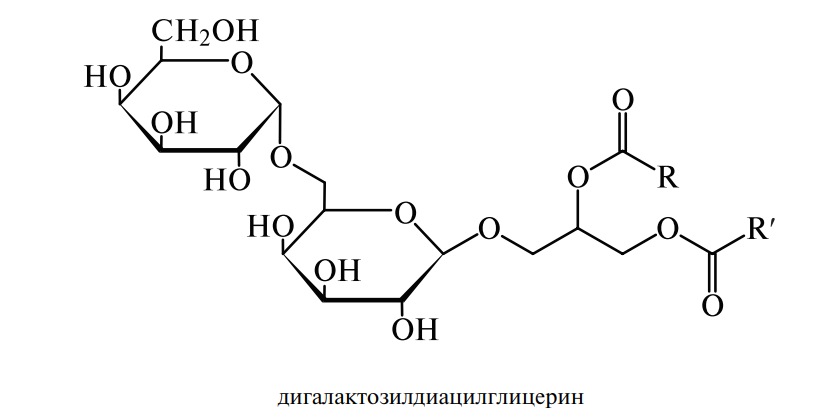
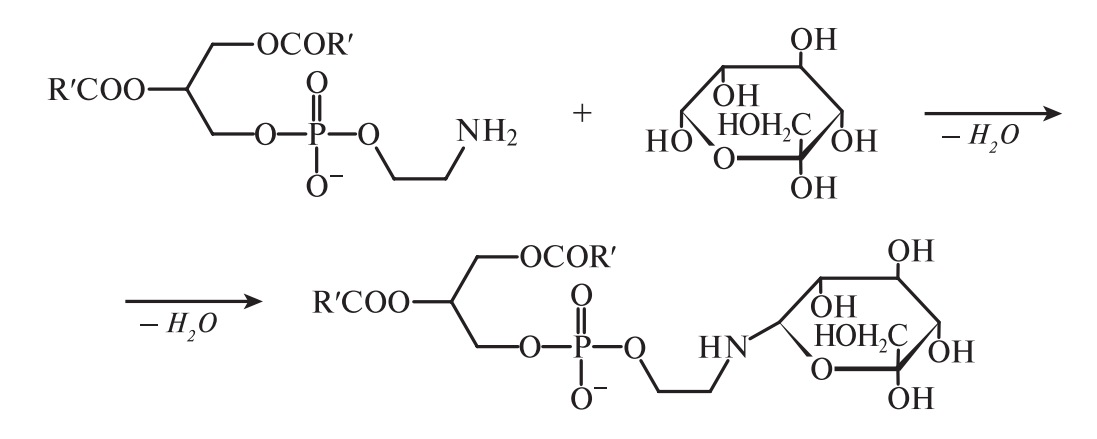
В состав сложных липидов растительных масел и жиров входят гликолипиды. Гликолипидами называется большая и разнообразная по строению группа нейтральных липидов, содержащих остатки моноз. Они широко (обычно в небольших количествах) содержатся в растениях (липиды пшеницы, овса, кукурузы, подсолнечника), животных и микроорганизмах. Гликолипиды выполняют структурные функции, участвуют в построении мембран, им принадлежит важная роль в формировании клейковинных белков пшеницы, определяющих хлебопекарное достоинство муки. Чаще всего в построении молекул гликолипидов участвуют D-галактоза, D-глюкоза, D-манноза.
где R, R′ — углеводородные радикалы.
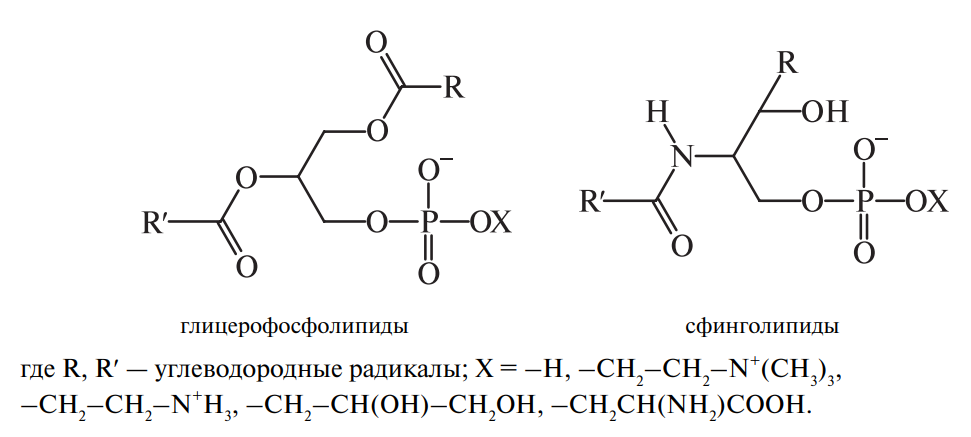
Важнейшими представителями сложных липидов являются фосфолипиды. Молекулы фосфолипидов построены из остатков спиртов (глицерина, сфингозина), жирных кислот, фосфорной кислоты (Н3РО4), а также содержат азотистые основания (чаще всего холин [НО-СН2-СН2-(СН3)3N+]ОН–или этаноламин HO-CH2-CH2-NH2 ), остатки аминокислот и некоторых других соединений. Общие формулы фосфолипидов, содержащих остатки глицерина и сфингозина, имеют следующий вид:
В молекуле фосфолипидов имеются заместители двух типов: гидрофильные и гидрофобные. В качестве гидрофильных (полярных) группировок выступают остатки фосфорной кислоты и азотистого основания («голова»), а гидрофобных (неполярных) — углеводородные радикалы («хвосты»). Пространственная структура фосфолипидов представлена на рис. 2. Фосфолипиды (фосфатиды) — обязательные компоненты растений.
Ниже приведено содержание фосфолипидов в различных культурах (в %):
- Соя 1,8
- Хлопчатник 1,7
- Подсолнечник 1,7
- Kлещевина 0,3
- Лен 0,6
- Пшеница 0,54
- Рожь 0,6
- Kукуруза 0,9
Состав жирных кислот фосфолипидов и ацилглицеринов, выделенных из одного и того же сырья, неидентичен. Так, в высокоэруковых сортах рапсового масла содержится около 60 % эруковой кислоты, в фосфолипидах — 11–12 %. Подавляющее большинство фосфолипидов имеет в своем составе остатки одной насыщенной (обычно в положении 1) и одной ненасыщенной (в положении 2) кислоты.
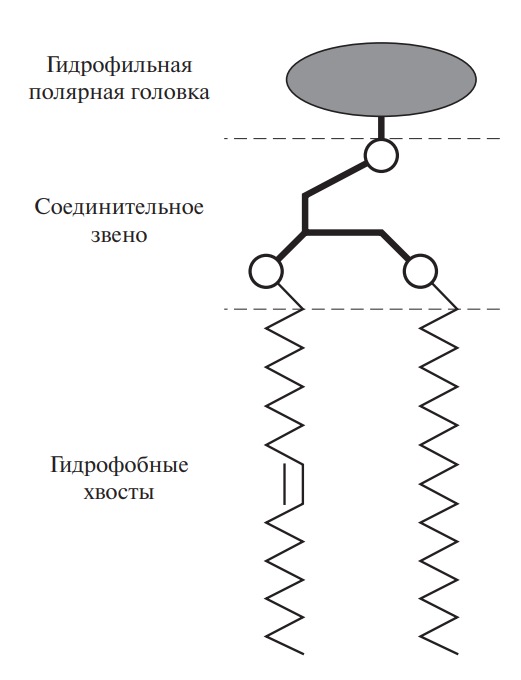
Несмотря на рассмотренное выше структурное многообразие, молекулы большинства фосфолипидов построены по общему принципу. В их состав входят, с одной стороны, гидрофобные, отличающиеся низким сродством к воде, липофильные углеводородные остатки, с другой — гидрофильные группы. Они получили название «полярных головок».
Построенные таким образом амфифильныe (обладающие двойным сродством) молекулы липидов легко ориентируются. Гидрофобные хвосты (см. pис. 2) стараются попасть в масляную фазу, гидрофильные группы создают границу раздела между водой и гидрофобной фазой.
Рис. 2. Схема наиболее вероятной структуры фосфолипидов
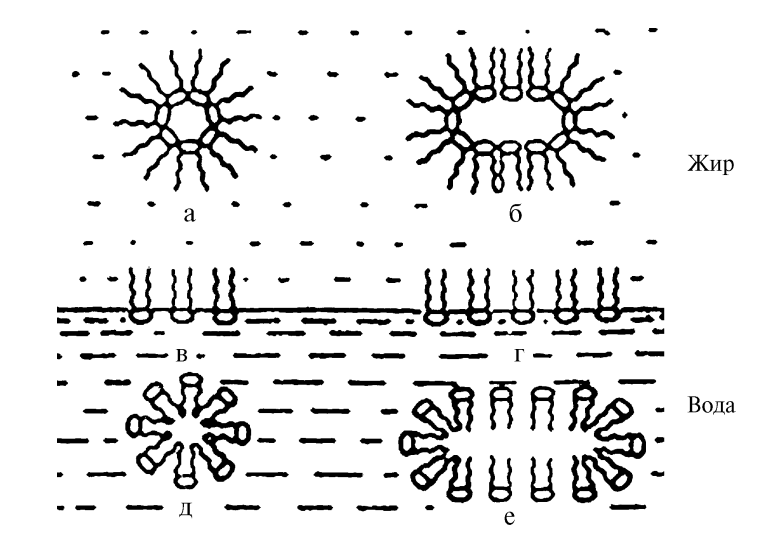
В маслах фосфолипиды в зависимости от концентрации могут присутствовать в виде индивидуальных молекул, а также в виде групп ассоциированных молекул — мицелл (рис. 3). При низкой концентрации получаются сферические мицеллы, в которых полярные части молекул образуют внешний слой, а гидрофобные — внутренний; при повышенной концентрации мицеллы группируются в длинные цилиндры. При дальнейшем росте концентрации образуется сферический тип жидкокристаллической структуры — ламеллярная (слоистая), состоящая из бимолекулярных слоев липидов, разделенных слоями воды. Последующее объединение мицелл приводит к выпадению их в виде осадка (фосфатидная эмульсия, ФУЗ). Эта особенность фосфолипидов используется для их выделения. Особенности перехода одной структуры в другую определяются не только концентрацией фосфолипидов, но и их составом, температурой и т. д.
Рис. 3. Структура мицелл фосфолипидов в жировой и водной фазах и ориентация фосфолипидов на поверхности разделов фаз: сферические (а) и пластинчатые (б) мицеллы фосфолипидов в жире; ориентация отдельных молекул (в) и монослоя фосфолипидов (г) на границе раздела фаз жир (масло)–вода; сферические (д) и пластинчатые (е) мицеллы фосфолипидов в воде
Фосфолипиды вместе с белками и углеводами участвуют в построении мембран (перегородок) клеток и субклеточных структур (органелл), выполняя роль несущих конструкций мембран, регулируют поступление в клетку и ее структуры разнообразных соединений. Липиды по их функциям в организме часто делят на две группы — запасные (резервные) и структурные (протоплазматические). Это деление условное, но оно широко применяется. Отдельные авторы, подчеркивая защитные функции липидов, выделяют некоторые из них в особую группу (например, воски).
Запасные липиды, в основном жиры (ацилглицерины), обладая высокой калорийностью, являются энергетическим и строительным резервом организма, который используется им при недостатке питания и заболеваниях. Высокая калорийность жира позволяет организму в экстремальных ситуациях существовать за счет его запасов («жировых депо») в течение нескольких недель. До 90 % всех видов растений содержат запасные липиды, главным образом в семенах. Запасные липиды являются защитными веществами, помогающими растению переносить неблагоприятные воздействия внешней среды, например низкие температуры. Запасные липиды животных и рыб, концентрируясь в подкожной жировой ткани, защищают организм от травм. Воски, которые выполняют защитные
функции, также могут быть условно отнесены к защитным липидам. Запасные липиды у большинства растений и животных являются основной по массе группой липидов (иногда до 95–96 %) и относительно легко извлекаются из жиросодержащего материала неполярными растворителями («свободные липиды»).
Структурные липиды (в первую очередь фосфолипиды) образуют сложные комплексы с белками (липопротеиды), углеводами, из которых построены мембраны клеток и клеточных структур, и участвуют в разнообразных сложных процессах, протекающих в клетках. По массе они составляют значительно меньшую группу липидов (в масличных семенах 3–5 %). Это трудноизвлекаемые «связанные» и «прочно связанные» липиды. Для их извлечения необходимо предварительно разрушить их связь с белками, углеводами и другими компонентами клетки. Связанные липиды выделяются гидрофильными полярными растворителями или их смесями (хлороформ — метанол, хлороформ — этанол), которые разрушают некоторые белково-липидные, гликолипидные соединения.
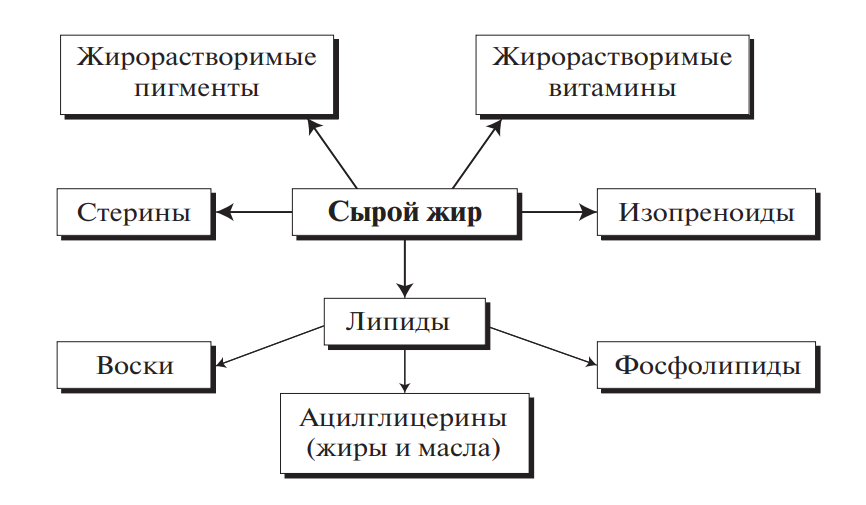
Прочно связанные липиды извлекаются после обработки липидсодержащего материала спиртовым раствором щелочи при кипячении для разрушения прочных комплексов липидов с нелипидными компонентами. При этом может происходить гидролиз отдельных групп липидов и омыление жирных кислот щелочью. При извлечении липидов из масличного сырья в масло переходит большая группа сопутствующих жирам жирорастворимых веществ: пигменты, жирорастворимые витамины, изопреноиды и некоторые другие соединения. Они играют большую роль в пищевой технологии и влияют на пищевую и физиологическую ценность полученных продуктов питания. Извлекаемая из семян смесь, состоящая из разных групп липидов и растворенных в них сопутствующих веществ, получила название сырого жира (рис. 4).
Рис. 4. Основные компоненты сырого жира
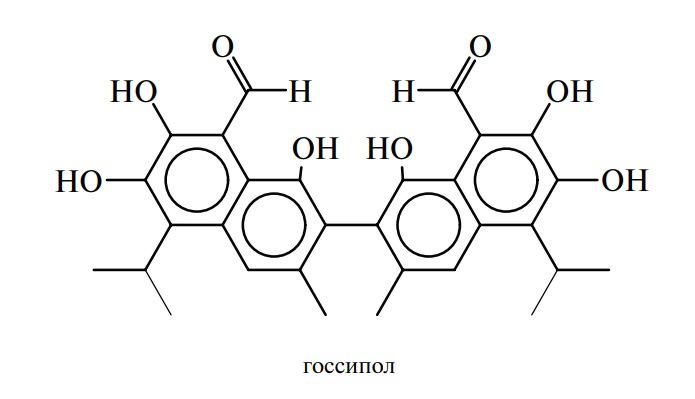
Среди жирорастворимых пигментов — веществ, определяющих окраску масел и жиров, — наиболее распространены каротиноиды и хлорофиллы. В хлопковых семенах содержится пигмент госсипол. Госсипол и продукты его превращения окрашивают хлопковые масла в темно-желтый или коричневый цвет. Госсипол, содержащийся в семенах, листьях, стеблях хлопчатника, — токсичное вещество. Его содержание в ядре семян большинства промышленных сортов хлопчатника колеблется от 0,14 до 2,5 %. По структуре госсипол представляет собой димер нафталина, содержащий гидроксильные, альдегидные, метильные и изопропильные заместители:
При хранении и нагревании нерафинированных хлопковых масел госсипол образует целый ряд соединений, обусловливающих их темную окраску.
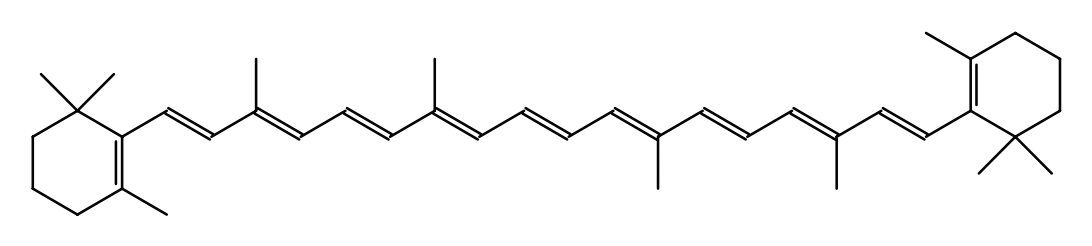
Каротиноиды — это растительные красно-желтые пигменты, определяющие окраску ряда жиров, а также овощей и фруктов, яичного желтка и многих других продуктов. По своей химической природе это углеводороды С40Н56 — каротины и их кислородсодержащие производные. Среди них необходимо отметить β-каротин:
Помимо красящих свойств, отдельные каротиноиды обладают провитаминными свойствами, так как распадаясь в живом организме, они превращаются в витамин А. Другой группой природных жирорастворимых пигментов, придающих зеленую окраску маслам и жирам, а также многим овощам (лук, салат, укроп и т. д.), являются хлорофиллы.
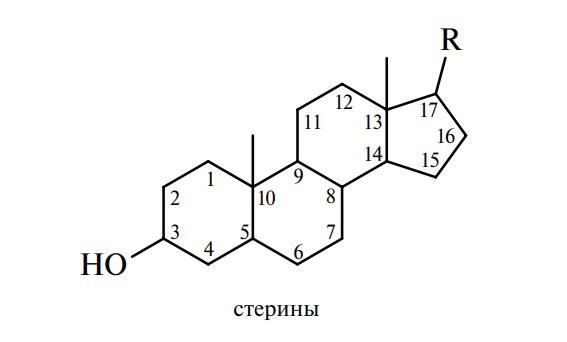
Среди сопутствующих жирам неомыляемых веществ важное место занимают циклические спирты и их эфиры — стеролы и стерины:
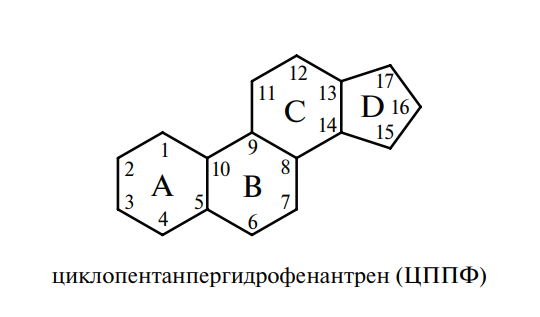
Стерины — алициклические вещества, входящие в группу стероидов; обычно они представляют собой кристаллические одноатомные спирты (стеролы) или их эфиры (стерины). Различают зоостерины, выделяемые из животных объектов, фитостерины (из растений), микостерины, выделяемые из грибов. Стерины имеют в своей основе структуру циклопентанпергидрофенантрена:
В настоящем параграфе мы остановимся только на некоторых представителях этой группы.
В молекуле стеринов (см. формулу) в положении 3 находится гидроксильная (ОН) группа и разветвленная углеродная цепь в положении 17. Не растворимые в воде стерины хорошо растворимы в жирах.
Ниже приведено содержание стеринов (в % от массы масла) в различных культурах:
- Хлопчатник 1,60
- Соя 0,35
- Рапс 0,30
- Лен 0,40
- Арахис 0,25
Стерины и их производные, несмотря на их невысокое содержание, играют исключительно важную роль в жизни всех живых организмов.
В виде сложных комплексов с белками они входят в состав протоплазмы и мембран, регулируют обмен веществ в клетке.
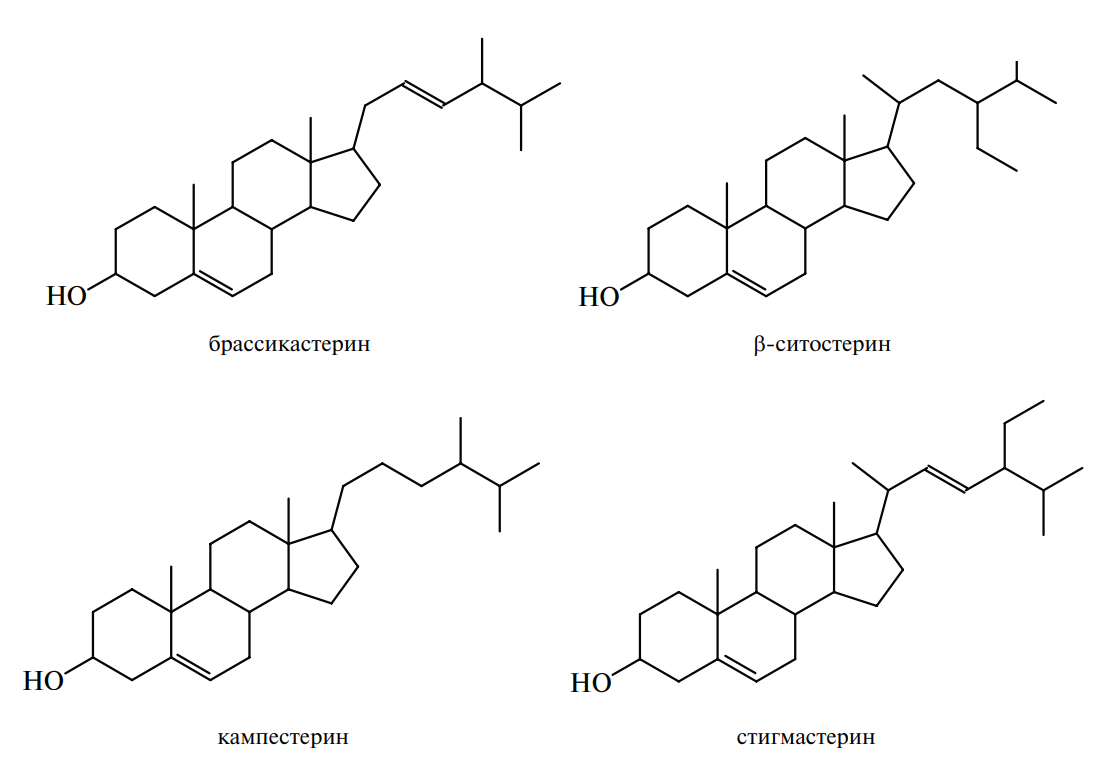
Типичными представителями растительных стеролов, содержащихся в сыром жире, являются брассикастерин, стигмастерин, кампестерин,
В сыром жире они обычно встречаются в виде эфиров пальмитиновой, олеиновой, линолевой и линоленовой кислот.
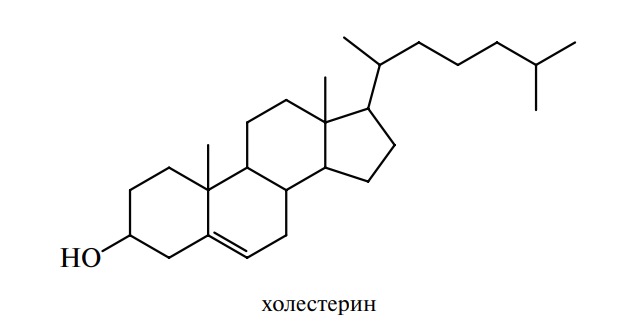
Холестерин обнаружен в тканях всех животных и отсутствует или присутствует в незначительном количестве в растениях.
Он является структурным компонентом клетки, участвует в обмене желчных кислот, гормонов; 70–80 % холестерина в организме человека синтезируется в печени и других тканях. Содержание холестерина (в %) в масле и других продуктах питания приведено ниже:
- Масло сливочное 0,17–0,21
- Яйца 0,57
- Сыры 0,28–1,61
- Мясо 0,06–0,10
В маслах и жирах, выделенных из различных объектов, содержатся насыщенные и ненасыщенные углеводороды С10–С40 различного строения. Большая часть их — изопреноиды (молекулы которых построены из различного числа остатков изопрена); к ним относятся и приведенные выше каротиноиды, сквален (углеводород С30Н50). Иногда к ним относят и стерины.
Жиры нестойки при хранении. Они являются наиболее лабильными компонентами пищевого сырья и готовых пищевых продуктов. Нестойкость жиров — следствие особенностей их химического строения. Превращения ацилглицеринов можно разделить на реакции, протекающие с участием сложноэфирных групп, и на реакции, протекающие с участием углеводородных радикалов.
2. Реакции ацилглицеринов с участием сложноэфирных групп
2.1. Гидролиз триацилглицеринов
Под влиянием щелочей, кислот, фермента липазы триацилглицерины гидролизуются с образованием ди-, затем моноацилглицеринов и в конечном счете жирных кислот и глицерина.
Результаты гидролиза выражаются схемой:
В присутствии кислотных катализаторов (сульфокислоты, H2SO4) процесс ведут при 100 °С в избытке воды. При отсутствии катализаторов расщепление проводят при температуре 220–225 °С под давлением 2–2,5 МПа («безреактивное» расщепление). Гидролиз концентрированными водными растворами гидроксида натрия (омыление) является основой процесса получения («варки») мыла. На скорость гидролиза ацилглицерина влияют строение и положение ацилов, температура, катализаторы. С ростом длины углеродной цепи, увеличением ненасыщенности (при той же длине углеродной цепи) ацилов скорость гидролиза снижается. Гидролиз ацилглицеринов под действием липазы протекает ступенчато. При этом наблюдается определенная селективность: на первой стадии образуются 1,2-диацилглицерины, на второй — 2-моноацилглицерины. Скорость гидролиза моноацилглицеринов (МАГ) выше, чем триацилглицеринов; диацилглицерины (ДАГ) занимают промежуточное положение.
Гидролиз триацилглицеринов широко применяется в технике для получения жирных кислот, глицерина, моно- и диацилглицеринов.
Гидролитический распад жиров, липидов зерна, муки, крупы и других жиросодержащих пищевых продуктов является одной из причин ухудшения их качества, в конечном счете порчи. Особенно ускоряется этот процесс при повышении влажности хранящихся продуктов, температуры, активности липазы. Скорость и глубину гидролиза масел и жиров (в том числе содержащихся в пищевом сырье и в готовых продуктах) можно охарактеризовать с помощью кислотного числа. Кислотное число для ряда пищевых продуктов нормируется стандартами и является одним из показателей, характеризующих их качество.
2.2. Переэтерификация
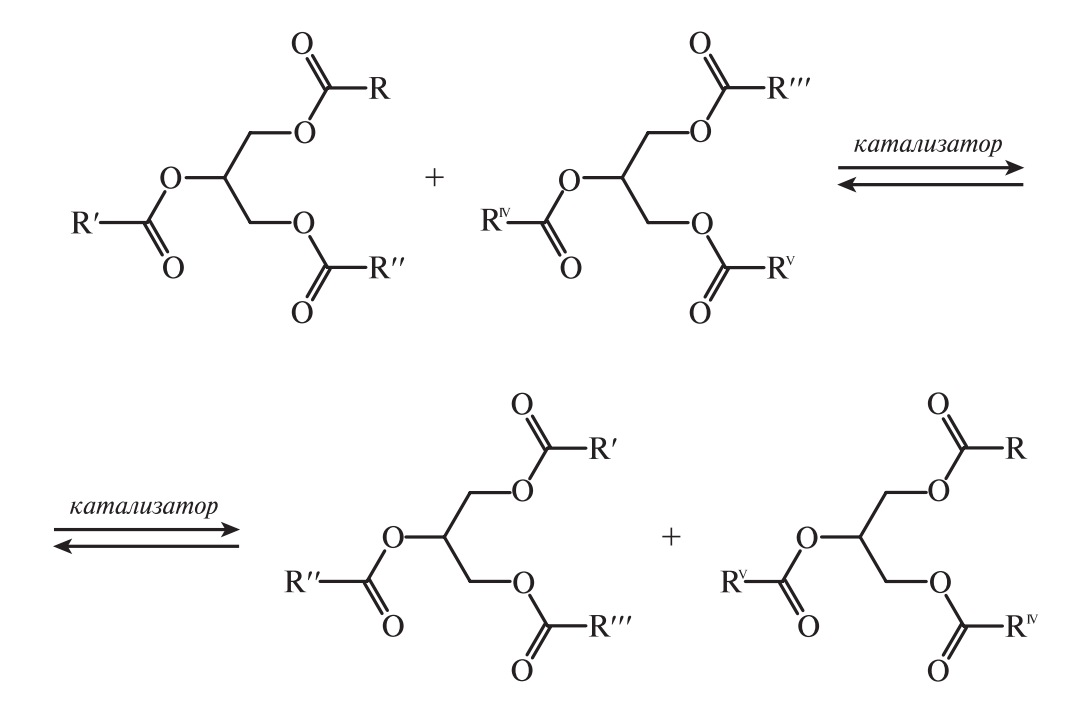
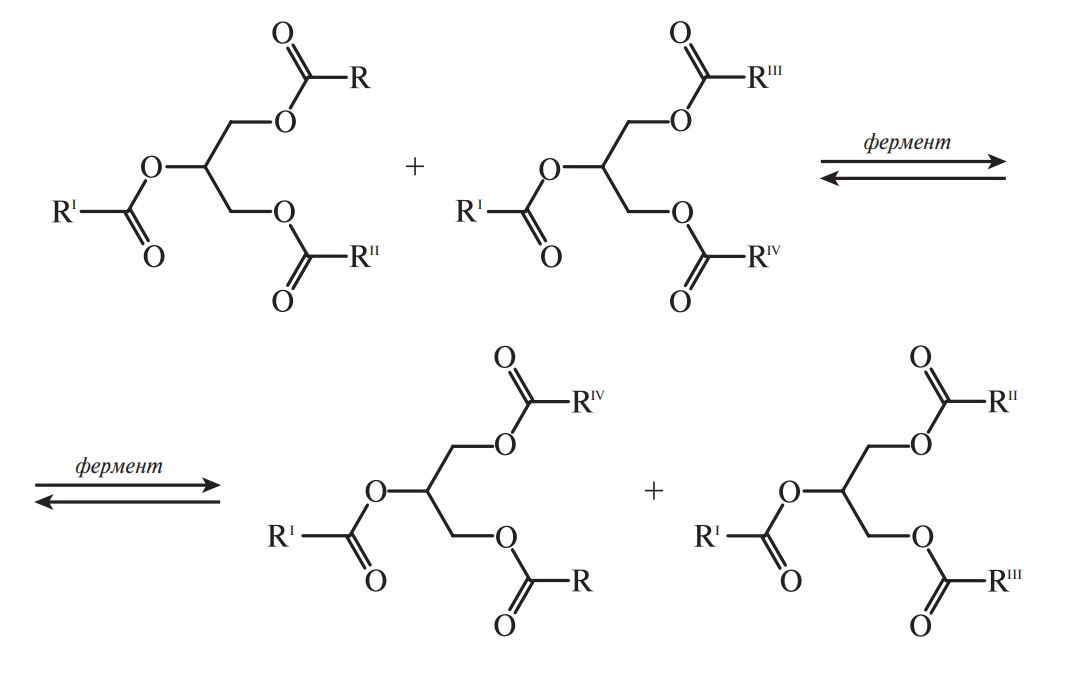
Большое практическое значение имеет группа реакций, при которых идет обмен ацильных групп (ацильная миграция), приводящий к образованию молекул новых ацилглицеринов. Различают химическую и энзимную переэтерификации. При химической переэтерификации триацилглицерины при температуре 80–90 °С в присутствии катализаторов (метилат и этилат натрия, натрий и калий, алюмосиликаты) способны обмениваться ацилами. При этом ацильная миграция происходит как внутри молекулы ацилглицерина (внутримолекулярная переэтерификация), так и между различными молекулами ацилглицеринов (межмолекулярная переэтерификация).
При переэтерификации с участием химических катализаторов состав жирных кислот жира не меняется, происходит их статистическое распределение в смеси триглицеридов, что приводит к изменению физико-химических свойств жировых смесей в результате изменения молекулярного состава. Увеличение числа ацилглицериновых компонентов в жире приводит к снижению температуры плавления и твердости жира, повышению его пластичности.
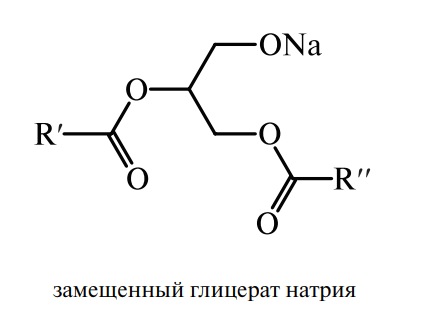
Истинным катализатором химической переэтерификации является глицерат натрия, образующийся при взаимодействии алкоголята натрия с триацилглицерином (или щелочи с глицерином).
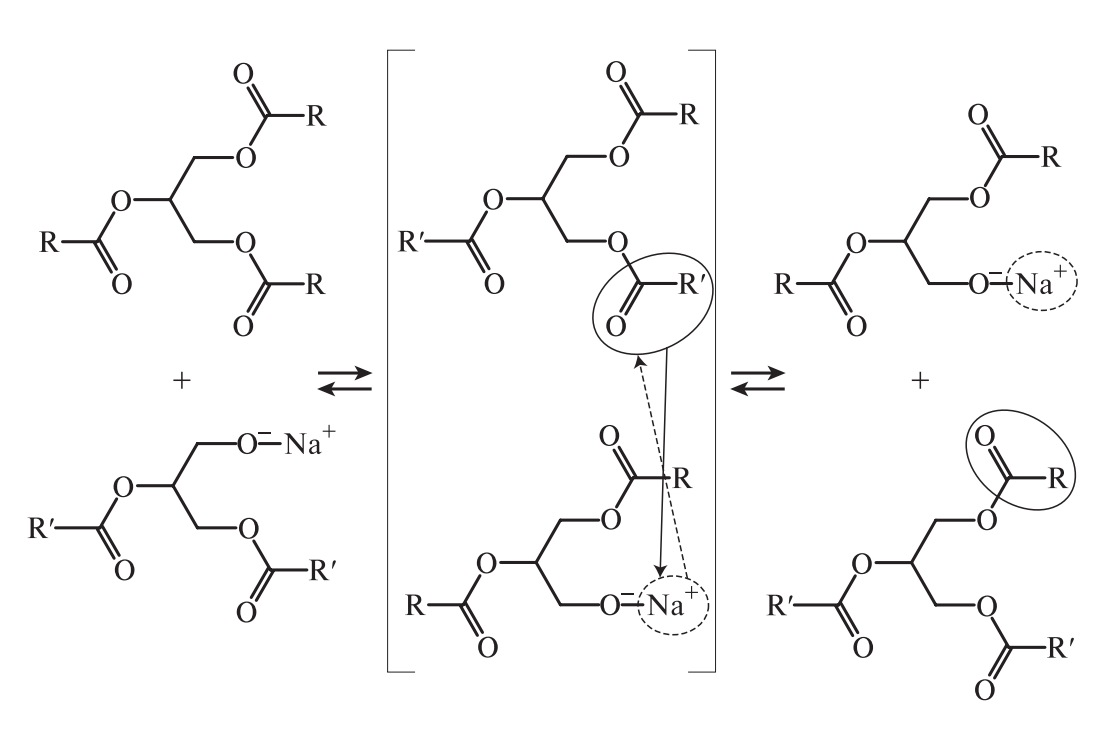
Механизм реакции химической переэтерификации заключается во взаимодействии карбонильной группы C=O сложного эфира со спиртовыми группами:
Образовавшийся глицерат взаимодействует с новой молекулой триацилглицерина. Скорость химической переэтерификации зависит от ацилглицеринового и жирно-кислотного состава жира, количества и активности катализатора, температуры.
Ферментная переэтерификация с применением липазных препаратов с многократным использованием ферментных систем позволяет создать жировые продукты нужного триацилглицеринового (триацилглицеродного) состава; при этом происходит как внутримолекулярная, так и межмолекулярная переэтерификация с сохранением ацила во 2-м положении.
В готовом продукте снижается содержание триненасыщенных и тринасыщенных ацилглицеринов, повышается содержание среднеплавких моно- и динасыщенных ацилглицеринов разных кислот.
Переэтерификация высокоплавких животных и растительных жиров с жидкими растительными маслами позволяет получить пищевые пластичные жиры с высоким содержанием линолевой кислоты при отсутствии трансизомеров жирных кислот. Готовые переэтерифицированные жиры используют в качестве компонентов маргариновой продукции, при производстве спредов. Переэтерифицированные жиры специального назначения применяются в хлебопечении, при производстве аналогов молочного жира, кондитерского жира, комбинированных жиров и т. д.
3. Реакции ацилглицеринов с участием углеводородных радикалов
3.1. Присоединение водорода (гидрирование ацилглицеринов)
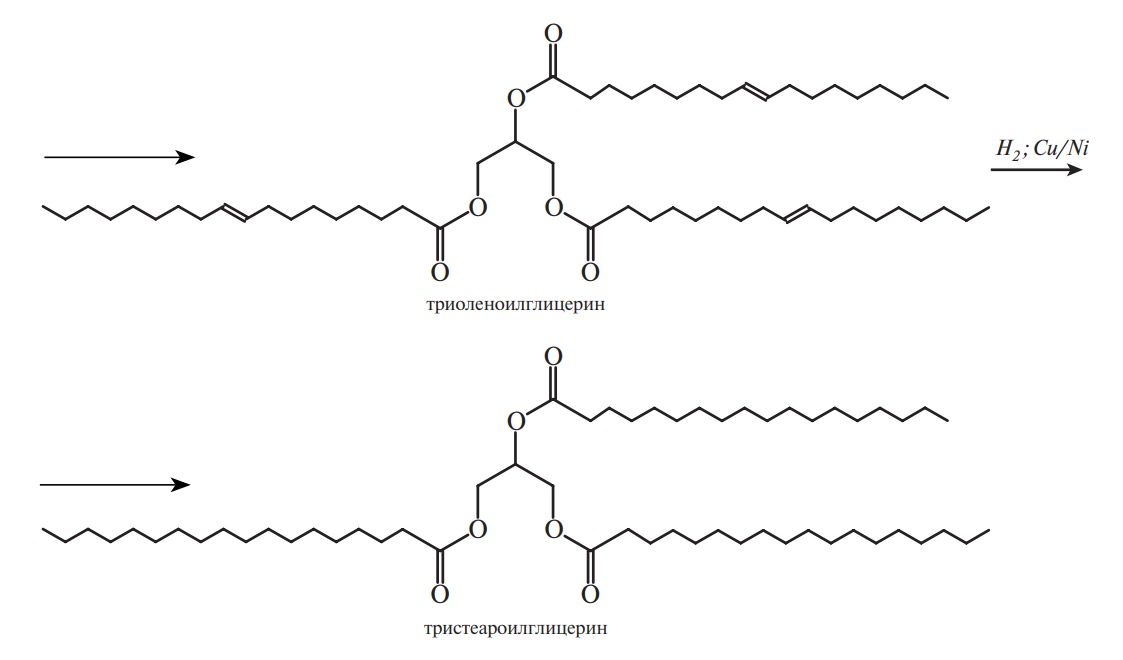
Гидрирование масел и жиров молекулярным водородом в промышленности проводят при температурах 180–240 °С в присутствии никелевых или медно-никелевых катализаторов, при давлении, как правило, близком к атмосферному. Задача гидрогенизации масел и жиров — целенаправленное изменение жирно-кислотного состава исходного жира в результате частичного или полного присоединения водорода к остаткам ненасыщенных жирных кислот, входящих в состав ацилглицеринов подсолнечного, хлопкового, соевого, рапсового и других жидких растительных масел.
Основная химическая реакция, протекающая при гидрогенизации, — присоединение водорода к двойным связям остатков непредельных жирных кислот:
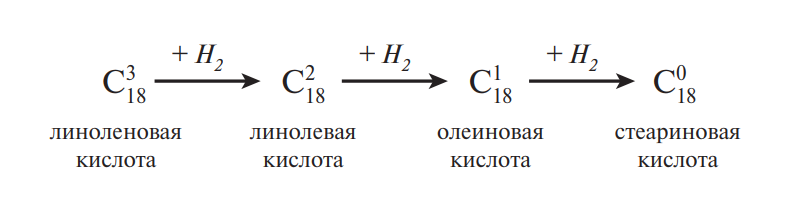
Подбирая соответствующие условия реакции, удается осуществить этот процесс селективно (избирательно), гидрируя сначала в основном ацилы линоленовой кислоты до линолевой, затем линолевой до олеиновой, а уже потом остатки олеиновой (если это необходимо) до стеариновой кислоты, и получить продукт с заранее заданными свойствами, называемый саломасом:
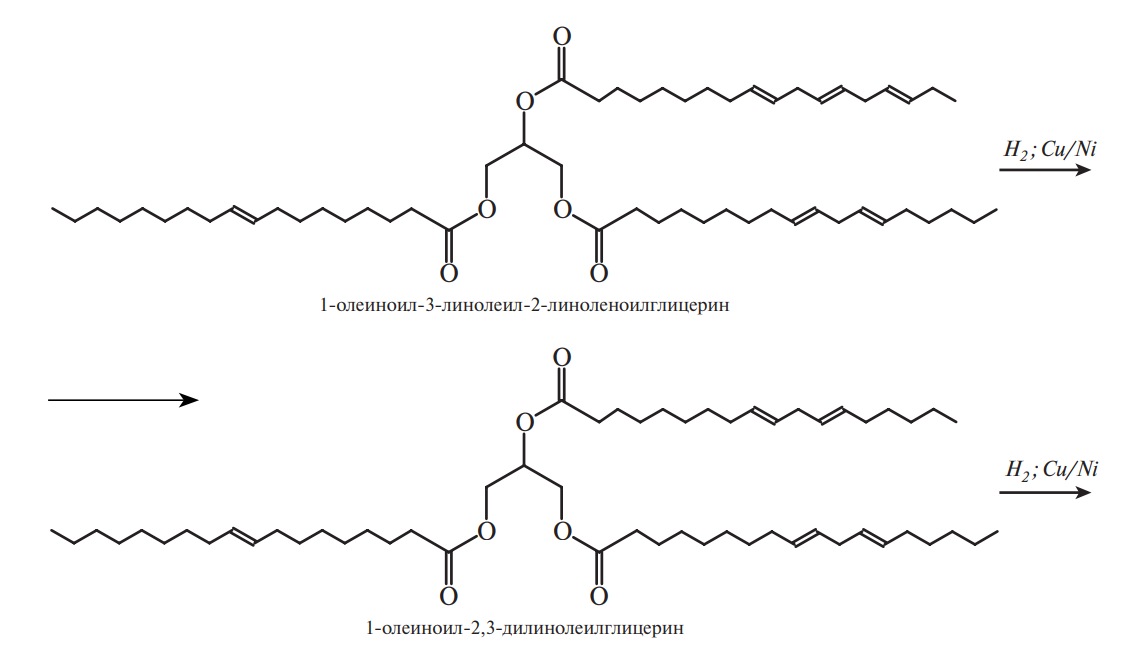
Процесс гидрирования отдельных ненасыщенных триацилглицеринов может быть представлен в следующем виде:
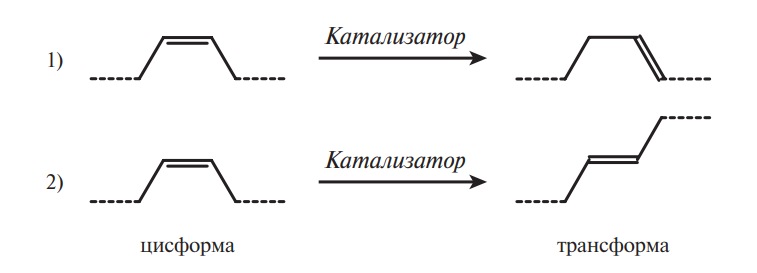
Селективность (избирательность) гидрирования объясняется большей скоростью гидрирования ацилов более ненасыщенных кислот. Гидрирование масел и жиров является гетерогенным процессом, протекающим на границе раздела фаз: смесь ацилглицеринов — катализатор. Параллельно с присоединением водорода к двойным связям (гидрирование) на поверхности катализатора происходит смещение С=С-связи (структурная изомеризация, 1) и геометрическая изомеризация (цистрансизомеризация, 2).
В отличие от гидрирования, реакции изомеризации (1, 2), идущие на поверхности катализатора, не требуют расхода водорода. Предпочтительное протекание реакций (селективность) по одному из возможных направлений определяется свойствами катализатора и условиями проведения процесса. В процессе гидрогенизации может проходить и частичная переэтерификация.
Образование трансизомеров жирных кислот (содержание их в саломасах может достигать 30–40 %), является крайне нежелательным процессом. Потребление жиров с высоким содержанием трансизомеров, по мнению специалистов, приводит к более интенсивному развитию атеросклероза, стенокардии, аритмии и сердечной недостаточности.
3.2. Окисление ацилглицеринов
Жиры и масла, особенно содержащие радикалы ненасыщенных жирных кислот, окисляются кислородом воздуха. Первыми продуктами окисления являются разнообразные по строению гидропероксиды. Они получили название первичных продуктов окисления.
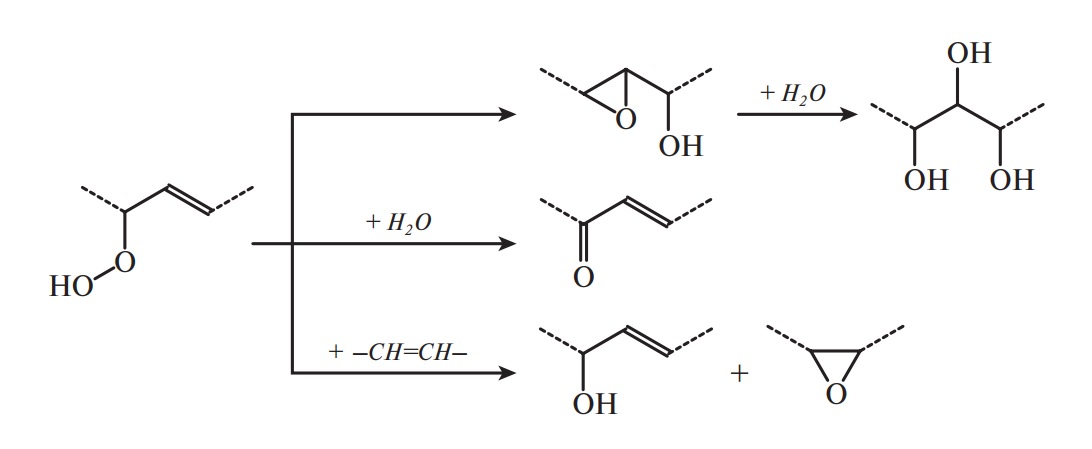
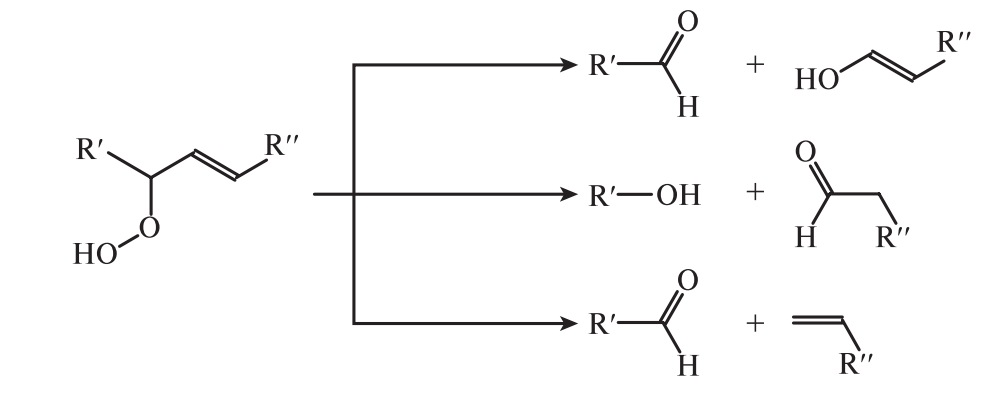
Преимущественно окисляется группа -СН -, соседняя с двойной связью (α-положение), а с наибольшей скоростью — расположенная между двумя двойными связями. Образовавшиеся гидропероксиды неустойчивы; в результате их сложных превращений образуются вторичные продукты окисления: окси- и эпоксисоединения, спирты, альдегиды, кетоны, кислоты и их производные с углеродной цепочкой различной длины.
Образование вторичных продуктов окисления может сопровождаться разрывом углеродной цепи:
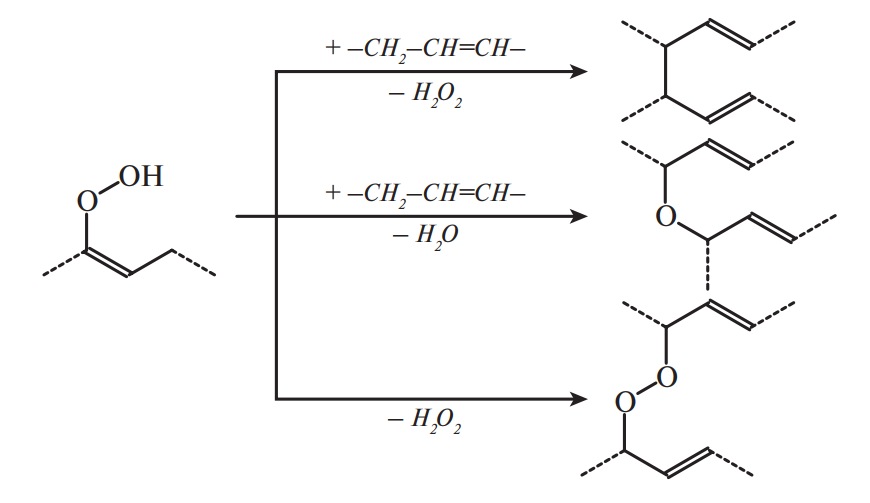
Окисление ацилглицеринов кислородом воздуха — автокаталитический процесс, идущий по цепному пути с вырожденным разветвлением. Образовавшиеся продукты окисления способны к полимеризации и поликонденсации:
Направление и глубина окисления масел и жиров зависят в первую очередь oт их ацилглицеринового состава: с увеличением степени непредельности жирных кислот, входящих в состав ацилглицеринов, скорость их окисления возрастает. В ряду эфиров олеиновой (С 1 18 ), линолевой (С 2 18 ) и линоленовой (C 3 18) кислот соотношение скорости окисления 1 : 27 : 77.
Ацилглицерины насыщенных кислот кислородом воздуха при обычных условиях практически не окисляются. Кроме того, на скорость окисления влияет присутствие влаги, металлов переменной валентности.
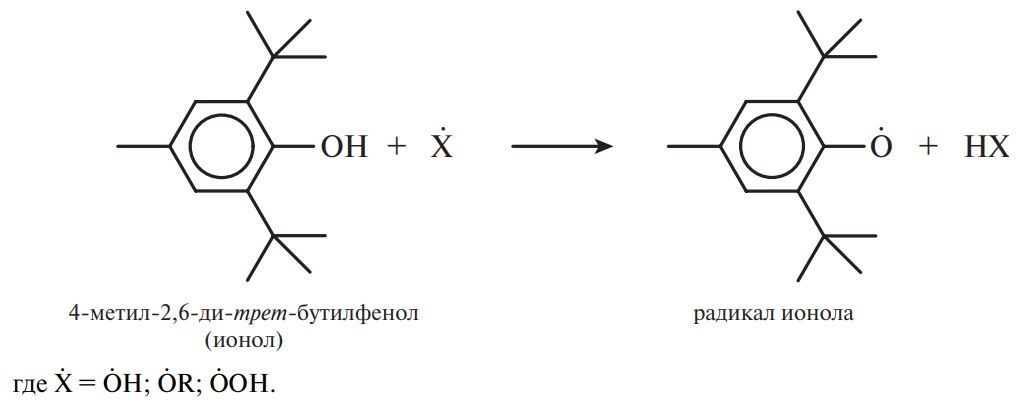
Большое влияние на скорость окисления оказывают антиокислители (ингибиторы) — вещества, добавление которых приводит к обрыву цепей окисления. Активные радикалы, которые инициируют процесс окисления, образуют стабильные радикалы, которые не участвуют в этом процессе:
Среди антиоксидантов наибольшее значение имеют соединения фенольной природы: ионол (БОТ), БОА, пропилгаллаты. Из природных антиокислителей наибольшее значение принадлежит токоферолам, сезамолу (кунжутное масло), госсиполу (хлопковое масло).
При введении антиоксидантов в количестве 0,01 % стойкость жиров к окислению увеличивается в 10–15 раз.
Активность и продолжительность действия антиоксидантов увеличивается в присутствии синергистов (от греч. synergos — действующий вместе). Действие синергистов может быть обусловлено рядом причин, главная из них — способность дезактивировать ионы металлов переменной валентности (Рb, Сu, Со, Mn, Fe и т. д.), играющих роль катализаторов окисления. Активными синергистами являются комплексоны (окси- и аминокислоты, производные фосфорной и фосфоновой кислот и др.). Применение в качестве комплексонов нашли лимонная и аскорбиновая кислоты. Синергистами являются фосфолипиды.
Скорость окисления жиров уменьшается при понижении содержания кислорода в окружающей среде. На этом основан способ xpaнения масел и жиров в среде с пониженным содержанием кислорода (например, в среде с повышенным содержанием азота). Окисление жиров ускоряется с повышением температуры хранения и под воздействием световой энергии. Ионы металлов переходной валентности — железа, меди, марганца и других — могут оказывать как каталитическое, так и ингибирующее (замедляющее) действие на процесс автоокисления жиров.
Окисление липидов может проходить и под действием биологических катализаторов — липоксигеназ.
Ферментативное окислительное прогоркание характерно для липидного комплекса хранящихся масличных семян, зерна, продуктов их переработки (мука, крупа). Оно протекает при участии ферментов липазы и липоксигеназы.
Липаза осуществляет гидролиз триацилглицеринов, липоксигеназа катализирует образование гидропероксидов ненасыщенных жирных кислот (главным образом линолевой и линоленовой). Свободные жирные кислоты окисляются быстрее, чем их остатки, входящие в молекулы жира.
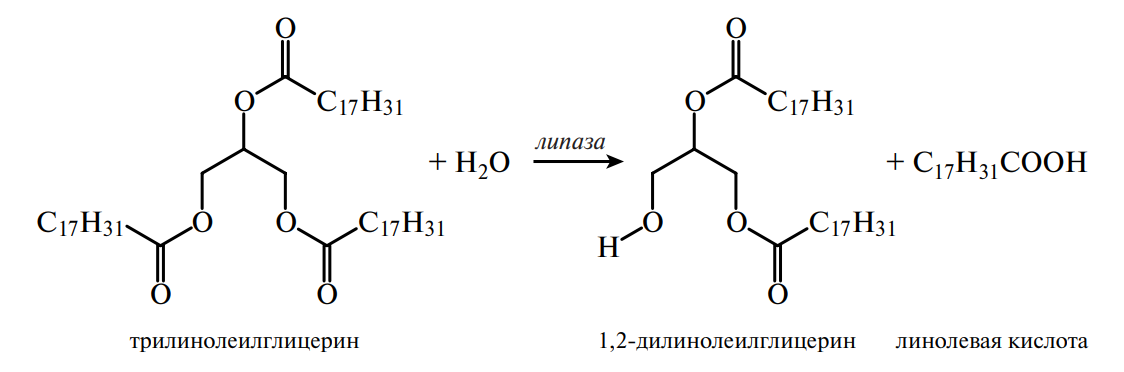
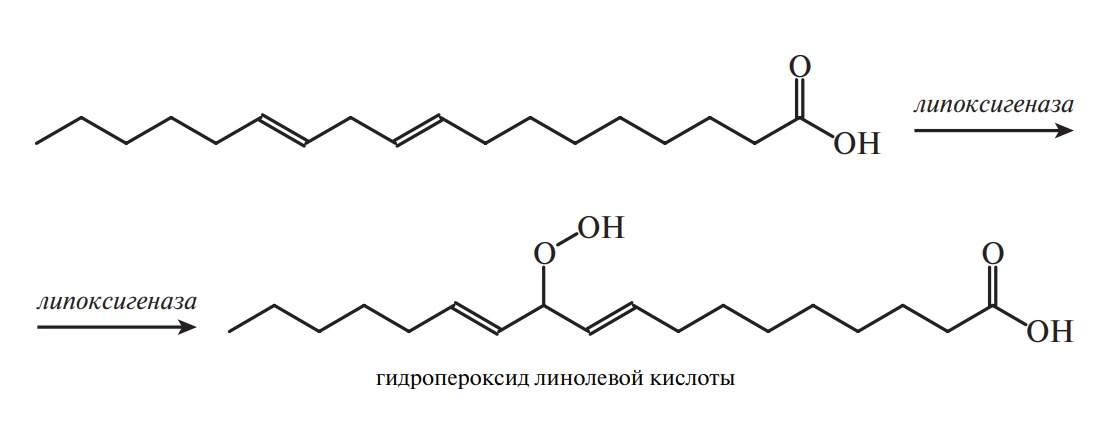
Ферментативное прогоркание начинается с гидролиза жира ферментом липазой:
Образовавшаяся в результате гидролиза линолевая кислота окисляется при участии фермента липоксигеназы:
Гидролиз образовавшегося 1,2-дилинолеилглицерина и окисление гидропероксида могут продолжаться и дальше. Образующиеся вторичные продукты окисления (альдегиды, кетоны и другие соединения) являются причиной ухудшения качества пищевого сырья и многих липидсодержащих продуктов.
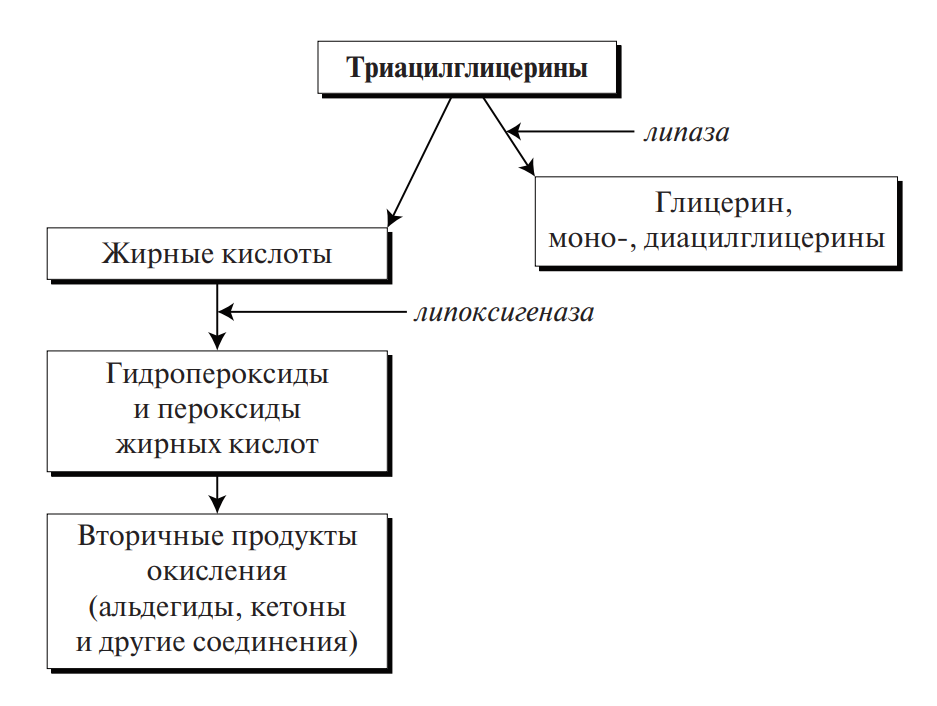
В общем виде этот процесс может быть представлен схемой (рис. 5).
Как видно из этой схемы, в данном случае липаза и липоксигеназа действуют кооперативно.
Рис. 5. Общая схема ферментативного прогоркания жира
Первый этап — расщепление триацилглицеринов с образованием свободных жирных кислот (см. рис. 5) — является примером ферментативного гидролитического прогоркания. Гидролитическое прогоркание может проходить и без участия ферментов (неферментативный гидролиз).
В каждом отдельном случае, в зависимости от характера жиросодержащих пищевых продуктов или пищевого сырья и условий, при которых они находятся, прогоркание будет проходить по одному из рассмотренных нами типов, а иногда (например, при хранении маргарина, молочного жира, муки, крупы) может проходить ферментативное и неферментативное прогоркание, взаимно дополняя друг друга.
При хранении растительные и животные жиры, жиросодержащие продукты (масличные семена, мука, крупа, кондитерские изделия и т. д.) под влиянием кислорода воздуха, света (особенно прямого солнечного, ультрафиолетового), влаги, ферментов постепенно приобретают неприятный вкус и запах. Некоторые из них обесцвечиваются. В них накапливаются вредные для организма человека продукты окисления. В результате снижается их пищевая и физиологическая ценность, при этом они могут оказаться непригодными для употребления (пищевая порча жиров).
Органолептическая оценка пищевой порчи масел и жиров очень субъективна. На начальном этапе порчи появляется неприятный вкус, не свойственный оцениваемому маслу или жиру; жир может выступать раздражителем («царапание») в горле, вызывать ощущение жжения. Несколько позднее появляется неприятный запах (иногда «запах олифы»). При качественной оценке порчи сливочного масла, маргарина используют термины «осаливание», «сырный привкус», «олеиногость» и, наконец, «прогорклость». Совокупность процессов, протекающих при пищевой порче жира, получила название прогоркания.
Прогоркание жиров и жиросодержащих продуктов — результат сложных химических и биохимических процессов, протекающих в липидном комплексе. Различаются окислительное и гидролитическое прогоркание. Оба эти вида прогоркания могут быть разделены в зависимости от факторов, ускоряющих (катализирующих) их, на автокаталитическое (неферментативное) и ферментативное (биохимическое). Жиры и масла, особенно содержащие остатки ненасыщенных жирных кислот (линоленовой, линолевой, олеиновой), при контакте с воздухом растворяют его компоненты, в том числе кислород, и окисляются.
Начальными продуктами окисления являются, как уже указывалось, разнообразные по строению пероксиды и гидропероксиды. Они получили название первичных продуктов окисления. В результате сложных превращений пероксидов образуются вторичные продукты окисления: спирты, альдегиды, кетоны, кислоты с углеродной цепочкой меньшей длины, чем в исходном жире, а также их разнообразные производные. Именно эти вещества вызывают появление неприятного привкуса, свойственного прогорканию, а входящие в их состав летучие соединения обусловливают в то же время и ухудшение запаха.
Пищевая порча жира сопровождается изменением не только ацилглицеринов, но и сопутствующих веществ. Например, обесцвечивание растительных масел при осаливании связано с окислением каротиноидов. Темный цвет масел, полученных из пораженных плесенью семян, обусловлен окислением микотоксинов. Очень темная (от коричневой до черной) окраска хлопкового масла обусловлена продуктами окисления госсипола. Порча жира сопровождается и целым рядом реакций деструкции и полимеризации. Деструкция фосфатидилхолина с образованием легколетучего триметиламина (CH3)3N обусловливает селедочный запах осаленных жиров. Окисление липидов приводит не только к ухудшению
качества пищевых продуктов, снижению их пищевой ценности, образованию вредных для организма человека соединений, но и к большим потерям продуктов. Поэтому необходимо применять все меры по предотвращению или замедлению прогоркания жиров и жиросодержащих пищевых продуктов. Жиры и содержащие их пищевые продукты обладают неодинаковой устойчивостью при хранении. Она зависит от их жирно-кислотного состава, характера примесей, наличия и активности ферментов; все это должно определять условия их упаковки, режимы и допустимые сроки хранения. Наименее стойки при хранении сливочное масло, маргарин, куриный жир.
4. Свойства и превращения глицерофосфолипидов
Глицерофосфолипиды — бесцветные вещества, без запаха, хорошо растворимы в жидких углеводородах и их галогенпроизводных, отдельные группы различаются растворимостью в спиртах, ацетоне. Они существуют в нескольких полимерных формах и плавятся в две стадии. Обладают оптической активностью. Выделенные из природных объектов фосфолипиды — аморфные вещества, перекристаллизованные из органических растворителей, — имеют кристаллическую структуру.
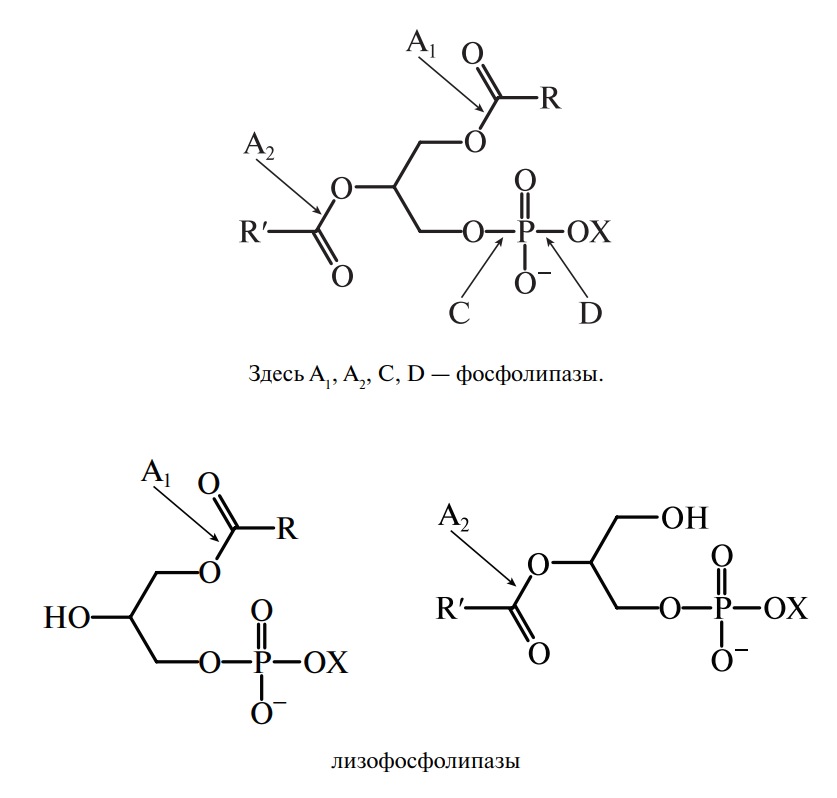
Химические превращения глицерофосфолипидов обусловлены характером и строением структурных компонентов и видами химических связей. Для них характерны реакции гидролиза кислотами и щелочами. Существует несколько видов фосфолипаз (А1, А2, В, С, D), различающихся характером действия на субстрат. Они обнаружены в природных объектах.
Принципиальная схема действия фосфолипаз на фосфолипиды:
Полярные группы молекул фосфолипидов взаимодействуют с полярными группами молекул белков, углеводов, диполями воды.
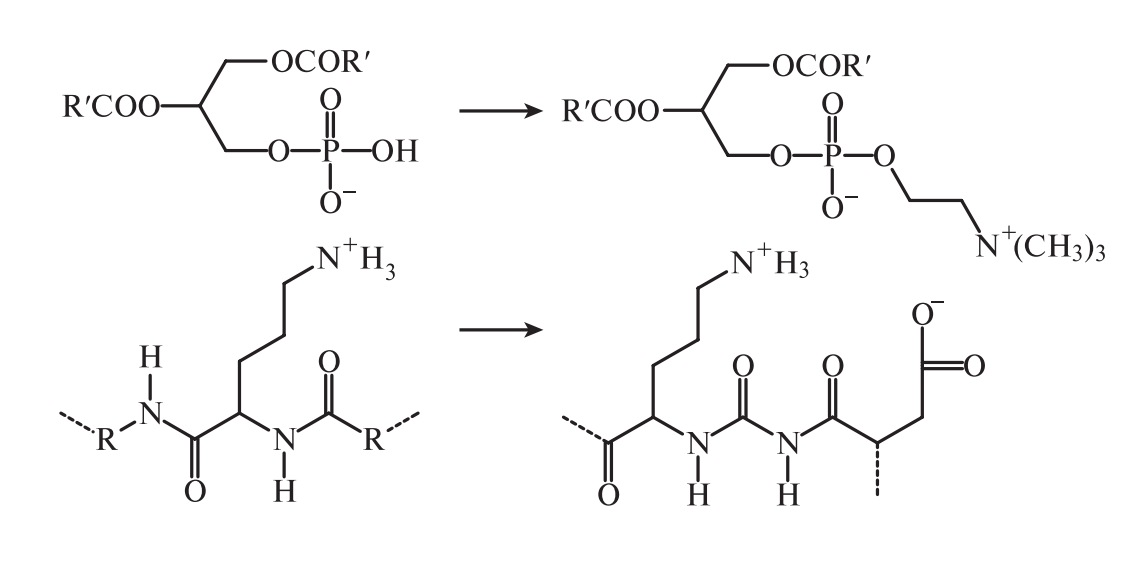
Некоторая часть фосфолипидов не выделяется из масел при гидратации или выделяется только с помощью специальных приемов гидратации масел (негидратируемые фосфолипиды). По современным представлениям, это комплексные соединения фосфолипидов с ионами металлов (Са2+, Мg2+, Сu2+, Fе2+ и Fе3+; последние являются катализаторами процессов окисления), а также соединения со стеролами и алифатическими спиртами. В результате энзимической и химической модификации в промышленности получают различные виды производных фосфолипидов (лецитинов): гидролизованные лецитины, гидроксилированные, ацилированные с различными гидрофильно-липофильными характеристиками (ГЛБ от 2 до 12). Они нашли широкое применение в пищевой промышленности.
5. Методы выделения липидов из сырья и пищевых продуктов и их анализ
Анализ липидов и продуктов их превращений является сложной задачей, требующей применения наряду с классическими химическими методами современных физико-химических методов исследования (хроматографии, спектроскопии, рентгеноструктурного анализа и т. д.).
Изучение липидов начинается с определения их количества (содержания) в пищевых продуктах. Для этого используются методы определения содержания липидов непосредственно в объекте (ЯМР, ИК-спектроскопия) и методы, основанные на извлечении липидов из пищевого продукта (свободные, связанные, прочно связанные липиды). Свободные липиды экстрагируются из анализируемого продукта неполярными растворителями (гексаном, диэтиловым эфиром), связанные — системами растворителей, содержащими, как правило, спирт (смесь хлороформа и метанола, взятых в объемном соотношении 2 : 1). Прочно связанные липиды получают из обработанного щелочами и кислотами шрота, оставшегося после выделения связанных липидов. Основные требования, предъявляемые к методам выделения, — полнота выделения и сохранение нативности выделенных липидов.
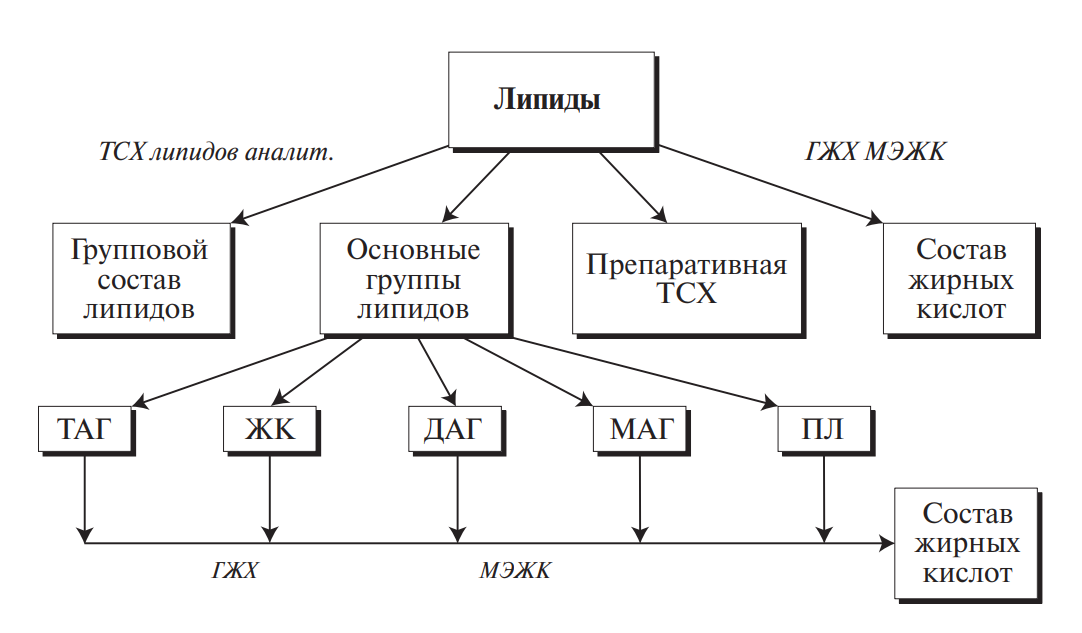
Химический состав липидов, выделенных из пищевого сырья и продуктов, исследуется по схеме, приведенной на рис. 6, причем в каждом конкретном случае выбирают тот набор анализов, который позволяет получить максимальный объем интересующей исследователей информации. Подробное описание методов выделения и исследования липидов приведено в специальных руководствах.
В практике пищевой промышленности состав и качество жиров и масел характеризуют с помощью разнообразных аналитических «чисел», подразумевая под ними расход определенных реагентов на реакции с жиром. Наибольшее значение имеют числа: кислотное, омыления, йодное, аназидиновое.
Кислотным числом называется показатель, характеризующий количество свободных жирных кислот, содержащихся в жире. Он выражается в миллиграммах едкого калия, затраченного на нейтрализацию свободных жирных кислот, содержащихся в 1 г жира. Учитывая, что хранение пищевых продуктов, содержащих жиры и масла, всегда сопровождается гидролизом последних, по величине кислотного числа можно, до известной степени, судить об их качестве. В заводской практике кислотное число используется при расчете количества щелочи, необходимой для рафинации жиров и масел.
Рис. 6. Общая схема анализа жиров
Число омыления равно количеству миллиграммов едкого калия, необходимого для омыления глицеридов и нейтрализации свободных жирных кислот в 1 г жира или масла. По числу омыления можно судить о средней молекулярной массе входящих в состав липидов жирных кислот и определить при мыловарении количество щелочи, необходимое для омыления жира.
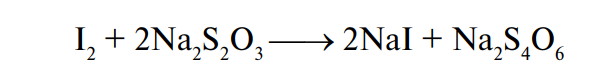
Йодное число — показатель, характеризующий непредельность жирных кислот, входящих в состав жира. Оно выражается в процентах йода, эквивалентного галогену, присоединяющемуся к 100 г жира. Существует несколько методов определения йодного числа. Одним из наиболее распространенных является бромометрический метод. При этом применяется раствор брома в безводном метиловом спирте, насыщенном бромистым натрием. Бром образует непрочное комплексное соединение с бромистым натрием:
Отщепляясь, бром реагирует с ненасыщенными глицеридами:
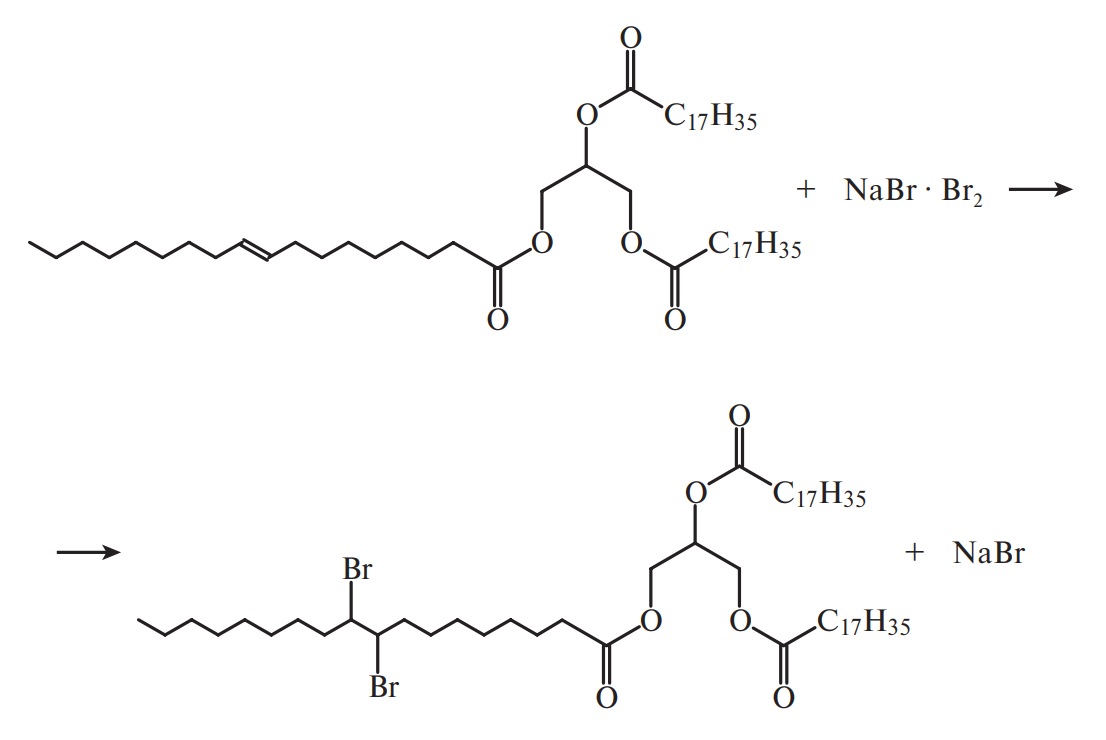
Зная исходное количество брома, можно легко вычислить йодное число жира. Йодное число широко применяется для определения вида жира, способности его к «высыханию», расчета потребного количества водорода на его гидрогенизацию.
Величины указанных констант для отдельных жиров, не подвергшихся разрушению, колеблются в незначительных пределах и характеризуют вид жира и его качество (табл. 2).
Таблица 2. Содержание жирных кислот (в%) и характеристики масел и жиров
| Жиры и масла | Содержание и состав жирных кислот | Характеристика | ||||
| насыщенных | ненасыщенных | основных | Температура застывания, °С | Число омыления | Иодное число | |
| Масла | ||||||
| Соевое | 14—20 | 75—86 | С 2 18 46—65 | –18 | 191—193 | 120—140 |
| Хлопковое | 22—30 | 75—76 | С 2 18 45—56 | 2—4 | 191—198 | 101—116 |
| Подсолнечное | 10—12 | До 90 | C 2 18 46—70 | 16—18 | 186—194 | 119—136 |
| Рапсовое | 2—6 | 94—98 | С 1 18 6—44 1—52 | 0—10 | 167—181 | 94—103 |
| Оливковое | 9—18 | 82—91 | С 1 18 70—82 | 0—6 | 185—200 | 72—89 |
| Kокосовое | До 90 | 1 | С 0 12 44—52 С 0 14 13—18 | 16—25 | 251—264 | 7—12 |
| Пальмовое | 44—57 | 43—56 | С 0 16 39—47 С 2 18 45—50 | 31—41 | 196—210 | 52—58 |
| Пальмо-ядровое | 79—83 | 17—21 | С 0 16 10—19 | 19—24 | 240—257 | 15—20 |
| Масло какао | 58—60 | 40—42 | С 1 18 23—25 С 0 16 31—34 | 21—27 | 192—196 | 34—36 |
| Льняное | 6—9 | 91—94 | С 3 18 41—60 | 18—27 | 191—195 | 175—190 |
| Животные жиры | ||||||
| Говяжий | 45—60 | 43—52 | С 1 18 24—29 43—44 | 30—38 | 190—200 | 32—47 |
| Бараний | 52—62 | 38—48 | С 0 18 25—31 С 1 18 36—42 | 32—45 | 192—198 | 31—46 |
| Свиной | 33—49 | 48—64 | С 1 18 25—32 34—44 | 22—32 | 193—200 | 46—66 |
| Kитовый | 10—22 | 48—90 | — | — | 181—193 | 100—161 |
6. Пищевая ценность масел и жиров
Растительные жиры и масла являются важным компонентом пищи, источником энергетического и пластического материала для человека, поставщиком ряда необходимых для него веществ (непредельных жирных кислот, фосфолипидов, жирорастворимых витаминов, стеринов), то есть они являются незаменимыми факторами питания, определяющими его биологическую эффективность. Рекомендуемое содержание жира в рационе человека (по калорийности) составляет 30–33 %; для населения южных зон нашей страны рекомендуется его 27–28 %, северных — 38–40 % или 90–107 г в сутки, в том числе непосредственно в виде жиров 45–50 г.
Длительное ограничение жиров в питании или систематическое использование жиров с пониженным содержанием необходимых компонентов, в том числе сливочного масла, приводит к отклонениям в физиологическом состоянии организма: нарушается деятельность центральной нервной системы, снижается устойчивость организма к инфекциям (иммунитет), сокращается продолжительность жизни. Но и избыточное потребление жиров нежелательно, оно приводит к ожирению, сердечно-сосудистым заболеваниям, преждевременному старению.
В составе пищевых продуктов различают видимые жиры (растительные масла, животные жиры, сливочное масло, маргарин, кулинарный жир, спреды, майонезы, соусы) и невидимые жиры (жир в мясе и мясопродуктах, рыбе, молоке и молочных продуктах, крупе, хлебобулочных и кондитерских изделиях). Это, конечно, условное деление, но оно широко применяется.
Наиболее важные источники жиров в питании: растительные масла (в рафинированных маслах 99,7–99,8 % жира); сливочное масло (61,5– 82,5 % липидов); маргарин (до 82,0 % жира); комбинированные жиры (50–72 % жира); кулинарные жиры (99 % жира); молочные продукты (3,5–30 % жира); некоторые виды кондитерских изделий — шоколад (35–40 %), отдельные сорта конфет (до 35 %), печенье (10–11 %); крупы — гречневая (3,3 %), овсяная (6,1 %); сыры (25–50 %); продукты из свинины, колбасные изделия (10–23 % жира). Часть этих продуктов является источником растительных жиров (растительные масла, крупы), другие — животных жиров.
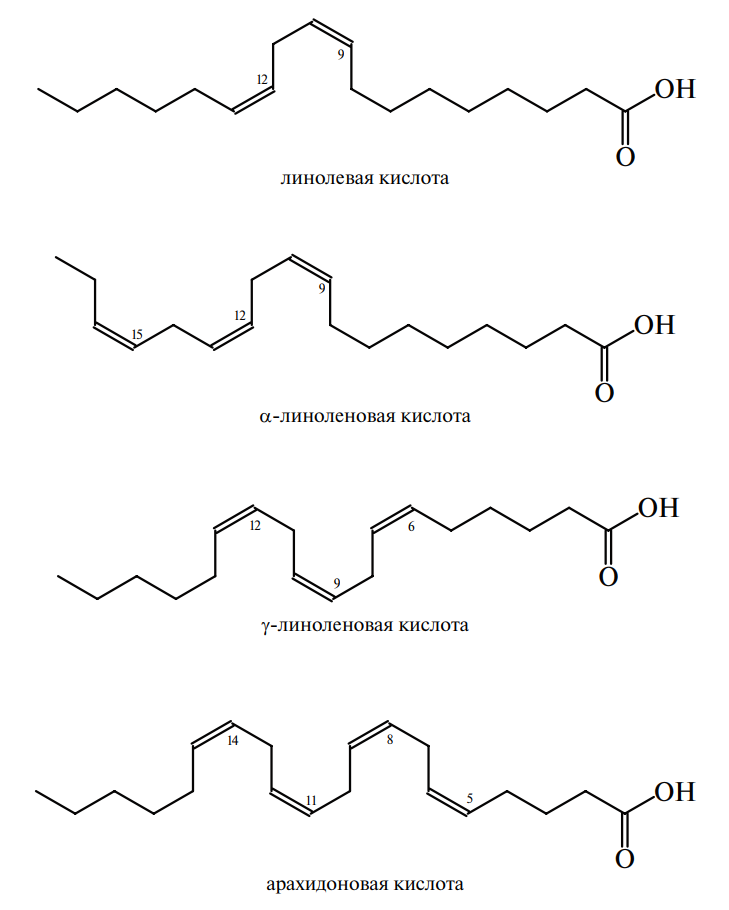
В питании имеет значение не только количество, но и химический состав употребляемых жиров, особенно содержание полиненасыщенных кислот с определенным положением двойных связей и цисконфигурацией (линолевая кислота С 2 18 ; альфа- и гамма-линоленовая С 3 18 ; олеиновая С 1 18 ; арахидоновая С 4 20; полиненасыщенные жирные кислоты с 5–6 двойными связями семейства омега-3).
Линолевая и линоленовая кислоты не синтезируются в организме человека, арахидоновая — синтезируется из линолевой кислоты при участии витамина В6. Поэтому они получили название «незаменимых» или «эссенциальных» кислот. Линоленовая кислота образует другие полиненасыщенные жирные кислоты. В состав полиненасыщенных жирных кислот семейства омега-3 входят: α-линоленовая, эйкозапентаеновая, докозагексаеновая кислоты. Линолевая, γ-линоленовая, арахидоновая кислоты входят в семейство омега-6. Рекомендуемое Институтом питания РАМН соотношение омега 6 : омега 3 в рационе составляет для здорового человека 5–10 : 1,2, для лечебного питания — 3–5 : 1,2.
Более 50 лет назад была доказана необходимость присутствия ряда этих структурных компонентов липидов для нормального функционирования и развития нашего организма. Они участвуют в построении клеточных мембран, в синтезе простагландинов, в регулировании обмена веществ в клетках, кровяного давления, агрегации тромбоцитов, способствуют выведению из организма избыточного количества холестерина, предупреждая и ослабляя атеросклероз, повышают эластичность стенок кровеносных сосудов. Но эти функции выполняют только цисизомеры ненасыщенных кислот. При отсутствии «эссенциальных» кислот прекращается рост организма и возникают тяжелые заболевания. Биологическая активность указанных кислот неодинакова. Наибольшей активностью обладает арахидоновая кислота, высокой — линолевая, активность линоленовой кислоты значительно (в 8–10 раз) ниже линолевой.
В последнее время особое внимание привлекают ненасыщенные жирные кислоты семейства омега-3, присутствующие в липидах рыб.
Среди продуктов питания наиболее богаты полиненасыщенными кислотами растительные масла (см. табл. 2), особенно кукурузное, подсолнечное, соевое. Содержание в них линолевой кислоты достигает 50–60 %, значительно меньше ее в маргарине — до 20 %, крайне мало в животных жирах (в говяжьем жире — 0,6 %). Арахидоновая кислота в продуктах питания содержится в незначительном количестве, а в растительных маслах ее практически нет. В наибольшем количестве арахидоновая кислота содержится в яйцах — 0,5, субпродуктах 0,2–0,3, мозгах — 0,5 %.
В настоящее время считают, что суточная потребность в линолевой кислоте должна составлять 6–10 г, минимальная — 2–6 г, а ее суммарное содержание в жирах пищевого рациона — не менее 4 % от общей калорийности. Следовательно, состав жирных кислот липидов в пищевых продуктах, предназначенных для питания молодого, здорового организма, должен быть сбалансированным: 10–20 % — полиненасыщенных, 50–60 % — мононенасыщенных и 30 % насыщенных, часть из которых должна быть со средней длиной цепи. Это обеспечивается при использовании в рационе 1/3 растительных и 2/3 животных жиров. Для людей пожилого возраста и больных сердечно-сосудистыми заболеваниями содержание линолевой кислоты должно составлять около 40 %, соотношение полиненасыщенных и насыщенных кислот — приближаться к 2 : 1, соотношение линолевой и линоленовой кислот — 10 : 1 (Институт питания РАМН).
Способность жирных кислот, входящих в состав липидов, наиболее полно обеспечивать синтез структурных компонентов клеточных мембран характеризуют с помощью специального коэффициента (Институт питания РАМН), отражающего соотношение количества арахидоновой кислоты, которая является главным представителем полиненасыщенных жирных кислот в мембранных липидах, к сумме всех других полиненасыщенных жирных кислот с 20 и 22 атомами углерода. Этот коэффициент получил название коэффициента эффективности метаболизации эссенциальных жирных кислот (КЭМ):
По современным представлениям наиболее целесообразно использовать в каждый отдельный прием пищи жиры, имеющие сбалансированный состав, а не потреблять жировые продукты различного состава в течение суток.
Важной в питании группой липидов являются фосфолипиды, участвующие в построении клеточных мембран и транспорте жира в организме; они способствуют лучшему усвоению жиров и препятствуют ожирению печени. Общая потребность человека в фосфолипидах — до 5–10 г в сутки.
Отдельно хочется остановиться на физиологической роли холестерина. Как известно, при повышении его уровня в крови опасность возникновения и развития атеросклероза возрастает; много холестерина содержится в яйцах (0,57 %), сливочном масле (0,2–0,3 %), субпродуктах (0,2–0,3 %). Суточное его потребление с пищей не должно превышать 0,5 г. Растительные жиры — единственный источник витамина Е и β-каротина, животные жиры — витаминов А и D.
7. Превращения липидов при производстве продуктов питания
При получении продуктов питания в ходе технологического потока липиды исходного сырья (зерно, крупа, мясо и молоко, жиры и масла, плоды, овощи и др.) претерпевают разнообразные превращения; значительные изменения происходят и в липидном комплексе хранящихся продуктов. Все это сказывается на их составе, а следовательно, на пищевой и биологической эффективности готовых продуктов.
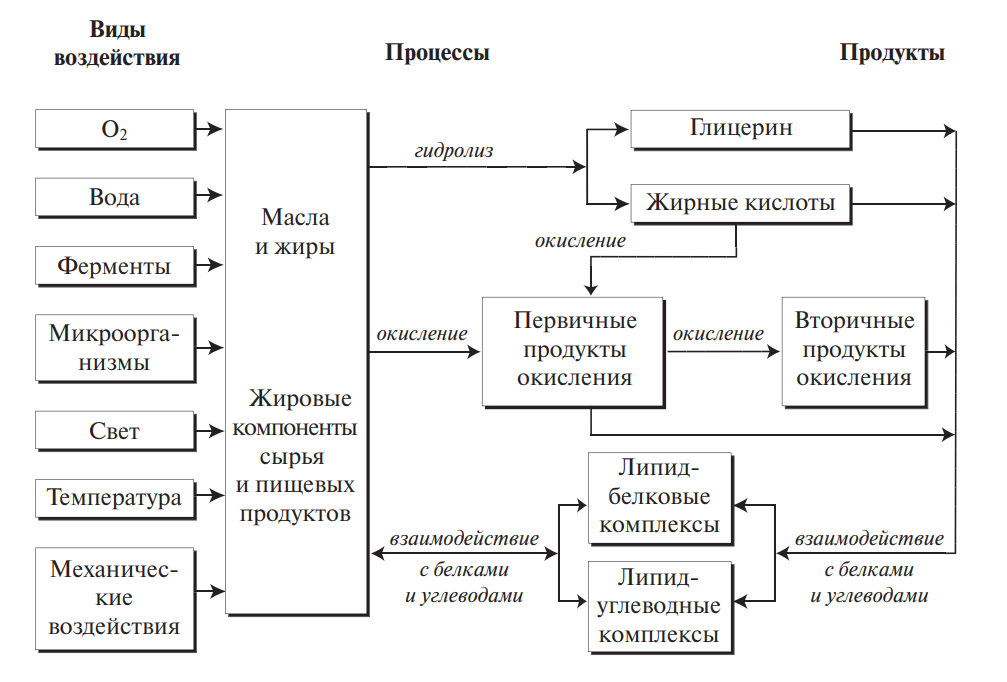
С главными направлениями этих превращений вы познакомились: гидролиз липидов, окислительное и биохимическое прогоркание. Но в пищевом сырье, полуфабрикатах и готовых продуктах они могут протекать одновременно, в виде идущих параллельно, связанных между собой превращений. В упрощенной форме это представлено на рис. 7.
Глубина и интенсивность этих процессов зависят от химического состава липидов, характера сопутствующих, добавляемых и образующихся веществ (например, антиоксидантов, меланоидинов), влажности, присутствия микроорганизмов, активности ферментов, контакта с кислородом воздуха, а следовательно, от способа упаковки жира и многих других факторов. Все перечисленное говорит о многообразии, сложности и противоречивости процессов, протекающих в липидном комплексе. Так, в растительных маслах, содержащих значительное количество ненасыщенных жирных кислот, протекают главным образом процессы автоокисления кислородом воздуха.
Рис. 7. Превращения липидов в технологическом процессе
Благодаря низкой влажности, отсутствию минеральных веществ липиды не поражаются микроорганизмами и в темноте могут храниться относительно длительное время. Лучшими условиями их сохранности в специальных баках-резервуарах являются: температура — 4–6 °С, относительная влажность воздуха — 75 %. В быту их следует хранить в закрытой стеклянной таре в темноте, оставляя минимальным воздушное пространство в бутыли. Животные жиры (говяжий, свиной, бараний) по своему жирно-кислотному составу (незначительное содержание высоконепредельных жирных кислот) должны были бы обладать высокой устойчивостью при хранении. Но они практически не содержат антиоксидантов и это снижает их стойкость.
Наиболее неустойчивыми являются сливочное масло, маргарины, комбинированные масла. Высокая влажность, наличие белковых и минеральных веществ способствуют развитию микрофлоры, а следовательно, интенсивному развитию процессов биохимического прогоркания. Одними из основных факторов, обеспечивающих сохранность сливочного масла и маргарина, являются низкая температура и отсутствие света, внесение консервантов и антиоксидантов (для маргаринов, комбинированных масел). Не менее сложные процессы протекают при хранении в липидном комплексе пищевого сырья и готовых продуктов. Так, при хранении пшеничной муки идут процессы гидролитического и окислительного прогоркания, образующиеся продукты взаимодействуют с белками, влияя на хлебопекарное достоинство пшеничной муки. При развитии окислительных процессов в продуктах накапливаются нежелательные для организма человека вещества, поэтому защита липидов от окисления является важной задачей.