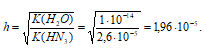- Гидразин
- Структурная формула
- Свойства
- Гидразин как восстановитель
- Обнаружение
- Получение
- Применение
- Токсичность
- Гидразин. Свойства, токсичность
- Физико-химические свойства.
- Токсикокинетика
- Основные проявления интоксикации
- Механизм токсического действия
- Гидразин гидрат (гидразин диамид): о бщее определение
- Применение
- Получение
- Идентификация
- Физические данные
- Пожар и взрыв
- Влияние на организм
- Стабильность
- Разлив и очищение
- Профилактика
- Безопасность
- Гидразин
- Содержание
- Свойства
- Гидразин как восстановитель
- Обнаружение
- Получение
- Применение
- Ракетное топливо
- Токсичность
- Характеристика химических свойств азидоводорода (азотистоводородной кислоты) и его солей
Гидразин
Гидразин в Энциклопедическом словаре:
Гидразин — (диамид) — N2H4, бесцветная жидкость, tпл 1,5 .С, tкип 113,5 .С;неограниченно растворим в воде; взрывоопасен и ядовит. Применяют впроизводстве пластмасс, каучуков, инсектицидов, порообразователей, ВВ; горючий компонент ракетного топлива.
Значение слова Гидразин по словарю Брокгауза и Ефрона:
Гидразин (хим.), или диамид, NH2.(NH2). — При кипячении раствора триазоуксусной (см. это сл.) кислоты с слабой серной кислотой образуется (1887, Курциус) сернокислая соль гидразина и щавелевая кислота: C3H3N6.(CO2H)3 + 6H2O + 3H2SO4 = 3C2H2O4 + 3N2 Н 4.H2SO4. При разложении этой соли щелочью получается гидрат гидразина N 2H4. Н 2 O; он представляет малоподвижную жидкость со слабым, очень неприятным, запахом, сильно преломляющую свет, кипящую при 119°, уд. в. 1,0305.
Гидрат обладает сильными щелочными свойствами, едким щелочным вкусом, пары его, при перегонке, разъедают даже стекло; он смешивается во всех пропорциях с водой и спиртом; застывает в кристаллическую массу при сильном охлаждении (ниже — 40°); при 100° в пустоте остается неразложенным, обладая частицей вышеприведенного состава. Окисьбария, ВаО, отнимает от гидрата воду, при чем выделяется свободный Г. N 2H4 [Его аналог есть жидкийфосфор,водород Р 2H4. По закону замещений (см. это сл.), если азот дает аммиак NH 3. то NH 2 есть одноатомный остаток,способныйзаменять водород.
Если эта замена произойдет в самом аммиаке NH 3, то получится Г. NH 2(NH2). Δ.],который сильно дымить на воздухе, образуя с водяным паромснова гидрат. Г. обладает в высокой степени восстановительной способностью.Кроме вышеупомянутой соли с серной кислотой, трудно растворимой в воде при обыкновенной температуре, известна легкорастворимая (N 2H4)2 Н 2 SО 4. С галоидоводородными кислотами Г. дает соли такого состава: например для соляной кислоты — N 2H3.(HCl)4 и N 2H4.HCl, а для йодисто-водородной кроме того и более сложную (N 2H4)3(HJ)2.
Все эти соли хорошо кристаллизуются. Подобногидроксиламину (см. это слово) Г. реагирует с альдегидами, кетонами, а также с кетонокислотами, образуя сложные производные. Г. получается еще из альдегидаммиака, послеобработки его азотистой кислотой и восстановления, и из продукта восстановления диазоуксусного эфира CHN 2.CO2(C2H5). Продукты замещения водорода гидразина углеводородными остатками, аналогичные аминам, получены раньше самого гидразина.
Это одно и двузамещенные гидразины, NHR. (NH 2) и NR 2(NH2), где R = метилу (CН 3)2, этилу (C 2H5)1, фенилу (C 6H5)1 или другому углеводородному радикалу, эквивалентному одному атому водорода. Производные, содержащие жирные радикалы, получаются при восстановлении нитрозоаминов и нитрозомочевин (замещенных); ароматические производные — при восстановлении диазосоединений; фенилгидразин, например, C 6H5.NH.NH2 хорошо получается при действии смеси олова и соляной кислоты на хлористый диазобензол: C6H5.N2 Cl + 4Н = C 6H5.N2H3.HCl.
Замещенные гидразины, подобно самому гидразину, обладают основными свойствами, образуя соли с одним или двумя (при жирных) эквивалентами кислоты. Они реагируют также с альдегидами и кетонами, образуя гидразоны, а с глюкозами (см. Глюкозы) и озазоны; для получения этих производных пользуются раствором смеси хлористо-водородной соли фенилгидразина с избытком уксуснокислого натрия (реактив Э. Фишера); в таком растворе фенилгидразин находится в свободном виде, потому что соляная к. превращается в хлористый натрий,освобождая уксусную кислоту, с которой фенилгидразин не соединяется.
Многоразличные производные гидразина и замещенных гидразинов носят общее название гидразиновых производных. Симметрично замещенные гидразины называются гидразосоединениями, например гидразобензол (C 6H5)HNNH(C6H5); они получаются при действии восстановляющих веществ на азосоединения (см. это слово), а также из однозамещенных гидразинов: при действии хлортринитробензола на фенилгидразин образуется тринитрогидразобензол: (С 6H2)HN.NH2 + С 6H2(NO2)3Cl = (C6H5)HN. NH.[C6H2(NO2)3] + HCl. С. С. Колотов.Δ.
Гидразин(дополнение к статье) — см. также Нитрогуанидин и Нитрозоамины.
Определение слова «Гидразин» по БСЭ:
Гидразин — диамид, H2N-NH2, бесцветная, гигроскопичная, дымящая на воздухе жидкость; tкип 113,5°C, tпл 2°C, плотность 1,008 г/смі (при 20°C). Г. неограниченно растворим в воде и низших спиртах. Нерастворим в углеводородах и др. органических растворителях. Водные растворы Г. обладают основными свойствами (6/0603831.tif = 8,5· 10−7).
С кислотами образует соли гидразония, например N2H5Cl, N2H6Cl2. Г. характеризуется высокой диэлектрической проницаемостью (52,9 при 20°C) и способен растворятьмногие неорганические соли. Г. — эндотермическое соединение; теплота образования
ΔH°298 (ж) = 50,24 кдж/моль (12,05 ккал/моль). При нагревании до 200-300°C Г. разлагается на N2 и NH3. В присутствии Fe2O3 воспламеняется при комнатной температуре. С воздухом пары Г. при содержании 4,67% по объёму и выше образуют взрывоопасные смеси.
Жидкий Г. не чувствителен к удару, трению и детонации. Токсичен; предельно допустимая концентрация в воздухе 0,0001 мг/л. Получают Г. окислением NH3 или мочевины гипохлоритом. Применяют в органическом синтезе, производстве пластмасс, резины, инсектицидов, взрывчатых веществ, как горючийкомпонент в жидких ракетных топливах. См. также Диметилгидразин.
Лит.: Одрит Л. и Огг Б., Химия гидразина, пер. с англ., М., 1954. В. С. Лапик.

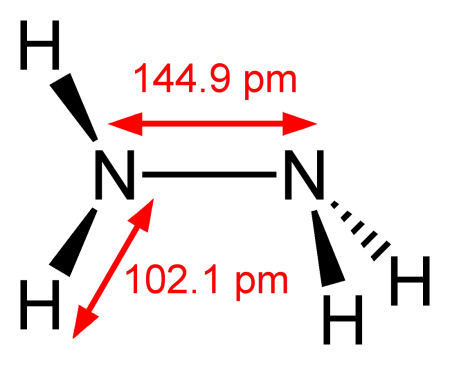
Структурная формула
 |  |
Истинная, эмпирическая, или брутто-формула: H4N2
Химический состав Гидразина
СимволЭлементАтомный весЧисло атомовПроцент массы
| H | Водород | 1.008 | 4 | 12,6% |
| N | Азот | 14.007 | 2 | 87,4% |
Молекулярная масса: 32.046
Гидразин — (диамид) H2N—NH2 — бесцветная, сильно гигроскопическая жидкость с неприятным запахом.
Молекула H4N2 состоит из двух групп NH2, повёрнутых друг относительно друга, что обусловливает полярность молекулы гидразина, μ = 0,62·10−29 Кл · м. Смешивается в любых соотношениях с водой, жидким аммиаком, этанолом; в неполярных растворителях растворяется плохо. Образует органические производные: алкилгидразины и арилгидразины.
Был открыт в 1887 году Теодором Курциусом.
Свойства
Термодинамически гидразин значительно менее устойчив, чем аммиак, так как связь N—N не очень прочна: разложение гидразина — экзотермическая реакция, протекающая в отсутствие катализаторов при 200—300 °С.
Переходные металлы (Co, Ni, Cu, Ag) катализируют разложение гидразина, при катализе платиной, родием и палладием основными продуктами разложения являются азот и водород. Благодаря наличию двух неподелённых пар электронов у атомов азота, гидразин способен к присоединению одного или двух ионов водорода. При присоединении одного протона получаются соединения гидразиния с зарядом 1+, двух протонов — гидразония с зарядом 2+, содержащие соответственно ионы N2H5+ и N2H62+.
Водные растворы гидразина обладают основными свойствами, но его основность значительно меньше, чем у аммиака. Известны соли гидразина — хлорид гидразиния N2H5Cl, сульфат гидразония N2H6SO4 и т. д. Иногда их формулы записывают N2H4 · HCl, N2H4 · H2SO4 и т. д. и называют гидрохлорид гидразина, сульфат гидразина и т. д. Большинство таких солей растворимо в воде. Соли гидразина бесцветны, почти все хорошо растворимы в воде. К числу важнейших относится сульфат гидразина N2H5 · H2SO4.
Гидразин как восстановитель
Гидразин — энергичный восстановитель.
В растворах гидразин обычно также окисляется до азота. Восстановить гидразин до аммиака можно только сильными восстановителями, такими, как Sn2+, Ti3+, водородом в момент выделения (Zn + HCl). Окисляется кислородом воздуха до азота, аммиака и воды. Известны многие органические производные гидразина.
Гидразин, а также гидразин-гидрат, гидразин-сульфат, гидразин-хлорид, широко применяются в качестве восстановителей золота, серебра, платиновых металлов из разбавленных растворов их солей. Медь в аналогичных условиях восстанавливается до закиси. В органическом синтезе гидразин применяется для восстановления карбонильной группы альдегидов и кетонов до метиленовой по Кижнеру—Вольфу (реакция Кижнера—Вольфа), реакция идёт через образование гидразонов, расщепляющихся затем под действием сильных оснований.
Обнаружение
Качественной реакцией на гидразин служит образование окрашенных гидразонов с некоторыми альдегидами, в частности — с p-диметиламинобензальдегидом.
Получение
Гидразин получают окислением аммиака NH3 или мочевины CO(NH2)2 гипохлоритом натрия NaClO (метод Рашига).
Реакция проводится при температуре 160 °C и давлении 2,5−3,0 МПа. Синтез гидразина окислением мочевины гипохлоритом по механизму аналогичен синтезу аминов из амидов по Гофману. Реакция проводится при температуре
100 °C и атмосферном давлении.
Применение
Гидразин применяют в органическом синтезе, в производстве пластмасс, резины, инсектицидов, взрывчатых веществ, в качестве компонента ракетного топлива. Гидразина сульфат применяется в случае таких заболеваний, как неоперабельные прогрессирующие распространенные формы, рецидивы и метастазы злокачественных опухолей — рак легкого (особенно немелкоклеточный), молочных желез, желудка, поджелудочной железы, гортани, эндометрия, шейки матки, десмоидный рак, саркома мягких тканей, фибросаркома, нейробластома, лимфогранулематоз, лимфосаркома (монотерапия или в составе полихимиотерапии).
Гидразин и его производные (метилгидразин, несимметричный диметилгидразин и их смеси (аэрозин)) широко распространены как ракетное горючее.
Они могут быть использованы в паре с самыми разными окислителями, а некоторые и в качестве однокомпонентного топлива, в этом случае рабочим телом двигателя являются продукты разложения на катализаторе. Последнее удобно для маломощных двигателей. Во время Второй мировой войны гидразин применялся в Германии в качестве одного из компонентов топлива для реактивных истребителей «Мессершмитт Ме-163» (C-Stoff, содержащий до 30 % гидрата гидразина) и ракет «Фау-2» (B-Stoff, 75 % гидразина).
ОкислительУдельная тяга (Р1, с*)Температура сгорания °СПлотность топлива г/см³Прирост скорости, ΔVид,25, м/сВесовое содерж.горючего %
| Фтор | 364,4 с | °С | 1,314 | 5197 м/с | 31 % |
| Тетрафторгидразин | 334,7 с | °С | 1,105 | 4346 м/с | 23,5 % |
| Кислород | 312,9 с | °С | 1,065 | 3980 м/с | 52 % |
| Азотная кислота | 279,1 с | °С | 1,254 | 5197 м/с | 40 % |
- Удельная тяга равна отношению тяги к весовому расходу топлива; в этом случае она измеряется в секундах (с = Н·с/Н = кгс·с/кгс).
Для перевода весовой удельной тяги в массовую её надо умножить на ускорение свободного падения (примерно равное 9,81 м/с²)
Гидразин также применяется в качестве топлива в гидразин-воздушных низкотемпературных топливных элементах.
Жидкая смесь гидразина и нитрата аммония используется как мощное взрывчатое средство с нулевым кислородным балансом — астролита, который, однако, в настоящее время практического значения не имеет. Гидразин широко применяется в химической промышленности в качестве восстановителя кислорода, содержащегося в деминерализованной воде, применяемой для питания котлов (котельные установки, производства аммиака, слабой азотной кислоты и др.).
При этом протекает следующая химическая реакция: N2H4 + O2 = N2 + 2H2O.
Токсичность
Гидразин и большинство его производных очень токсичны.
Небольшие концентрации гидразина вызывают раздражение глаз, дыхательных путей. При повышении концентрации начинается головокружение, головная боль и тошнота. Далее следуют судороги, токсический отёк лёгких, а за ними — кома и смерть. ПДК в воздухе рабочей зоны = 0,1 мг/м2. Относится к первому классу опасности.
Гидрази́н (диамид) H2N—NH2 — бесцветная, сильно гигроскопическая жидкость с неприятным запахом.
Молекула N2H4 состоит из двух групп NH2, повёрнутых друг относительно друга, что обусловливает полярность молекулы гидразина, μ = 0,62 Кл · м. Смешивается в любых соотношениях с водой, жидким аммиаком, этанолом; в неполярных растворителях растворяется плохо.
Образует органические производные: алкилгидразины и арилгидразины.
Был открыт в 1887 году Теодором Курциусом.
Термодинамически гидразин значительно менее устойчив, чем аммиак, так как связь N—N не очень прочна: разложение гидразина — экзотермическая реакция, протекающая в отсутствие катализаторов при 200—300 °С:
Переходные металлы (Co, Ni, Cu, Ag) катализируют разложение гидразина, при катализе платиной, родием и палладием основными продуктами разложения являются азот и водород:
Благодаря наличию двух неподелённых пар электронов у атомов азота, гидразин способен к присоединению одного или двух ионов водорода.
При присоединении одного протона получаются соединения гидразиния с зарядом 1+, двух протонов — гидразония с зарядом 2+, содержащие соответственно ионы N2H5+ и N2H62+.
Водные растворы гидразина обладают основными свойствами, но его основность значительно меньше, чем у аммиака:
(для аммиака Kb = 1,78)
Протонирование второй неподеленной пары электронов протекает ещё труднее:
Известны соли гидразина — хлорид гидразиния N2H5Cl, сульфат гидразиния N2H6SO4 и т. д. Иногда их формулы записывают N2H4 · HCl, N2H4 · H2SO4 и т. д. и называют гидрохлорид гидразина, сульфат гидразина и т. д. Большинство таких солей растворимо в воде.
Соли гидразина бесцветны, почти все хорошо растворимы в воде. К числу важнейших относится сульфат гидразина N2H4 · H2SO4.
=== Гидразин как восстановитель === Гидразин — энергичный восстановитель.
В растворах гидразин обычно также окисляется до азота:
Восстановить гидразин до аммиака можно только сильными восстановителями, такими, как Sn2+, Ti3+, водородом в момент выделения (Zn + HCl):
Окисляется кислородом воздуха до азота, аммиака и воды.
Известны многие органические производные гидразина. Гидразин, а также гидразин-гидрат, гидразин-сульфат, гидразин-хлорид, широко применяются в качестве восстановителей золота, серебра, платиновых металлов из разбавленных растворов их солей.
Медь в аналогичных условиях восстанавливается до закиси.
В органическом синтезе гидразин применяется для восстановления карбонильной группы альдегидов и кетонов до метиленовой по Кижнеру—Вольфу (реакция Кижнера—Вольфа), реакция идёт через образование гидразонов, расщепляющихся затем под действием сильных оснований.
=== Обнаружение === Качественной реакцией на гидразин служит образование окрашенных гидразонов с некоторыми альдегидами, в частности — с p-диметиламинобензальдегидом.
== Получение == Гидразин получают окислением аммиака NH3 или мочевины CO(NH2)2 гипохлоритом натрия NaClO (метод Рашига):
реакция проводится при температуре 160 °C и давлении 2,5−3,0 МПа.
Синтез гидразина окислением мочевины гипохлоритом по механизму аналогичен синтезу аминов из амидов по Гофману: :: реакция проводится при температуре
100 °C и атмосферном давлении.
Применяется также метод Байера:
Гидразин применяют в органическом синтезе, в производстве пластмасс, резины, инсектицидов, взрывчатых веществ, в качестве компонента ракетного топлива.
Гидразина сульфат применяется в случае таких заболеваний, как неоперабельные прогрессирующие распространенные формы, рецидивы и метастазы злокачественных опухолей — рак лёгкого (особенно немелкоклеточный), молочных желез, желудка, поджелудочной железы, гортани, эндометрия, шейки матки, десмоидный рак, саркома мягких тканей, фибросаркома, нейробластома, лимфогранулематоз, лимфосаркома (монотерапия или в составе полихимиотерапии).
Гидразин также применяется в качестве топлива в гидразин-воздушных низкотемпературных топливных элементах.
Жидкая смесь гидразина и нитрата аммония используется как мощное взрывчатое средство с нулевым кислородным балансом — астролита, который, однако, в настоящее время практического значения не имеет.
Гидразин широко применяется в химической промышленности в качестве восстановителя кислорода, содержащегося в деминерализованной воде, применяемой для питания котлов (котельные установки, производства аммиака, слабой азотной кислоты и другое).
При этом протекает следующая химическая реакция: N2H4 + O2 = N2 + 2H2O.
Во время Второй мировой войны гидразин применялся в Германии в качестве одного из компонентов топлива для реактивных истребителей «Мессершмитт Ме-163» (C-Stoff, содержащий до 30 % гидрата гидразина).
Гидразин и его производные (метилгидразин, несимметричный диметилгидразин и их смеси (аэрозин)) широко распространены как ракетное горючее.
Они могут быть использованы в паре с самыми разными окислителями, а некоторые и в качестве однокомпонентного топлива, в этом случае рабочим телом двигателя являются продукты разложения на катализаторе.
Последнее удобно для маломощных двигателей.
* Удельная тяга равна отношению тяги к весовому расходу топлива; в этом случае она измеряется в секундах (с = Н·с/Н = кгс·с/кгс). Для перевода весовой удельной тяги в массовую её надо умножить на ускорение свободного падения (примерно равное 9,81 м/с²)
== Токсичность == Гидразин и большинство его производных очень токсичны.
Небольшие концентрации гидразина вызывают раздражение глаз, дыхательных путей. При повышении концентрации начинается головокружение, головная боль и тошнота. Далее следуют судороги, токсический отёк лёгких, а за ними — кома и смерть. ПДК в воздухе рабочей зоны = 0,1 мг/м3. Относится к первому классу опасности.
Категория:Соединения азота Категория:Соединения водорода Категория:Гидразины Категория:Ракетное топливо Категория:Чрезвычайно опасные вещества Категория:Соединения азота по алфавиту
Texte soumis à la licence CC-BY-SA.
Source : Article https://ru.wikipedia.org/wiki/Гидразин de Wikipédia
Гидразин. Свойства, токсичность
Гидразин применяется в производстве лекарств, пластмасс, резин, инсектицидов, взрывчатых веществ, в качестве консерванта и как компонент ракетного топлива.
Физико-химические свойства.
Гидразин – бесцветная маслянистая жидкость с запахом аммиака. Летуч. Плотность пара в 1,1 раза выше плотности воздуха. Вещество хорошо растворяется в воде. Водные растворы обладают свойствами оснований.
Разлагается при нагревании. Гидразин и его производные (монометилгидразин и диметилгидразин) – легковоспламеняющиеся вещества; горят с образованием летучих высокотоксичных нитросоединений.
Летальная доза гидразина для грызунов при введении в желудок составляет около 60 мг/кг, диметилгидразина — 33 мг/кг. При ингаляции паров в течение 4 часов, смертельной является концентрация гидразина 0,32 г/м3, диметилгидразина — 0,11 г/м3 (в 200 — 500 раз менее токсичны, чем зарин).
Токсикокинетика
В организм гидразин и его алкильные производные в виде пара и аэрозоля проникает ингаляционно и через кожу, в виде жидкости – через кожные покровы и при приеме внутрь.
Проникновению веществ через кожу способствует повреждающее действие токсикантов на покровные ткани. С кровью распределяются в органах и тканях, легко проникают через ГЭБ. Элиминация гидразина из организма частично осуществляется за счет выделения с мочой в неизмененном виде, частично за счет метаболизма. Основной путь метаболических превращений – конъюгация с эндогенным уридином, фосфатом, ацетатом при участии соответствующих трансфераз (реакции конъюгации) и биологическое окисление, активируемое микросомальными цитохром-Р450-зависимыми оксидазами смешанной функции, до азота, диимида и диазена.
Пораженные, подвергшиеся санитарной обработке, не представляют опасности для окружающих.
Основные проявления интоксикации
Пары гидразина вызывают сильное раздражение слизистых оболочек глаз, дыхательных путей. При тяжелых поражения возможно развитие токсического отека легких, токсической пневмонии. Жидкий гидразин (в эпицентре аварии) при попадании на кожу или глаза вызывает химический ожог ткани и сопутствующие этому общие реакции организма.
Местное действие на покровные ткани диметилгидразина выражено значительно слабее.
При резорбции гидразина к проявлениям местного действия токсикантов присоединяются признаки поражения ЦНС, крови, печени и почек. Симптоматика отравления развивается спустя 30-90 мин от начала воздействия.
При легкой интоксикации (наиболее вероятная форма поражения в зоне химического заражения) появляются беспокойство, возбуждение, чувство страха, бессонница.
Нарушение работоспособности в течение суток и более.
При поступлении в организм в дозах, близких к смертельным, вещества вызывают тошноту, рвоту, нарушение сознания, клонико-тонические судороги, приступы которых чередуются с периодами ремиссии.
У пострадавших развивается коматозное состояние на фоне нарушений функций сердечно-сосудистой системы (брадикардия, коллапс). По выходе из комы наблюдается психоз с бредом, слуховыми и зрительными галлюцинациями. Состояние психоза может продолжаться в течение нескольких дней.
Характерным проявлением интоксикации являются метгемоглобинемия, гемолиз (метгемоглобинообразование более характерно для арильных производных гидразина, например фенилгидразина).
Максимум снижения содержания эритроцитов в крови отмечается к 10-м суткам.
Механизм токсического действия
Основными механизмами, лежащими в основе токсического действия гидразина и его производных на ЦНС, являются:
1) снижение содержания пиридоксальфосфата в тканях мозга;
2) инактивация ферментов, кофактором которых является пиридоксальфосфат и, в частности, энзимов, участвующих в метаболизме ГАМК;
3) снижение содержания ГАМК и, как следствие этого, подавление тормозных процессов в ЦНС;
4) снижение активности моноаминоксидазы (МАО) и повышение содержания биогенных аминов (норадреналин, дофамина, серотонина) в ЦНС.
Мероприятия медицинской защиты
Специальные санитарно-гигиенические мероприятия:
— использование индивидуальных технических средств защиты (средства защиты кожи и органов дыхания) в зоне химического заражения;
— участие медицинской службы в проведении химической разведки в районе расположения войск; проведение экспертизы воды и продовольствия на зараженность ОВТВ;
— запрет на использование воды и продовольствия из непроверенных источников;
— обучение личного состава правилам поведения на зараженной местности.
Специальные профилактические медицинские мероприятия:
— проведение санитарной обработки пораженных на передовых этапах медицинской эвакуации.
Специальные лечебные мероприятия:
— применение антидотов и средств патогенетической и симптоматической терапии состояний, угрожающих жизни, здоровью, дееспособности, в ходе оказания первой (само-взаимопомощь), доврачебной и первой врачебной (элементы) помощи пострадавшим.
— подготовка и проведение эвакуации
Средства медицинской защиты
При попадании гидразина на поверхность кожи, в глаза первая помощь оказывается в соответствии с общими принципами оказания помощи отравленным.
В отношении легко отравленных осуществляются мероприятия, проводимые при оказании помощи пораженным и другими веществами раздражающего действия. При тяжелых поражениях кожи и глаз мероприятия аналогичны, проводимым при отравлении ипритом.
При ингаляционном поражении мероприятия должны быть направлены на профилактику, а в случае необходимости – на раннее лечение токсического отека легких.
В процессе целенаправленного поиска антидотов резорбтивного действия гидразина испытаны вещества, обладающие химическим, биохимическим и физиологическим антагонизмом к токсиканту.
Биохимическим антагонистом гидразина является пиридоксин.
Людям, отравленным гидразинами, пиридоксин (витамин В6) с лечебной целью вводят в форме 5% раствора в дозе 25 мг/кг (1/4 дозы в/в, 3/4 — в/м); при необходимости инъекцию повторяют через каждые 2 ч.
Эффективными оказались препараты из группы производных бензодиазепина. Эти вещества потенцируют действия ГАМК в ГАМК-эргических синапсах центральной нервной системы. Диазепам (седуксен) в дозе 5-10 мг/кг в 100% случаев предотвращает острую гибель экспериментальных животных, отравленных гидразином в смертельной дозе.
Производные барбитуровой кислоты (фенобарбитал) и оксазолидиндионы (триметадион) также подавляют судороги, вызываемые производными гидразина.
Дибензодиазепины (клозапин) снижают выраженность психотических реакций, развивающихся при легкой и средней степени тяжести отравления гидразином.
Вещества малотоксичны, обладают слабым седативным и гипотензивным действием. Клозапин назначают в дозе 25 — 100 мг (таблетки).
Из указанных препаратов достаточной эффективностью, переносимостью и удобством применения в полевых условиях отличаются диазепам и клозапин, которые и могут быть рекомендованы как средства медицинской защиты: клозапин — при возбуждении, чувстве страха; диазепам — при появлении судорогстроением, но и особенностями токсического действия. Вещества одной группы при тяжелых интоксикациях вызывают развитие судорожного синдрома, комы и гибели пострадавшего, как правило, от остановки дыхания и сердечной деятельности на фоне истощения энергетических ресурсов организма.
Другие – первично вызывают паралич произвольной мускулатуры, в том числе и дыхательной, и гибели от асфиксии.
Гидразин гидрат (гидразин диамид): о бщее определение
Гидразин Гидрат (1:1) с регистрационным номером CAS: 7803-57-8 представляет собой бесцветную дымящуюся жидкость со слабым запахом аммиака. Имеет и другие регистрационные номера: 65209-65-6, 65492-74-2, 79785-97-0.
Химически стабильное вещество, имеет целый ряд несовместимостей.
Принадлежит к категориям: биохимия; реагенты для синтеза олигосахарида; синтетическая органическая химия.
Применение
Вещество гидразин гидрат применяется в производстве и используется в лабораторных условиях:
- в качестве восстановителя для гидрата гидразина;
- в медицине;
- входит в состав пестицидов, красителей, пенообразователей;
- служит антиоксидантом материалов;
- для производства металлов высокой чистоты;
- для изготовления синтетических волокон;
- редко – для изготовления ракет и взрывчатых веществ.
Получение
Есть несколько способов получения гидрата гидразина.
Например, его можно приготовить с помощью мочевины: смешать гипохлорит натрия и гидроксид натрия в определенном соотношении, добавить смесь мочевины и небольшое количество перманганата калия при перемешивании. Затем пропустить пар в реакторе при 103-104°С.
После начала реакции окисления 40% реактива получается путем фракционной перегонки, 80% путем дегидратации с каустической содой – в вакууме.
NH2ONH2 + NaClO + 2NaOH → N2H4·H2O + NaCl + Na2CO3
Идентификация
Название: Гидразин Гидрат / Hydrazine hydrate
Синонимы: Гидразин диамид / Nitrogen hydride; Hydrazine hydroxid; Hydrazine, monohydrate; Hydrazinium hydroxide.
Формула: H4N2·H2O / H6N2O
ГОСТ 5832-76 (не действует)
Физические данные
Физическое состояние: дымящаяся жидкость
Цвет: белый, бесцветный
Форма: кристаллы
Запах: слабый аммиачный
Молекулярная масса: 50.06
Температура кипения: 113.5°C при 760 мм рт.ст.
Температура плавления: 51.5°C
Давление пара: 20,7 мм рт.ст. при 25°С
Плотность: 1.032 г/см3
Растворимость: смешивается со спиртами, немного с углеводородами, не растворим в хлороформе и эфире
Чистота: не ниже 98%
Пожар и взрыв
Температура вспышки: 75ºС
Материал не горит и сгорает с трудом. Для тушения пожара, рядом или в эпицентре которого расположен гидразин гидрат, используется вода.
Может воспламеняться от тепла, искр или пламенны.
Пары могут образовывать с воздухом взрывоопасные смеси.
Влияние на организм
Опасное вещество – гидразин гидрат оказывает негативное влияние на организм: вызывает ожоги, рак, аллергию при контакте с кожей. Пары реагента раздражают слизистые оболочки, носовую полость, горло, верхние дыхательные пути.
Стабильность
Несовместимость: окислители, оксиды тяжелых металлов, обезвоживающие агенты, щелочные металлы, ржавчина, соли серебра.
Остаток от обезвоженного гидразина с барием или оксидом кальция разлагается с выделением тепла в дневное время и, наконец, взрывается.
Разлив и очищение
Крайне токсично для водных организмов, может вызывать долгосрочные неблагоприятные изменения в водной среде.
Удалять гидразин со сточных вод можно с помощью активированного угля и меди ионных катализаторов.
В случае разлива удалить источники возгорания, накрыть место разлива абсорбирующий материалом, собрать в контейнер для утилизации.
Утилизировать необходимо по протоколу утилизации опасных отходов.
Профилактика
Избегать попадания на кожу и в глаза, не вдыхать пары, избегать прямого контакта, не трогать сломанные контейнера.
Смывать водой или мылом с водой, но не в канализацию.
Безопасность
Символ опасности: T, N.
Коды риска:
- 20/21/22 – Опасно при вдыхании, попадании на кожу и проглатывании;
- 45 – Может вызвать рак;
- 34 – Вызывает ожоги;
- 43 – Может вызвать сенсибилизацию при попадании на кожу;
- 51/53 – Токсично для водных организмов, может вызывать продолжительные неблагоприятные изменения в водной среде;
- 50/53 – Очень токсично для водных организмов, может вызывать продолжительные неблагоприятные изменения в водной среде;
- 23/24/25 – Токсично при вдыхании, попадании на кожу и проглатывании;
- 10 – Огнеопасно.
Коды безопасности:
- 45 – В случае аварии или при плохом самочувствии немедленно обратиться за медицинской помощью (по возможности предъявить этикетку материала);
Гидразин
| Гидразин | |
|---|---|
 | |
 | |
 | |
| Систематическое наименование | Гидразин |
| Хим. формула | N2H4 |
| Состояние | бесцветная жидкость |
| Молярная масса | 32,05 г/моль |
| Плотность | 1,01 г/см³ |
| Энергия ионизации | 8,93 ± 0,01 эВ |
| Т. плав. | +2 °C |
| Т. кип. | 114 °C |
| Т. всп. | 99 ± 0 °F |
| Пр. взрв. | 2,9 ± 0,1 об.% |
| Давление пара | 10 ± 1 мм рт.ст. |
| pKa | 8,1 ± 0,01 |
| Растворимость в воде | смешивается |
| Рег. номер CAS | [302-01-2] |
| PubChem | 9321 |
| Рег. номер EINECS | 206-114-9 |
| SMILES | |
| RTECS | MU7175000 |
| ChEBI | 15571 |
| Номер ООН | 2029 |
| ChemSpider | 8960 |
| Пиктограммы СГС |     |
| Приводятся данные для стандартных условий (25 °C, 100 кПа), если не указано иного. | |
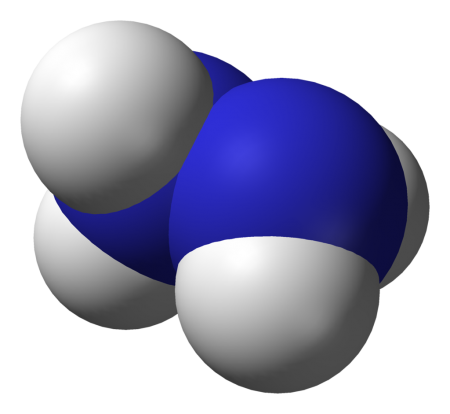
Гидразин (диамин) H2N—NH2 — бесцветная, чрезвычайно токсичная, сильно гигроскопическая жидкость, с неприятным запахом.
Молекула N2H4 состоит из двух групп NH2, повёрнутых друг относительно друга, что обусловливает полярность молекулы гидразина, μ = 0,62⋅10 −29 Кл · м. Смешивается в любых соотношениях с водой, жидким аммиаком, этанолом; в неполярных растворителях растворяется плохо. Образует органические производные: алкилгидразины и арилгидразины.
Был открыт в 1887 году Теодором Курциусом.
Содержание
- 1 Свойства
- 1.1 Гидразин как восстановитель
- 1.2 Обнаружение
- 2 Получение
- 3 Применение
- 3.1 Ракетное топливо
- 4 Токсичность
Свойства
Термодинамически гидразин значительно менее устойчив, чем аммиак, так как связь N—N не очень прочна: разложение гидразина — экзотермическая реакция, протекающая в отсутствие катализаторов при 200—300 °C:
Переходные металлы (Co, Ni, Cu, Ag) катализируют разложение гидразина. При катализе платиной, родием и палладием основными продуктами разложения являются азот и водород:
Благодаря наличию двух неподелённых пар электронов у атомов азота, гидразин способен к присоединению одного или двух ионов водорода. При присоединении одного протона получаются соединения гидразиния с зарядом 1+, двух протонов — гидразония с зарядом 2+, содержащие соответственно ионы N2H5 + и N2H6 2+ . Водные растворы гидразина обладают основными свойствами, но его основность значительно меньше, чем у аммиака:
(для аммиака Kb = 1,78⋅10 −5 )
Протонирование второй неподеленной пары электронов протекает ещё труднее:
Известны соли гидразина — хлорид гидразиния (Гидразин солянокислый) N2H5Cl, сульфат гидразиния (Гидразин сернокислый N2H6SO4 и т. д. Иногда их формулы записывают N2H4 · HCl, N2H4 · H2SO4 и т. д. и называют гидрохлорид гидразина, сульфат гидразина и т. д. Большинство таких солей растворимо в воде.
Соли гидразина бесцветны, почти все хорошо растворимы в воде. К числу важнейших относится сульфат гидразина N2H4 · H2SO4.
Гидразин как восстановитель
Гидразин — энергичный восстановитель. В растворах гидразин обычно также окисляется до азота:
Восстановить гидразин до аммиака можно только сильными восстановителями, такими, как Sn 2+ , Ti 3+ , водородом в момент выделения ( Zn + HCl ):
Окисляется кислородом воздуха до азота, аммиака и воды. Известны многие органические производные гидразина. Гидразин, а также гидразин-гидрат, гидразин-сульфат, гидразин-хлорид, широко применяются в качестве восстановителей золота, серебра, платиновых металлов из разбавленных растворов их солей. Медь в аналогичных условиях восстанавливается до закиси.
В органическом синтезе гидразин применяется для восстановления карбонильной группы альдегидов и кетонов до метиленовой по Кижнеру — Вольфу (реакция Кижнера — Вольфа), реакция идёт через образование гидразонов, расщепляющихся затем под действием сильных оснований.
Обнаружение
Качественной реакцией на гидразин служит образование окрашенных гидразонов с некоторыми альдегидами, в частности — с p-диметиламинобензальдегидом.
Получение
Гидразин получают окислением аммиака NH3 или мочевины CO(NH2)2 гипохлоритом натрия NaClO (метод Рашига):
реакция проводится при температуре 160 °C и давлении 2,5—3,0 МПа.
Синтез гидразина окислением мочевины гипохлоритом по механизму аналогичен синтезу аминов из амидов по Гофману:
реакция проводится при температуре
100 °C и атмосферном давлении.
Применяется также метод Байера:
2NH3 + H2O2 ⟶ N2H4 + 2H2O
Применение
Гидразин применяют в органическом синтезе, в производстве пластмасс, резины, инсектицидов, взрывчатых веществ, в качестве компонента ракетного топлива, как восстановитель при выделении золота из растворов.
Гидразина сульфат применяется в случае таких заболеваний, как неоперабельные прогрессирующие распространённые формы, рецидивы и метастазы злокачественных опухолей — рак лёгкого (особенно немелкоклеточный), молочных желёз, желудка, поджелудочной железы, гортани, эндометрия, шейки матки, десмоидный рак, саркома мягких тканей, фибросаркома, нейробластома, лимфогранулематоз, лимфосаркома (монотерапия или в составе полихимиотерапии).
Гидразин также применяется в качестве топлива в гидразин-воздушных низкотемпературных топливных элементах.
Жидкая смесь гидразина и нитрата аммония используется как мощное взрывчатое средство с нулевым кислородным балансом — астролит, который, однако, в настоящее время практического значения не имеет.
Гидразин широко применяется в химической промышленности в качестве восстановителя кислорода, содержащегося в деминерализованной воде, применяемой для питания котлов (котельные установки, производства аммиака, слабой азотной кислоты и другое). При этом протекает следующая химическая реакция:
Ракетное топливо
Во время Второй мировой войны гидразин применялся в Германии в качестве одного из компонентов топлива для реактивных истребителей «Мессершмитт Ме-163» (C-Stoff, содержащий до 30 % гидрата гидразина).
Гидразин и его производные (метилгидразин, несимметричный диметилгидразин и их смеси (аэрозин)) широко распространены как ракетное горючее. Они могут быть использованы в паре с самыми разными окислителями, а некоторые и в качестве однокомпонентного топлива, в этом случае рабочим телом двигателя являются продукты разложения на катализаторе. Последнее удобно для маломощных двигателей.
| Окислитель | Удельная тяга (P1, с*) | Температура сгорания °C | Плотность топлива г/см³ | Прирост скорости, ΔVид, 25, м/с | Весовое содержание горючего % |
|---|---|---|---|---|---|
| Фтор | 364,4 с | °C | 1,314 | 5197 м/с | 31 % |
| Тетрафторгидразин | 334,7 с | °C | 1,105 | 4346 м/с | 23,5 % |
| ClF3 | 294,6 с | °C | 1,507 | 4509 м/с | 27 % |
| ClF5 | 312,0 с | °C | 1,458 | 4697 м/с | 26,93 % |
| Перхлорилфторид | 295,3 с | °C | 1,327 | 4233 м/с | 40 % |
| Фторид кислорода | 345,9 с | °C | 1,263 | 4830 м/с | 40 % |
| Кислород | 312,9 с | °C | 1,065 | 3980 м/с | 52 % |
| Пероксид водорода | 286,9 с | °C | 1,261 | 4003 м/с | 33 % |
| N2O4 | 291,1 с | °C | 1,217 | 3985 м/с | 43 % |
| Азотная кислота | 279,1 с | °C | 1,254 | 3883 м/с | 40 % |
- Удельная тяга равна отношению тяги к весовому расходу топлива; в этом случае она измеряется в секундах (с = Н·с/Н = кгс·с/кгс). Для перевода весовой удельной тяги в массовую её надо умножить на ускорение свободного падения (примерно равное 9,81 м/с²). В ракетно-космической сфере для обозначения чаще используют термин «удельный импульс тяги» (выражаемый в м/с) или просто «удельный импульс» (в секундах). Выраженная в м/с, эта величина характеризует скорость истечения реактивной струи (приблизительно, с учётом дополнительного слагаемого в формуле тяги ЖРД). Удельный импульс является важнейшей характеристикой совершенства ракетных двигателей. Зависит от типа применяемой топливной пары, схемы и конструкции двигателя и других параметров.
Токсичность
Гидразин и большинство его производных очень токсичны. Небольшие концентрации гидразина вызывают раздражение глаз, дыхательных путей. При повышении концентрации начинается головокружение, головная боль и тошнота. Далее следуют судороги, токсический отёк лёгких, а за ними — кома и смерть. ПДК в воздухе рабочей зоны = 0,1 мг/м 3 . Относится к первому классу опасности
Характеристика химических свойств азидоводорода (азотистоводородной кислоты) и его солей
Задача 891.
Какими свойствами обладает азидоводород (азотистоводородная кислота) и его соли? Можно ли получить НN3 непосредственным взаимодействием азота и водорода? Ответ мотивировать.
Решение:
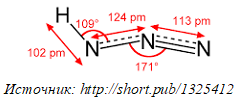
Азидоводород HN3 принадлежит к числу слабых кислот (КD = 3 . 10 -5 ). Структурная формула HN3 имеет вид:
В водном растворе он диссоциирует на ионы Н + и N3 — :
Соли азидоводорода хорошо растворимы в воде, например, азиды щелочных металлов. Сама азотистоводородная кислота и её соли (кроме солей щелочных и щелочно-земельных металлов) являются сильными взрывчатыми веществами.
Азидоводород HN3 получают действием ортофосфорной кислоты на азид натрия NaN3, который синтезируют из амида натрия:
Азидоводород можно получить из гидразина и азотистой кислоты:
Действием серной кислоты на азиды металлов:
Химические свойства азидоводорода
1) Как кислота азидоводород вступает в реакцию нейтрализации с основаниями:
2) Как окислитель азидоводород вступает в реакции окисления-восстановления:
В этих реакциях азидоводород проявляет двойственную функцию как окислителя (понижат степень окисления азота до -3) и как восстановителя (повышат степень окисления азота до 0).
3) Азидоводород как восстановитель:
Восстановительные свойства азидоводорода в растворе обусловлены легкостью превращения его в молекулярный азот:
Азидоводород нельзя получить непосредственно из азота и водорода, так как азот и водород реагируют друг с другом с образованием аммиака.
Задача 892.
Закончить уравнения реакций и указать функцию HN3 (кислотную, окислительную, восстановительную) в каждой из них:
а) HN3 + KMnO4 + H2SO4 ↔ N2 + MnSO4 +;
б) HN3 + 3HI ↔ ;
в) HN3 + Cu ↔ ;
г) HN3 + NaOH ↔ .
Решение:
а) 10HN3 + 2KMnO4 + 3H2SO4 ↔ 15N2 + 2MnSO4 + K2SO4 + 8H2O
Азидоводород в данной реакции проявляет окислительную функцию, является восстановителем.
Азидоводород в данной реакции проявляет восстановительную функции, является окислителем.
Азидоводород в данной реакции проявляет восстановительную функции, является окислителем .
В данной реакции азидоводород проявляет свойства кислоты.
Задача 893.
Вычислить рН 0,1 н. раствора NaN3 и степень гидролиза соли.
Решение:
NaN3 – соль сильного основания и слабой кислоты гидролизуется по аниону:
Избыток ионов ОН – , образующихся при гидролизе соли, придаёт раствору щелочную среду, рН > 7.
Находим рН раствора:
[OH – ] = h . CM = (1,96 . 10 -6 ) . 10 -1 = 1,96 . 10 -5 .
рОН = -lg[OH – ] = -lg1,96 . 10 -6 = 6 – lg1,96 = 6 – 0,29 = 5,71
рН = 14 – рОН = 14 – 5,71 = 8,29.
Ответ: 8,29; 1,96 . 10-6.
Задача 894.
Закончить уравнения реакций:
Какова функция гидразина в этих реакциях?
Решение:
В обеих реакциях гидразин проявляет свойства восстановителя, изменяя степень окисления от -2 до 0.