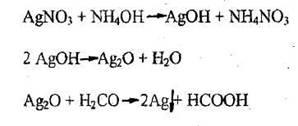Лабораторная работа №2.
Тема: Карбонильные органические соединения.
Цель: исследовать химические свойства и осуществить качественные реакции на карбонильные соединения.
Опыт 1. Цветная реакция на альдегиды с фуксинсернистой кислотой.
Реактивы и материалы: формальдегид, 40%-ный водный раствор; этаналь; фуксинсернистая кислота.
В две пробирки помещают по 2 капли раствора фуксинсернистой кислоты и добавляют в одну из них 2 капли раствора формальдегида, в другую – 2 капли этаналя. Раствор фуксинсернистой кислоты при добавлении раствора формальдегида постепенно окрашивается в фиолетовый цвет, при добавлении этаналя – в розово-фиолетовый цвет.
Опыт 2. Самоокисление водных растворов формальдегида.
Реактивы и материалы: формальдегид, 40%-ный водный раствор, метиловый красный, раствор.
В пробирку помещают 2—3 капли раствора формальдегида и добавляют 1 каплю индикатора метилового красного. Раствор принимает красную окраску, что указывает на кислую реакцию.
Альдегиды очень легко окисляются. В водных растворах они могут окисляться до кислоты за счет кислорода другой молекулы альдегида, восстанавливая ее в спирт — происходит реакция окислительного восстановления (дисмутации):
H-C-H + H-C-H → HCOOH + CH3OH
Опыт 3. Окисление альдегидов аммиачным раствором оксида серебра (реакция «серебряного зеркала»).
Реактивы и материалы: формальдегид, 40%-ный водный раствор; аммиак, 2 н. раствор; нитрат серебра, 0,2 н. раствор.
В чистую пробирку вводят 2 капли раствора нитрата серебра и прибавляют каплю аммиака. Образующийся бурый осадок гидроксида серебра растворяют, добавляя избыток (1-2 капли) раствора аммиака.
Затем прибавляют каплю раствора формальдегида и медленно подогревают содержимое пробирки над пламенем горелки. При осторожном нагревании содержимое пробирки буреет и на ее стенках может выделиться серебро в виде блестящего зеркального налета (комплексный ион металла восстанавливается до металлического серебра). Альдегид окисляется до кислоты, которая образует аммониевую соль.
Опыт 4. Окисление альдегидов гидроксидом меди (II).
Реактивы и материалы: формальдегид, 40%-ный водный раствор; сульфат меди CuSO4, 0,2 н. раствор; едкий натр, 2 н. раствор.
В пробирку помещают 4 капли раствора едкого натра, разбавляют 4 каплями воды и добавляют 2 капли раствора сульфата меди (II). К выпавшему осадку гидроксида меди (II) прибавляют 1 каплю раствора формальдегида и взбалтывают содержимое пробирки.
Нагревают над пламенем горелки до кипения только верхнюю часть раствора так, чтобы нижняя часть оставалась для контроля холодной. В нагретой части пробирки выделяется желтый осадок гидроксида меди (I) (СuОН), переходящий в красный оксид меди (I) (Сu2О), а иногда на стенках пробирки выделяется даже металлическая медь.
Повторите этот опыт, заменив раствор формальдегида раствором этаналя.
Опыт 5. Реакция бензальдегида с гидросульфитом натрия.
Реактивы и оборудование: бензальдегид; гидросульфит натрия (насыщенный раствор); водяная баня.
В пробирку помещают 3 капли бензойного альдегида, добавляют 5 капель насыщенного раствора гидросульфита натрия и энергично встряхивают смесь. Образуются кристаллы гидросульфитного соединения.
Затем к смеси добавляют 6 капель воды и помещают пробирку в горячую водяную баню. Кристаллы быстро исчезают, в растворе появляются маслянистые капли ощущается характерный запах бензальдегида.
При нагревании в водном растворе гидросульфитное соединение легко разлагается на исходные вещества:
Опыт 6. Свойства ализарина.
Реактивы и оборудование: ализарин; алюминиевые квасцы, насыщенный водный раствор; едкий нарт, 0,1 н. раствор; белая хлопчатобумажная ткань; фарфоровая чашка.
В пробирку помещают 3-5 капель ализарина, добавляют 6 капель щелочи и тщательно взбалтывают. Получается раствор, окрашенный в фиолетовый цвет.
1.В пробирку помещают 2 капли раствора ализарина и добавляют 3 капли раствора квасцов. Образуется оранжево-красный осадок алюминиевого ализаринового лака.
2.Кусочек белой ткани простирывают с мылом и тщательно прополаскивают в воде. В фарфоровую чашечку наливают раствор квасцов, пропитывают им ткань и отжимают.
В пробирку помещают 5 капель щелочного раствора ализарина, нагревают и в горячий раствор погружают кусочек «протравленной» ткани на 1-2 мин. Затем ткань, окрашенную в красный цвет, промывают водой.
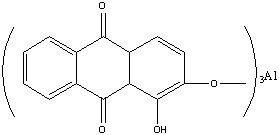
Ализарин — протравной краситель. С алюминиевой протравой он дает ярко-красную окраску; с оловянной — фиолетово-красную; с железной — черно-фиолетовую. С ионами этих металлов ализарин образует хелатные соединения за счет групп С=О и группы -ОН, находящейся в α-положении:
Видео:Качественная реакция на ФОРМАЛЬДЕГИД. Реакция с САЛИЦИЛОВОЙ и КОНЦЕНТРИРОВАННОЙ СЕРНОЙ КИСЛОТАМИ.Скачать

Фуксинсернистая кислота формальдегид уравнение реакции
16 лет успешной работы в сфере подготовки к ЕГЭ и ОГЭ!
1602 поступивших (100%) в лучшие вузы Москвы
Подготовка к ЕГЭ, ОГЭ и предметным Олимпиадам в Москве
| До окончания записи осталось: | |||||||
| Записаться на экспресс-курс! | |||||||
- home
- map
У Вас возникли вопросы?
Мы обязательно Вам перезвоним:
Качественная реакция на альдегиды с фунсинсернистой кислотой
Формалин – это раствор формальдегида с концентрацией 40%. Качественные реакции на формалин – это цветные реакции на определение альдегидной группы в составе формальдегида. Одной из них является реакция с фуксинсернистой кислотой.
Качественная реакция на формалин проводится следующим образом: бесцветный раствор фуксинсернистой кислоты смешивается с бесцветным раствором формалина. Постепенно раствор окрашивается в фиолетовый цвет — качественная реакция на формалин. Значит в растворе есть альдегид.
Видео:Качественная реакция на альдегиды с фуксинсернистой кислотойСкачать

Формальдегид. Химико-токсикологический анализ.
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
Формальдегид
Формальдегид (от лат. formica «муравей») — бесцветный газ с резким запахом, хорошо растворимый в воде, спиртах и полярных растворителях. Ирритант, токсичен.
Формальдегид НСНО (муравьиный альдегид, метаналь) представляет собой бесцветный газ с резким раздражающим запахом. Хорошо растворим в воде, спиртах и других полярных растворителях. Чистый газообразный формальдегид относительно стабилен при 80-100 °С, при температурах ниже 80 °С полимеризуется; процесс ускоряется в присутствии полярных растворителей, в том числе воды.
Формалин – водный раствор формальдегида (обычно 37 – 40 %), содержащий 6-15 % метанола (ингибитор полимеризации формальдегида). Представляет собой бесцветную жидкость с характерным острым запахом.
Формальдегид используют в органическом синтезе, в производстве синтетических смол и пластмасс, для синтеза многих лекарственных средств и красителей, для дубления кож, как дезинфицирующее, антисептическое и дезодорирующее средство.
При вдыхании воздуха, содержащего большое количество формальдегида, развиваются явления острого отравления со слезотечением, резким кашлем, чувством стеснения в груди.
При приёме внутрь (в большинстве случаев ошибочном) в результате всасывания формальдегида наблюдается потеря сознания, судороги, угнетение нервных центров, раздражение почек.
Качественное обнаружение
- Реакция с резорцином в щелочной среде
Появляется розовая или малиновая окраска.
Реакция не специфична (дают алкилгалогениды и др.).
Чувствительность 0,03 мкг.
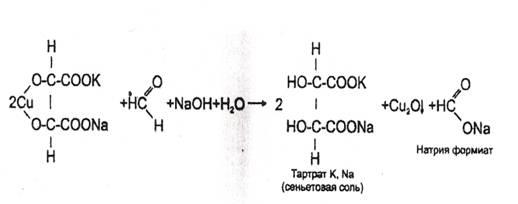
- Реакция с реактивом Фелинга
В пробирку вносят 1 мл исследуемого раствора, прибавляют 1–2 кап. 10% раствора гидроксида натрия до щелочной реакции (по лакмусу), а затем добавляют 2-3 кап. реактива Фелинга (готовится перед употреблением путем смешивания равных количеств растворов Фелинга №1 и №2).
Жидкость сильно взбалтывают и нагревают. При охлаждении на дне пробирки виден желтый или красный осадок оксида меди (I).
Реакция не специфична (дают алкилгалогениды и другие). Имеет отрицательное судебно-химическое значение.
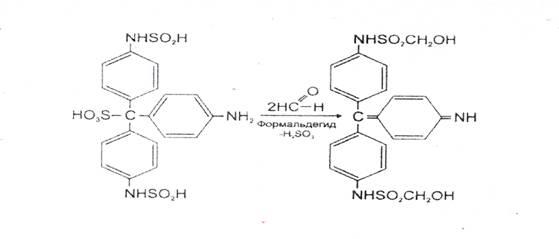
3. Реакция с фуксинсернистой кислотой (реактив Шиффа)
Появляется сине- или красно-фиолетовая окраска, иногда не сразу, а через 10-15 мин.
Чувствительность реакции 0,03 мкг.
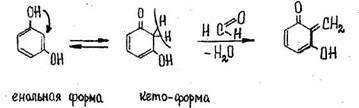
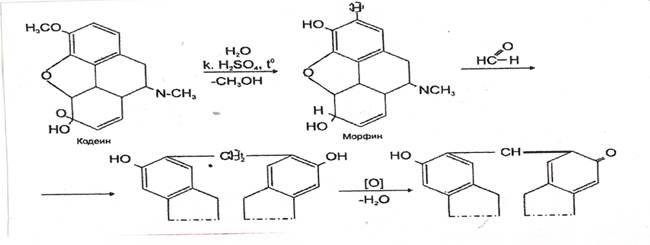
4. Реакция с кодеином и концентрированной серной кислотой
Через 5-10 мин. появляется сине – или красно-фиолетовое окрашивание.
Реакция специфична, имеет положительное судебнохимическое значение.
Чувствительность реакции 0,02 мкг.
- Реакция с хромотроповой кислотой (1,8-диоксинафталтн-3,6-дисульфокислота) в присутствии концентрированной серной кислоты
В фарфоровую чашку вносят 1 мл исследуемого раствора, а затем прибавляют 5 мл концентрированной кислоты серной и несколько кристаллов кислоты хромотроповой. Наблюдается фиолетовая или красно-фиолетовая окраска.
Реакция специфична, имеет положительное судебно-химическое значение. Чувствительность 1 мкг.
- Реакция восстановления ионов серебра (реакция «серебряного зеркала»)
Реакция не специфична, имеет отрицательное судебно-химическое значение.
Чувствительность реакции – сотые доли микрограмма.
🎬 Видео
Опыты по химии. Взаимодействие формальдегида с фуксинсернистой кислотойСкачать

10.3. Альдегиды и кетоны: Химические свойства. ЕГЭ по химииСкачать

Кач. реакция на альдегиды с фунсинсернистой кислотойСкачать

Получение фуксинсернистой кислотыСкачать

Качественная реакция на альдегиды с гидроксидом медиСкачать

Качественная реакция на формальдегид с хромотроповой кислотойСкачать

Опыты по химии. Окисление муравьиного альдегида гидроксидом меди (II)Скачать

Синтез ФОРМАЛЬДЕГИД HCOH. Реакция УРОТРОПИНА и СЕРНОЙ КИСЛОТЫ. Опыты по химии. Chemical experimentsСкачать

25. Схема реакции и химическое уравнениеСкачать

Качественные реакции на альдегидыСкачать

Качественная реакция на альдегиды с фуксинсернистой кислотой (Введение)Скачать

Подлинность ДИМЕДРОЛА. Реакция с концентрированной СЕРНОЙ и АЗОТНОЙ КИСЛОТОЙ. Опыты по химииСкачать

Качественная реакция на альдегиды с фуксинсернистой кислотой (Вывод)Скачать

Формальдегид. Химические свойства.Скачать

РЕАКЦИЯ ЭТЕРИФИКАЦИИСкачать

Окислительно-восстановительные реакции в кислой среде. Упрощенный подход.Скачать

65. Что такое реакция гидратации и реакция дегидратацииСкачать

Реакции окисления, нуклеофильного присоединения альдегидов и кетонов. 11 класс.Скачать