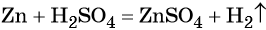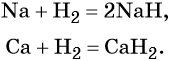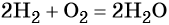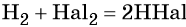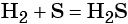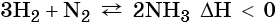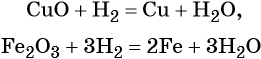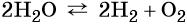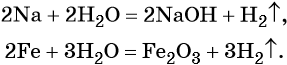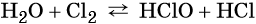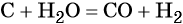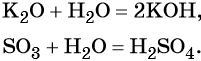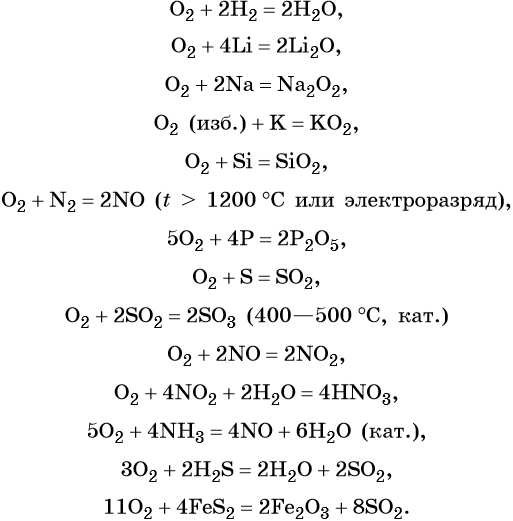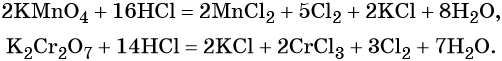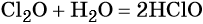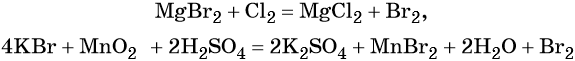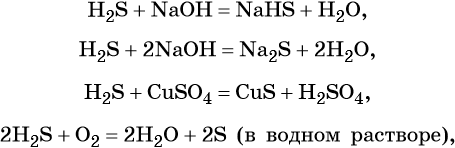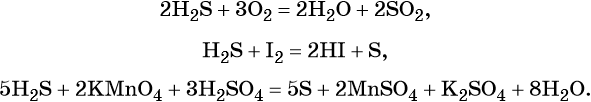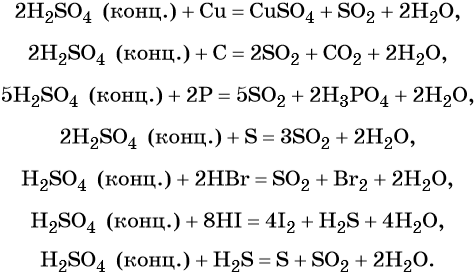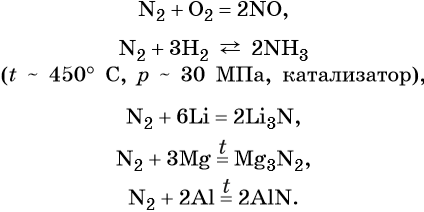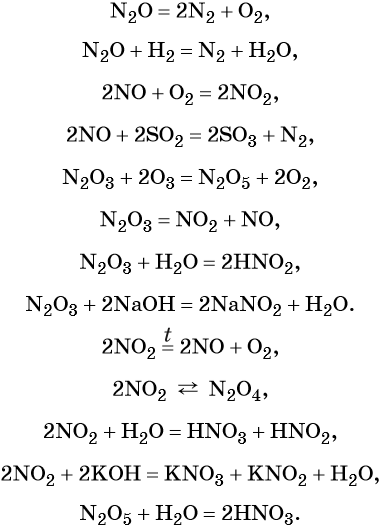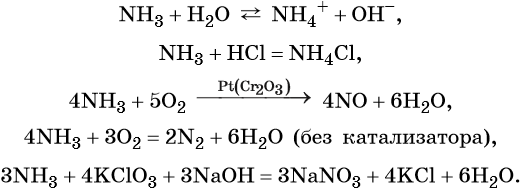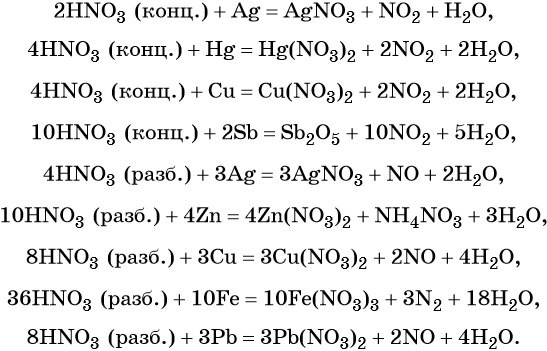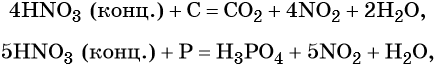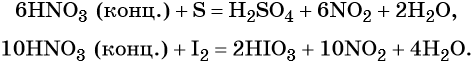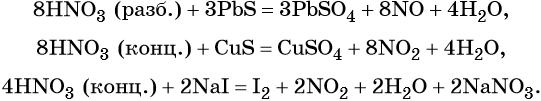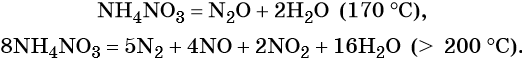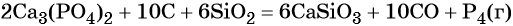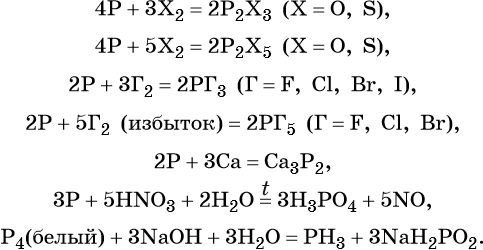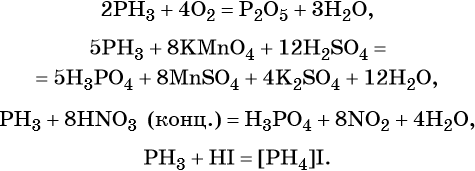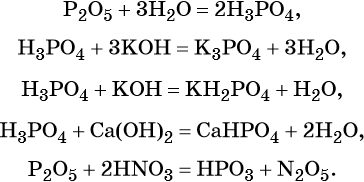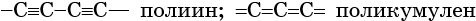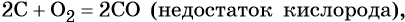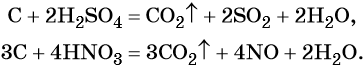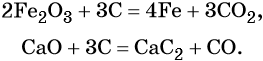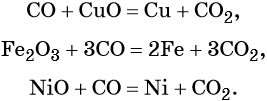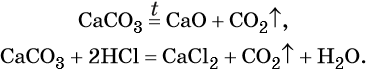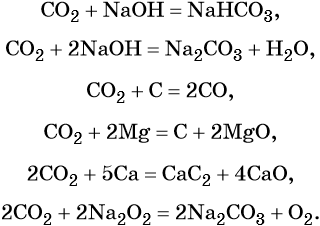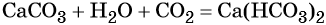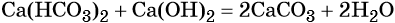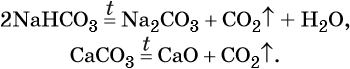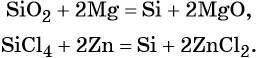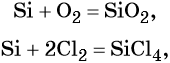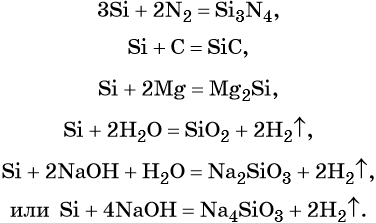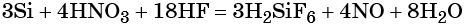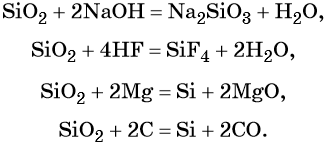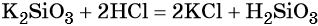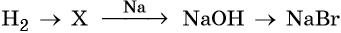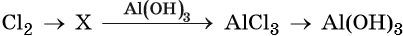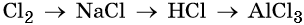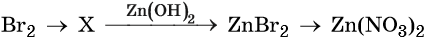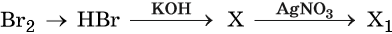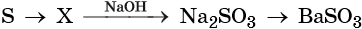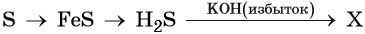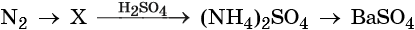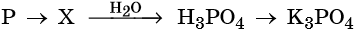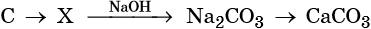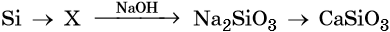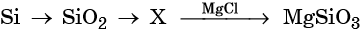- Фосфор
- Положение в периодической системе химических элементов
- Электронное строение фосфора
- Физические свойства и нахождение в природе
- Соединения фосфора
- Способы получения фосфора
- Химические свойства фосфора
- Фосфин
- Строение молекулы и физические свойства
- Способы получения фосфина
- Химические свойства фосфина
- Фосфиды
- Способы получения фосфидов
- Химические свойства фосфидов
- Оксиды фосфора
- Оксид фосфора (III)
- Оксид фосфора (V)
- Фосфорная кислота
- Строение молекулы и физические свойства
- Способы получения
- Химические свойства
- Фосфористая кислота
- Соли фосфорной кислоты — фосфаты
- 2.3.3. Химические свойства азота и фосфора.
- Химические свойства азота
- Взаимодействие азота с металлами
- Взаимодействие азота с неметаллами
- Взаимодействие азота со сложными веществами
- Химические свойства фосфора
- Взаимодействие фосфора с неметаллами
- Взаимодействие фосфора с металлами
- Взаимодействие фосфора со сложными веществами
- Химические свойства простых веществ-неметаллов: водорода, кислорода, галогенов, серы, азота, фосфора, углерода, кремния
- Водород
- Кислород
- Галогены
- Фосфор
- Углерод
- Кремний
- Тренировочные задания
Фосфор
Положение в периодической системе химических элементов
Фосфор расположен в главной подгруппе V группы (или в 15 группе в современной форме ПСХЭ) и в третьем периоде периодической системы химических элементов Д.И. Менделеева.
Электронное строение фосфора
Электронная конфигурация фосфора в основном состоянии :
Атом фосфора содержит на внешнем энергетическом уровне 3 неспаренных электрона и одну неподеленную электронную пару в основном энергетическом состоянии. Следовательно, атом фосфора может образовывать 3 связи по обменному механизму. Однако, в отличие от азота, за счет вакантной 3d орбитали атом фосфора может переходить в возбужденное энергетическое состояние.
Электронная конфигурация фосфора в возбужденном состоянии:
При этом один электрон из неподеленной электронной пары на 3s-орбитали переходит на переходит на 3d-орбиталь. Для атома фосфора в возбужденном энергетическом состоянии характерна валентность V.
Таким образом, максимальная валентность фосфора в соединениях равна V (в отличие от азота). Также характерная валентность фосфора в соединениях — III.
Степени окисления атома фосфора – от -3 до +5. Характерные степени окисления -3, 0, +1, +3, +5.
Физические свойства и нахождение в природе
Фосфор образует различные простые вещества (аллотропные модификации).
Белый фосфор — это вещество состава P4. Мягкий, бесцветный, ядовитый, имеет характерный чесночный запах. Молекулярная кристаллическая решетка, а следовательно, невысокая температура плавления (44°С), высокая летучесть. Очень реакционно способен, самовоспламеняется на воздухе.
Покрытие бумаги раствором белого фосфора в сероуглероде. Спустя некоторое время, когда сероуглерод испаряется, фосфор воспламеняет бумагу (процесс лег в основу различных фокусов с самовозгоранием или получением огня из ничего):
Белый фосфор можно расплавить в ёмкости с тёплой водой, поскольку он имеет температуру плавления в 44,15 °C.
Красный фосфор – это модификация с атомной кристаллической решеткой . Формула красного фосфора Pn, это полимер со сложной структурой. Твердое вещество без запаха, красно-бурого цвета, не ядовитое. Это гораздо более устойчивая модификация, чем белый фосфор. В темноте не светится. Образуется из белого фосфора при t=250-300 о С без доступа воздуха.
Черный фосфор – то наиболее стабильная термодинамически и химически наименее активная форма элементарного фосфора. Чёрный фосфор — это чёрное вещество с металлическим блеском, жирное на ощупь и весьма похожее на графит, полностью нерастворимое в воде или органических растворителях.
Известны также такие модификации, как желтый фосфор и металлический фосфор. Желтый фосфор – это неочищенный белый фосфор. При очень высоком давлении фосфор переходит в новую модификацию – металлический фосфор , который очень хорошо проводит электрический ток.
В природе фосфор встречается только в виде соединений. В основном это апатиты (например, Ca3(PO4)2), фосфориты и др. Фосфор входит в состав важнейших биологических соединений —фосфолипидов.
Соединения фосфора
Типичные соединения фосфора:
| Степень окисления | Типичные соединения |
| +5 | оксид фосфора (V) P2O5 ортофосфорная кислота H3PO4 метафосфорная кислота HPO3 Галогенангидриды: PОCl3, PCl5 |
| +3 | Оксид фосфора (III) P2O3 Галогенангидриды: PCl3 |
| +1 | Фосфорноватистая кислота H3PO2 Соли фосфорноватистой кислоты — гипофосфиты: MeH2PO2 |
| -3 | Фосфин PH3 Фосфиды металлов MeP |
Способы получения фосфора
1. Белый фосфор получают из природных фосфатов , прокаливая их с коксом и песком в электрической печи:
2. Вместо фосфатов можно использовать другие неорганические соединения фосфора, например , метафосфорную кислоту.
4HPO3 + 10C → P4 + 2H2O + 10 CO
3. Красный и черный фосфор получают из белого фосфора.
Химические свойства фосфора
При нормальных условиях фосфор довольно химически активен.
1. Фосфор проявляет свойства окислителя (с элементами, которые расположены ниже и левее в Периодической системе) и свойства восстановителя (с элементами, расположенными выше и правее). Поэтому фосфор реагирует с металлами и неметаллами .
1.1. При взаимодействии с кислородом воздуха образу
ются оксиды – ангидриды соответствующих кислот :
Горение белого фосфора:
Горение красного фосфора:
1.2. При взаимодействии фосфора с галогенами образуются галогениды с общей формулой PHal3 и PHal5:
Фосфор реагирует с бромом:
1.3. При взаимодействии фосфора с серой образуются сульфиды:
1.4. При взаимодействии с металлами фосфор проявляет свойства окислителя, продукты реакции называют фосфидами.
Например , кальций и магний реагируют с фосфором с образованием фосфидов кальция и магния:
Еще пример : натрий взаимодействует с фосфором с образованием фосфида натрия:
P + 3Na → Na3P
1.5. С водородом фосфор непосредственно не взаимодействует.
2. Со сложными веществами фосфор реагирует, проявляя окислительные и восстановительные свойства. Фосфор диспропорционирует при взаимодействии с некоторыми веществами.
2.1. При взаимодействии с окислителями фосфор окисляется до оксида фосфора (V) или до фосфорной кислоты.
Например , азотная кислота окисляет фосфор до фосфорной кислоты:
Серная кислота также окисляет фосфор:
Соединения хлора, например , бертолетова соль , также окисляют фосфор:
Реакция красного фосфора с бертолетовой солью. Этот процесс заложен в принципе возгорания спички при трении её о шершавую поверхность коробка.
Некоторые металлы-сильные окислители также окисляют фосфор. Например , оксид серебра (I) :
2.2. При растворении в щелочах фосфор диспропорционирует до гипофосфита и фосфина.
Например , фосфор реагирует с гидроксидом калия:
Или с гидроксидом кальция:
Фосфин
Строение молекулы и физические свойства
Фосфин PH3 – это бинарное соединение водорода с фосфором, относится к летучим водородным соединениям. Следовательно, фосфин газ, с неприятным запахом, бесцветный, мало растворимый в воде, химически нестойкий и ядовитый. Водородные связи между молекулами фосфина не образуются. В твердом состоянии имеет молекулярную кристаллическую решетку.
Геометрическая форма молекулы фосфина похожа на структуру аммиака — правильная треугольная пирамида. Но валентный угол H-P-H меньше, чем угол H-N-H в аммиаке и составляет 93,5 о .
У атома фосфора в фосфине на внешнем энергетическом уровне остается неподеленная электронная пара. Эта электронная пара оказывает значительное влияние на свойства фосфина, а также на его структуру. Электронная структура фосфина — тетраэдр , с атомом фосфора в центре.
Способы получения фосфина
В лаборатории фосфин получают водным или кислотным гидролизом фосфидов – бинарных соединений фосфора и металлов.
Например , фосфин образуется при водном гидролизе фосфида кальция:
Или при кислотном гидролизе, например , фосфида магния в соляной кислоте:
Еще один лабораторный способ получения фосфина – диспропорционирование фосфора в щелочах.
Например , фосфор реагирует с гидроксидом калия с образованием гипофосфита калия и фосфина:
Химические свойства фосфина
1. В водном растворе фосфин проявляет очень слабые основные свойства (за счет неподеленной электронной пары). Принимая протон (ион H + ), он превращается в ион фосфония. Основные свойства фосфина гораздо слабее основных свойств аммиака. Проявляются при взаимодействии с безводными кислотами .
Например , фосфин реагирует с йодоводородной кислотой:
Соли фосфония неустойчивые, легко гидролизуются.
2. Фосфин PH3 – сильный восстановитель за счет фосфора в степени окисления -3. На воздухе самопроизвольно самовоспламеняется:
3. Как сильный восстановитель, фосфин легко окисляется под действием окислителей.
Например , азотная кислота окисляет фосфин. При этом фосфор переходит в степень окисления +5 и образует фосфорную кислоту.
Серная кислота также окисляет фосфин:
С фосфином также реагируют другие соединения фосфора, с более высокими степенями окисления фосфора.
Например , хлорид фосфора (III) окисляет фосфин:
2PH3 + 2PCl3 → 4P + 6HCl
Фосфиды
Фосфиды – это бинарные соединения фосфора и металлов или некоторых неметаллов .
Способы получения фосфидов
Фосфиды получают при взаимодействии фосфора с металлами . При этом фосфор проявляет свойства окислителя.
Например , фосфор взаимодействует с магнием и кальцием:
Фосфор взаимодействует с натрием:
P + 3Na → Na3P
Химические свойства фосфидов
1. Фосфиды легко разлагаются водой или кислотами с образованием фосфина.
Например , фосфид кальция разлагается водой:
Фосфид магния разлагается соляной кислотой:
2. Фосфиды металлов проявляют сильные восстановительные свойства за счет фосфора в степени окисления -3 .
Оксиды фосфора
| Оксиды азота | Цвет | Фаза | Характер оксида |
| P2O3 Оксид фосфора (III), фосфористый ангидрид | белый | твердый | кислотный |
| P2O5 Оксид фосфора(V), фосфорный ангидрид | белый | твердый | кислотный |
Оксид фосфора (III)
Оксид фосфора (III) – это кислотный оксид . Белые кристаллы при обычных условиях. Пары состоят из молекул P4O6.
Получить оксид фосфора (III) можно окислением фосфора при недостатке кислорода :
Химические свойства оксида фосфора (III):
Оксид фосфора (III) очень ядовит и неустойчив. Для P2O3 (P4O6) характерны два типа реакций.
1. Поскольку фосфор в оксиде фосфора (III) проявляет промежуточную степень окисления, то он принимает участие в окислительно-восстановительных процессах, повышая либо понижая степень окисления атома фосфора. Характерны для P2O3 реакции диспропорционирования.
Например , оксид фосфора (III) диспропорционирует в горячей воде:
2. При взаимодействии с окислителями P2O3 проявляет свойства восстановителя.
Например , N2O окисляется кислородом:
3. С другой стороны Р2О3 проявляет свойства кислотного оксида (ангидрид фосфористой кислоты), взаимодействуя с водой с образованием фосфористой кислоты:
а со щелочами – с образованием солей (фосфитов):
Оксид фосфора (V)
Оксид фосфора (V) – это кислотный оксид. В нормальных условиях образует белые кристаллы. В парах состоит из молекул P4О10. Очень гигроскопичен (используется как осушитель газов и жидкостей).
Способы получения. Оксид фосфора (V) получают сжиганием фосфора в избытке кислорода.
Химические свойства.
1. Оксид фосфора (V) – очень гигроскопичное вещество, которое используется для осушения газов. Обладая высоким сродством к воде, оксид фосфора (V) дегидратирует до ангидридов неорганические и органические кислоты.
Например , оксид фосфора (V) дегидратирует серную, азотную и уксусную кислоты:
2. Фосфорный ангидрид является типичным кислотным оксидом , взаимодействует с водой с образованием фосфорных кислот:
В зависимости от количества воды и от других условий образуются мета-фосфорная, орто-фосфорная или пиро-фосфорная кислота:
Видеоопыт взаимодействия оксида фосфора с водой можно посмотреть здесь.
3. Как кислотный оксид, оксид фосфора (V) взаимодействует с основными оксидами и основаниями .
Например , оксид фосфора (V) взаимодействует с гидроксидом натрия. При этом образуются средние или кислые соли:
Еще пример : оксид фосфора взаимодействует с оксидом бария (при сплавлении):
Фосфорная кислота
Строение молекулы и физические свойства
Фосфор в степени окисления +5 образует несколько кислот: орто-фосфорную H3PO4, мета-фосфорную HPO3, пиро-фосфорную H4P2O7.
Фосфорная кислота H3PO4 – это кислота средней силы, трехосновная, прочная и нелетучая. При обычных условиях фосфорная кислота – твердое вещество, хорошо растворимое в воде и гигроскопичное.
Валентность фосфора в фосфорной кислоте равна V.
При температуре выше +213 °C орто-фосфорная кислота переходит в пирофосфорную H4P2O7.
При взаимодействии высшего оксида фосфора с водой на холоде образуется метафосфорная кислота HPO3, представляющая собой прозрачную стекловидную массу.
Способы получения
Наибольшее практическое значение из фосфорных кислот имеет орто-фосфорная кислота.
1. Получить орто-фосфорную кислоту можно взаимодействием оксида фосфора (V) с водой:
2. Еще один способ получения фосфорной кислоты — вытеснение фосфорной кислоты из солей (фосфатов, гидрофосфатов и дигидрофосфатов) под действием более сильных кислот (серной, азотной, соляной и др.) .
Промышленный способ получения фосфорной кислоты обработка фосфорита концентрированной серной кислотой:
3. Фосфорную кислоту также можно получить жестким окислением соединений фосфора в водном растворе в присутствии кислот.
Например , концентрированная азотная кислота окисляет фосфор до фосфорной кислоты:
Химические свойства
Фосфорная кислота – это кислота средней силы (по второй и третьей ступени слабая) .
1. Фосфорная кислота частично и ступенчато диссоциирует в водном растворе.
HPO4 2– ⇄ H + + PO4 3–
2. Фосфорная кислота реагирует с основными оксидами, основаниями, амфотерными оксидами и амфотерными гидроксидами.
Например , фосфорная кислота взаимодействует с оксидом магния:
Еще пример : при взаимодействии фосфорной кислоты с гидроксидом калия образуются фосфаты, гидрофосфаты или дигидрофосфаты:
3. Фосфорная кислота вытесняет более слабые кислоты из их солей (карбонатов, сульфидов и др.). Также фосфорная кислота вступает в обменные реакции с солями.
Например , фосфорная кислота взаимодействует с гидрокарбонатом натрия:
4. При нагревании H3PO4 до 200°С происходит отщепление от нее молекулы воды с образованием пирофосфорной кислоты H2P2O7:
5. Фосфорная кислота взаимодействует с металлами, которые расположены в ряду активности металлов до водорода. При этом образуются соль и водород.
Например , фосфорная кислота реагирует с магнием:
Фосфорная кислота взаимодействует также с аммиаком с образованием солей аммония:
7. Качественная реакция на фосфат-ионы и фосфорную кислоту — взаимодействие с нитратом серебра. При этом образуется ярко-желтый осадок фосфата серебра:
Видеоопыт взаимодействия фосфата натрия и нитрата серебра в растворе (качественная реакция на фосфат-ион) можно посмотреть здесь.
Фосфористая кислота
Фосфористая кислота H3PO3 — это двухосновная кислородсодержащая кислота. При нормальных условиях бесцветное кристаллическое вещество, хорошо растворимое в воде.
Валентность фосфора в фосфористой кислота равна V, а степень окисления +3.
Получение фосфористой кислоты.
Фосфористую кислоту можно получить гидролизом галогенидов фосфора (III).
Например , гидролизом хлорида фосфора (III):
Фосфористую кислоту можно получить также взаимодействием оксида фосфора (III) с водой:
Химические свойства.
1. Фосфористая кислота H3PO3 в водном растворе — двухосновная кислота средней силы. Взаимодействует с основаниями с образованием солей-фосфитов.
Например , при взаимодействии с гидроксидом натрия фосфористая кислота образует фосфит натрия:
2. При нагревании фосфористая кислота разлагается на фосфин (Р -3 ) и фосфорную кислоту (Р +5 ):
3. За счет фосфора в степени окисления +3 фосфористая кислота проявляет восстановительные свойства .
Например , H3PO3 окисляется перманганатом калия в кислой среде:
Еще пример : фосфористая кислота окисляется соединениями ртути (II):
Соли фосфорной кислоты — фосфаты
Фосфорная кислота образует разные типы солей: средние – фосфаты, кислые – гидрофосфаты, дигидрофосфаты.
1. Качественная реакция на фосфаты — взаимодействие с нитратом серебра. При этом образуется желтый осадок фосфата серебра.
2. Нерастворимые фосфаты растворяются под действием сильных кислот, либо под действием фосфорной кислоты.
Например , фосфат кальция реагирует с фосфорной кислотой с образованием дигидрофосфата кальция:
Фосфат кальция растворяется под действием серной кислоты:
3. За счет фосфора со степенью окисления +5 фосфаты проявляют слабые окислительные свойства и могут взаимодействовать с восстановителями.
Например , фосфат кальция при сплавлении реагирует с углеродом с образованием фосфида кальция и угарного газа:
Фосфат кальция также восстанавливается алюминием при сплавлении:
4. Гидрофосфаты могут взаимодействовать и с более сильными кислотами, и с щелочами . Под действием фосфорной кислоты гидрофосфаты переходят в дигидрофосфаты.
Например , гидрофосфат калия взаимодействует с фосфорной кислотой с образованием дигидрофосфата калия:
Под действием едкого кали гидрофосфат калия образует более среднюю соль — фосфат калия:
5. Дигидрофосфаты могут взаимодействовать с более сильными кислотами и щелочами , но не реагируют с фосфорной кислотой.
Например , дигидрофосфат натрия взаимодействует с избытком гидроксида натрия с образованием фосфата:
2.3.3. Химические свойства азота и фосфора.
Химические свойства азота
Химический элемент азот образует только одно простое вещество. Данное вещество является газообразным и образовано двухатомными молекулами, т.е. имеет формулу N2. Не смотря то, что химический элемент азот имеет высокую электроотрицательность, молекулярный азот N2 является крайне инертным веществом. Обусловлен данный факт тем, что в молекуле азота имеет место крайне прочная тройная связь (N≡N). По этой причине практически все реакции с азотом протекают только при повышенных температурах.
Взаимодействие азота с металлами
Единственное вещество, которое реагирует с азотом в обычных условиях – литий:
Интересным является тот факт, что с остальными активными металлами, т.е. щелочными и щелочноземельными, азот реагирует только при нагревании:
Взаимодействие азота с металлами средней и низкой активности (кроме Pt и Au) также возможно, однако требует несравнимо более высоких температур.
Нитриды активных металлов легко гидролизуются водой:
А также растворами кислот, например:
Взаимодействие азота с неметаллами
Азот реагирует с водородом при нагревании в присутствии катализаторов. Реакция является обратимой, поэтому для повышения выхода аммиака в промышленности процесс ведут при высоком давлении:
Как восстановитель азот реагирует со фтором и кислородом. Со фтором реакция идет при действии электрического разряда:
С кислородом реакция идет под действием электрического разряда или при температуре более 2000 о С и является обратимой:
Из неметаллов азот не реагирует с галогенами и серой.
Взаимодействие азота со сложными веществами
В рамках школьного курса ЕГЭ можно считать, что азот не реагирует ни с какими сложными веществами кроме гидридов активных металлов:
Химические свойства фосфора
Существует несколько аллотропных модификаций фосфора., в частности белый фосфор, красный фосфор и черный фосфор.
Белый фосфор образован четырехатомными молекулами P4, не является устойчивой модификацией фосфора. Ядовит. При комнатной температуре мягкий и подобно воску легко режется ножом. На воздухе медленно окисляется, и из-за особенностей механизма такого окисления светится в темноте (явление хемилюминесценции). Даже при слабом нагревании возможно самопроизвольное воспламенение белого фосфора.
Из всех аллотропных модификаций белый фосфор наиболее активен.
Красный фосфор состоит из длинных молекул переменного состава Pn. В некоторых источниках указывается то, что он имеет атомное строение, но корректнее все-таки считать его строение молекулярным. Вследствие особенностей строения является менее активным веществом по сравнению с белым фосфором, в частности в отличие от белого фосфора на воздухе окисляется значительно медленнее и для его воспламенения требуется поджиг.
Черный фосфор состоит из непрерывных цепей Pn и имеет слоистую структуру схожую со структурой графита, из-за чего и внешне похож на него. Данная аллотропная модификация имеет атомное строение. Самый устойчивый из всех аллотропных модификаций фосфора, наиболее химически пассивен. По этой причине, рассмотренные ниже химические свойства фосфора следует относить прежде всего к белому и красному фосфору.
Взаимодействие фосфора с неметаллами
Реакционная способность фосфора является более высокой, чем у азота. Так, фосфор способен гореть после поджига при обычных условиях, образуя кислотный оксид Р2O5:
а при недостатке кислорода оксид фосфора (III):
Реакция с галогенами также протекает интенсивно. Так, при хлорировании и бромировании фосфора в зависимости от пропорций реагентов образуются тригалогениды или пентагалогениды фосфора:
Ввиду существенно более слабых окислительных свойства йода по сравнению с остальными галогенами, возможно окисление фосфора йодом только до степени окисления +3:
В отличие от азота фосфор с водородом не реагирует.
Взаимодействие фосфора с металлами
Фосфор реагирует при нагревании с активными металлами и металлами средней активности образуя фосфиды:
Фосфиды активных металлов подобно нитридам гидролизуются водой:
А также водными растворами кислот-неокислителей:
Взаимодействие фосфора со сложными веществами
Фосфор окисляется кислотами окислителями, в частности, концентрированными азотной и серной кислотами:
Следует знать, что белый фосфор реагирует с водными растворами щелочей. Однако, ввиду специфичности умение записывать уравнения таких взаимодействий на ЕГЭ по химии пока еще не требовалось.
Тем не менее, тем, кто претендует на 100 баллов, для собственного спокойствия, можно запомнить следующие особенности взаимодействия фосфора с растворами щелочей на холоду и при нагревании.
На холоду взаимодействие белого фосфора с растворами щелочей протекает медленно. Реакция сопровождается образованием газа с запахом тухлой рыбы — фосфина и соединения с редкой степенью окисления фосфора +1:
При взаимодействии белого фосфора с концентрированным раствором щелочи при кипячении выделяется водород и образуется фосфит:
Химические свойства простых веществ-неметаллов: водорода, кислорода, галогенов, серы, азота, фосфора, углерода, кремния
Водород
Химический элемент водород занимает особое положение в периодической системе Д.И. Менделеева. По числу валентных электронов, способности образовывать в растворах гидратный ион H + он сходен с щелочными металлами, и его следует поместить в I группу. По числу электронов, необходимых для завершения внешней электронной оболочки, значению энергии ионизации, способности проявлять отрицательную степень окисления, малому атомному радиусу водород следует поместить в VII группу периодической системы. Таким образом, размещение водорода в той или иной группе периодической системы в значительной мере условно, но в большинстве случаев его помещают в VII группу.
Электронная формула водорода 1s 1 . Единственный валентный электрон находится непосредственно в сфере действия атомного ядра. Простота электронной конфигурации водорода отнюдь не означает, что химические свойства этого элемента просты. Напротив, химия водорода во многом отличается от химии других элементов. Водород в своих соединениях способен проявлять степени окисления +1 и –1.
Существует большое количество методов получения водорода. В лаборатории его получают взаимодействием некоторых металлов с кислотами, например:
Водород можно получить электролизом водных растворов серной кислоты или щелочей. При этом происходит процесс выделения водорода на катоде и кислорода на аноде.
В промышленности водород получают главным образом из природных и попутных газов, продуктов газификации топлива и коксового газа.
Простое вещество водород, H2, представляет собой горючий газ без цвета и запаха. Температура кипения –252,8 °C. Водород в 14,5 раза легче воздуха, мало растворим в воде.
Молекула водорода устойчива, обладает большой прочностью. Из-за высокой энергии диссоциации распад молекул H2 на атомы происходит в заметной степени лишь при температуре выше 2000 °C.
Для водорода возможны положительная и отрицательная степени окисления, поэтому в химических реакциях водород может проявлять как окислительные, так и восстановительные свойства. В тех случаях, когда водород выступает в качестве окислителя, он ведёт себя подобно галогенам, образуя аналогичные галогенидам гидриды (гидридами называют группу химических соединений водорода с металлами и менее электроотрицательными, чем он, элементами):
По окислительной активности водород существенно уступает галогенам. Поэтому ионный характер проявляют лишь гидриды щелочных и щёлочноземельных металлов. Ионные, а также комплексные гидриды, например, являются сильными восстановителями. Их широко используют в химических синтезах.
В большинстве реакций водород ведёт себя как восстановитель. При нормальных условиях водород не взаимодействует с кислородом, однако при поджигании реакция протекает со взрывом:
Смесь двух объёмов водорода с одним объёмом кислорода называют гремучим газом. При контролируемом горении происходит выделение большого количества тепла, и температура водородно-кислородного пламени достигает 3000 °С.
Реакция с галогенами протекает в зависимости от природы галогена по-разному:
С фтором такая реакция идёт со взрывом даже при низких температурах. С хлором на свету реакция также протекает со взрывом. С бромом реакция идёт значительно медленнее, а с йодом не доходит до конца даже при высокой температуре. Механизм этих реакций радикальный.
При повышенной температуре водород взаимодействует с элементами VI группы — серой, селеном, теллуром, например:
Очень важной является реакция водорода с азотом. Эта реакция обратима. Для смещения равновесия в сторону образования аммиака используют повышенное давление. В промышленности данный процесс осуществляют при температуре 450—500 °С, давлении 30 МПа, в присутствии различных катализаторов:
Водород восстанавливает многие металлы из оксидов, например:
Данную реакцию используют для получения некоторых чистых металлов.
Огромную роль играют реакции гидрирования органических соединений, которые широко используют как в лабораторной практике, так и в промышленном органическом синтезе.
Сокращение природных источников углеводородного сырья, загрязнение окружающей среды продуктами сгорания топлива повышают интерес к водороду как к экологически чистому топливу. Вероятно, водород будет играть важную роль в энергетике будущего.
В настоящее время водород широко применяют в промышленности для синтеза аммиака, метанола, гидрогенизации твёрдого и жидкого топлива, в органическом синтезе, для сварки и резки металлов и т. д.
Вода H2O, оксид водорода, является важнейшим химическим соединением. При нормальных условиях вода — бесцветная жидкость, без запаха и вкуса. Вода — самое распространённое вещество на поверхности Земли. В человеческом организме содержится 63—68 % воды.
Вода является стабильным соединением, её разложение на кислород и водород происходит лишь под действием постоянного электрического тока или при температуре около 2000 °C:
Вода непосредственно взаимодействует с металлами, стоящими в ряду стандартных электронных потенциалов до водорода. Продуктами реакции в зависимости от природы металла могут быть соответствующие гидроксиды и оксиды. Скорость реакции в зависимости от природы металла также изменяется в широких пределах. Так, натрий вступает в реакцию с водой уже при комнатной температуре, реакция сопровождается выделением большого количества тепла; железо реагирует с водой при температуре 800 °С.
Вода может вступать в реакцию со многими неметаллами, так, при обычных условиях вода обратимо взаимодействует с хлором:
При повышенной температуре вода взаимодействует с углем с образованием так называемого синтез-газа — смеси оксида углерода (II) и водорода:
При обычных условиях вода реагирует со многими основными и кислотными оксидами с образованием оснований и кислот соответственно:
Реакция идёт до конца, если соответствующее основание или кислота растворимы в воде.
Кислород
Химический элемент кислород расположен во 2-м периоде VIA подгруппе. Его электронная формула 1s 2 2s 2 2p 4 . Простое вещество кислород — газ без цвета и запаха, мало растворим в воде. Сильный окислитель. Его характерные химические свойства:
Реакции простых и сложных веществ с кислородом часто сопровождаются выделением тепла и света. Такие реакции называют реакциями горения.
Кислород широко используется практически во всех областях химической промышленности: для производства чугуна и стали, производства азотной и серной кислоты. Огромное количество кислорода потребляется в процессах тепловой энергетики.
В последние годы обострилась проблема сохранения запасов кислорода в атмосфере. До настоящего времени единственным источником, пополняющим запасы атмосферного кислорода, является жизнедеятельность зелёных растений.
Галогены
В VIIА группе находятся фтор, хлор, бром, йод и астат. Эти элементы называют также галогенами (в переводе — рождающие соли).
На внешнем энергетическом уровне всех этих элементов находятся 7 электронов (конфигурации ns 2 np 5 ), наиболее характерные степени окисления –1, +1, +5 и +7 (кроме фтора).
Атомы всех галогенов образуют простые вещества состава Hal2.
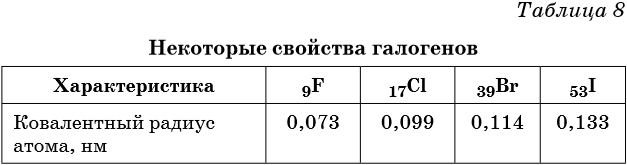
Галогены являются типичными неметаллами. При переходе от фтора к астату происходит увеличение радиуса атома, неметаллические свойства падают, происходит уменьшение окислительных и увеличение восстановительных свойств.
Физические свойства галогенов приведены в таблице 8.
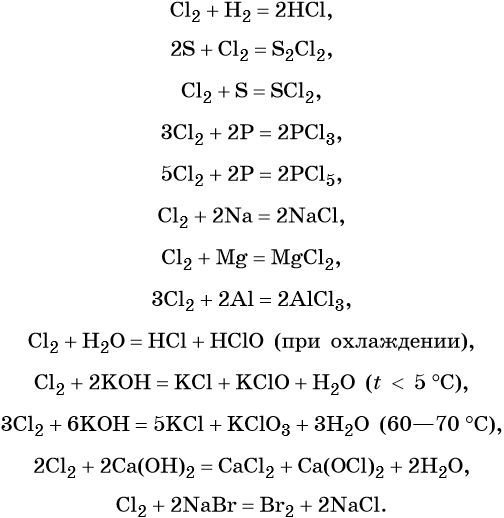
В химическом отношении галогены весьма активны. Их реакционная способность убывает с увеличением порядкового номера. Некоторые характерные для них реакции приведены ниже на примере хлора:
Водородные соединения галогенов — галогеноводороды имеют общую формулу HHal. Их водные растворы являются кислотами, сила которых возрастает от HF к HI.
Галогенводородные кислоты (за исключением HF) способны реагировать с такими сильными окислителями, как KMnO4, MnO2, K2Cr2O7, CrO3 и другими, с образованием галогенов:
Галогены образуют ряд оксидов, например, для хлора известны кислотные оксиды состава Cl2O, ClO2, ClO3, Cl2O7. Все эти соединения получают косвенными методами. Они являются сильными окислителями и взрывоопасными веществами.
Наиболее устойчивым из оксидов хлора является Cl2O7. Оксиды хлора легко реагируют с водой, образуя кислородсодержащие кислоты: хлорноватистую HClO, хлористую HClO2, хлорноватую HClO3 и хлорную HClO4, например:
В промышленности бром получают при вытеснении хлором из бромидов, а в лабораторной практике — окислением бромидов:
Простое вещество бром является сильным окислителем, легко вступает в реакции со многими простыми веществами, образуя бромиды; вытесняет йод из йодидов.
Простое вещество йод, I2, представляет собой чёрные с металлическим блеском кристаллы, которые возгоняются, т. е. переходят в пар, минуя жидкое состояние. Йод мало растворим в воде, но довольно хорошо растворяется в некоторых органических растворителях (спирт, бензол и т. д.).
Йод является довольно сильным окислителем, способным к окислению ряда металлов и некоторых неметаллов.
Химический элемент сера расположен в 3-м периоде VIA подгруппе. Его электронная формула 1s 2 2s 2 2p 6 3s 2 3p 4 . Простое вещество сера — неметалл жёлтого цвета. Существует в двух аллотропных модификациях: ромбическая и моноклинная и в аморфной форме (пластическая сера). Проявляет как окислительные, так и восстановительные свойства. Возможны реакции диспропорционирования. Её характерные химические свойства:
Сера образует летучее водородное соединение — сероводород. Его водный раствор представляет собой слабую двухосновную кислоту. Для сероводорода характерны также восстановительные свойства:
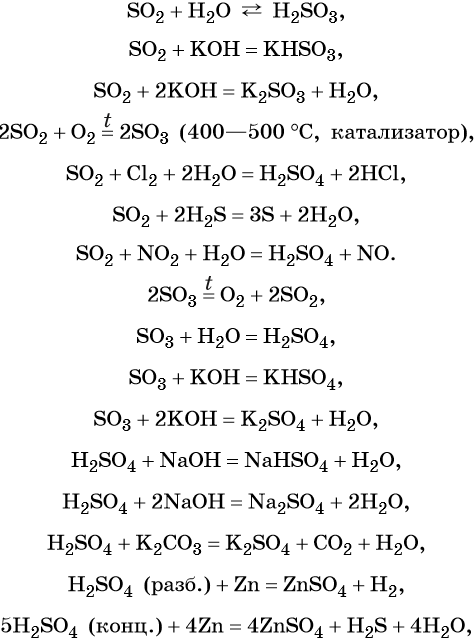
Сера образует два кислотных оксида: оксид серы (IV) SO2 и оксид серы (VI) SO3. Первому соответствует слабая, существующая только в растворе сернистая кислота H2SO3; второму — сильная двухосновная серная кислота H2SO4. Концентрированная серная кислота проявляет сильные окислительные свойства. Ниже приведены характерные для этих соединений реакции:
Серная кислота в больших количествах производится в промышленности. Все промышленные методы производства серной кислоты основаны на первоначальном получении оксида серы (IV), его окислении в оксид серы (VI) и взаимодействии последнего с водой.
Химический элемент азот — находится во 2-м периоде, V группе, главной подгруппе периодической системы Д.И. Менделеева. Его электронная формула 1s 2 2s 2 2p 3 . В своих соединениях азот проявляет степени окисления –3, –2, +1,+2, +3, +4, +5.
Простое вещество азот — газ без цвета и запаха, малорастворимый в воде. Типичный неметалл. В обычных условиях химически мало активен. При нагревании вступает в окислительно-восстановительные реакции.
Азот образует оксиды состава N2O, NO, N2O3, NO2, N2O4, N2O5. При этом N2O, NO, являются несолеобразующими оксидами, для которых характерны окислительно-восстановительные реакции; N2O3, NO2, N2O4, N2O5 — солеобразующие кислотные оксиды, для которых также характерны окислительно-восстановительные реакции, в том числе реакции диспропорционирования.
Химические свойства оксидов азота:
Азот образует летучее водородное соединение состава NH3, аммиак. При обычных условиях это бесцветный газ с характерным резким запахом; температура кипения –33,7 °C, температура плавления –77,8 °C. Аммиак хорошо растворим в воде (700 объёмов NH3 на 1 объём воды при 20 °C) и ряде органических растворителей (спирт, ацетон, хлороформ, бензол).
Химические свойства аммиака:
Азот образует азотистую кислоту HNO2 (в свободном виде известна только в газовой фазе или растворах). Это слабая кислота, её соли называют нитритами.
Кроме того, азот образует очень сильную азотную кислоту HNO3. Особенностью азотной кислоты является то, что при её окислительно-восстановительных реакциях с металлами не выделяется водород, а образуются различные оксиды азота или соли аммония, например:
В реакциях с неметаллами концентрированная азотная кислота ведёт себя как сильный окислитель:
Также азотная кислота способна окислять сульфиды, йодиды и т. д.:
Подчеркнём ещё раз. Запись уравнений окислительно-восстановительных реакций с участием HNO3 обычно условна. Как правило, в них указывают лишь продукт, образующийся в большем количестве. В некоторых из таких реакций в качестве продукта восстановления обнаружен водород (реакция разбавленной HNO3 с Mg и Mn).
Соли азотной кислоты называют нитратами. Все нитраты хорошо растворимы в воде. Нитраты термически нестабильны и при нагревании легко разлагаются.
Особые случаи разложения нитрата аммония:
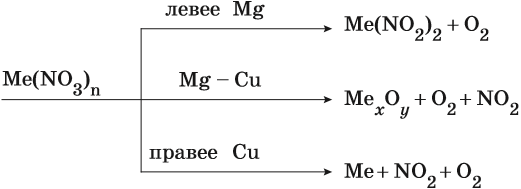
Общие закономерности термического разложения нитратов:
Фосфор
Химический элемент фосфор расположен в 3-м периоде, V группе, главной подгруппе периодической системы Д.И. Менделеева. Его электронная формула 1s 2 2s 2 2p 6 3s 2 3p 3 .
Простое вещество фосфор существует в виде нескольких аллотропных модификаций (аллотропия состава). Белый фосфор Р4, при комнатной температуре мягкий, плавится, кипит без разложения. Красный фосфор Pn, состоит из полимерных молекул разной длины. При нагревании возгоняется. Чёрный фосфор состоит из непрерывных цепей Pn, имеет слоистую структуру, по внешнему виду похож на графит. Наиболее реакционноспособным является белый фосфор.
В промышленности фосфор получают прокаливанием фосфата кальция с углём и песком при 1500 °C:
В приведённые ниже реакции вступают любые модификации фосфора, если нет особых оговорок:
Фосфор образует летучее водородное соединение — фосфин, PH3. Это газообразное соединение с крайне неприятным резким запахом. Его соли в отличие от солей аммиака существуют только при низких температурах. Фосфин легко вступает в окислительно-восстановительные реакции:
Фосфор образует два кислотных оксида: P2O3 и P2O5. Последнему соответствует фосфорная (ортофосфорная) кислота H3PO4. Это трёхосновная кислота средней силы, которая образует три ряда солей: средние (фосфаты) и кислые (гидро- и дигидрофосфаты). Ниже приведены уравнения химических реакций, характерные для данных соединений:
Углерод
Химический элемент углерод расположен во 2-м периоде, главной подгруппе IV группы периодической системы Д.И. Менделеева, его электронная формула 1s 2 2s 2 2p 2 , наиболее характерные степени окисления –4, +2, +4.
Для углерода известны стабильные аллотропные модификации (графит, алмаз, аллотропия строения), в виде которых он встречается в природе, а также полученные лабораторным путём карбин и фуллерены.
Алмаз — кристаллическое вещество с атомной координационной кубической решёткой. Каждый атом углерода в алмазе находится в состоянии sp 3 -гибридизации и образует равноценные прочные связи с четырьмя соседними атомами углерода. Это обуславливает исключительную твёрдость алмаза и отсутствие в обычных условиях электропроводности.
В графите атомы углерода находятся в состоянии sp 2 -гибридизации. Атомы углерода объединены в бесконечные слои из шестичленных колец, стабилизированные ω-связью, делокализованные в пределах всего слоя. Этим объясняется металлический блеск и электрическая проводимость графита. Углеродные слои объединены в кристаллическую решётку в основном за счёт межмолекулярных сил. Прочность химических связей в плоскости макромолекулы значительно больше, чем между слоями, поэтому графит довольно мягок, легко расслаивается и химически несколько активнее алмаза.
В состав древесного угля, сажи и кокса входят очень мелкие кристаллы графита с очень большой поверхностью, которые называют аморфным углеродом.
В карбине атом углерода находится в состоянии sp-гибридизации. Его кристаллическая решётка построена из прямолинейных цепочек двух видов:
Карбин представляет собой порошок чёрного цвета с плотностью 1,9—2,0 г/см 3 , является полупроводником.
Аллотропные модификации углерода могут переходить друг в друга при определённых условиях. Так, при нагревании без доступа воздуха при температуре 1750 °С алмаз переходит в графит.
В нормальных условиях углерод весьма инертен, однако при высоких температурах он вступает в реакции с различными веществами, причём самой реакционноспособной формой является аморфный углерод, менее активен графит, а самый инертный — алмаз.
Реакции, характерные для углерода:
Углерод устойчив к действию кислот и щелочей. Только горячие концентрированные азотная и серная кислоты могут окислить его до оксида углерода (IV):
Углерод восстанавливает многие металлы из их оксидов. При этом в зависимости от природы металла образуются либо чистые металлы (оксиды железа, кадмия, меди, свинца), либо соответствующие карбиды (оксиды кальция, ванадия, тантала), например:
Углерод образует два оксида: CO и CO2.
Оксид углерода (II) CO (угарный газ) представляет собой бесцветный газ без запаха, плохо растворимый в воде. Это соединение является сильным восстановителем. Он горит на воздухе с выделением большого количества теплоты, благодаря чему CO является хорошим газообразным топливом.
Оксид углерода (II) восстанавливает многие металлы из их оксидов:
Оксид углерода (II) является несолеобразующим оксидом, с водой и щелочами он не реагирует.
Оксид углерода (IV) CO2 (углекислый газ) представляет собой бесцветный, без запаха, негорючий газ, малорастворимый в воде. В технике его обычно получают термическим разложением CaCO3, а в лабораторной практике — действием на CaCO3 соляной кислоты:
Оксид углерода (IV) является кислотным оксидом. Его характерные химические свойства:
Оксиду углерода (IV) соответствует очень слабая двухосновная угольная кислота H2CO3, которая не существует в чистом виде. Она образует два ряда солей: средние — карбонаты, например карбонат кальция CaCO3, и кислые — гидрокарбонаты, например Ca(HCO3)2 — гидрокарбонат кальция.
Карбонаты переходят в гидрокарбонаты под действием избытка углекислого газа в водной среде:
Гидрокарбонат кальция превращается в карбонат под действием гидроксида кальция:
Гидрокарбонаты и карбонаты разлагаются при нагревании:
Кремний
Химический элемент кремний находится в 3-м периоде IVА группе периодической системы Д.И. Менделеева. Его электронная формула 1s 2 2s 2 2p 6 3s 2 3p 2 , наиболее характерные степени окисления –4, +4.
Кремний получают восстановлением его оксида магнием или углеродом в электрических печах, а кремний высокой чистоты — восстановлением SiCl4 цинком или водородом, например:
Кремний может существовать в кристаллической или аморфной форме. В обычных условиях кремний довольно устойчив, причём аморфный кремний более реакционноспособен, чем кристаллический. Для кремния наиболее устойчива степень окисления +4.
Реакции, характерные для кремния:
Кремний не реагирует с кислотами (за исключением HF), пассивируется кислотами-окислителями, но хорошо растворяется в смеси плавиковой и азотной кислот, что можно описать уравнением:
Оксид кремния (IV), SiO2 (кремнезём), в природе встречается в основном в виде минерала кварца. В химическом отношении довольно устойчив, проявляет свойства кислотного оксида.
Свойства оксида кремния (IV):
Кремний образует кислоты переменного содержания SiO2 и H2O. Соединение состава H2SiO3 в чистом виде не выделено, но для упрощения допускается его запись в уравнениях реакций:
Тренировочные задания
1. Водород при соответствующих условиях вступает в реакцию с каждым из двух веществ:
1) кислородом и железом
2) серой и хромом
3) оксидом углерода (II) и соляной кислотой
4) азотом и натрием
2. Верны ли следующие утверждения о водороде?
А. Перекись водорода можно получить сжиганием водорода в избытке кислорода.
Б. Реакция между водородом и серой идёт без катализатора.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
3. Кислород при соответствующих условиях вступает в реакцию с каждым из двух веществ:
1) гелием и железом
2) фосфором и цинком
3) оксидом кремния (IV) и хлором
4) хлоридом калия и серой
4. Верны ли следующие утверждения о кислороде?
А. Кислород не реагирует с хлором.
Б. Реакция кислорода с серой даёт SO2.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
5. Фтор при соответствующих условиях вступает в реакцию с каждым из двух веществ:
1) гелием и железом
2) аргоном и азотной кислотой
3) оксидом углерода (IV) и неоном
4) водой и натрием
6. Верны ли следующие утверждения о фторе?
А. Реакция избытка фтора с фосфором приводит к PF5.
Б. Фтор реагирует с водой.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
7. Хлор при соответствующих условиях вступает в реакцию с каждым из двух веществ:
1) кислородом и железом
2) фосфором и серной кислотой
3) оксидом кремния (IV) и неоном
4) бромидом калия и серой
8. Верны ли следующие утверждения о хлоре?
А. Пары хлора легче воздуха.
Б. В заимодействие хлора с кислородом приводит к оксиду хлора (V).
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
9. Бром при соответствующих условиях вступает в реакцию с каждым из двух веществ:
1) фосфором и железом
2) фосфором и серной кислотой
3) оксидом кремния (IV) и хлором
4) бромидом калия и серой
10. Верны ли следующие утверждения о броме?
А. Бром не вступает в реакцию с водородом.
Б. Бром вытесняет хлор из хлоридов.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
11. Йод при соответствующих условиях вступает в реакцию с каждым из двух веществ:
1) гелием и железом
2) фосфором и кальцием
3) оксидом кремния (IV) и хлором
4) хлоридом калия и серой
12. Верны ли следующие утверждения о йоде?
А. Раствор йода обладает бактерицидными свойствами.
Б. Йод реагирует с хлоридом кальция.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
13. Сера при соответствующих условиях вступает в реакцию с каждым из двух веществ:
1) натрием и железом
2) фосфором и оксидом цинком
3) оксидом кремния (IV) и хлором
4) хлоридом калия и бромидом натрия
14. Верны ли следующие утверждения о сере?
А. При сплавлении серы и кальция образуется CaS.
Б. При реакции серы с кислородом образуется SO2.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
15. Азот при соответствующих условиях вступает в реакцию с каждым из двух веществ:
1) литием и хлоридом кальция
2) хлором и оксидом кальция
3) оксидом кремния (IV) и хлором
4) литием и кальцием
16. Верны ли следующие утверждения об азоте?
А. В промышленности реакцию азота и водорода осуществляют под высоким давлением в присутствии катализатора.
Б. При взаимодействии азота и натрия образуется Na3N.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
17. Фосфор при соответствующих условиях вступает в реакцию с каждым из двух веществ:
1) натрием и сульфидом кальция
2) хлором и кислородом
3) оксидом углерода (IV) и серой
4) серой и оксидом цинка
18. Верны ли следующие утверждения о фосфоре?
А. Реакция фосфора с хлором идёт только в присутствии катализатора.
Б. При реакции фосфора с избытком серы образуются только P2S3.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
19. Углерод при соответствующих условиях вступает в реакцию с каждым из двух веществ:
1) кальцием и сульфатом бария
2) хлором и неоном
3) оксидом фосфора (V) и серой
4) серой и гидроксидом цинка
20. Верны ли следующие утверждения об углероде?
А. При взаимодействии углерода с натрием образуется карбид состава Na2C2.
Б. Углерод реагирует с оксидом кальция с образованием CaC2.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
21. Кремний при соответствующих условиях вступает в реакцию с каждым из двух веществ:
1) кислородом и гидроксидом натрия
2) хлором и неоном
3) оксидом фосфора (V) и серой
4) серой и гидроксидом цинка
22. Верны ли следующие утверждения о кремнии?
А. При взаимодействии кремния с углеродом образуется карбид состава SiC.
Б. Кремний реагирует с магнием с образованием Mg2Si.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
23. Установите соответствие между реагирующими веществами и продуктами реакций.
24. Установите соответствие между реагирующими веществами и продуктами реакций.
25. Установите соответствие между реагирующими веществами и продуктами реакций.
26. Установите соответствие между реагирующими веществами и продуктами реакций.
27. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) Cl2 + Fe →
Б) Cl2 + Cr →
В) Cl2 (изб.) + P →
28. Установите соответствие между реагирующими веществами и продуктами реакций.
ПРОДУКТЫ РЕАКЦИИ
1) NaClO3 + NaCl + H2O
2) NaCl + NaClO + H2O
3) NaClO3 + NaCl
4) NaCl + Br2
5) NaClBr
29. Установите соответствие между реагирующими веществами и продуктами реакций.
ПРОДУКТЫ РЕАКЦИИ
1) NaClI
2) NaBrO + NaBr
3) NaBrO3 + NaBr + H2O
4) NaBrO + NaBr + H2O
5) NaBr + I2
30. Установите соответствие между реагирующими веществами и продуктами реакций.
ПРОДУКТЫ РЕАКЦИИ
1) NaBr + NaBrO3 + H2O
2) NaBr + NaBrO + H2O
3) I Br
4) H2SO4 + HBr
5) HBr + SO3
31. Установите соответствие между реагирующими веществами и продуктами реакций.
32. Установите соответствие между реагирующими веществами и продуктами реакций.
33. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) S + Na →
Б) S + HI →
В) S + NaOH →
34. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) S + Cl2 (недост.) →
Б) S + HNO3 (конц.) →
В) S + O2 →+
35. Установите соответствие между реагирующими веществами и продуктами реакций.
36. Установите соответствие между реагирующими веществами и продуктами реакций.
37. Установите соответствие между реагирующими веществами и продуктами реакций.
38. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) P + Br2 (недост.) →
Б) P + Li
В) P + HNO3 (конц.) →
39. Установите соответствие между реагирующими веществами и продуктами реакций.
40. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) C + H2O →
Б) C + HNO3 →
В) C + S →
41. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) Si + O2 →
Б) Si + S →
В) S i + Mg →
42. Установите соответствие между реагирующими веществами и продуктами реакций.
РЕАГИРУЮЩИЕ ВЕЩЕСТВА
А) Si + Cl2 →
Б) Si + C →
В) Si + NaOH →
43. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
44. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
45. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
46. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
47. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
48. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
49. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для второго превращения составьте сокращённое ионное уравнение реакции.
50. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
51. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
52. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
53. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.
54. Дана схема превращений:
Напишите молекулярные уравнения реакций, с помощью которых можно осуществить указанные превращения. Для третьего превращения составьте сокращённое ионное уравнение реакции.