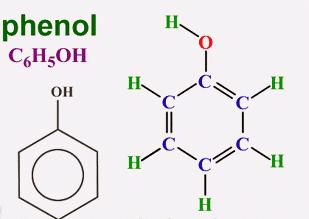
Почему мутнеет водный раствор фенолята натрия: а) если к нему добавляют соляную кислоту; б) если через него пропускают оксид углерода (IV)? Приведите уравнения соответствующих реакций.
а) Соляная кислота является сильной кислотой, поэтому она легко вытесняет фенол из его соли. Фенол нерастворим в воде, поэтому водный раствор фенолята натрия мутнеет.
 | + | HCl | ⟶ |  | + | NaCl |
б) При пропускании оксида углерода (IV) через водный раствор фенолята натрия, образуется слабая угольная кислота, которая вытесняет фенол из его соли. Фенол нерастворим в воде, поэтому водный раствор фенолята натрия также мутнеет. Данный опыт говорит о том, что фенол проявляет более слабые кислотные свойства, чем угольная кислота.
- Фенол кислота слабая он может быть вытеснен из солей сильной кислотой напишите уравнение реакции
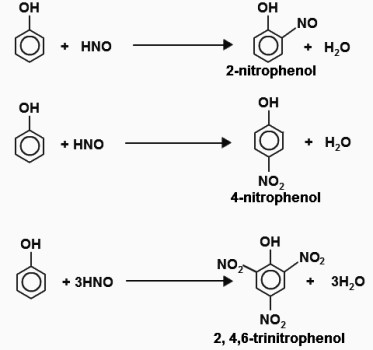
- Качественные реакции на фенол. Получение фенолов: реакции
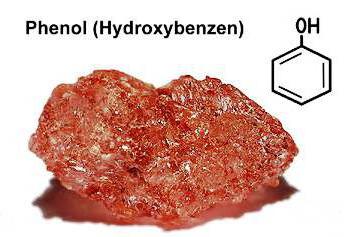
- Фенол (гидроксибензол)
- Особенности строения молекулы
- Кислотные свойства
- Реакция фенола с натрием и щелочью
- Реакции бензольного кольца
- Качественные реакции на фенол. Список
- Получение фенолов
- Использование фенолов
Фенол кислота слабая он может быть вытеснен из солей сильной кислотой напишите уравнение реакции
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 1
Приведите молекулярную и структурную формулы фенола.
Молекулярная формула фенола: C6H5OH.
Структурная формула фенола: 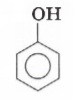
Найдите черты сходства и различия в строении молекул фенола и этанола.
Сходство: молекулы имеют в своём составе гидроксильную группу ОН, которая связана с атомом углерода.
Различия: в молекуле фенола гидроксильная группа связана с ароматическим радикалом, а в этаноле ― с алкильным радикалом.
Задание 2 Как взаимное влияние фенильного радикала и гидроксильной группы отражается на свойствах фенола? Ответ проиллюстрируйте уравнениями химических реакций.
Влияние фенильного радикала –C6H5 на гидроксильную группу выражается в значительном усилении кислотных свойств, так, например, фенол, в отличие от спиртов, вступает в реакцию нейтрализации со щелочами:
C6H5OH + NaOH ⟶ C6H5ONa + H2O
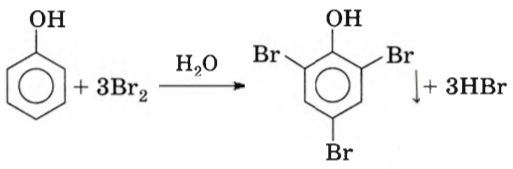
Влияние гидроксильной группы на фенильный радикал –C6H5 выражается в значительном облегчении протекания реакции по фенильному радикалу, так, например, для бромирования фенола, в отличие от бензола, не требуется катализатор и замещаются сразу три атома водорода в положениях 2, 4 и 6 с образованием белого нерастворимого осадка 2,4,6-трибромфенола:
Задание 3
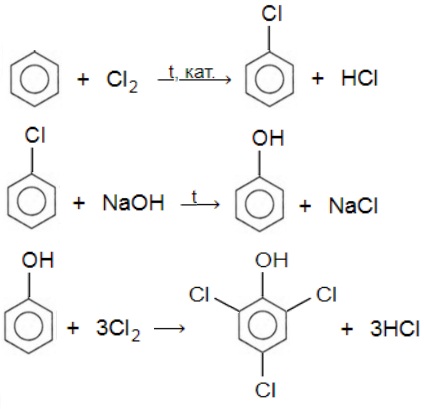
В настоящее время вместо фенола в качестве дезинфицирующего средства используют 2,4,6-трихлорфенол. Предложите способ его получения исходя из бензола. Напишите уравнения соответствующих реакций.
или
С6H6 + Cl2 t,кат. ⟶ C6H5Cl + HCl
C6H5Cl + NaOH t ⟶ C6H5OH + NaCl
C6H5OH + 3Cl2 ⟶ C6H2Cl3OH + 3HCl
Задание 4
В результате взаимодействия 47 г водного раствора фенола с бромной водой выпало 1,655 г осадка. Рассчитайте массовую долю фенола в исходном растворе.
Дано: m(раствора)=47 г, m(C6H2 Br3OH )=1,655 г
Найти: ω(C6H5OH)—?
Решение
1. Количество вещества осадка рассчитываем по формуле: n=m/M, где M ― молярная масса.
M( C6H2Br3OH )=331 г/моль
n( C6H2Br3OH )=m( C6H2 Br3OH )/M( C6H2 Br3OH )=1,655 г : 331 г/моль=0,005 моль
2. Составим химическое уравнение:
C6H5OH + 3Br2 = C6H2Br3OH↓ + 3HBr
По уравнению реакции n(C6H5OH):n(C6H2Br3OH)=1:1, количество вещества одинаковое, поэтому
n( C6H5OH )=n( C6H2 Br3OH )=0,005 моль
3. Рассчитываем массу фенола количеством вещества 0,005 моль по формуле: m = n • M, где M ― молярная масса.
M ( C6H5OH )=94 г/моль
m( C6H5OH )=n ( C6H5OH ) • M( C6H5OH )=0,005 моль • 94 г/моль=0,47 г
4. Рассчитываем массовую долю фенола в растворе:
ω ( C6H5OH )=( m ( C6H5OH ):m(раствора)) • 100%=(0,47 г : 47 г) •100%=1%
Ответ: 1%
Задание 5
В трёх пробирках без подписи находятся водные растворы пропанола-1, глицерина и фенола. С помощью каких реагентов можно определить каждый из растворов?
Качественной реакцией на фенол является реакция с бромной водой при комнатной температуре, в результате образуется белый осадок.
Качественной рекцией на глицерин (мноатономный спирт) является реакция со свежеполученным осадком гидроксида меди (II), в результате которой образуется раствор ярко-синего цвета.
Определить раствор пропанола-1 можно при помощи оксида меди (II), при его добавлении, наблюдается окисление спирта до альдегида, и раствор приобретает фруктовый запах.
Задание 6
Фенолят натрия взаимодействует с углекислым газом с образованием гидрокарбоната натрия и фенола согласно уравнению C6H5ONa + CO2 + H2O ⟶ C6H5OH + NaHCO3 Какой вывод относительно кислотных свойств фенола и угольной кислоты можно сделать на основании этой реакции? Фенол является слабой кислотой, при этом кислотные свойства фенола настолько слабые, что даже такая слабая кислота, как угольная, вытесняет фенол из раствора его солей .
Задание 7
Опишите физические свойства фенола.
Фенол ― бесцветные кристаллы, розовеющие при хранении на воздухе, с температурой плавления 41°C и температурой кипения 181,2°C, летучие, имеют специфический стойкий запах (запах гуаши, или так называемый «карболовый запах»). При комнатной температуре фенол растворим в воде незначительно, а при нагревании до 70°С растворяется полностью.
Найдите в Интернете данные о растворимости фенола в воде при различных температурах. Постройте график температурной зависимости растворимости фенола в воде.
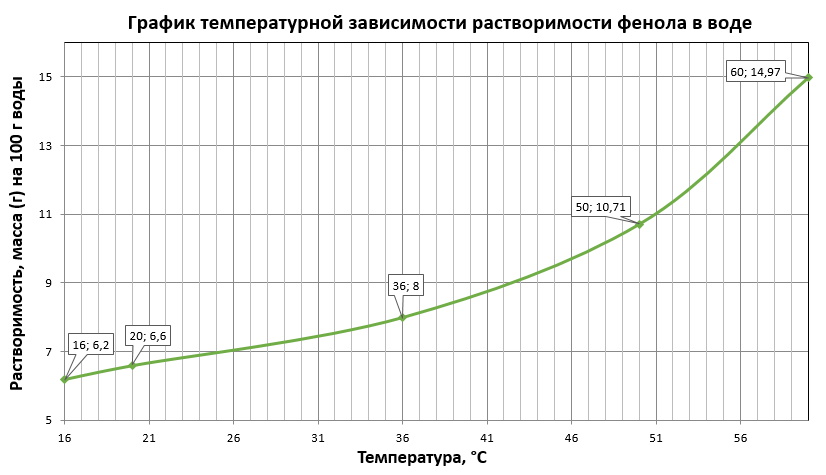
В справочнике химика нашли, що 1 г кристаллического фенола растворяется в 15 г воды при 20 0 С, поэтому в 100 г воды при 20 0 С растворится 6,6 г фенола, следовательно первая координата (20;6,6). Остальные координаты берем из других справочников в интернете: (16;6,2); (36;8); (50;10,71); (60;14,97).
Построили график температурной зависимости растворимости фенола в воде:
Качественные реакции на фенол. Получение фенолов: реакции
Карболовая кислота — одно из названий фенола, указывающее на его особое поведение в химических процессах. Это вещество легче, чем бензол вступает в реакции нуклеофильного замещения. Присущие соединению кислотные свойства объясняются подвижностью атома водорода в гидроксильной группе, связанной с кольцом. Изучение строения молекулы и качественные реакции на фенол позволяют отнести вещество к ароматическим соединениям — производным бензола.
Фенол (гидроксибензол)
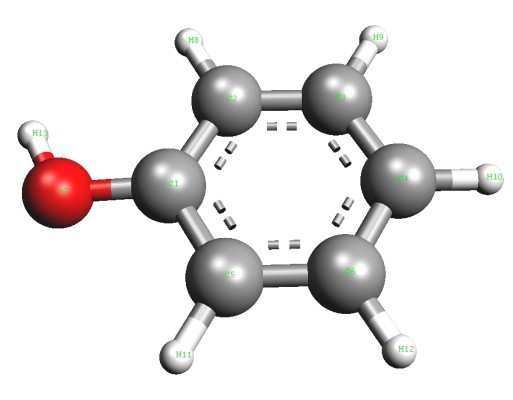
В 1834 году немецкий химик Рунге выделил карболовую кислоту из каменноугольной смолы, но не сумел расшифровать ее состав. Позже другие исследователи предложили формулу и отнесли новое соединение к ароматическим спиртам. Простейший представитель этой группы — фенол (гидроксибензол). В чистом виде это вещество представляет собой прозрачные кристаллы, обладающие характерным запахом. На воздухе цвет фенола может измениться, стать розовым или красным. Для ароматического спирта характерна плохая растворимость в холодной воде и хорошая — в органических растворителях. Плавится фенол при температуре 43°C. Является токсичным соединением, при попадании на кожу вызывает сильные ожоги. Ароматическая часть молекулы представлена радикалом фенилом (C6H5—). Непосредственно с одним из атомов углерода связан кислород гидроксильной группы (—OH). Присутствие каждой из частиц доказывает соответствующая качественная реакция на фенол. Формула, показывающая общее содержание атомов химических элементов в молекуле — C6H6O. Строение отражают структурные формулы, включающие цикл Кекуле и функциональную группу — гидроксильную. Наглядное представление о молекуле ароматического спирта дают шаростержневые модели.
Особенности строения молекулы
Взаимовлияние бензольного ядра и ОН-группы определяет химические реакции фенола с металлами, галогенами, другими веществами. Наличие атома кислорода, связанного с ароматическим циклом, ведет к перераспределению электронной плотности в молекуле. Связь O—H становится более полярной, что приводит к увеличению подвижности водорода в гидроксильной группе. Протон может замещаться на атомы металла, что указывает на кислотность фенола. В свою очередь, ОН-группа повышает реакционные свойства бензольного кольца. Увеличивается делокализация электронов и способность к электрофильному замещению в ядре. При этом возрастает подвижность атомов водорода, связанных с углеродом в орто- и параположении (2, 4, 6). Такой эффект обусловлен наличием донора электронной плотности — гидроксильной группы. Благодаря ее влиянию фенол активнее чем бензол ведет себя в реакциях с некоторыми веществами, а новые заместители ориентируются в орто- и пара-положения.
Кислотные свойства
В гидроксильной группе ароматических спиртов атом кислорода приобретает положительный заряд, ослабляющий его связь с водородом. Высвобождение протона облегчается, поэтому фенол ведет себя как слабая кислота, но более сильная, чем спирты. Качественные реакции на фенол включают испытание лакмусовой бумажкой, которая в присутствии протонов изменяет цвет с синего на розовый. Наличие атомов галогенов или нитрогрупп, связанных с бензольным кольцом, приводит к росту активности водорода. Эффект наблюдается в молекулах нитропроизводных фенола. Понижают кислотность такие заместители, как аминогруппа и алкил (CH3—, C2H5— и другие). К соединениям, объединяющим в своем составе бензольное кольцо, гидроксильную группу и радикал метил, относится крезол. Его свойства слабее, чем карболовой кислоты.
Реакция фенола с натрием и щелочью
Реакции бензольного кольца
Ароматические свойства обусловлены делокализацией электронов в бензольном ядре. Водород из состава кольца замещается на атомы галогенов, нитрогруппу. Подобный процесс в молекуле фенола проходит легче, чем у бензола. Один из примеров — бромирование. На бензол галоген действует в присутствие катализатора, получается бромбензол. Фенол реагирует с бромной водой при обычных условиях. В результате взаимодействия образуется белый осадок 2,4,6-трибромфенола, появление которого позволяет отличить испытуемое вещество от похожих на него ароматических соединений. Бромирование — качественная реакция на фенол. Уравнение: C6H5—OH + 3Br2 = C6H2Br3 + HBr. Второй продукт реакции — бромоводород. При взаимодействии фенола с разбавленной азотной кислотой получаются нитропроизводные. Продукт реакции с концентрированной азотной кислотой — 2,4,6-тринитрофенол или пикриновая кислота имеет большое практическое значение.
Качественные реакции на фенол. Список
При взаимодействии веществ получаются определенные продукты, которые позволяют установить качественный состав исходных веществ. Ряд цветных реакций указывает на присутствие частиц, функциональных групп, что удобно использовать для химического анализа. Качественные реакции на фенол доказывают наличие в молекуле вещества ароматического кольца и OH-группы:
- В растворе фенола синяя лакмусовая бумажка краснеет.
- Цветные реакции на фенолы также проводят в слабой щелочной среде с солями диазония. Образуются желтые либо оранжевые азокрасители.
- Реагирует с бромной водой коричневого цвета, появляется белый осадок трибромфенола.
- В результате реакции с раствором хлорида железа получается феноксид трехвалентного железа — вещество синей, фиолетовой или зеленой окраски.
Получение фенолов
Производство фенола в промышленности идет в две либо три стадии. На первом этапе из пропилена и бензола в присутствии хлорида алюминия получают кумол (тривиальное название изопропилбензола). Уравнение реакции Фриделя-Крафтса: C6H5—OH + C3H6 = C9H12 (кумол). Бензол и пропилен в соотношении 3:1 пропускают над кислотным катализатором. Все чаще вместо традиционного катализатора — хлорида алюминия — используются экологически чистые цеолиты. На заключительной стадии проводят окисление кислородом в присутствии серной кислоты: C6H5—C3H7 + O2 = C6H5—OH + C3H6O. Фенолы могут быть получены из угля перегонкой, являются промежуточными соединениями в производстве других органических веществ.
Использование фенолов
Ароматические спирты находят широкое применение в производстве пластмасс, красителей, пестицидов и других веществ. Производство карболовой кислоты из бензола является первым шагом в создании ряда полимеров, в том числе поликарбонатов. Фенол вступает в реакцию с формальдегидом, получаются фенолформальдегидные смолы.
Циклогексанол служит сырьем для выпуска полиамидов. Фенолы применяются в качестве антисептиков и дезинфицирующих средств в дезодорантах, лосьонах. Используются для получения фенацетина, салициловой кислоты и других лекарственных препаратов. Фенолы находят применение в производстве смол, которые используются в электрических изделиях (выключатели, розетки). Они также используются в подготовке азокрасителей, например фениламина (анилина) . Пикриновая кислота, которая является нитропроизводным фенола, применяется для окрашивания тканей, изготовления взрывчатых веществ.