Наведите курсор на ячейку элемента, чтобы получить его краткое описание.
Чтобы получить подробное описание элемента, кликните по его названию.
| H + | Li + | K + | Na + | NH4 + | Ba 2+ | Ca 2+ | Mg 2+ | Sr 2+ | Al 3+ | Cr 3+ | Fe 2+ | Fe 3+ | Ni 2+ | Co 2+ | Mn 2+ | Zn 2+ | Ag + | Hg 2+ | Pb 2+ | Sn 2+ | Cu 2+ | |
| OH — | Р | Р | Р | Р | Р | М | Н | М | Н | Н | Н | Н | Н | Н | Н | Н | — | — | Н | Н | Н | |
| F — | Р | М | Р | Р | Р | М | Н | Н | М | М | Н | Н | Н | Р | Р | Р | Р | Р | — | Н | Р | Р |
| Cl — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | Р | М | Р | Р |
| Br — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Н | М | М | Р | Р |
| I — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | Р | ? | Р | Р | Р | Р | Н | Н | Н | М | ? |
| S 2- | М | Р | Р | Р | Р | — | — | — | Н | — | — | Н | — | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| HS — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | Н | ? | ? | ? | ? | ? | ? | ? |
| SO3 2- | Р | Р | Р | Р | Р | Н | Н | М | Н | ? | — | Н | ? | Н | Н | ? | М | М | — | Н | ? | ? |
| HSO3 — | Р | ? | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? |
| SO4 2- | Р | Р | Р | Р | Р | Н | М | Р | Н | Р | Р | Р | Р | Р | Р | Р | Р | М | — | Н | Р | Р |
| HSO4 — | Р | Р | Р | Р | Р | Р | Р | Р | — | ? | ? | ? | ? | ? | ? | ? | ? | ? | ? | Н | ? | ? |
| NO3 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р |
| NO2 — | Р | Р | Р | Р | Р | Р | Р | Р | Р | ? | ? | ? | ? | Р | М | ? | ? | М | ? | ? | ? | ? |
| PO4 3- | Р | Н | Р | Р | — | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н | Н |
| CO3 2- | Р | Р | Р | Р | Р | Н | Н | Н | Н | ? | ? | Н | ? | Н | Н | Н | Н | Н | ? | Н | ? | Н |
| CH3COO — | Р | Р | Р | Р | Р | Р | Р | Р | Р | — | Р | Р | — | Р | Р | Р | Р | Р | Р | Р | — | Р |
| SiO3 2- | Н | Н | Р | Р | ? | Н | Н | Н | Н | ? | ? | Н | ? | ? | ? | Н | Н | ? | ? | Н | ? | ? |
| Растворимые (>1%) | Нерастворимые ( Спасибо! Ваша заявка отправлена, преподаватель свяжется с вами в ближайшее время. Вы можете также связаться с преподавателем напрямую: 8(906)72 3-11-5 2 Скопируйте эту ссылку, чтобы разместить результат запроса » » на другом сайте. Изображение вещества/реакции можно сохранить или скопировать, кликнув по нему правой кнопкой мыши. Если вы считаете, что результат запроса » » содержит ошибку, нажмите на кнопку «Отправить». Этим вы поможете сделать сайт лучше. К сожалению, регистрация на сайте пока недоступна. На сайте есть сноски двух типов: Подсказки — помогают вспомнить определения терминов или поясняют информацию, которая может быть сложна для начинающего. Дополнительная информация — такие сноски содержат примечания или уточнения, выходящие за рамки базовой школьной химии, нужны для углубленного изучения. Здесь вы можете выбрать параметры отображения органических соединений. Содержание
10 класс , Напишите уравнение реакции этиламина с уксусной кислотой?Химия | 10 — 11 классы 10 класс , Напишите уравнение реакции этиламина с уксусной кислотой. Ну вообще то у ввс изображен этиловый спирт и уксусная кислота. И эта реакция называется этерификацией. C2H5OH + CH3COOH = > ; CH3COOC2H5 + H2O Получился сложный эфир и вода Если вам нужна реакция взаимодействия этиламина с уксусной кислотой то : C2H5NH2 + CH3COOH = [C2H5NH3]CH3COO Напишите пожалуйста 5 реакций уксусной кислоты с COOH?Напишите пожалуйста 5 реакций уксусной кислоты с COOH. Напишите уравнения реакций получения метилового эфира уксусной кислоты?Напишите уравнения реакций получения метилового эфира уксусной кислоты. Напишите уравнения реакций получения уксусной кислоты CH3COOH из карбида кальция?Напишите уравнения реакций получения уксусной кислоты CH3COOH из карбида кальция. Напишите уравнение реакции между этиламином и азотной кислотой?Напишите уравнение реакции между этиламином и азотной кислотой. 1)Этиламин + ангидрид уксусной кислоты 2)Этиламин + хлорэтан 3)пропилендиамин — 1, 2 + бромоводородная кислота Помогите, плиииз?1)Этиламин + ангидрид уксусной кислоты 2)Этиламин + хлорэтан 3)пропилендиамин — 1, 2 + бромоводородная кислота Помогите, плиииз. Напишите пожалуйста уравнение реакции уксусной кислоты с оксидом натрия?Напишите пожалуйста уравнение реакции уксусной кислоты с оксидом натрия. Напишите 3 уравнения химических реакций , показывающих А)сходство в химическх свойствах муравьиной и уксусной кислоты Б)отличие муравьиной кислоты от уксусной В)сходство муравьиной или уксусной кислот?Напишите 3 уравнения химических реакций , показывающих А)сходство в химическх свойствах муравьиной и уксусной кислоты Б)отличие муравьиной кислоты от уксусной В)сходство муравьиной или уксусной кислот неорганическими кислотами Что такое (ледяная)уксусная кислота. Напишите пожалуйста уравнения реакций : этилового спирта, муравьинной кислоты и уксусной кислоты?Напишите пожалуйста уравнения реакций : этилового спирта, муравьинной кислоты и уксусной кислоты. Напишите уравнение реакции фенола ( C6H5OH ) с уксусной кислотой ( CH3COOH )?Напишите уравнение реакции фенола ( C6H5OH ) с уксусной кислотой ( CH3COOH ). Напишите уравнение реакции между уксусной кислотой и пропанолом — 1 с образованием сложного эфира?Напишите уравнение реакции между уксусной кислотой и пропанолом — 1 с образованием сложного эфира. На этой странице вы найдете ответ на вопрос 10 класс , Напишите уравнение реакции этиламина с уксусной кислотой?. Вопрос соответствует категории Химия и уровню подготовки учащихся 10 — 11 классов классов. Если ответ полностью не удовлетворяет критериям поиска, ниже можно ознакомиться с вариантами ответов других посетителей страницы или обсудить с ними интересующую тему. Здесь также можно воспользоваться «умным поиском», который покажет аналогичные вопросы в этой категории. Если ни один из предложенных ответов не подходит, попробуйте самостоятельно сформулировать вопрос иначе, нажав кнопку вверху страницы. АминыАмины — органические соединения, продукты замещения атомов водорода в аммиаке NH3 различными углеводородными радикалами. Функциональная группой аминов является аминогруппа — NH2. Классификация аминовПо числу углеводородных радикалов амины подразделяются на первичные, вторичные и третичные. Запомните, что основные свойства аминов выражены тем сильнее, чем больше электронной плотности присутствует на атоме азота. Однако, у третичных аминов три углеводородных радикала создают значительные затруднения для химических реакций. Таким образом, у третичных аминов основные свойства выражены слабее, чем у вторичных аминов. Основные свойства возрастают в ряду: третичные амины (слабые основные свойства) → первичные амины → вторичные амины (основные свойства хорошо выражены). Номенклатура и изомерия аминовНазвания аминов формируются путем добавления суффикса «амин» к названию соответствующего углеводородного радикала: метиламин, этиламин, пропиламин, изопропиламин, бутиламин и т.д. В случае если радикалов несколько, их перечисляют в алфавитном порядке. Общая формула предельных аминов CnH2n+3N. Атомы углерода находятся в sp3 гибридизации. Для аминов характерна структурная изомерия: углеродного скелета, положения функциональной группы и изомерия аминогруппы. Получение
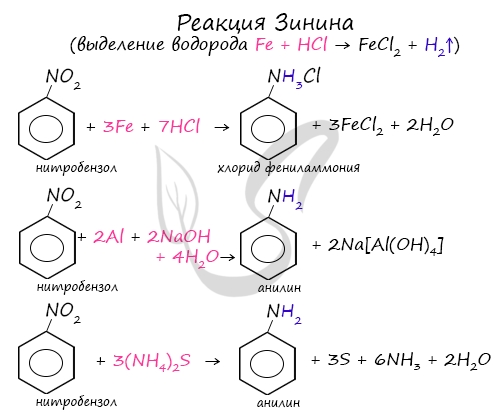
В основе этой реакции лежит замещение атома галогена в галогеналканах на аминогруппу, при этом образуются амин и соль аммония. При такой реакции нитрогруппа превращается в аминогруппу, образуется вода. Знаменитой является предложенная в 1842 году Н.Н. Зининым реакция получения аминов восстановления ароматических нитросоединений (анилина и других). Она возможна в нескольких вариантах, главное, чтобы в начале реакции выделился водород. Реакция сопровождается разрушением карбонильной группы и отщеплении ее от молекулы амида в виде воды. Этим способом в промышленности получают гексаметилендиамин, используемый в изготовлении волокна — нейлон. В промышленности амины получают реакцией аммиака со спиртами, в ходе которой происходит замещение гидроксогруппы на аминогруппу. В ходе реакции галогеналканов с аммиаком, аминами, становится возможным получение первичных, вторичных и третичных аминов. Химические свойства аминов
Как и аммиак, амины обладают основными свойствами, их растворы окрашивают лакмусовую бумажку в синий цвет. В реакции с водой амины образуют гидроксиды алкиламмония, которые аналогичны гидроксиду аммония. Анилин с водой не реагирует, так как является слабым основанием. Как основания, амины вступают в реакции с различными кислотами и образуют соли алкиламмония. Данная реакция помогает различить первичные, вторичные и третичные амины, которые по-разному с ней взаимодействуют. При конденсации первичных аминов с альдегидами и кетонами получают основания Шиффа, соединения, которые содержат фрагмент «N=C». Соли аминов легко разлагаются щелочами (растворимыми основаниями). В результате образуется исходный амин, соль кислоты и вода. При горении аминов азот чаще всего выделяется в молекулярном виде, так как для реакции азота с кислородом необходима очень высокая температура. Выделение углекислого газа и воды обыкновенно при горении органических веществ. © Беллевич Юрий Сергеевич 2018-2022 Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию. |